温敏性非对称偶氮聚合物的合成及性质
李广庆,赵鲲鸣,张海慧,崔桂花
(1.吉林医药学院,吉林吉林 132013;2.吉林市儿童医院,吉林吉林 132000)
偶氮染料是分子内具有一个或几个偶氮基的合成染料[1],偶氮苯类化合物因具有更多进入显色光区的π 电子而显色,是染料中品种最多、应用最广的一类合成染料,π 电子数越多,化合物的颜色越深。偶氮染料经过光辐照可发生光异构化,是研究最多和应用最广的光敏性功能物质。受到外界刺激(热、光等)时,偶氮苯所含基团表现出较高的活性,发生顺式到反式、反式到顺式的构型翻转[2-6]。通常情况下,反式构型的偶氮苯可以稳定存在于环境中(原因是偶氮苯的键角和异构化能垒比较特殊);但经过热、光等刺激后,偶氮苯类物质吸收一定的能量,克服偶氮键所产生的能垒,转变为能量较高的顺式构型。因为偶氮化合物具有这种特殊的性质,暴露在不同波长的光下会发生可逆的反式-顺式构型翻转产生光致变色现象,故可应用在光开关、光信息存储等领域[7-10]。近年来,偶氮聚合物的研究越来越受到人们的关注,原因是除可以发生特定的构型翻转外,在光诱导异构化时,其几何构型还会发生可逆转变,同时伴随着聚合物链结构的卷曲和伸展;若使用刚性基团将偶氮基团与聚合物连接,可实现偶氮苯光机械效应,与纳米技术有机结合可进行分子马达设计与制作。尽管偶氮聚合物在分子机械领域的应用尚不成熟,但是伴随着人们在该领域研究的深入,偶氮聚合物更多的应用价值会越来越多地被发掘。因此,本研究将偶氮单体与N-异丙基丙烯酰胺聚合后,利用偶氮聚合物优良的生物相容特性,将偶氮基团引入聚酰胺链中,以获得生物相容性良好的新型材料。
1 实验
1.1 材料和仪器
试剂:NaNO2[98%,西格玛奥德里奇(上海)贸易有限公司],4-甲氧基苯胺、苯酚(99%)、1,6-二溴己烷(98%)、丙酮(99%)、NaOH(分析纯)(上海阿拉丁生化科技股份有限公司),α-甲基丙烯酸[99%,梯希爱(上海)化成工业发展有限公司],N-异丙基丙烯酰胺(NIPAM),偶氮二异丁氰(AIBN)。
仪器:FTIR-8400S 型傅里叶变换红外光谱仪(日本岛津公司),Varian Unity 400 型核磁共振光谱仪(美国瓦里安公司),UV-1240型紫外可见光谱仪。
1.2 制备方法
将NaNO2(3.009 4 g)溶于去离子水(20 mL),缓慢加入到4-甲氧基苯胺(5.098 4 g)的盐酸溶液中,在0 ℃下强力搅拌2 h;将所得偶氮溶液加入到苯酚(4.090 2 g)的NaOH(4 g)溶液中,溶液颜色由棕色慢慢变为红褐色,反应2 h;用大量去离子水洗涤产物,除去过量的酸,使滤液pH 达到中性;用乙醇和水对粗产物进行重结晶,真空干燥,即得到4-羟基-4′-甲氧基偶氮苯(HEAB)。
取HEAB(2.43 g)、1,6-二溴己烷(14.67 g)、无水K2CO3(7.392 2 g)依次加入到100 mL 丙酮中,加热到75 ℃回流24 h,反应完成后趁热过滤,残留物用热丙酮清洗,收集滤液,真空蒸馏丙酮,残留物倒入冷的石油醚(30~60 ℃)中沉淀。在乙酸乙酯中热过滤重结晶两次,即得到1-溴-6-(4-甲氧基偶氮苯-4′-氧)己烷(BrEAB)。
将α-甲基丙烯酸(0.200 4 g)和KHCO3(0.100 2 g)溶解在10 mL N,N′-二甲基甲酰胺(DMF)中,然后在搅拌下缓慢加入BrEAB(0.391 2 g),在65 ℃水浴中反应4 h,旋蒸除去DMF,通过硅胶层析柱进一步纯化产物,得到的固体即为6-(4′-甲氧基-4-氧基偶氮苯)-甲基丙烯酸己酯(AzoMA)。
S-1-十二烷基-S′-(α,α"-二甲基-α"-乙酸)三硫代碳酸酯(DMP)的制备参照文献[11-12]。将DMP(20 mg)、NIPAM(1.27 mg)、1,3,5-三氧杂环己烷(50.44 mg)、AIBN(0.24 mg)溶解到5 mL 无水DMF 中,通氮气15 min,抽真空,重复3次;将反应瓶置于70 ℃油浴锅中反应,每隔一段时间取出一定量样品进行GPC测试,选取合适的分子质量,待反应完成后打开瓶塞将反应液暴露于空气中,减压旋蒸除去溶剂,在乙醚中沉淀,重复3 次,过滤蒸干即得到含有PNIPAM 大分子的链转移剂。
将AzoMA(0.132 g)、PNIPAM(152.7 mg)、AIBN(3.3 mg)依次加入到3 mL 无水苯甲醚中,在氮气条件下反应15 min,除氧-冷冻-解冻两次后80 ℃反应24 h,用CHCl2进行稀释,在30~60 ℃石油醚中沉淀,过滤,重复3 次,即得到二元嵌段共聚物PNIPAM-b-PAzoMA。
反应式如下:
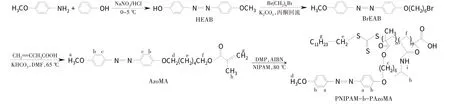
2 结果与讨论
2.1 AzoMA 的结构及表征
2.1.1 红外光谱
制备不饱和的AzoMA 须首先合成活性比较高的前驱体偶氮苯衍生物。由图1a 可知,3 413 cm-1处为HEAB 中—OH 的伸缩振动峰,1 600、1 585 cm-1处的峰均归属于HEAB 中的偶氮基团,由此可断定已获得HEAB。与图1a 比较,图1b 中3 435 cm-1处的羟基峰消失,而在2 942、2 862 cm-1处出现两个明显的特征吸收峰,分别归属于甲基和亚甲基,1 600、1 585 cm-1处的峰型和图1a 一致,说明已成功将HEAB 转变为BrEAB。图1c 中各处峰的峰型和位置与图1a、图1b 基本一致,不同之处是在1 704 cm-1处出现了酯基的C吸收峰,证明已初步制备出产物AzoMA。图1d中,3 301 cm-1处为PNIPAM 仲酰胺特征峰,1 652 cm-1处为酰胺Ⅰ带(主要为的伸缩振动吸收峰),1 558 cm-1处为酰胺Ⅱ带(主要为的弯曲振动吸收峰),1 281 cm-1处为—COOH的特征吸收峰。由此说明已成功合成二元嵌段聚合物PNIPAM-b-PAzoMA。

图1 HEAB(a)、BrEAB(b)、AzoMA(c)和PNIPAM-b-PAzoMA(d)的红外光谱图
2.1.2 核磁共振氢谱
由图2 可以看出,化学位移δ=7.86、6.99 处的两个峰均归属于AzoMA 苯环中的质子。由于AzoMA 上不饱和双键所处的化学环境不同,双键中的两个H产生两个比较明显的峰。δ=6.09、5.55 处的峰归属于AzoMA 丙烯酸己酯中丙烯基上的质子,δ=4.16、4.03分别为AzoMA 上和氧原子相连的亚甲基质子峰,δ=3.87为甲氧基中的质子峰,化合物其他官能团中的质子在图中均已标记,且每个峰都能找到匹配的质子,峰面积与对应的氢数成正比。

图2 AzoMA 的核磁共振氢谱
通过核磁共振氢谱图和红外光谱图可以判定已经成功合成了单体AzoMA。
由图3 可知,δ=7.85、6.98 处的峰均归属于偶氮苯上的苯环质子,δ=3.99 为偶氮苯上与氧原子相连的亚甲基质子峰,δ=3.89 处的峰归属于偶氮苯上和氧原子相连的甲基,在δ=6.55、3.98、2.89、1.75 和1.04 处出现的质子峰分别对应于PNIPAM 重复单元酰胺基团中的N—H、异丙基C—H、次甲基C—H、亚甲基C—H和甲基C—H,且峰面积与聚合物中对应的氢数成正比。通过核磁共振氢谱图可以判定已经成功合成了PNIPAM-b-PAzoMA 二元嵌段共聚物。
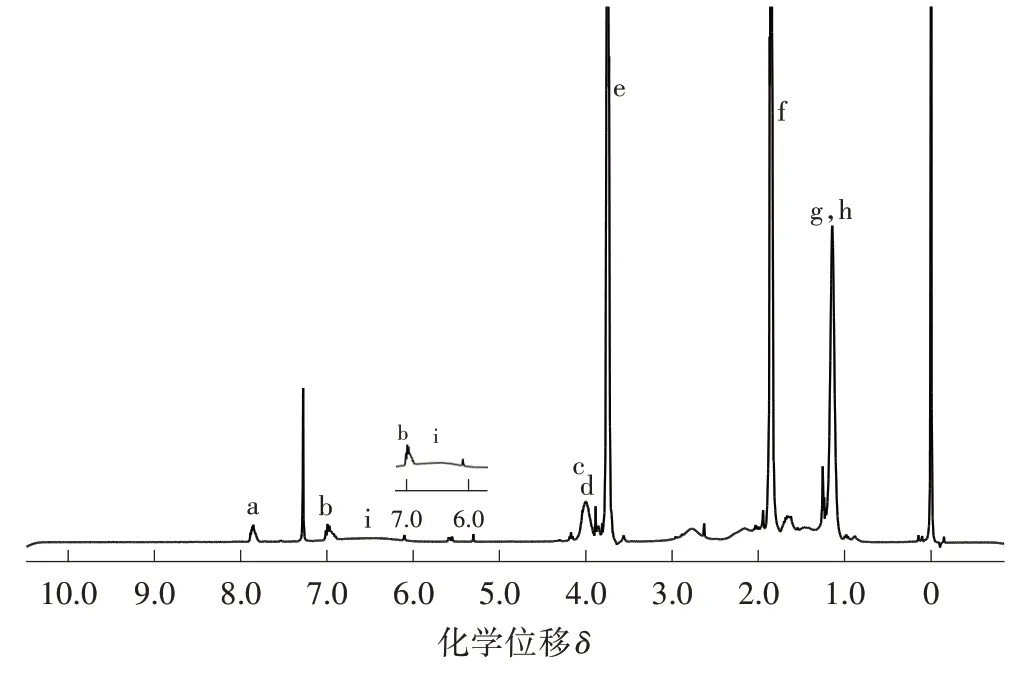
图3 PNIPAM-b-PAzoMA 的核磁共振氢谱
2.2 PNIPAM-b-PAzoMA 的性质
由图4 可知,未经紫外光照射时,偶氮苯基团主要是反式构型,在358 nm 处有强吸收峰,在450 nm处吸收峰相对较弱;随着紫外光照射时间的延长,450 nm 处的吸收峰逐渐变强。这是因为随着紫外光照射时间的延长,以顺式构型存在的偶氮苯增加,以反式构型存在的偶氮苯减少,而反式构型偶氮苯的摩尔消光系数大于顺式构型偶氮苯,所以反式-顺式转换过程吸光度降低。当紫外光照射时间足够长时,偶氮苯顺式-反式构型达到平衡,紫外可见光谱不再发生变化。
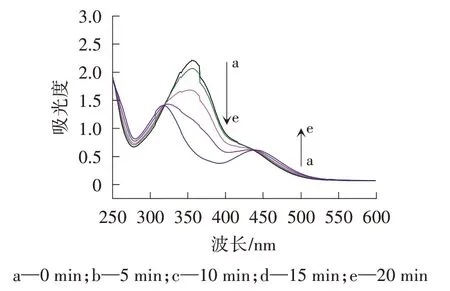
图4 PNIPAM-b-PAzoMA 水溶液在照射不同时间下的紫外可见光谱图

图5 PNIPAM-b-PAzoMA 的温度敏感循环曲线图
3 结论
利用重氮法制备了一种含不饱和键的非对称偶氮单体AzoMA。经365 nm 紫外光照射后,AzoMA 会经历反式-顺式的构型转变,是一种良好的光敏感聚合物单体。经RAFT 法AzoMA 与NIPAM 聚合形成末端羧基化非对称型温敏性偶氮聚合物。在紫外光的照射下,AzoMA 中的偶氮苯基团顺式构型比例逐渐增多;当紫外光照射时间足够长时,偶氮苯顺式-反式构型达到平衡。聚合物具有良好的光变色性能,结合NIPAM 的温敏性,未来将成为一种新型温敏性感光变色高分子材料。

