以酚醛树脂为碳源原位合成富锂层状相/尖晶石/碳核壳结构正极材料及其电化学性能
陆 地, 郑春满, 陈宇方, 李宇杰, 张红梅
(1. 国防科技大学空天科学学院, 长沙 410073;2. 特种化学电源国家重点实验室, 贵州梅岭电源有限公司, 遵义 563003)
富锂层状正极材料高容量和低成本的特性使其备受关注, 但是材料较差的倍率性能和循环性能阻碍了其进一步发展与应用[1]. 材料较差的电化学性能是由其较差的本征电导能力、锂离子扩散能力以及不稳定的晶体结构所致[2,3]. 材料需要经历活化过程以实现其高容量. 活化过程中锂离子从Li2MnO3的晶格中脱出形成Li2O和MnO2[4], 释放出来的氧会在材料中产生氧空位, 这些氧空位又会使过渡金属离子的迁移能垒降低, 从而导致层状相晶相转变程度加剧. 另一方面, 释放出来的氧气会与电解液反应生成不稳定的固体电解质界面膜, 导致极化阻抗增大[5]. 此外, 作为复合相的层状相本身不稳定的晶体结构也面临着不可避免的离子迁移和晶相转变问题[6]. 所有这些问题的共同作用导致富锂层状正极材料较差的倍率性能和循环稳定性, 限制了材料的商业化应用[1].
改善富锂层状正极材料倍率性能和循环稳定性的方法主要包括离子掺杂[7~9]、表面包覆[10~17]以及特殊形貌设计[2,18~21]. 研究发现, Li2MnO3相的活化以及层状相的晶相转变过程是由材料表面向体相进行的[5]. 因此表面改性被认为是一种重要的改性方式. 研究者们利用金属氟化物[10]、氧化物[11,13,14]或快离子导体[12,15,16]等材料对富锂正极材料的表面进行改性以稳定表面晶格并抑制副反应. 但是, 这些包覆材料单独使用均存在一定的局限性, 无法同时改进材料的离子电导率和电子电导率[22]. 近年来, 研究者们发现采用尖晶石相正极材料作为富锂正极材料的表面包覆层可以明显提升正极材料的倍率性能和循环稳定性[23]. 尖晶石复合可以为层状正极材料提供三维锂离子通道, 从而使材料体相内锂离子迁移能力得到明显提升, 同时尖晶石相和层状相较高的晶格匹配度以及尖晶石相较好的晶格稳定性为富锂正极材料提供了一个结构稳定的包覆层, 从而提高了富锂正极材料的表面结构稳定性, 限制了材料不可逆的“氧流失”和晶相转变[24]. 但尖晶石相本身的电子电导性较差, 且存在Jahn-Teller效应和一定程度的副反应[24]. 石墨烯等碳材料具有良好的导电性, 对于提升电极材料电化学性能具有显著作用, 是推动新能源器件发展的重要材料之一[25~29]. 研究发现, 碳包覆可以有效提升锰酸锂尖晶石相正极材料的电导率和电化学稳定性[7]. 通过构建碳-尖晶石双包覆层可以实现富锂层状正极材料电子电导和离子电导能力的同步提升. 有研究者通过聚多巴胺[2,30]和碳纳米管[22]作为碳包覆层原位衍生尖晶石相的方式构建了碳-尖晶石双层包覆结构, 但作为碳源的聚多巴胺和碳纳米管较高的成本和严苛的反应条件限制了该方法的进一步应用.
本文采用酚醛树脂作为碳源在富锂正极材料表面构建了碳包覆层, 通过高温碳热反应进一步将表面层的富锂正极材料转化为尖晶石相, 构建了碳-尖晶石双包覆层结构, 并研究了材料的电化学性能.
1 实验部分
1.1 试剂与仪器
六水合硫酸镍、七水合硫酸钴、一水合硫酸锰、碳酸钠、氨水、乙醇和N-甲基吡咯烷酮(分析纯, 国药集团化学试剂有限公司); 聚偏氟乙烯(PVDF, 分析纯, 比利时Solvay公司); 锂片(电池级, 天津中能有限公司); 六氟磷酸锂(LiPF6)、碳酸乙烯酯(EC, 电池级)和碳酸甲乙酯(EMC, 电池级)(南京莫杰斯能源材料有限公司); Celgard 2320型隔膜(电池级, 美国Celgard公司); 铝箔和电池壳(电池级, 深圳市科晶智达科技有限公司); 导电助剂Super P(30~40 nm, 电池级, 上海杉杉化工厂).
德国布鲁克公司Bruker Advance D8型X射线衍射仪(XRD, CuKα射线,λ=0.15418 nm, 工作电压40 kV, 工作电流40 mA, 扫描范围10°~80°, 扫描速度0.5°/min); 日本日立高新技术公司Hitachi S-4800型场发射扫描电子显微镜(FESEM, 加速电压为5 kV). 美国Thermo Scientific公司Escalab 250Xi型光电子能谱仪(Al阳极单色化X射线源,hν=1486 eV, 采用结合能位于284.6 eV的污染碳C1s峰进行能量校正); 德国Eltra公司CS2000型碳硫分析仪; 美国FEI公司Tecnai G2 F20型透射电子显微镜(TEM); 武汉蓝电电子股份有限公司Land 2100型电化学测试仪; 美国Ametek公司Princeton VesaSTAT型电化学工作站.
1.2 富锂层状相/尖晶石/碳复合正极材料的制备
将含1 mol/L的NiSO4·6H2, CoSO4·7H2O和MnSO4·H2O的混合溶液(摩尔比1∶1∶4)泵入四颈烧瓶反应器中, 在Ar气氛下, 分别向连续搅拌下的烧瓶中加入1 mol/L Na2CO3水溶液和0.1 mol/L的NH3·H2O, 通过调节NH3·H2O的泵入速率控制反应体系pH值为8.0, 水浴温度控制在60 ℃. 将产物用乙醇和去离子水各洗涤3次, 于80 ℃下烘干12 h得到碳酸盐前驱体. 将得到的碳酸盐前驱体和过量5%(质量分数)的Li2CO3充分混合后, 在马弗炉中于500 ℃煅烧5 h, 再于900 ℃煅烧15 h, 即得到富锂正极材料(标记为LR).
将0.2 g间苯二酚溶解于50 mL去离子水中, 加入1.0 g制得的富锂正极材料并均匀分散, 超声10 min后, 在持续搅拌下依次加入0.1 g质量分数为37%的甲醛溶液和5 mL质量分数为30%的氨水溶液. 室温下持续搅拌12 h后过滤, 使用乙醇和去离子水反复洗涤3次, 于80 ℃下干燥12 h, 得到酚醛树脂包覆的富锂层状正极材料. 将干燥后的材料在空气气氛下以5 ℃/min的升温速率升到450 ℃并保温5 h, 即得到富锂层状相/尖晶石/碳 3层核壳结构正极材料(标记为LR@S@C).
2 结果与讨论
2.1 材料的制备与表征
Scheme 1给出了LR@S@C复合正极材料的合成过程. 首先, 间苯二酚和甲醛在氨水的催化下在富锂层状正极材料表面逐渐聚合形成了一层均匀的酚醛树脂包覆层. 在随后的450 ℃高温热处理过程中, 酚醛树脂包覆层碳化, 并通过碳热反应使表层的富锂层状正极材料原位转化为尖晶石相, 从而构建起尖晶石和碳的双重包覆层.
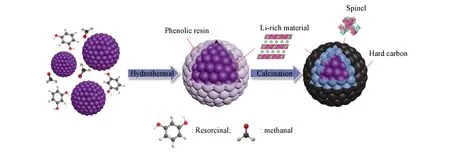
Scheme 1 Fabrication of LR@S@HC
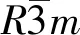
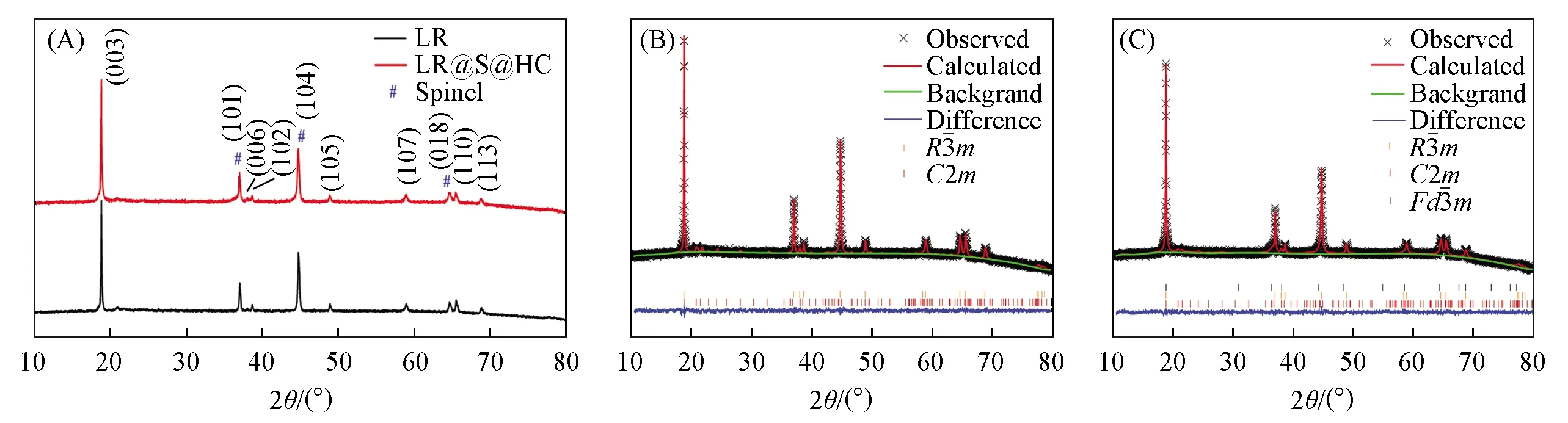
Fig.1 XRD patterns of samples(A) and refinement results of LR(B) and LR@S@HC(C)

Table 1 XRD refined results of samples
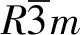
图4为改性前后的富锂层状正极材料的XPS谱图. XPS表面元素组成分析结果表明, 改性后材料

Fig.2 SEM images of LR(A,B) and LR@S@HC(C,D)

Fig.3 HRTEM and related FFT(insets) images of LR(A) and LR@S@HC(B,C)
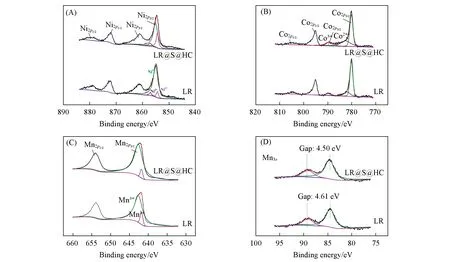
Fig.4 XPS spectra of LR and LR@S@HC
表面Ni和Mn的比例有所升高, 这是由于材料表面形成了镍锰尖晶石. 通过分峰软件对Ni, Co的2p轨道和Mn的2p, 3s轨道进行分峰处理, 分峰结果如图4(A)所示. Ni的2p3/2轨道可以分为+2价和+3价Ni的轨道, 改性之后, +2价Ni含量明显增多, 说明Ni元素在改性中呈还原趋势. Co的+2价和+3价离子的2p3/2主峰区分并不明显, 但卫星峰峰位差异较大, 因此通过对卫星峰分峰获得价态信息. 分峰结果表明, 改性后Co3+的比例由24%下降为20%[图4(B)], 说明Co在改性后被部分还原. 结合Mn的2p和3s轨道光电子能谱能够更加准确地得到Mn的价态信息. 图4(C)中, 对Mn2p轨道分峰可以发现Mn3+的比例由7.5%减少为5.3%, 说明Mn的价态升高; 此外, 图4(D)中Mn3s轨道峰裂分的间距减小, 进一步说明Mn在改性后价态升高.
2.2 电化学性能
图5(A)对比了LR和LR@S@HC材料的首次充放电曲线. 如图所示, 在0.2C倍率下, 包覆后材料的放电比容量由240.9 mA·h/g提升至275 mA·h/g, 首次库仑效率由70.8% 提升至80.6%. 材料在2.75 V和4.65 V左右出现了对应于尖晶石相的充放电平台. 图5(B)示出了材料在改性前后的倍率性能. 如图所示, 在相同倍率下, 包覆材料均显示出更高的放电比容量; 且随着倍率提高, 包覆材料与未包覆材料的放电比容量差异也增大. 在5C倍率下, 材料的放电比容量由80.4 mA·h/g 提升到135.1 mA·h/g. 可见, 尖晶石和碳的双层包覆可以有效提升材料的大电流放电和高倍率性能. 这得益于碳包覆所形成的导电网络和原位衍生尖晶石相提供的三维离子传输通道, 双层包覆结构可以有效提升锂离子和电子的传导速率. 在0.2C倍率下循环70次后包覆材料的放电比容量仍然保持在234.1 mA·h/g, 相比未包覆材料提升了6.50%[图5(C)], 在0.5C倍率下循环100次后包覆材料的放电比容量保持在218.7 mA·h/g, 相比未包覆材料提升了6.67%[图5(D)].
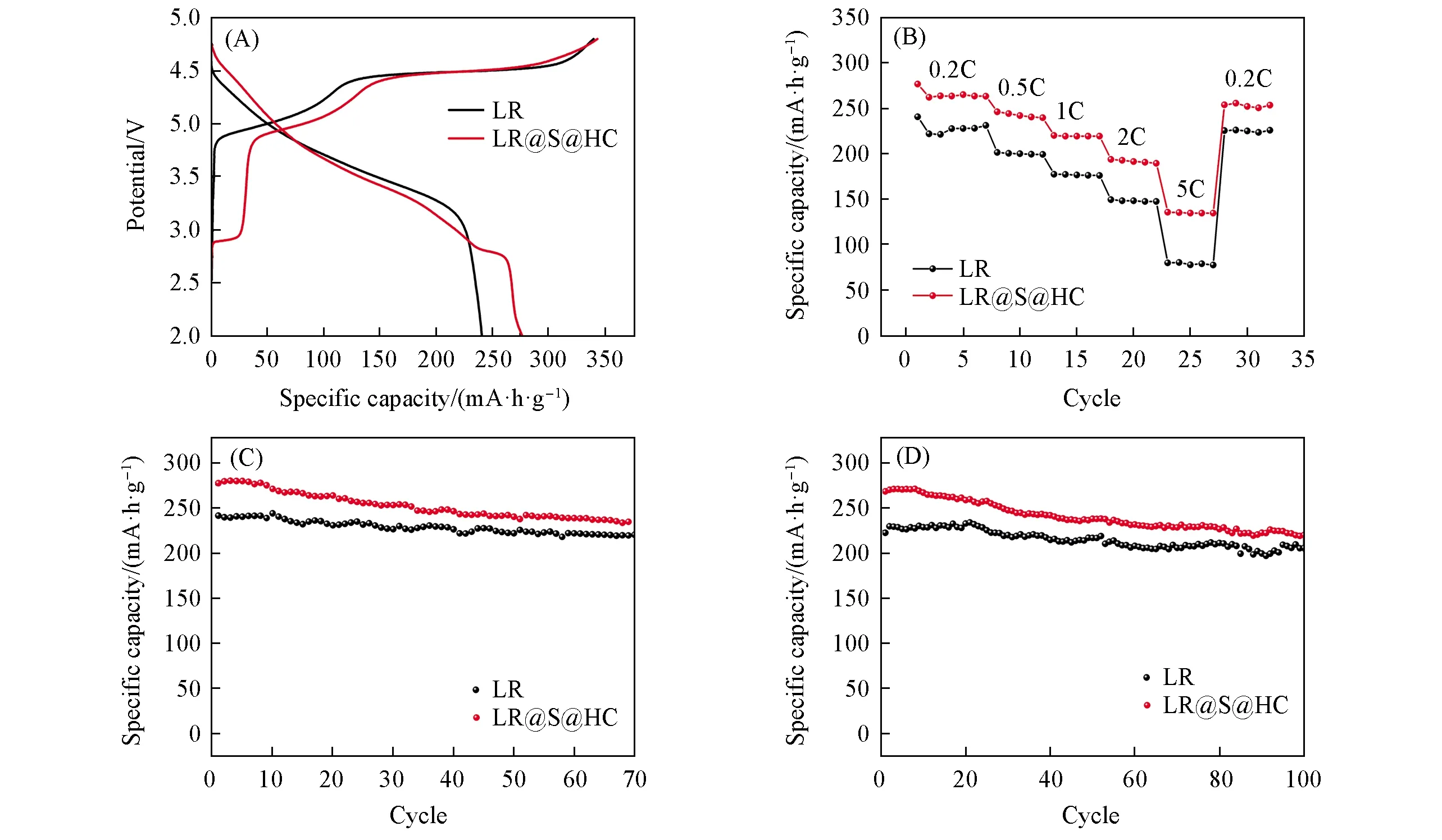
Fig.5 Initial charge/discharge profiles(A), rate performance(B) and cycle performance at 0.2C rate(C) and 0.5C rate(D) of the samples
为了进一步研究原位衍生尖晶石相及碳包覆提升富锂正极材料电化学性能的机理, 对材料进行了电化学阻抗(EIS)测试, 测试结果如图6(A)所示. 采用图中所示的等效电路对材料的阻抗谱进行拟合, 其中高频区域与实轴的交点与欧姆内阻(Rs)有关, 中频区的半圆与电解质/电极界面的电荷转移阻抗(Rct)有关. 改性后材料的Rs由1.60 Ω减小到1.39 Ω,Rct由210.1 Ω减小到159.0 Ω, 其中Rs的减小说明材料的表面导电性提升,Rct的减小说明锂离子迁移能力提高. 通过低频区域阻抗Zre与频率的二分之一次方(ω-1/2)的拟合线性关系曲线[图6(B)]和方程, 由斜率值可计算得到锂离子扩散系数(DLi), 改性后材料的DLi由1.2472×10-15cm2/s提升到1.4417×10-14cm2/s, 表明锂离子在材料体相内的迁移能力提高, 这与尖晶石相包覆层所形成的三维锂离子通道有关. EIS测试结果表明, 碳和尖晶石双包覆层有效提高了材料的电子电导和锂离子传输能力, 从而使材料极化阻抗减小, 倍率性能提高.
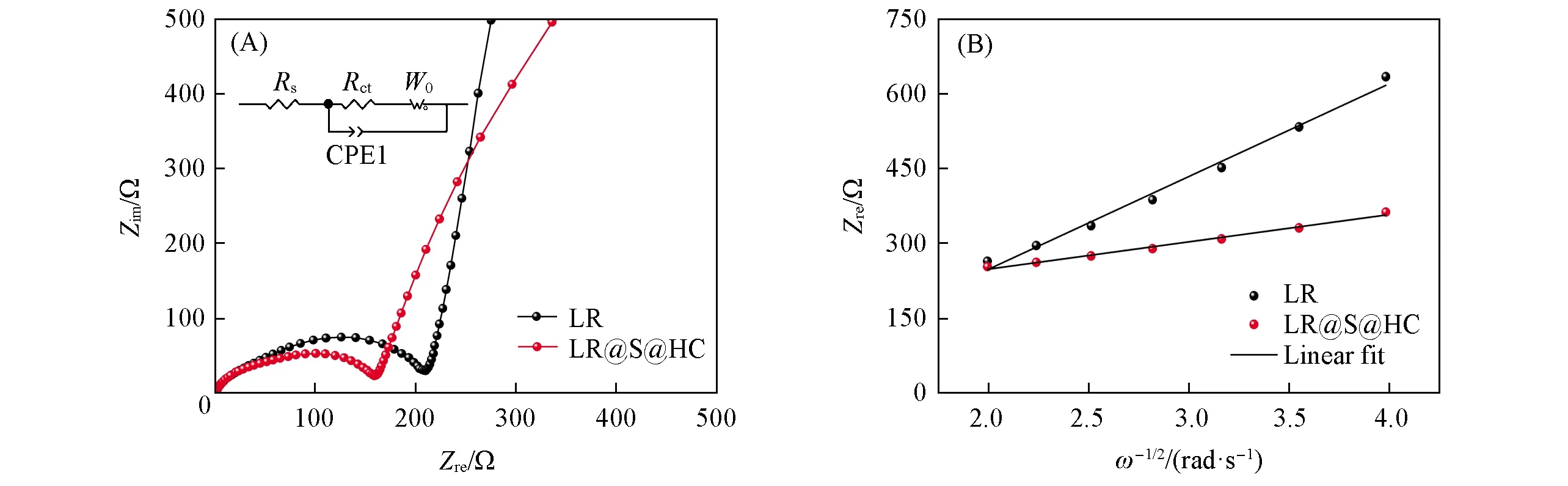
Fig.6 EIS results and equivalent circuit diagram(inset)(A) and relationship between Zre and ω-1/2(B) of the samples
3 结 论
首先在富锂层状正极材料表面构造了一层均匀的酚醛树脂包覆层, 之后通过热处理和原位诱导的方式得到了碳和尖晶石双重包覆的核壳结构正极材料. 双包覆层结构的构建使层状相c轴延长, 同时尖晶石相提供了三维离子传输通道, 从而使锂离子在正极材料体相内的扩散迁移能力得到明显提高; 另一方面, 材料表面形成的碳包覆层提供了电子快速迁移的路径. 在两者的综合作用下, 包覆后材料电化学阻抗明显减小, 在0.2C倍率下的放电比容量由240.9 mA·h/g提升至275 mA·h/g, 在5C倍率下的放电比容量由80.4 mA·h/g提升到135.1 mA·h/g. 同时材料晶格参数的变化说明包覆材料的晶格规整度提升, 0.5C倍率下循环100次后的容量保留率提升了6.67%. 这种以酚醛树脂为碳材料构建富锂层状相/尖晶石碳/多相复合结构的方式对其它类型多晶相复合富锂正极材料的晶相调控具有借鉴意义.

