十二氢十二硼酸双(二烷基-5-氨基四唑)盐的晶体结构及性能分析
孟令超, 绳利丽, 单自兴,2, 杨荣杰, 周智明
(1. 北京理工大学材料学院, 北京 100081;2. 武汉大学化学学院, 武汉 430072;3. 北京理工大学化学与化工学院, 北京 100081)
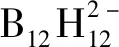
富氮杂环化合物是高能量密度材料的重要组成部分, 咪唑、三唑、四唑和呋喃等富氮杂环化合物的研究已有大量报道[4~10]. 四唑类含能化合物具有能量密度高、生成热高及安全性好等优点, 分解产生的气体以氮气为主, 可降低固体推进剂特征信号, 分解产物中不含氯元素, 与常见含能材料(如高氯酸铵等)相比更为绿色环保, 在含能材料领域受到了广泛关注[9,10]. 以5-氨基四唑为配体的含能配合物作为常见的含能材料, 氮含量及正生成焓较高, 其1位上的H在一定条件下被烷基取代后, 能够提高其稳定性, 从而提升5-氨基四唑的安全性能[11~15].
将高能四唑阳离子与高能硼氢阴离子结合, 可以得到一类新的生成热高且热稳定性好的高能材料[15~19]. 2016年, Hansen等[1]合成了能量较高的富氮十二氢十二硼酸盐. 目前已报道的含5-氨基四唑盐及十二氢十二硼酸盐只有双四唑取代硼氢盐和二十面体闭笼型十二氢十二硼酸5-氨基四唑盐, 前者易吸湿, 制备与纯化复杂, 实际应用前景较差[10].
前文[2]报道了11种新型高氮多硼含能材料十二氢十二硼酸双(二烷基-5-氨基四唑)盐的制备方法、波谱分析和热性能. 本文在此基础上, 培养了这11种化合物的单晶, 利用X射线单晶衍射对其进行了结构表征; 并利用Gaussian和EXPLO5软件对生成热与爆热等进行了计算, 研究了取代基对产物生成热和爆热等参数的影响.
1 实验部分
1.1 试剂与仪器
参照文献[19]方法制备烷基-5-氨基四唑(烷基分别为甲基、乙基、正丁基和正己基)和2-烷基-5-氨基四唑(烷基分别为甲基和乙基); 碘甲烷(MeI, 纯度99%)购于南京哈伯医药科技有限公司; 碘乙烷(EtI, 纯度99%)购于南京哈伯医药科技有限公司; 参照文献[20]方法制备十二氢十二硼酸钾(K2B12H12); 乙腈(分析纯)购于北京市通广精细化工公司; 去离子水(化学纯)购于北京化学试剂公司.
AFC-10/Saturn 724+型CCD面探X射线单晶衍射仪(XRD, 日本Rigaku公司); 204 F1型差示扫描量热仪(DSC, 德国Netzsch公司); micro TOF-QⅡ型电喷雾四级杆飞行时间质谱仪(ESI-HRMS, 德国Bruker公司).
1.2 实验过程
参照文献[2]方法制备11种十二氢十二硼酸双(二烷基-5-氨基四唑)盐: 十二氢十二硼酸双(1,4-二甲基-5-氨基四唑)盐(1)、十二氢十二硼酸双(1-乙基-4-甲基-5-氨基四唑)盐(2)、十二氢十二硼酸双(1,4-二乙基-5-氨基四唑)盐(3)、十二氢十二硼酸双(1-甲基-4-正丁基-5-氨基四唑)盐(4)、十二氢十二硼酸双(1-乙基-4-正丁基-5-氨基四唑)盐(5)、十二氢十二硼酸双(1-甲基-4-正己基-5-氨基四唑)盐(6)、十二氢十二硼酸双(1-乙基-4-正己基-5-氨基四唑)盐(7)、十二氢十二硼酸双(1,3-二甲基-5-氨基四唑)盐(8)、十二氢十二硼酸双(1-甲基-3-乙基-5-氨基四唑)盐(9)、十二氢十二硼酸双(1,3-二乙基-5-氨基四唑)盐(10)和十二氢十二硼酸双(1-乙基-3-甲基-5-氨基四唑)盐(11).
分别将11种十二氢十二硼酸双(二烷基-5-氨基四唑)盐加入到去离子水中, 于65 ℃加热0.5 h, 冷却重结晶, 得到11种十二氢十二硼酸双(二烷基-5-氨基四唑)盐的晶体.
在153(2) K温度下, 选取一定大小的晶体, 以石墨单色化的MoKα射线(λ=0.071073 nm)为衍射源, 用Xscan程序收集衍射数据. 强度数据经半经验吸收校正, 使用SHELXTL-97程序[21~23]以直接法解出结构, 采用全矩阵最小二乘法对结构进行精修, 分别得到11个化合物的晶体结构.
所得单晶数据已收录到英国剑桥晶体数据库中心, 化合物1~11的CCDC编号分别为: 181045, 1811048, 1811044, 1811051, 1811049, 181052, 1811050, 1811043, 1811047, 1811042, 1811046. 11种化合物的理化性质列于表1.
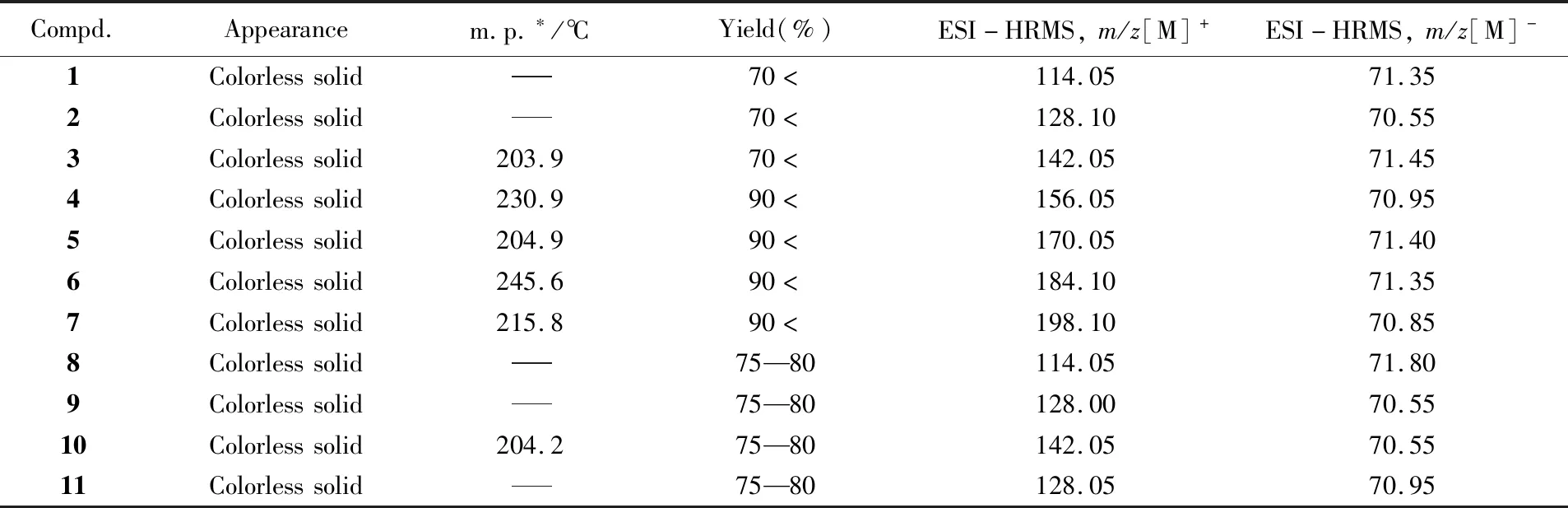
Table 1 Appearance, melting points, yields and ESI-HRMS data of compounds 1—11
* Melting endothermic peak of compounds1,2,8,9and11did not appear strongly decomposing effect occurs directly, it showed that rapid decomposition occured before melting crystallization.
2 结果与讨论
2.1 十二氢十二硼酸双(二烷基-5-氨基四唑)盐的结构分析
图1示出了11种化合物的分子结构, 其中红色代表B原子, 棕色代表C原子, 蓝色代表N原子, 白色代表H原子, 绿色代表O原子. 测试结果表明, 化合物1和3的结构中分别有1个和2个结晶水, 其它各化合物并不含结晶水. 在得到11种目标化合物晶体结构后, 将其于80 ℃真空干燥, 化合物1和3的外观由无色晶体变为白色粉末, 分析认为化合物1和3的晶体结构被破坏, 证明结晶水是化合物1和3晶体的组成部分, 一旦脱除结晶水, 其晶体结构将会被破坏, 出现塌陷. 化合物1和3的热失重分析结果见本文支持信息图S1.
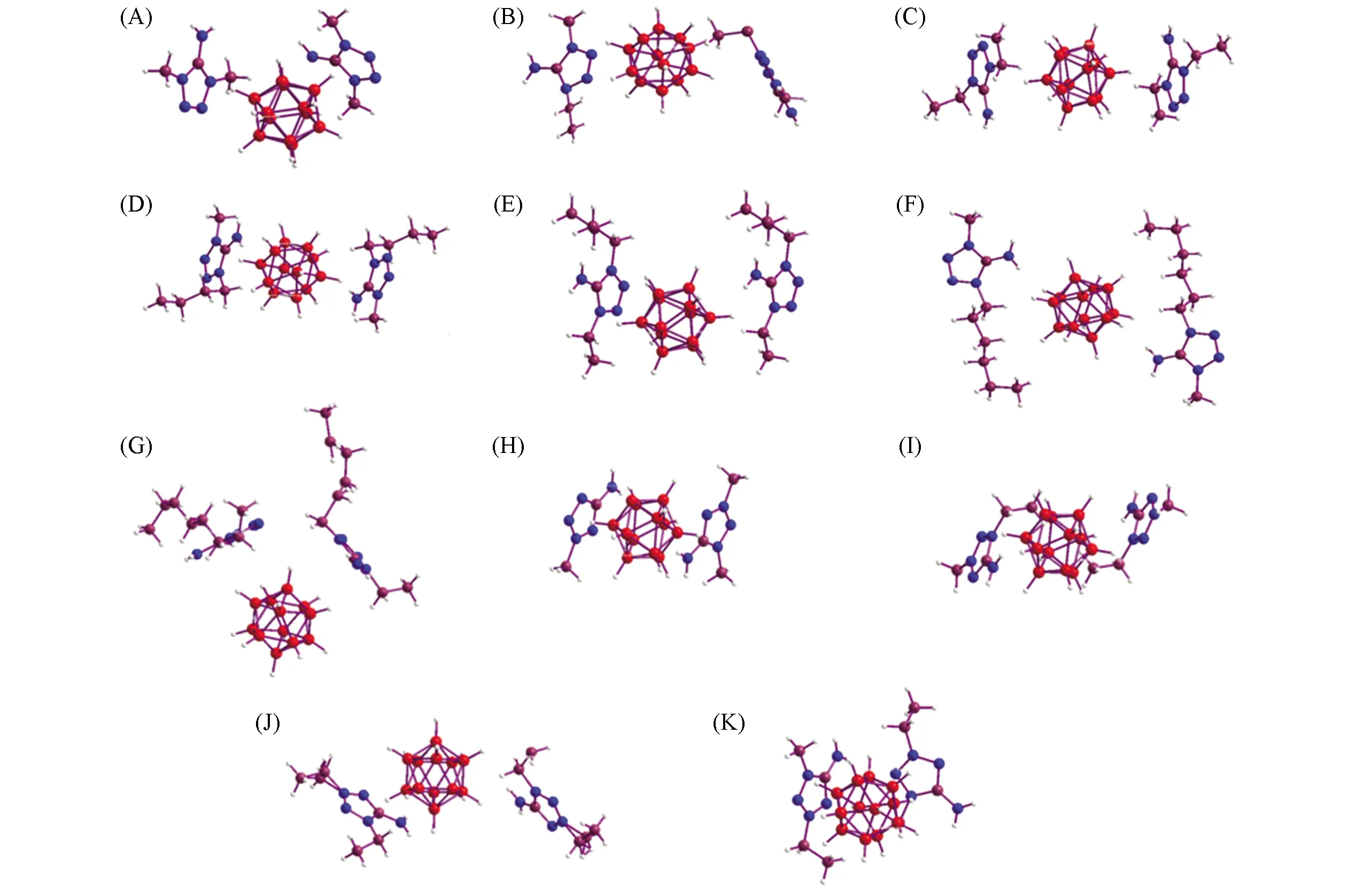
Fig.1 Crystal structures of compounds 1(A), 2(B), 3(C), 4(D), 5(E), 6(F), 7(G), 8(H), 9(I), 10(J) and 11(K)
化合物1和3结晶水中的O原子与四唑环上氨基取代基中N原子的距离分别为0.2814和0.2796 nm, 由此推断存在分子内氢键.
11种化合物的分子堆砌结构见图2, 化合物3~6和9在空间上各单元呈平行排列的层状结构. 由表S1和S2(见本文支持信息)可知, 化合物2,7,8,10和11属于单斜晶系; 化合物1,3~6和9属于三斜晶系. 其中, 十二氢十二硼酸双(1,4-二甲基-5-氨基四唑)盐和十二氢十二硼酸双(1,4-二乙基-5-氨基四唑)盐均属于三斜晶系; 十二氢十二硼酸双(1,3-二甲基-5-氨基四唑)盐和十二氢十二硼酸双(1,3-二乙基-5-氨基四唑)盐属于单斜晶系. 可见, 基团取代位置不同会导致其空间晶型存在差异.

Fig.2 Spatial structures of compounds 1(A), 2(B), 3(C), 4(D), 5(E), 6(F), 7(G), 8(H), 9(I), 10(J) and 11(K)
对烷基取代5-氨基四唑同一位置的化合物1~7进行分析发现, 该类化合物的密度随取代烷基碳原子数的增多而下降, 且与形成的晶系类型无关; 而化合物8~10的密度随取代烷基碳原子数的增多而下降; 化合物11和8的取代烷基类型相同, 晶体堆砌结构不同导致二者的密度不同. 化合物9分子中双烷基取代的5-氨基四唑阳离子与硼笼阴离子并列排布, 即氨基四唑环所在的平面与硼笼相交; 而化合物11中的氨基四唑环所在的平面不与硼笼相交, 这2种氨基四唑环的排布方式带来了相同原子数占空间体积的不同, 影响了其密度. 五元环结构不是芳香体系, 使晶体中面与面之间的相互作用较弱, 堆积不够紧密, 对其密度有一定的影响.
化合物7的晶胞中分子数(Z)为16个, 化合物8的晶胞分子数为4个, 其余均为1~2个. 化合物7的晶胞体积(V=13.039 nm3)远大于其它化合物, 化合物7的烷基取代基为正己基和乙基, 与其它化合物的烷基取代基相比链段最长, 己基的空间构型类型多, 导致化合物7的晶胞中含有不同构型和空间位置的阴阳离子数量最多, 体积最大.
2.2 取代基对十二氢十二硼酸阴离子键长的影响
B—B键长分析结果(表2)表明, 硼笼不是各键完全相等高度对称的正二十面体结构. 笼型结构中靠近烷基取代5-氨基四唑的部分受到电荷的吸引, 靠近阳离子的B—B键变长, 硼笼略有变形. 在不同晶胞中, 存在的重复硼笼阴离子和烷基取代5-氨基四唑阳离子的数量不同, 键长也略有不同, 键长的变化取决于B—B键受周围电荷吸引的程度.
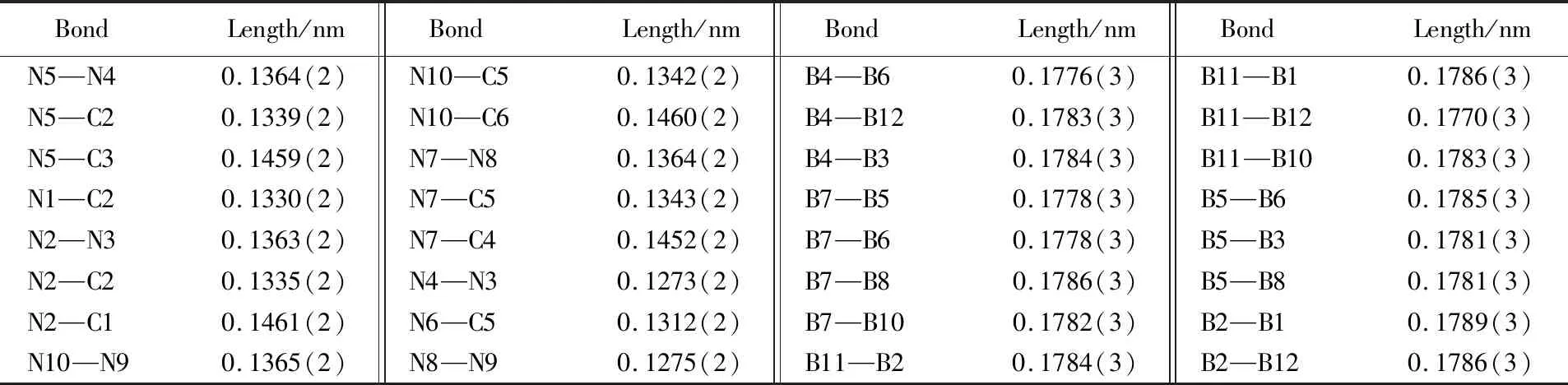
Table 2 Selected bond lengths(nm) of compound 1
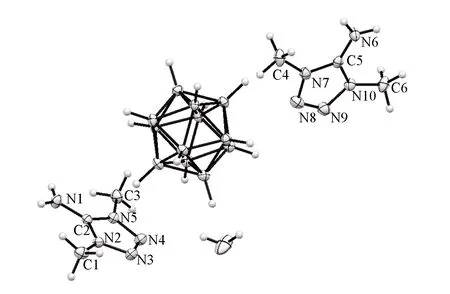
Fig.3 Molecular structure and spatial structure of compound 1
图3示出了化合物1的晶胞重复结构, 可见, 晶胞由2个1,4-二甲基-5-氨基四唑阳离子和1个十二氢十二硼酸阴离子组成, 其中2个1,4-二甲基-5-氨基四唑阳离子取代基的化学键键长略有差别. 对于同在氨基与四唑环上的C—N键, C5—N6的键长为0.1312 nm, 而C2—N1的键长为0.1330 nm, 表明晶格中C—N键长与硼笼的相对距离有关. 与四唑环相连的烷基取代基键长接近, C4—N7键长为0.1452 nm, C6—N10键长为0.1460 nm; 另一个处于晶格不同位置的四唑环上烷基取代基的键长分别为0.1461 nm(C1—N2)和0.1459 nm(C3—N5). 化合物3中, 与四唑环相连的2个乙基的C—N键长分别为0.1474和0.1470 nm; 化合物4中, 与四唑环相连的甲基C—N键长为0.1464 nm, 丁基C—N键长为0.1468 nm; 化合物5中, 与四唑环相连的乙基C—N键长为0.1474 nm, 丁基C—N键长为0.1468 nm; 化合物6中, 与四唑环相连的甲基C—N键长为0.1466 nm, 己基C—N键长为0.1469 nm. 分析上述数据发现, 不同烷基间供电作用差异小, 碳原子数增加对四唑环相连C—N键长无明显影响. 化合物1~11的阴阳离子被固定在晶格中, 与溶液状态相比, 其化学键伸展旋转受到限制更大, 键长取决于化学键在晶格中的相对位置.
比较了烷基不同取代位置的C—N键长, 对于化合物8, 1位取代的甲基C—N键长为0.1451 nm, 3位取代的甲基C—N键长为0.1461 nm; 对于化合物10, 有2种相对不同位置的阳离子, 1位取代的乙基C—N键长分别为0.1451和0.1468 nm, 3位取代的乙基C—N键长分别为0.1468和0.1505 nm. 键长的变化与烷基碳原子数和取代位置均无明显联系, 而与自身所在的晶格位置有关.
2.3 十二氢十二硼酸双(二烷基-5-氨基四唑)盐的生成热与爆热分析
采用量子化学综合软件包Gaussian 09软件计算了化合物的生成热. 在B3LYP/6-31+G**水平下进行结构优化和频率分析, 在MP2(full)/6-311++G**水平下计算了单点能量. 所有优化的结构均为势能面上的真实能量最小点, 无虚频, 分别计算了化合物1~11的生成热. 基于生成热和密度, 利用EXPLO5计算了其爆轰性能. 由表3可见, 化合物1~7中烷基化5-氨基四唑的取代位置均为1位和4位, 化合物8~11中烷基化5-氨基四唑的取代位置均为1位和3位, 同一取代位置化合物的生成热和爆热随烷基取代基碳原子数的增多而下降. 与化合物1相比, 化合物7的生成热和爆热分别下降34.86%和37.42%. 化合物9和化合11的取代基相同, 相同取代基分别取代了四唑环上的不同位置, 是同分异构体, 生成焓相近. 化合物2的爆速和爆压最高, 分别达到6390.1 m/s和11.528 GPa. 化合物1和8中烷基化5-氨基四唑的取代基团均为2个甲基, 但与化合物1相比, 化合物8的生成焓下降56.51%, 爆热下降19.46%, 表明1,4取代的化合物的生成焓和爆热要优于1,3取代的化合物. 生成热与爆热的下降不利于化合物在含能领域的应用.
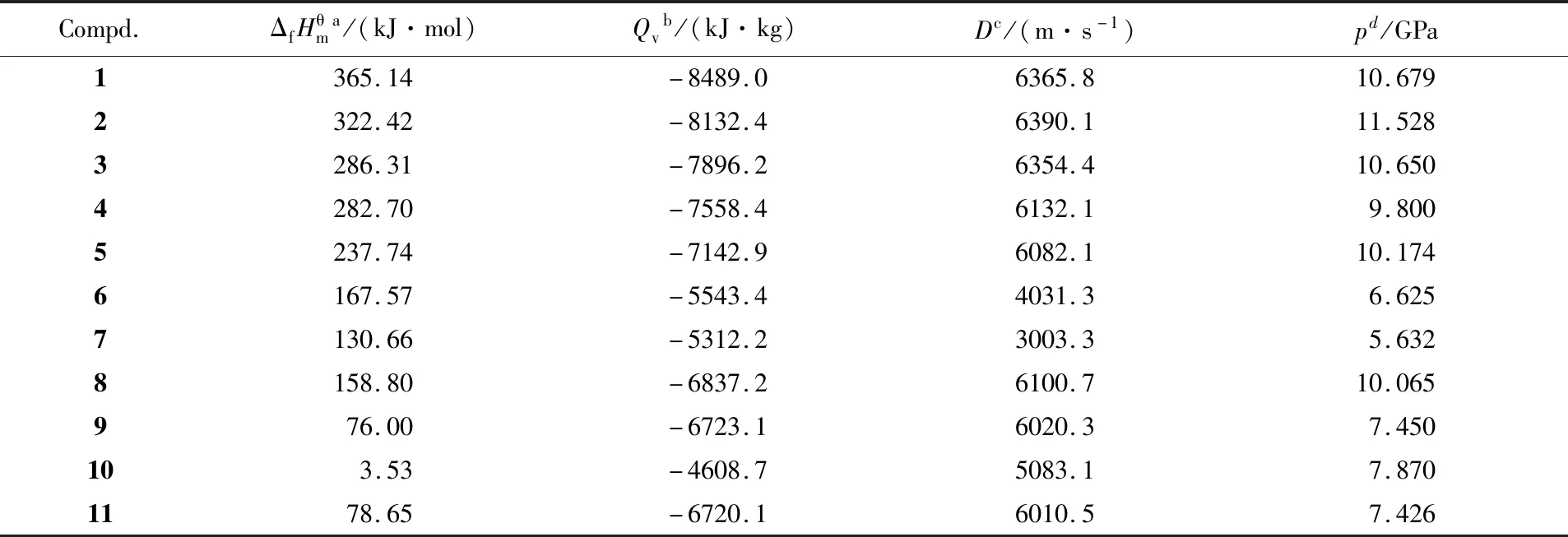
Table 3 Heat and explosive properties of compounds 1—11
a. Enthalpy of formation;b. explosion heat;c. detonation velocity;d. explosion pressure.
3 结 论
11种十二氢十二硼双(二烷基-5-氨基四唑)盐晶体的晶型有2类, 分别为单斜晶系和三斜晶系, 所属晶系与其中烷基取代基的位置相关. 11种化合物晶体的密度介于1.097~1.229 g/cm3之间. 1,4取代的化合物1~7的密度随取代烷基碳原子数增多而下降, 且与所形成的晶系类型无关; 而1,3取代的化合物8~10的密度随取代烷基碳原子数的增多而下降; 化合物11与化合物8取代烷基类型相同, 晶体堆砌结构不同导致密度存在差异. 化合物1和3的单晶结构中存在结晶水, 结晶水中的O原子与氨基中的N原子存在氢键相互作用. 11种化合物中阳离子的取代基与四唑相连的C—N键长取决于其在晶胞中的相对位置. 化合物的生成热与爆热随烷基取代基的碳原子数增多而下降, 与黑索今等硝胺类炸药相比, 这些化合物具有良好的爆轰性能, 化合物2的爆速达到6390.1 m/s, 爆压达到11.528 GPa.
支持信息见http://www.cjcu.jlu.edu.cn/CN/10.7503/cjcu20200115.

