蒸硒渣处理过程的优化研究
房孟钊,方 准,赵浩然
(1.大冶有色金属有限责任公司,湖北 黄石 435002;2.有色金属冶金与循环利用湖北省重点实验室,湖北黄石 435002)
目前,大冶有色金属有限责任公司冶炼厂稀贵车间针对铜阳极泥的处理过程[1~6],在高温高酸分铜工序中出现了严重的金属损失情况,尤其是碲的损失,有25%以上的碲进入分铜后液中,分铜后液直接蒸发结晶生产为硫酸铜[7~12],因此,这部分碲造成直接损失而无法回收;在氯化分金工序中,由于氧化剂加入不到位而造成有价金属金、铂、钯、碲在每年的生产中经常出现未被完全浸出,未被浸出的贵金属金、铂、钯留在分银渣中而无法回收;10%~15%的碲未被浸出而直接进入分金渣,最后,一部分进入分银后液而影响粗银粉的品位,一部分留在分银渣中,直接造成碲的损失而无法回收。在前期的小试试验探索中,针对分铜工序与氯化分金工序尝试改为水浸分铜与控电位氯化氧化分金,各项指标基本达到要求。因此,本研究重点在于进一步优化水浸分铜工序与控电位氯化氧化分金工序的条件控制,降低有价金属的损失。
1 试 验
1.1 试验原料
大冶有色金属有限责任公司冶炼厂稀贵车间的铜阳极泥经过回转窑硫酸化焙烧后得到的蒸硒渣,其主要成分见表1。

表1 蒸硒渣主要成分分析结果 %
1.2 旧工艺流程
大冶有色金属有限责任公司冶炼厂稀贵车间现在针对铜阳极泥处理过程的工艺流程如图1所示。
1.3 新工艺流程
针对目前稀贵车间的铜阳极泥处理过程中出现的问题,考虑将分铜浸出工序改为水浸分铜、氯化分金工序改为控电位氯化氧化分金,其新工艺流程如图2所示。
2 结果与讨论
根据新工艺流程,本研究对关键步骤水浸分铜工序、控电位氯化氧化分金工序等进行了一系列条件优化试验,其中水浸分铜进行了NaCl加入量条件试验等,分金步骤进行了反应时间、硫酸酸度、NaCl加入量的条件试验。
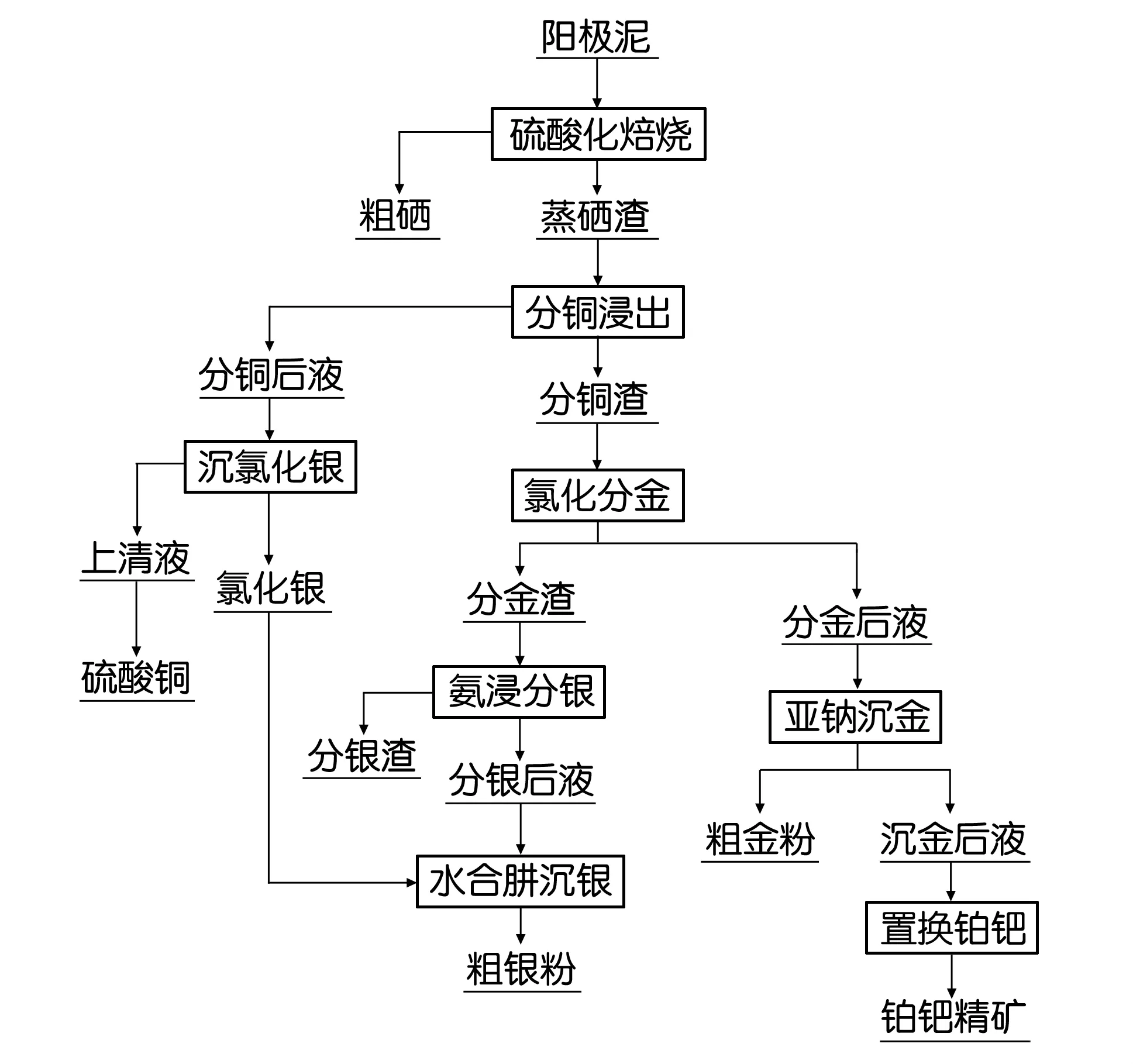
图1 旧铜阳极泥处理工艺流程图
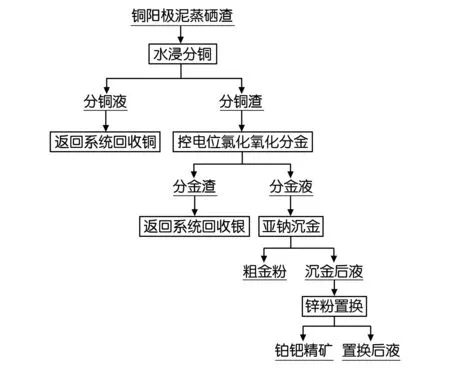
图2 蒸硒渣处理工艺流程图
2.1 水浸分铜
水浸分铜的试验条件包括:NaCl加入量、反应时间、液固比。分别加入NaCl理论量的0.5倍、1倍、1.2倍、1.5倍、2倍为条件进行试验,NaCl理论量的计算方法如下:不添加NaCl水浸分铜时,未浸出的Cu全部转化为CuCl2所需NaCl的量,以及浸出的Ag全部转化为AgCl所需NaCl的量,两者相加即为理论量。按照前期的小试探索试验,不添加NaCl时,铜的浸出率为80%左右,银的浸出率为20%~30%,本试验按原料中铜的20%转化为CuCl2加上银的30%转化为AgCl共所需的NaCl量为理论量,得到的试验结果见表2。从表2中可知,随着NaCl量的增加,这些元素的浸出率均有所提高。添加NaCl为理论量的0.5倍时,铜的浸出率为91%左右,碲浸出损失<3%,银元素基本不损失。当添加理论量及以上的NaCl时,铜的浸出率可达到95%以上,银基本未被浸出,碲的浸出损失<5%。故以添加理论量的NaCl为最佳添加量,即可使铜浸出率达到97%,碲浸出损失控制在5%以内,银基本不损失。
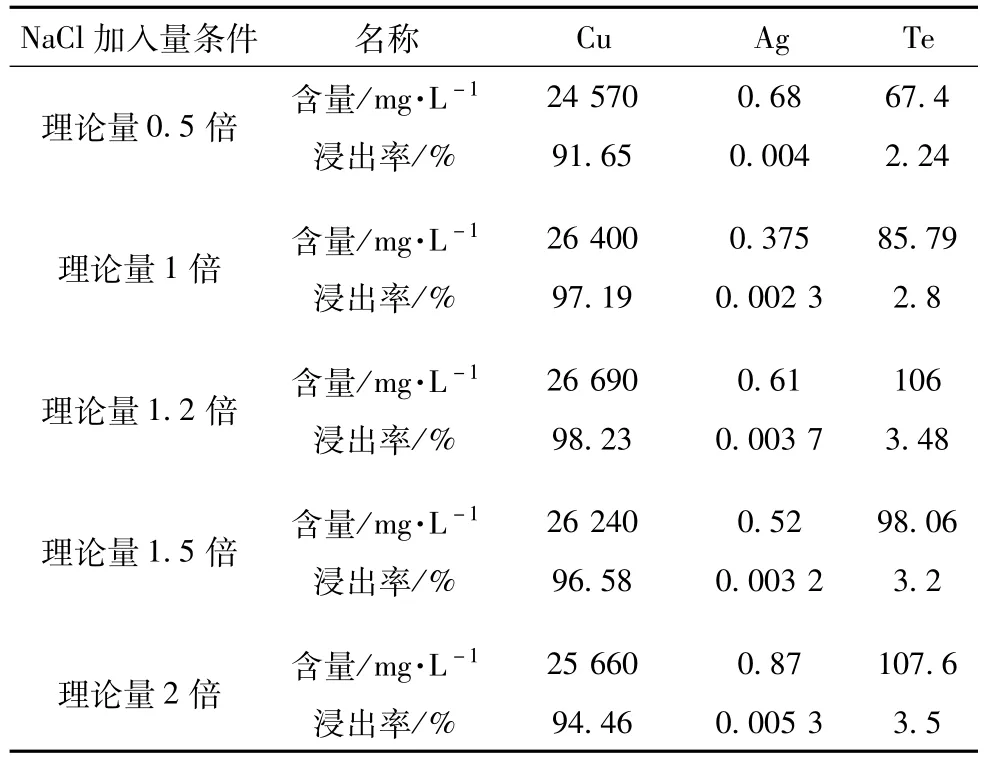
表2 水浸分铜时加入不同量的NaCl的各元素浸出率
铜的浸出率水平已基本达到生产要求,根据现有条件,进行了3 kg级放大试验,以此验证上述小试试验结果。
反应过程如下:称取3 kg蒸硒渣样品,同时称取180 g理论反应用量的NaCl,液固比4∶1,常温搅拌2 h。得到结果见表3。从表3可知,对水浸步骤进行放大验证试验,铜的浸出率仍然能够达到先前的技术水平。
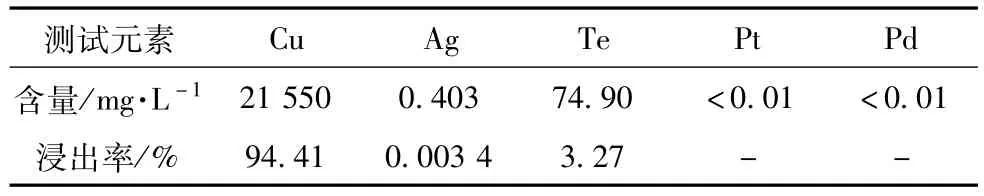
表3 水浸液中各元素浸出率
据此结果,在现场进行扩大试验验证,由于现场搅拌条件(约为100~200 r/min)与实验室(可达300 r/min)不一致,导致铜的浸出率有所下降,故在实验室对搅拌速率进行了条件试验,结果如图3所示。从图3中可看出,铜的浸出率与搅拌速率大小有一定的关系,随其增大而浸出率升高,根据数据可推测出实验室条件下搅拌速率在200~300 r/min时,铜的浸出率即可达到94%以上。从试验结果可以推断,水浸分铜反应可能主要为界面扩散控制,因此与蒸硒渣的粒度、颗粒分散度以及颗粒相与液相相对运动速率有关,生产上水浸分铜的浸出率之所以达不到实验室水平,主要是生产过程中搅拌速率较低,蒸硒渣颗粒没有充分分散的缘故,所以,生产上可以采取提高搅拌速率、预浸提高颗粒分散性和球磨降低颗粒粒度来提高界面扩散速度。
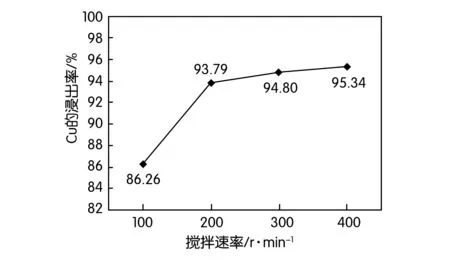
图3 不同搅拌速率下铜的浸出率
对于提高搅拌速率的方法来说,需要对现有搅拌设备进行改造,且搅拌速率过大对反应过程控制、设备的处理能力等方面都会有较大影响。对于先将蒸硒渣进行预浸静置处理,提高颗粒分散度的工艺,由于预浸时间相对较长,要求预浸反应的容器体积相对较大,这样会造成投资相对较大,且由于预浸时间长,物料回收周期也会相应延长,不利于资金流转。
预浸不同时间对铜浸出率的影响如图4所示,从图4中可以看出,在100 r/min条件下,要使铜的浸出率达到94%以上,预浸至少需12 h。在实际生产中,这可能会导致时间成本过大,同时增加的静置罐也增加了成本;若采用球磨工艺,可以大大缩减处理时间,其时间成本可能在1 h以内,由于蒸硒渣相对较易分散,球磨能耗也较小。故可考虑先将蒸硒渣球磨,再进行水浸步骤,以达到上述试验效果。
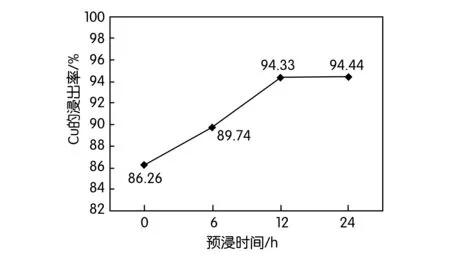
图4 预浸不同时间后100 r/min下铜的浸出率
2.2 控电位氯化氧化分金
分金的试验条件包括:氧化剂加入量、反应时间、酸度、NaCl加入量等,其中氧化剂加入量通过电位控制,反应时间试验条件为1 h、2 h,硫酸酸度试验条件为 1 mol/L、2 mol/L、3 mol/L,NaCl加入量试验条件为25%、35%、45%。试验结果见表4~表6。从表4中可看出,反应时间延长1 h,碲的浸出率大有提高,故以2 h为最佳反应条件。表5中显示,酸度为2 mol/L时,碲的浸出率最高;当酸度为3 mol/L时,碲的浸出率有所降低。故以2 mol/L为最佳反应体系酸度;表6中显示,随着NaCl加入量增大,碲的浸出率均有所提高,当NaCl加入量为45%时,碲的浸出率反而有所下降,说明NaCl量的增加对碲的浸出效果不大。

表4 分金时反应时间条件试验
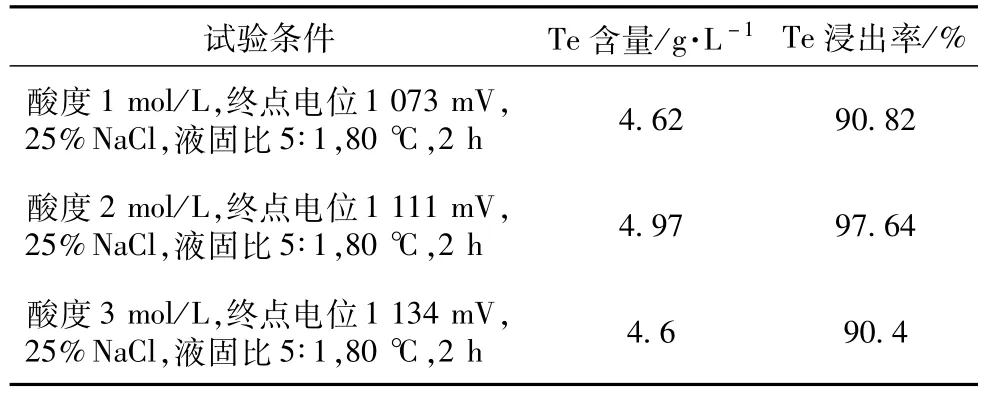
表5 分金时酸度条件试验
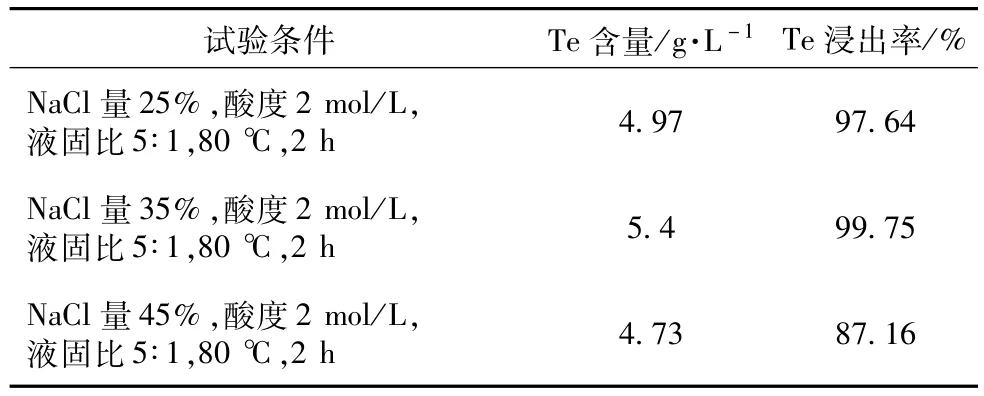
表6 分金时NaCl加入量条件试验
针对酸耗问题,结合控电位氯化氧化分金酸度条件试验情况可知,尽管酸度为2 mol/L时的综合性能最佳,但当酸度为1 mol/L时,碲的浸出率仍然能够达到90%以上,故将酸度调整为1 mol/L。对水浸渣进行研磨细化,具体条件为水浸渣不经研磨、水浸渣过200目筛、水浸渣过400目筛后分别控电位氯化氧化分金,结果见表7。随着粒度的逐渐减小,损失了关键元素碲的浸出率,因此通过研磨细化的方式并没有达到预期的效果。降低NaCl的加入量,并严格控制电位,具体设定条件为NaCl的加入量分别为25%、20%、10%,结果见表8。在酸度为1 mol/L的条件下,随着NaCl含量的降低,对碲的浸出基本无影响。当NaCl含量降为20%时,已基本达到现场实际生产时的水平,此时碲的浸出率达到最佳水平。
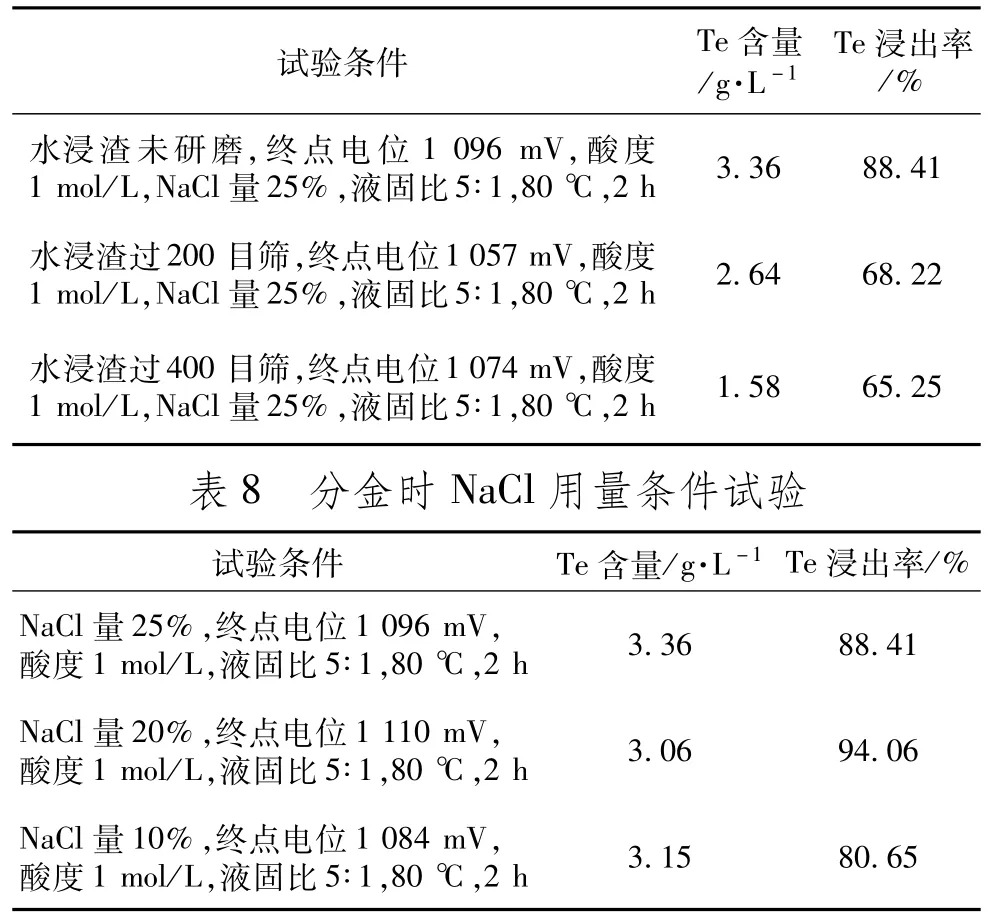
表7 分金时粒度条件试验
降低酸度后,对液固比、电位控制等条件做了更细化的试验,如图 5所示,液固比3∶1、4∶1、5∶1,对比这些条件下需加入的氧化剂NaClO3的量与电位的关系,结果见表9。
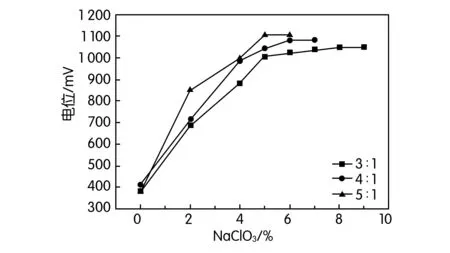
图5 不同液固比条件下NaClO3加入量与电位的关系
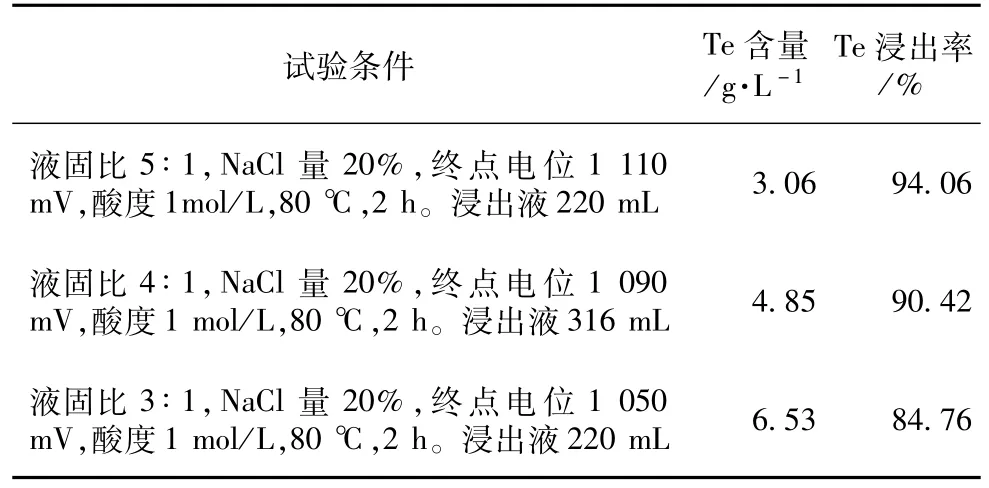
表9 不同液固比条件试验
从图5和表9中可看出,液固比越高,碲的浸出率越高,所需氧化剂加入量越少,当液固比≥4∶1时,碲的浸出率>90%,所需氧化剂≤水浸渣量的4%,溶液体系的终点电位为1 100 mV左右。综上,以酸度为 1 mol/L,NaCl加入量为 20%、液固比 5∶1、NaClO3加入量4%,80℃下反应2 h,控制终点电位在1 100 mV左右为控电位氯化氧化分金最佳试验条件,此时金、铂、钯基本被浸出至溶液中,碲的浸出率可达到94%以上,银元素基本留在分金渣中。
2.3 亚钠沉金
取试验得到的浸出液,边搅拌边缓慢加入亚硫酸钠溶液,维持反应温度在29~30℃,控制电位至所需电位后停止加入,反应1 h,静置4 h左右,洗涤过滤。监测电位点超过5个,终点电位为650~750 mV之间,沉金后液见表10,金的还原率达到了95%以上,其它元素的还原率均较低,说明经过控电位氯化氧化分金的进一步优化之后,亚钠沉金步骤中得到的粗金粉纯度也较之前提高了许多。

表10 沉金后液试验结果
2.4 全流程验证试验
根据上述试验结果,为了验证各阶段的工艺条件,进行了全流程试验。
1.水浸分铜:取300 g蒸硒渣,加入自来水,液固比4∶1,常温下搅拌2 h后过滤。试验结果见表11,试验结果显示,Cu的浸出率95%以上,Te浸出率为3%左右,Pt、Pd基本未浸出。因此第一步的水浸效果能够达到条件试验时的技术水平,符合后续流程验证的要求。
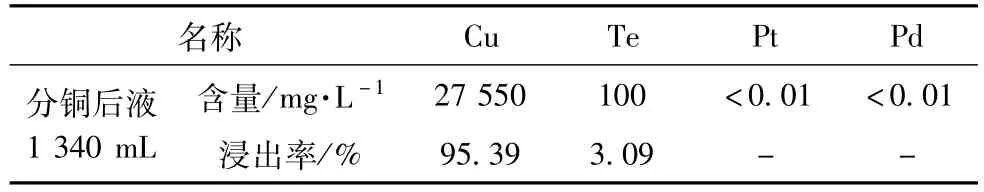
表11 分铜试验结果
2.控电位氯化氧化分金:取分铜后的全部水浸渣,按液固比5∶1加入1 mol/L的 H2SO4溶液,加入水浸渣干渣量20%的NaCl,升温至80℃,边搅拌边加入NaClO3饱和溶液,控制电位至所需电位,稳定后保温2 h。分金试验结果见表12,Au的浸出率97%以上,Te的浸出率92%以上,Pt、Pd基本全部浸出。
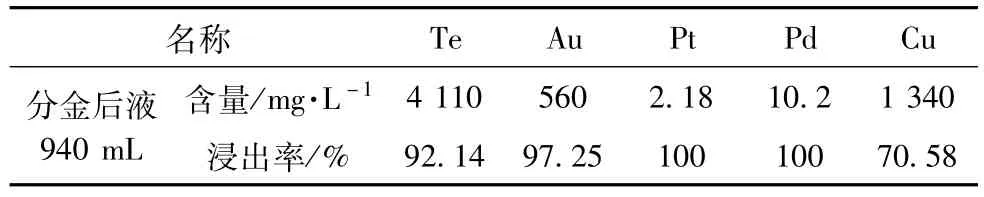
表12 分金试验结果
3.亚钠沉金:取定量分金后液,维持反应温度在29~30℃,边搅拌边缓慢加入亚硫酸钠溶液,控制电位至所需电位,反应1 h,静置4 h左右,洗涤过滤,结果见表 13,亚钠沉金过程中,Au的还原率为81.91%,Pt基本未被还原,Te和Pd有部分损失。
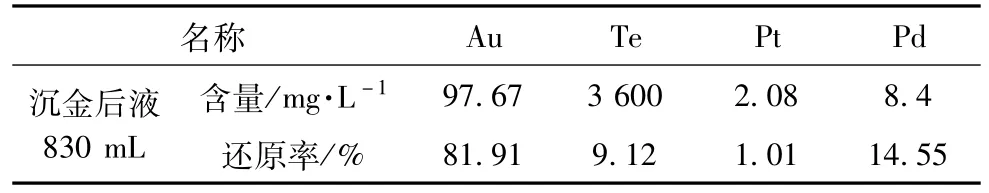
表13 亚钠沉金试验结果
4.锌粉置换:取定量沉金后液,将其pH调至3.5左右,常温搅拌并加入过量锌粉,反应2 h,结果见表14,锌粉置换后,Te、Pt、Pd的还原率都在99%以上。
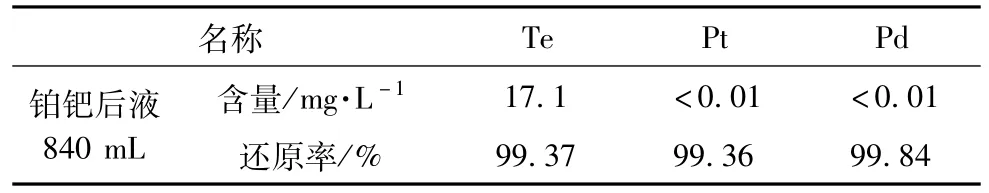
表14 锌粉置换试验结果
综上所述,全流程试验结果表明,在最终优化的试验条件下,Cu的浸出率在95%以上;Te在水浸分铜时的分散损失为3%左右,进入分金后液中约为92%;Ag基本不损失,留在分金渣中进行下一步回收;Au基本进入分金后液中,其它过程基本不损失;Pt、Pd在水浸分铜和氯化分金过程中基本没有损失。因此,在实验室条件下,新工艺流程能够达到指标要求。
通过试验确定的流程,水浸分铜可显著减少碲的分散,提高分铜液中硫酸铜纯度,减少分铜工序的酸耗。通过试验推断出水浸分铜生产过程中与实验室铜浸出率存在差异的原因,建议通过球磨化浆的方法改善水浸分铜的浸出率。
在氯化氧化分金的过程中,工艺流程采用较高的酸度进行氯化氧化浸出,减少氯化钠的加入量以减少银的损失,通过精确控制电位可以保证在高酸度条件下尽量多地浸出碲,尽量少地损失银等有价金属,同时也可以节省氧化剂的加入量。在控电位还原的过程中,也可通过精确控制电位减少还原剂加入量,减少贵金属的直收损失。因此,建议开发适应于生产的控电位系统,通过电位的精确控制,节省原材料消耗,提高碲等产品的回收率。
3 成本效益预计
与现有工艺流程相比,新的工艺流程方案在增加消耗很少的情况下,将Te的回收率大幅度提高,提高量约50%,具有非常可观的经济效益。
与现有工艺流程相比,工艺的主要差别在于:酸浸分铜改为水浸分铜;氯化氧化分金过程中,硫酸浓度比现有工艺略高,NaCl消耗降低;其它过程基本一致。总体上来说,三种主要试剂的消耗总量差异不大,具体对比见表15,处理5 t蒸硒渣,碲的回收率提高40%以上,能多回收约36 kg以上Te,当前Te的价格约300元/kg,因此,在成本不变的情况下,新的工艺流程处理5 t蒸硒渣可增加10 000元的经济效益,优势明显。
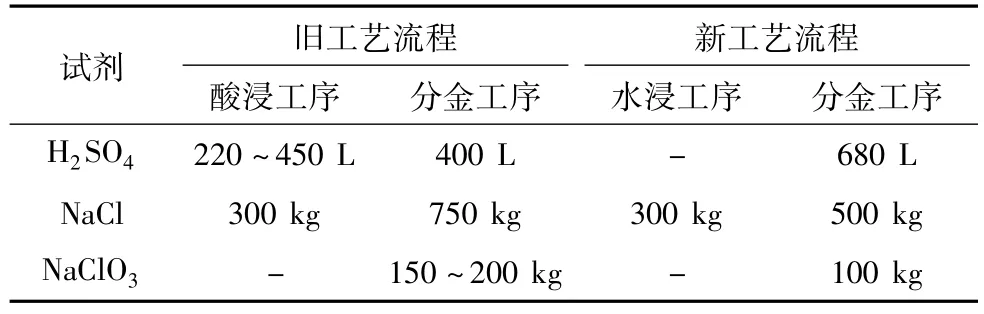
表15 试剂消耗量对比
4 结 论
1.通过水浸分铜、控电位氯化氧化分金、亚钠沉金、锌粉置换等试验,确定了蒸硒渣处理工艺流程。
2.对水浸分铜工序进行了条件优化试验,以添加6%的NaCl为最佳添加量,铜浸出率>95%,碲浸出损失为3%左右,金、铂、钯、银基本不进入溶液中。
3.水浸分铜反应主要是扩散反应控制,建议通过球磨化浆的办法提高水浸分铜的浸出率。
4.对控电位氯化氧化分金工序进行条件优化试验,以酸度为1 mol/L,NaCl加入量为20%、液固比5∶1、NaClO3加入量 4%,80℃下反应 2 h,控制终点氧还原电位在1 100 mV左右为最佳试验条件,此时金、铂、钯基本被浸出至溶液中,碲的浸出率可达到94%以上,银等其它元素基本留在分金渣中。
5.亚钠沉金时金的还原率为95%以上,沉金后液中金含量 <100 mg/L,其它元素基本不被还原。锌粉置换时铂、钯完全能被置换出来,置换后液中铂、钯含量均小于1 mg/L。
6.在成本不变的情况下,与现有工艺相比,新的工艺方案处理1 t蒸硒渣可增加2 000元的经济效益。

