糖尿病对心房颤动合并冠状动脉支架植入后患者预后的影响
李小龙,李田昌
心房颤动(房颤)是临床上最为常见的快速型心律失常,常与冠状动脉粥样硬化性心脏病(冠心病)合并存在。全球注册研究GARFIELD研究中国亚组分析数据显示,我国32.4%的房颤患者合并冠心病[1];约5%~10%房颤患者因冠心病需接受经皮冠状动脉介入治疗(PCI)[2]。与此同时,糖尿病是冠心病的独立危险因素,80%的糖尿病患者死于动脉粥样硬化性疾病[3],糖尿病患者中房颤的患病率逐年增加,血糖异常是诸多房颤危险因素中最重要的一个。与非糖尿病患者相比,糖尿病患者发生房颤风险增加40%[4];本研究旨在分析糖尿病对房颤合并冠状动脉(冠脉)支架植入后患者预后的影响,为临床预防和治疗奠定基础。
1 资料与方法
1.1 研究对象本文为多中心回顾性研究,选取北京市辖区内的中国医学科学院阜外心血管病医院,首都医科大学附属北京安贞医院,首都医科大学附属北京同仁医院,首都医科大学附属北京宣武医院,首都医科大学附属北京友谊医院,中国人民解放军总医院第一医学中心,中国人民解放军第六医学中心等共12家具有PCI资质且年收治急性冠脉综合征(ACS)患者100例以上的医院。
1.2 纳入标准①于2010年1月至2015年1月入院;②入院时接受PCI;③出院诊断为急性冠脉综合征合并房颤。
1.3 排除标准瓣膜性房颤、先天性心脏病、心肌病、严重肾功能不全(肌酐清除率<30 ml/min)、恶性肿瘤、外周动脉支架植入、自身免疫性疾病。
1.4 研究方法收集符合入选标准的患者2206例,排除失访患者,实际纳入患者1975例,根据是否合并糖尿病,分为糖尿病组(610例)及非糖尿病组(1365例),通过检索电子病历库收集患者的一般资料,包括基本信息、既往史及家族史、临床检验检查指标等。采用电话或门诊方式对患者进行定期随访,随访日期截止至2016年3月,平均随访时间(3.33±1.46)年。记录不良事件的发生情况,包括:①缺血性脑卒中发生情况;②主要不良心血管事件(MACE):全因死亡、非致死性心肌梗死和靶血管重建(溶栓、PCI、冠状动脉旁路移植);③出血事件:根据2011年欧洲出血学术研究会(BARC)制定的标准[5]:0型为无出血;1型为无需立即干预的出血;2型为需临床干预的出血,符合下列中至少1项:①需内科非手术干预;②需住院或提升治疗级别;③需要重新评估;3型为血红蛋白下降30~50 g/L或颅内出血;4型为冠脉旁路移植术相关出血;5型为致死性出血。治疗措施:患者入院时和出院时均常规使用阿司匹林等抗血小板,华法林抗凝,阿托伐他汀/瑞舒伐他汀调脂、β受体阻滞剂、血管紧张素转化酶抑制剂/血管紧张素受体拮抗剂(ACEI/ARB)及胰岛素等药物治疗。
1.5 统计学方法采用SPSS 22.0统计软件进行统计学分析,计量资料结果以均数±标准差(±s)表示,采用t检验;计数资料采用例数(百分比)表示,组间比较采用χ2检验。绘制不同终点事件Kaplan-Meier生存曲线,并采用Log-rank法进行检验;以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较糖尿病组年龄、体质指数(BMI)、收缩压、血尿素氮、CRUSADE评分、CHA2DS2-VASc评分、HAS-BLED评分高于非糖尿病组,糖尿病组肌酐清除率低于非糖尿病组,差异有统计学意义(P<0.05)。两组舒张压、血红蛋白、血白细胞、血小板、血肌酐、血尿酸、左室射血分数比较,差异无统计学意义(P>0.05)。糖尿病组PCI史、卒中史、高血压史、肾功能不全史比例高于非糖尿病组,两组ACS类型比较,差异有统计学意义(P<0.05)。两组性别、吸烟史、心功能不全史、房颤类型比较,差异无统计学意义(P>0.05)(表1)。
2.2 两组缺血性脑卒中发生率比较糖尿病组共纳入610例,缺血性脑卒中发生43例,发生率7.0%,平均缺血性脑卒中发病时间为(37.6±19.1)月。非糖尿病组共纳入1365例,缺血性脑卒中发生65例,发生率4.8%,平均缺血性脑卒中发病时间为(37.5±17.8)月。以缺血性脑卒中为终点事件绘制Kaplan-Meier生存曲线,并用Log-rank法进行检验,两组差异有统计学意义(χ2=3.982,P=0.046,图1)。
表1 两组一般资料比较(±s)

表1 两组一般资料比较(±s)
注:BMI:体质指数;SCr:血肌酐;BUN:血尿素;SUA:血尿酸;CCr:肌酐清除率;LVEF:左室射血分数;PCI:经皮冠状动脉介入治疗;ACS:急性冠脉综合征;UA:不稳定型心绞痛;STEMI:急性ST段抬高型心肌梗死;NSTEMI:急性非ST段抬高型心肌梗死;AF:心房颤动
项目 非糖尿病组(n=1365)糖尿病组(n=610)t/χ2值 P值年龄(岁) 66.1±9.7 67.2±9.4 -2.326 0.021 BMI(kg/m2) 25.8±3.4 26.4±3.4 -3.285 0.001收缩压(mmHg) 127.5±18.9 131.9±19.4 -4.766 <0.001舒张压(mmHg) 76.6±11.9 76.3±11.1 0.730 0.691血红蛋白(g/L) 137.6±17.5 135.2±17.6 2.803 0.005血白蛋白(×109/L) 7.3±2.5 7.4±2.5 -0.917 0.359血小板(×109/L) 197.6±71.5 191.4±54.1 1.913 0.056 SCr(μmol/L) 84.5±26.8 85.8±30.3 0.942 0.347 BUN(mmol/L) 6.1±2.1 6.7±2.8 -4.522 <0.001 SUA(μmol/L) 355.1±101.1 345.1±101.3 1.995 0.046 CCr(ml/min) 82.5±23.5 70.5±26.4 -11.234 <0.001 LVEF(%) 59.2±9.8 59.4±10.4 0.272 0.785 GRACE评分 121.1±30.9 120.9±31.1 0.093 0.926 CRUSADE评分 29.1±12.9 36.4±13.5 -11.596 <0.001 CHA2DS2-VASc评分 2.6±1.5 4.1±1.6 -18.621 <0.001 HAS-BLED评分 1.7±0.9 1.9±0.8 -4.581 <0.001男性(n,%) 999(73.2) 421(69.0) 3.629 0.057吸烟史(n,%) 634(46.4) 256(42.0) 3.417 0.065 PCI史(n,%) 226(16.6) 136(22.3) 9.274 0.002卒中史(n,%) 186(13.6) 113(18.5) 7.873 0.005高血压史(n,%) 983(72.0) 511(83.8) 31.626 <0.001心功能不全(n,%) 302(22.1) 149(24.4) 1.268 0.260肾功能不全(n,%) 39(2.9) 45(7.4) 21.150 <0.001 ACS类型 10.575 0.005 UA(n,%) 985(72.2) 475(77.9)NSTEMI(n,%) 141(10.3) 63(10.3)STEMI(n,%) 239(17.5) 72(11.8)AF类型 2.080 0.353阵发性AF(n,%) 1091(79.9) 487(79.8)持续性AF(n,%) 238(17.4) 100(16.4)永久性AF(n,%) 36(2.6) 23(3.8)
2.3 两组MACE发生率比较糖尿病组MACE发生155例,发生率25.4%,平均MACE发病时间为(36.1±19.0)月。非糖尿病组MACE发生280例,发生率20.5%,平均MACE发病时间为(35.7±18.3)月。以MACE为终点事件绘制Kaplan-Meier生存曲线,并用Log-rank 法进行检验,两组差异有统计学意义(χ2=3.994,P=0.046,图2);进一步比较两组全因死亡率,糖尿病组死亡89例,全因死亡率14.5%,非糖尿病组死亡138例,全因死亡率10.1%,以死亡为终点事件绘制Kaplan-Meier生存曲线,并用Log-rank法进行检验,两组差异有统计学意义(χ2=7.327,P=0.007,图3)。
2.4 两组出血事件发生率比较糖尿病组出血事件发生45例,发生率7.3%,平均出血事件发病时间为(37.4±18.9)月。非糖尿病组出血事件发生122例,发生率8.9%,平均出血事件发病时间为(37.0±18.1)月。以出血事件为终点事件绘制Kaplan-Meier生存曲线,并用Log-rank法进行检验,两组差异无统计学意义(χ2=1.221,P=0.269,图4)。
3 讨论

图1 两组缺血性脑卒中事件Kaplan-Meier生存曲线
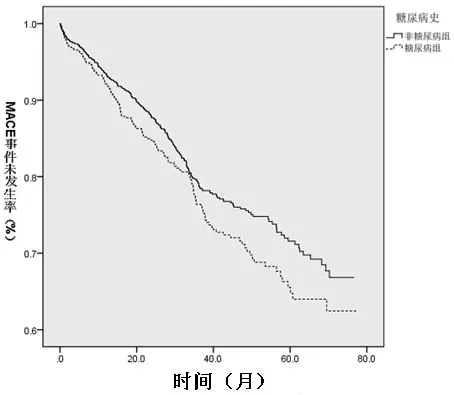
图2 两组MACE事件Kaplan-Meier生存曲线

图3 两组全因死亡事件Kaplan-Meier生存曲线

图4 两组出血事件Kaplan-Meier生存曲线
糖尿病作为冠心病及房颤发病的共同危险因素,临床工作中糖尿病、房颤、PCI后三种疾病并存患者并不少见,但国内关于糖尿病对房颤合并PCI后患者血栓事件及出血事件影响的研究较少,本研究旨在分析糖尿病对房颤合并PCI后患者缺血性卒中、MACE事件及出血事件影响。分析比较两组数据发现,糖尿病组缺血性脑卒中发生率7.0%,高于非糖尿病组4.8%,两组Kaplan-Meier生存曲线差异有统计学意义;合并糖尿病的房颤伴PCI后患者存在更高的血栓事件风险,提示糖尿病可以作为缺血性脑卒中发病的预测因子。欧洲心脏学年会上公布的RE-LY研究结果表明:与非糖尿病人群相比,合并糖尿病的房颤患者出血事件及缺血性脑卒中发生率均增高[6]。ASCEND研究同样发现合并糖尿病的房颤患者血栓栓塞事件发生率增加[7]。本研究糖尿病对血栓栓塞事件影响与RE-LY研究、ASCEND研究结果相似;糖尿病患者比非糖尿病患者脑卒中风险增加2倍[8]。血栓栓塞性并发症是房颤致死致残的主要原因,而缺血性脑卒中是最为常见的表现类型[9,10]。ESC房颤血栓危险度评分(CHADS2VASC)将女性、年龄>75岁、高血压、心力衰竭、糖尿病、卒中病史、血管性疾病史等纳入评分指标,推荐CHA2DS2-VASc评分≥2分患者应用口服抗凝药预防血栓栓赛事件[11-13]。我国抗凝治疗率明显低于全球数据(28.2%vs. 59%)[1]。基于本研究及国际相关研究结论,临床工作中合并糖尿病的房颤伴PCI后患者需重点关注缺血性脑卒中的预防,对于缺血性脑卒中高危患者积极应用抗凝治疗。
糖尿病是不良心血管事件独立预测因子,本研究中糖尿病组患者MACE事件及病死率高于非糖尿病组,差异有统计学意义。糖尿病是冠心病的危险因素,血糖监测与管理对于心血管事件的一级、二级预防尤为重要。既往研究表明糖尿病患者严格的血糖管理可以降低MACE事件发生率[14];血糖异常是否增加房颤合并PCI后患者出血风险目前尚无统一认识,房颤患者出血风险HAS-BLED评分标准不包括糖尿病史,急性冠脉综合征患者发生出血风险CRUSADE评分[15]将糖尿病史等纳入评分标准。本研究发现糖尿病组出血事件发生率7.3%,非糖尿病组出血事件发生率8.9%,两组Kaplan-Meier生存曲线差异无统计学意义,提示糖尿病不增加房颤合并PCI后患者出血事件风险,与RE-DUAL PCI研究糖尿病亚组分析结果一致[16]。
糖尿病患者脑卒中风险及病死率增加机制与损伤血管内皮相关;长期高糖刺激可通过多种途径损伤血管内皮细胞:①高血糖可激活细胞因子NFκb,进而促进单核细胞粘附血管内皮细胞[17,18];②糖基化终末产物可通过抑制内皮舒张因子(NO)产生损伤血管内皮[19];③高血糖及糖基化终末产物共同刺激下,内皮细胞通过NADPH氧化酶过度激活途径产生大量过氧化物导致氧化应激反应[20]。
综上,糖尿病可增加房颤合并PCI后患者缺血性脑卒中风险及病死率,加强糖尿病患者的治疗与管理对改善房颤合并PCI后患者预后有积极意义,血糖达标同时应重视生活方式、血压、血脂等危险因素的管理。糖尿病不增加房颤合并PCI后患者出血事件风险,糖尿病合并卒中高危的房颤患者不应顾虑出血风险而限制抗凝药物使用。

