陈皮苷钙、镁配合物的制备及其抗氧化作用研究
陈晓丹,王亮,黄文文
(1.盘锦职业技术学院,辽宁盘锦 124000;2.盘锦辽河口生态经济区,辽宁盘锦 124000;3.自然资源部第三海洋研究所,福建厦门 361005)
陈皮为芸香科植物橘(Citrus reticulata Blanco)及其栽培变种的干燥成熟果皮,主要含有挥发油、黄酮类化合物、生物碱和肌醇等成分[1-2],是我国传统的中草药之一,具有行气健脾和胃止呕燥湿化痰等功效。
羟基自由基是已知的最强氧化剂,几乎和所有的细胞成分发生反应,对机体危害极大,已证实与衰老、肿瘤、辐射损伤和细胞吞噬等有关。研究表明,类黄酮糖苷金属配合物形成后,其清除超氧阴离子的活性得到提高[3-4]。例如,芦丁、斛皮素和叶绿素与铜形成的配合物具有类似超氧化物歧化酶(SOD)的活性,比配体有更好的超氧阴离子清除活性;陈皮苷在与铜配合后,对维生素C缺乏和炎性水肿等疾病有更好的疗效。本文采用钙、镁离子制备陈皮苷金属配合物,并探究其抗氧化能力。
1 材料与方法
1.1 药品试剂
陈皮苷为自然资源部第三海洋研究所自制;水杨酸,湖北鑫润德化工有限公司;硫酸亚铁,西安锦源生物科技有限公司;乙醇、盐酸、柠檬酸、N-N-2-甲基甲酰胺(DMF)、碘化钾、硫代硫酸钠、氯化镁、氯化钙,成都市科隆化学品有限公司;双氧水,北京翰隆达科技发展有限公司;三羟甲基氨基甲烷(tris)南京化学试剂股份有限公司;邻苯三酚,武汉远成共创科技有限公司;磷酸,武汉卡诺斯科技有限公司。以上试剂均为分析纯。
1.2 仪器
UV-1800型紫外可见分光光度计,上海第三分析仪器厂;FA1140电子天平,上海天平仪器厂;电热恒温水浴槽,上海医疗器械三厂生产;80.2型低速台式离心机,江苏省金坛市医疗仪器厂;sy-1000超声波仪,上海宁商超声仪器有限公司。
1.3 试验方法
1.3.1 陈皮苷金属配合物的制备
配位能力的确证实验:分别配制40 mg/mL的陈皮苷与40 mg/mL氯化镁的二甲基甲酰胺(DMF)溶液(先用25 ℃水浴加热,再超声30 min,使物质充分溶解),将陈皮苷溶液以5 mL/次的速度加入10 mL氯化镁溶液中,并利用自动电位滴定仪测每次加入后的电导率与pH值,根据以上数据做出陈皮苷与镁的络合图,从而推测出两者的配位比。陈皮苷与氯化钙的配比能力测定也参考以上步骤。陈皮苷-MgCl2与陈皮苷-CaCl2的制备:根据文献[5-6],按照以上的配位比,配制20 mg/mL的陈皮苷-MgCl2与陈皮苷-CaCl2溶液,并用DMF将溶液分别稀释至1 mg/mL、10 mg/mL 和 20 mg/mL 3 个浓度梯度备用。
1.3.2 水杨酸法测定羟自由基清除能力
在试管中加入 9 mmol/L FeSO41 mL、9 mmol/L水杨酸-乙醇1 mL和待测溶液1 mL,再加入8.8 mmol/L H2O21 mL。37 ℃反应 0.5 h 后,12 000 r/min 离心 6 min,然后以DMF作参比,在510 nm下测定吸光度。以9 mmol/L FeSO41 mL、9 mmol/L 水杨酸 - 乙醇 1 mL、待测溶液1 mL和双蒸水1 mL作为待测溶液的本底吸收值。以DMF代替各个浓度的待测液,作为空白对照液的吸光值。
清除率计算公式如式1所示。

其中,A0为空白对照液的吸光度,AX为加入待测溶液后的吸光度,AX0为待测溶液的本底吸收值。每一吸光值平行测3次,取其平均值。
1.3.3 邻苯三酚自氧化法测定超氧自由基清除能力
根据文献[7-8],在试管中加入50 mmol/L的Tris-HCl缓冲液(pH 8.2)2.8 mL,待测液 0.1 mL,于 25 ℃保温 10 min,然后加入 25 ℃预温的 60 mmol/L 邻苯三酚 0.1 mL,总体积 3.0 mL,迅速摇匀,倒入 1 cm 比色皿中,在420 nm处每隔0.5 min测一次吸光值。以0.1 mL 10 mmol/L的盐酸代替邻苯三酚作为待测溶液的本底吸收值,以DMF代替各个浓度的待测液,作为空白对照液的吸光值。
对O2-·的相对清除率可用公式2计算。

其中,B0为空白对照液的吸光度随时间变化曲线的斜率值,BX为样品吸收值,BX0为待测溶液的本底吸收值,BX-BX0为加入待测溶液后的吸光度(除去本底吸收值)随时间变化曲线的斜率值。每一吸光值平行测3次,取其平均值。
1.3.4 碘量法测定过氧化氢清除率
取pH值3.0的0.1 mol/L柠檬酸缓冲液5 mL、待测溶液0.5 mL于容量瓶中,定溶至25 mL,加入0.1 mol/L 过氧化氢(随用随配)1 mL,置于 37 ℃恒温水浴中保持 20 min,取出,加入 10% KI溶液 2 mL、2 mol/L H3PO41 mL,暗处反应 120 min,用 0.002 mol/L Na2S2O3溶液滴定。以DMF为空白,按照公式3计算过氧化氢清除率。

式中,V0表示空白所消耗Na2S2O3的体积,V1表示添加样品后消耗Na2S2O3的体积。
2 结果与分析
2.1 陈皮苷-MgCl2的制备
陈皮苷添加量对MgCl2电导率和pH的影响见表1。由表1可知,混合体系电导率随陈皮苷溶液体积的增加而降低,同时pH值递增,说明生成配合物在DMF中的电迁徙率小于相应阳离子,即可推知配合物金属与配体的摩尔比可能是1∶2左右,以下实验中待测液按此配位比例配制。

表1 陈皮苷添加量对MgCl2电导率和pH的影响
2.2 陈皮苷-CaCl2的制备
陈皮苷添加量对CaCl2电导率和pH的影响见表2。由表2推知配合物金属与配体
的摩尔比可能是1∶2左右,以下实验中待测液按此配位比例配制。

表2 陈皮苷添加量对CaCl2电导率和pH的影响
2.3 羟自由基清除能力
实验表明,陈皮苷-MgCl2在1~20 mg/mL的浓度范围内,对羟自由基清除能力较弱;而陈皮苷-CaCl2具有较强的羟自由基清除能力,在20 mg/mL时,其羟自由基清除率为4.71%。
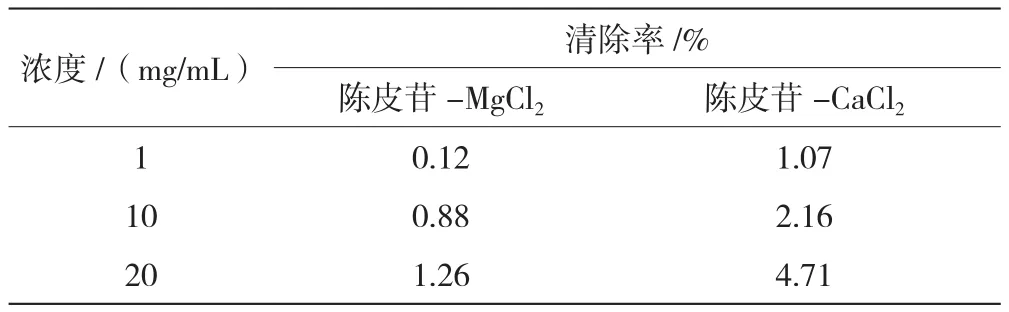
表3 不同浓度的陈皮苷Mg、Ca配合物羟自由基相对清除率
2.4 超氧自由基清除能力
陈皮苷Mg、Ca配合物超氧自由基相对清除率见表4。由表4可知,陈皮苷-MgCl2在1 mg/mL浓度下,与陈皮苷-CaCl2的超氧自由基相对清除率相当;随着浓度的增大,两种配合物清除超氧自由基的能力都增大;在20 mg/mL时,陈皮苷Mg、Ca配合物超氧自由基相对清除率分别达到15.89%和25.6%。

表4 不同浓度的陈皮苷Mg、Ca配合物超氧自由基相对清除率
2.5 过氧化氢清除实验
陈皮苷-MgCl2、陈皮苷-CaCl2清除过氧化氢的能力均较弱,其中陈皮苷-CaCl2浓度为20 mg/mL时,其过氧化氢相对清除率为3.89%。。

表5 不同浓度的陈皮苷Mg、Ca配合物过氧化氢相对清除率
3 结论与讨论
研究表明,陈皮苷Mg、Ca配合物的抗氧化能力大小为陈皮苷-CaCl2>陈皮苷-MgCl2,但其抗氧化能力仍低于陈皮苷-CuCl2[9-10],导致这种差异的原因可能在于陈皮苷可通过羰基和邻羟基与Cu(Ⅱ)形成2∶1配合物,配合物的相对稳定常数lgK为8.05,配位过程中有H+释放,在Cu(Ⅱ)催化氢过氧化物分解成自由基的反应体系中,加入陈皮苷,Cu(Ⅱ)被络合,抑制过氧化物分解,从而起到抗氧化作用,而制备的陈皮苷-MgCl2、陈皮苷-CaCl2形成的配合物可能相对不稳定,易解离,从而影响其抗氧化效果。因此,陈皮苷在形成金属配合物后的抗氧化性能的提高可能与金属离子亲脂性强弱有关,也有可能说明陈皮苷在形成配合物后,其活性中心由羟基转移到金属离子上,而不稳定的陈皮苷-MgCl2、陈皮苷-CaCl2配合物容易解离,其抗氧效果受到影响,但此项结论需要进一步证明。

