急性颈内动脉起始部和颅内大血管串联闭塞的血管内治疗
尚彦国 孙涛 王轩 高恺明 佟小光
急性缺血性卒中发病率、病残率和病死率均较高,业已证实静脉溶栓是其有效治疗方法[1⁃2]。但对于急性颅内大血管闭塞,静脉溶栓的血管再通率较低、预后较差。2015 年公布的血管内治疗急性缺血性卒中的多中心随机临床试验(MR CLEAN)[3]、前循环近端闭塞小病灶性卒中的血管内治疗并强调最短化CT 扫描至再通时间临床试验(ESCAPE)[4]和延长急性神经功能缺损至动脉内溶栓时间的临床试验(EXTEND⁃IA)[5]均证实,血管内支架取栓术治疗颈内动脉(ICA)颅内段和大脑中动脉(MCA)主干急性闭塞有肯定疗效。但是关于颈内动脉系统串联闭塞,即颈内动脉起始部闭塞串联颅内段或大脑中动脉闭塞的治疗方案尚未达成共识。笔者1 年内采用颈内动脉起始部支架植入术联合颅内动脉支架取栓术治疗5 例急性颈内动脉起始部和颅内大血管串联闭塞患者,取得较满意疗效,总结报告如下,以为急性颈内动脉系统串联闭塞的治疗提供借鉴。
资料与方法
一、临床资料
1.纳入标准 (1)头部MRI 证实梗死灶位于大脑中动脉供血区且梗死灶范围≤大脑中动脉供血区的1/3。(2)头部MRA 检查证实颈内动脉全程不显影。(3)年龄≥18 岁。(4)发病至入院时间≤6 h。(5)脑卒中前改良Rankin 量表(mRS)评分<2 分。(6)入院时美国国立卫生研究院卒中量表(NIHSS)评分≥6 分。(7)所有患者及其家属均对手术方案和风险知情并签署知情同意书。
2.排除标准 (1)头部CT 显示颅内出血。(2)头部MRI 显示梗死灶范围>大脑中动脉供血区的1/3。(3)近2 周内有大型外科手术史。(4)近3 周内发生内脏出血或颅内出血。(5)合并严重心、肺、肝、肾功能障碍。(6)合并严重糖尿病或高血压。(7)妊娠期女性。
3.一般资料 选择2018 年8-11 月在天津市环湖医院神经外科行血管内治疗的急性颈内动脉起始部和颅内大血管串联闭塞患者共5 例,均为男性;年龄50 ~78 岁,平均64 岁;发病至入院时间4 ~6 h,平均5 h;均呈急性起病,临床表现为不同程度偏瘫、失语和凝视;入院时NIHSS 评分15 ~20 分,平均为17 分。MRI 显示,梗死灶位于大脑中动脉供血区且梗死灶范围<大脑中动脉供血区的1/3;MRA 显示,同侧颈内动脉和大脑中动脉不显影。
二、研究方法
1.血管内治疗 患者仰卧位,于局部麻醉下经股动脉穿刺行脑血管造影术和血管内治疗。脑血管造影显示,单侧颈内动脉起始部闭塞串联颅内段以远或大脑中动脉闭塞。(1)颈内动脉起始部支架植入术:将8F Vista Britetip 导引导管(美国Johnson& Johnson 公司)或8F Merci 球囊导引导管(美国Stryker Corporation 公司)置入颈总动脉(CCA)近分叉 部,Synchro⁃14 微导丝(300 cm,美 国Stryker Corporation 公司)辅 助Rebar⁃18微导管(美国Medtronic 公司)通过颈内动脉起始部到达海绵窦段,经微导管注射对比剂确认微导管头端置于动脉腔内,导入Synchro⁃14 微导丝,撤出Rebar⁃18 微导管,经微导丝导入Lite PAC 微球囊(2 mm×20 mm,美国Bard 公司)扩张颈内动脉起始部,撤出微球囊,经微导丝导入Spider FX 保护伞(5 mm,美国Medtronic 公司)至颈内动脉岩骨段,撤出微导丝,经保护伞挺丝导入Lite PAC 球囊(4 mm×30 mm,美国Bard 公司)扩张颈内动脉起始部,撤出Lite PAC 球囊时需经导引导管负压抽吸,如果使用球囊导引导管,可临时充盈球囊阻断血流,经保护伞挺丝植入Protege 支架(8 mm×30 mm,美国Medtronic 公司)并释放于颈内动脉起始部,再经导引导管负压抽吸后回收保护伞,经导引导管注射对比剂确认颈内动脉起始部通畅。(2)颈内动脉颅内段和大脑中动脉支架取栓术:将6F Navien 中间导管(美国Medtronic 公司)置入颈内动脉海绵窦段,导入Synchro⁃14 微导丝(200 cm,美国Stryker Corporation 公司)和Rebar⁃18微导管通过颈内动脉颅内段和大脑中动脉闭塞处,经微导管注射对比剂确认微导管头端置于动脉腔内,置入Solitaire FR支架(4 mm × 20 mm,美 国Medtronic 公司)至颅内血管闭塞处,经Navien 中间导管负压抽吸,撤出Solitaire FR 支架和Rebar⁃18 微导管取栓,再次经Navien 中间导管抽吸以抽吸出残留血栓,撤出Navien 中间导管,经导引导管注射对比剂确认颈内动脉起始部、颈段、海绵窦段、颅内段和大脑中动脉均通畅,观察20 min,再次确认各动脉保持通畅,结束手术。(3)抗凝和抗血小板治疗:本组患者均超出静脉溶栓治疗时间窗,术前未予rt⁃PA静脉溶栓。脑血管造影即刻即予全身肝素化抗凝,静脉注射普通肝素4000 U,1 h 后追加2000 U,此后追加1000 U/h。血管内治疗开始时,先经导引导管注射替罗非班负荷剂量(0.50 mg),再静脉滴注(0.50 mg/h)抗血小板治疗,术后24 h 停用替罗非班,改为阿司匹林(100 mg/d)和氯吡格雷(75 mg/d)口服双联抗血小板治疗,持续至术后1 年。
2.围手术期处理 患者术后常规返回重症监护病房密切监护,术后12 ~24 h 复查头部CT 观察有否颅内出血,术后3 d 内复查头部MRI 和MRA 观察梗死灶范围有无扩大和颅内动脉恢复情况。如果患者恢复良好,术后4 d 即可出院;若仍遗留明显的神经功能缺损,术后3 d 转入神经内科继续治疗,2 周急性期后行康复治疗。
3.观察指标 记录颈内动脉起始部支架植入术和颅内动脉支架取栓术的成功率,以及手术并发症。术后即刻采用脑梗死溶栓血流分级(TICI)评价血管再通程度,TICI 分级2b ~3 级为血管完全再通,2a 级为血管部分再通,0 ~1 级为血管再通不良。分别于术后3 d、90 d 和1 年采用mRS 量表评价预后,mRS 评分≤2 分为预后良好,>2 分为预后不良。术后90 d 和1 年门诊复查颈部血管超声和主动脉弓至颅内血管CTA 观察动脉是否通畅。
结果
本组5 例患者入院至股动脉穿刺时间1.00 ~1.50 h,手术时间2 ~4 h;术中脑血管造影显示,左侧颈内动脉起始部闭塞及其颅内段和大脑中动脉不显影4 例、右侧1 例,对侧颈内动脉和双侧椎动脉均血流通畅,前交通动脉和后交通动脉未代偿。5 例患者均顺利完成颈内动脉起始部支架植入术以及颈内动脉颅内段和大脑中动脉支架取栓术,手术成功率为5/5,均未发生对比剂外溢和支架内血栓形成等手术并发症。术后即刻颅内血管TICI 分级为3 级2 例、2b 级2 例、2a 级1 例,血管再通率4/5。术后1 d神经功能均明显改善。术后3 d 有2 例仅遗留轻微失语或肌力减弱,mRS 评分为1 分,术后4 d 出院;有3 例仍遗留明显偏瘫和失语,但较术前明显改善,mRS 评分为3 分,遂转入神经内科继续治疗。术后90 d 随访时复查颈部血管超声,显示各动脉血流通畅;mRS 评分0 分2 例,2 分2 例,3 分1 例。术后1 年门诊复查颈部血管超声和主动脉弓至颅内血管CTA,显示各动脉血流通畅;均未再发生缺血性卒中,能够生活自理,mRS 评分0 分2 例、1 分3 例。
典型病例
患者 男性,69 岁,主因突发意识障碍伴右侧肢体活动不利4 小时,于2018 年9 月8 日急诊入院。急诊查体:呈昏睡状态,双侧瞳孔等大、等圆,直径约3 mm,对光反射灵敏,刺激睁眼,可发声但不能应答;刺激后左侧肢体可遵嘱活动,肌力4 级、肌张力正常,右侧肢体瘫痪,上肢肌力0 级、下肢2 级,肌张力降低;NIHSS 评分16 分。急诊行头部CT 检查排除颅内出血。MRI 显示,左大脑中动脉供血区小片状梗死灶(图1a ~1d)。MRA 显示,左颈内动脉和大脑中动脉不显影(图1e,1f)。临床诊断为左侧额叶急性缺血性卒中,左颈内动脉和大脑中动脉闭塞。遂急诊行局部麻醉下脑血管造影术,可见左颈内动脉起始部闭塞,左颈内动脉颅内段和大脑中动脉不显影,前交通动脉和后交通动脉代偿不明显(图1g,1h)。经征得患者家属同意后,同步行血管内治疗,先于颈内动脉起始部Protege 支架植入术,再顺行颈内动脉颅内段和大脑中动脉Solitaire FR支架取栓术,手术顺利。术中实时复查DSA 可见颈内动脉全程以及颈内动脉颅内段和大脑中动脉血流通畅(图1i,1j)。术后即刻TICI 分级为3 级。术后转入重症监护病房,12 小时后患者清醒,右侧肢体肌力恢复至4 级、左侧5 级。术后12 小时复查头部CT 未见颅内出血,术后36 小时复查MRI 显示梗死灶范围无扩大(图1k ~1n),复查MRA 显示颈内动脉颅内段和大脑中动脉显影良好(图1o,1p)。患者共住院4 天,出院时神志清楚,言语稍笨拙,四肢活动自如,可独立行走,NIHSS 评分为2 分,mRS 评分为1 分。术后3 个月随访时,mRS 评分0 分,复查颈部血管超声显示各动脉血流通畅;术后1 年随访时,mRS 评分0 分,复查颈部血管超声和主动脉弓至颅内血管CTA 显示各动脉血流通畅。
讨论
关于急性缺血性卒中的治疗,国内外已有成熟完备的系统性指南[6⁃7],其中颅内大血管闭塞致急性缺血性卒中行支架取栓术已得到充分肯定,但颈内动脉系统串联闭塞的处理尚未达成一致性意见。国内外学者均在利用现有技术探索串联闭塞的治疗方案,各项研究虽具体方法不同,但均报道了手术方法的安全性和有效性。
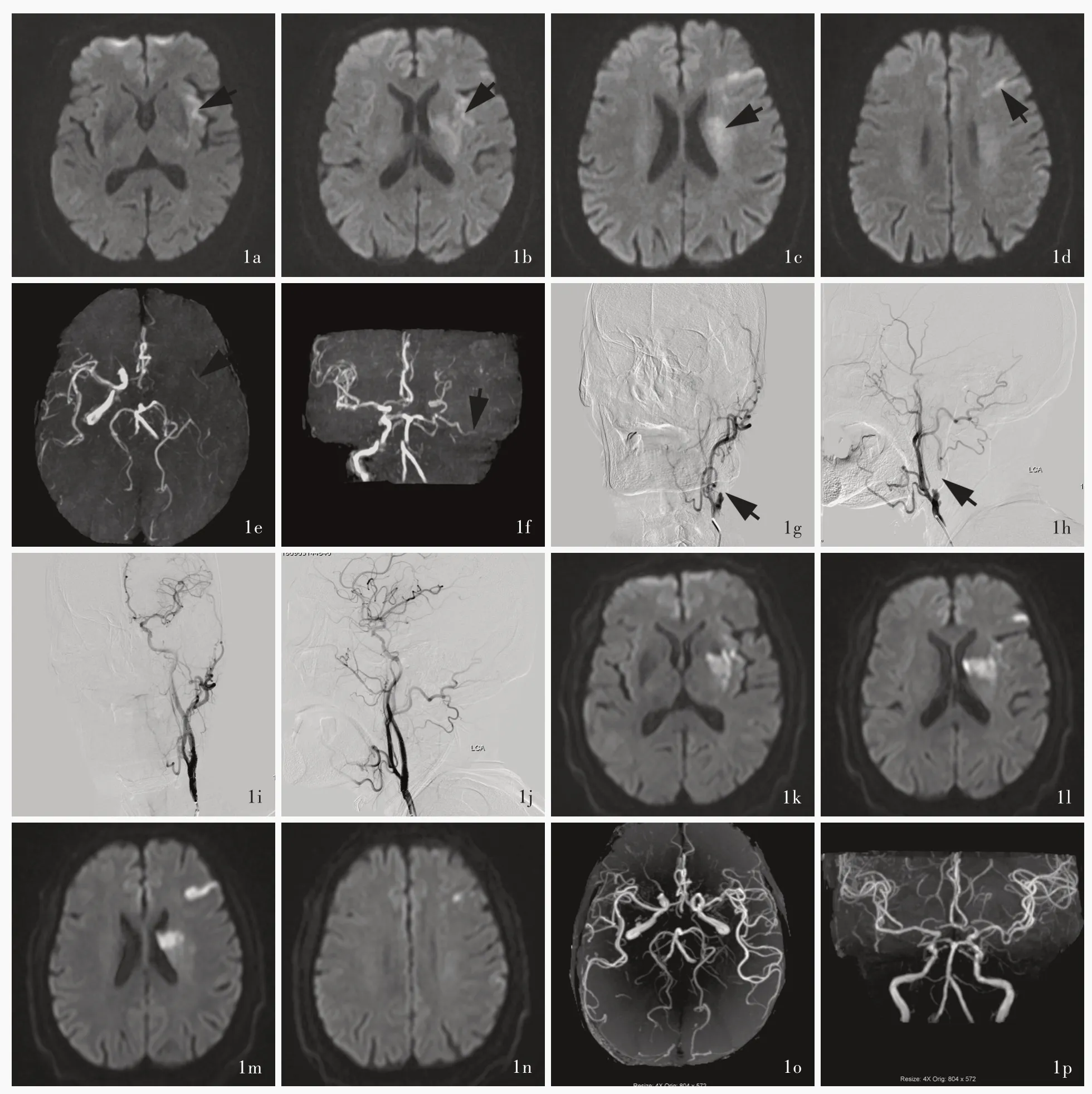
图1 手术前后头部影像学检查所见 1a ~1d 术前横断面DWI 显示左侧基底节区、侧脑室旁、岛叶和颞叶梗死灶(箭头所示)1e,1f 术前MRA 显示左颈内动脉颅内段和大脑中动脉不显影(箭头所示) 1g,1h 术中实时正位和侧位DSA 显示左颈内动脉起始部闭塞(箭头所示),颈内动脉颅内段和大脑中动脉不显影 1i,1j 经颈内动脉起始部支架植入术和颅内动脉支架取栓术后,实时DSA 显示左颈内动脉起始部、颅内段和大脑中动脉显影良好 1k ~1n 术后36 h 横断面DWI 显示梗死灶范围无扩大,未见颅内出血 1o,1p 术后MRA 显示左颈内动脉颅内段和大脑中动脉显影良好Figure 1 Pre⁃ and post⁃operative head imaging findings Preoperative axial DWI showed cerebral infarction at left basal ganglia,lateral ventricle, insular lobe and temporal lobe (arrows indicate, Panel 1a-1d). Preoperative MRA showed lack of left ICA and left MCA (arrows indicate; Panel 1e, 1f). Intraoperative anteroposterior (Panel 1g) and lateral (Panel 1h) DSA showed occlusion of left proximal through intracranial ICA and MCA (arrows indicate). Intraoperative DSA showed recanalization of proximal through intracranial ICA and MCA after proximal ICA stenting and intracranial stent thromboectomy (Panel 1i, 1j). Postoperative axial DWI showed no increase of cerebral infarction and no cerebral hemorrhage (Panel 1k-1n). Postoperative MRA showed totally recanalization of ICA and MCA (Panel 1o, 1p).
目前,针对颈内动脉起始部、颅内段和大脑中动脉串联闭塞的治疗常涉及顺行开通血管和逆行开通血管的优劣问题,顺行开通即先行颈内动脉起始部支架植入术,待起始部再通后再行颅内动脉支架取栓术;逆行开通即球囊扩张颈内动脉起始部使其再通后,先行颅内动脉支架取栓术,待颅内动脉血流通畅后再行颈内动脉起始部支架植入术或内膜剥脱术;两种手术方式均安全、有效[8⁃11]。顺行开通的原理是优先开通颈内动脉起始部以获得正向血流,因此,先行颈内动脉起始部支架植入术可以保证充足的正向血流,此时若仅合并大脑中动脉闭塞,正向血流可通过大脑前动脉皮质吻合支向大脑中动脉区域代偿供血,从而为颅内血管再通争取时间,同时颈内动脉起始部植入支架后可以减少粥样硬化斑块和血栓脱落顺行流入颅内血管的风险。然而,支持逆行开通的学者聚焦于,如果先在颈内动脉起始部植入支架,则中间导管通过颈内动脉起始部进入颈段和海绵窦段困难,且颅内动脉回收支架取栓时,取栓支架可能与颈内动脉起始部支架缠绕在一起[12]。逆行开通先行颅内动脉支架取栓术,可更早实现颅内血管再通,避免颈内动脉起始部支架植入术造成的颅内血管再通延误,也避免顺行开通造成的上述困难。然而在临床实践中,若前交通动脉或后交通动脉代偿良好,优先开通颅内血管可以较好地改善局部脑灌注;若前交通动脉和后交通动脉代偿不良,即使优先开通颅内血管,也无法获得充足的正向血流,而颈内动脉起始部仅予球囊扩张便行颅内动脉支架取栓术,可能导致颈内动脉起始部和颈段形成血栓,继发栓子脱落和颅内栓塞。
本组有4 例患者顺行开通血管,即先行颈内动脉起始部支架植入术,再行颈内动脉颅内段和大脑中动脉支架取栓术,手术顺利,成功血管再通。颈内动脉起始部植入支架后,置入中间导管确有一定困难,但解决并不难,通过转动导引导管改变其开口方向可以使中间导管通过颈内动脉起始部的支架进入颈段至海绵窦段,且行颅内动脉支架取栓术时未发生两种支架缠绕的问题,因此笔者认为,只要术中操作得当,上述问题可以避免。余1 例患者行颈内动脉起始部球囊扩张术开通颈内动脉颅外段后,可见大脑中动脉和大脑前动脉均闭塞,遂先行颅内动脉支架取栓术,颅内血管开通后近端形成血栓并脱落,堵塞颅内血管,遂再次先行颈内动脉起始部支架植入术、再行颅内动脉支架取栓术,延误手术时间。因此笔者更倾向于顺行开通血管。
逆行开通血管还可以先行颅内动脉支架取栓术,再行颈内动脉起始部内膜剥脱术[13]。通常认为,颈内动脉起始部支架植入术后常规予以抗血小板治疗可增加颅内出血风险,而颈内动脉起始部内膜剥脱术则可减少此类风险[13]。然而亦有学者认为,既然颅内动脉支架取栓术是微侵袭手术,那颈内动脉起始部也应采取微侵袭手术,即支架植入术,而内膜剥脱术则会面临手术创伤、神经功能障碍、动脉内急性血栓形成或颅内出血等诸多风险。因此笔者认为,颈内动脉系统串联闭塞是危急且复杂的情况,患者面临诸多不确定性和风险,不宜采取创伤较大的手术。本组5 例患者均行颈内动脉起始部支架植入术和抗凝、抗血小板治疗,均未发生颅内出血。颅内大血管再通后颅内出血与多种因素有关,包括术前已形成的梗死灶范围、颅内动脉支架取栓术中操作、术后血压控制等。
关于颈内动脉起始部支架植入术,有的术者倾向先植入支架、再球囊扩张,但笔者认为不妥,先植入支架再扩张球囊,可导致支架的金属丝切割颈内动脉内壁和斑块,增加斑块破裂脱落和局部血栓形成的危险。本组5 例患者均先扩张球囊再植入支架,均未发生支架内血栓形成。因此笔者建议,先以足够大的球囊扩张颈内动脉起始部,再植入支架,即可使颈内动脉起始部管径基本恢复正常,无需后扩张,亦无继发血栓事件。
颈内动脉系统串联闭塞的原因较多,本组5 例患者均考虑为大动脉粥样硬化所致,均行颈内动脉起始部支架植入术和颅内动脉支架取栓术、抗凝和抗血小板治疗,以及全面的内科治疗、康复治疗和脑卒中二级预防,神经功能逐渐恢复,预后良好,术后1 年未再发生缺血性卒中。
颈内动脉起始部闭塞串联颈内动脉颅内段或大脑中动脉闭塞致急性缺血性卒中患者,急诊行颈内动脉起始部支架植入术并顺行颅内动脉支架取栓术安全、有效。
利益冲突 无

