两种不同皮瓣游离方法在腔镜甲状腺手术中的疗效比较
吴卫文,甄杰生,袁超杰,程 健
台山市人民医院普通外科,广东台山 529200
近年来甲状腺结节的发病率不断升高,国内的发病率约20.6%[1],其中年轻患者比例也在逐年增大。随着患者对美容的不断追求,腔镜甲状腺得到蓬勃的发展。现已出现十余种不同的腔镜甲状腺手术入路,如颈部、全乳晕、胸乳、腋窝、锁骨下、耳后、口腔等,其中全乳晕入路应用最为广泛[2]。但不管何种方式均需要行皮瓣的游离。本研究通过比较使用腔镜剪刀+超声刀及单纯使用超声刀进行皮瓣游离的效果及术后情况,以期探讨两者在腔镜甲状腺手术中的疗效及安全性的差异。
1 资料与方法
1.1 研究对象及分组
2017年1月—2018年12月在广东省台山市人民医院收治并进行腔镜甲状腺的手术患者。纳入标准:(1)具有手术指征的甲状腺疾病;(2)患者有行腔镜甲状腺切除的意愿。排除标准:合并严重基础疾病影响手术,严重凝血功能障碍,既往有颈部手术、放射史,术中病理为恶性需行颈部淋巴结清扫,瘢痕体质者。符合条件者共128例,患者随机分为腔镜剪刀+超声刀及单纯使用超声刀两组,主刀均为具有丰富腔镜手术经验的主任医师进行。均以全乳晕入路进行手术。其中腔镜剪刀+超声刀60例、单纯超声刀68例。各组间年龄、性别、手术范围均无统计学差异,见表1。
1.2 手术方法
患者肩下放置软垫取头后仰过伸位,术者站在患者两腿之间,显示器位于患者头侧,扶镜者位于患者右侧。将1 mg 肾上腺素加入500 mL 生理盐水配成膨胀液。分别于右侧乳晕3 点钟边缘、左侧乳晕10 点钟边缘做一长约1 cm 弧形切口,右侧乳晕9点钟边缘做一长约0.5 cm 弧形切口,游离进入深筋膜后方,使用50 mL注射器分别于切口内向上将膨胀液注入拟分离区及3个穿刺器隧道皮下,量约100~150 mL。用游离棒沿皮下深筋膜向上钝性分离以达充分游离皮下组织目的。游离完成后再用纱布卷自上而下挤出皮下多余膨胀液。分别置入两个10 mm 及一个5 mm 穿刺器于相应切口。注入CO2气体,压力维持在7 mmHg(1 mmHg=0.133 kPe)。在腔镜直视下使用腔镜剪刀剪开皮下组织,遇血管或出血点则使用超声刀予以凝断、止血,范围上达甲状软骨结节,两侧至胸锁乳突肌后外侧缘,至此完成皮瓣游离。手术完成后缝合白线,于甲状腺窝及颈部皮下各放置1 条14 号脑室引流管。而单纯使用超声刀组则完全使用超声刀进行皮瓣游离,游离范围及术后引流管放置情况同腔镜剪刀+超声刀组。术后48 h 后颈部引流管引流量如无明显异常则计量后予以拔除。
1.3 观察指标
观察记录各组分离皮瓣的耗时、气体用量、术中出血量、术后48 h 皮下引流量,术后随访1 个月,记录患者局部皮肤感觉异常情况。皮肤感觉异常为手术区域皮肤的针刺感、蚁走感[3-4]。
1.4 统计学分析
应用SPSS 23.0 进行数据统计。计量资料以±s表示,采用t检验;计数资料采用卡方检验,P<0.05为差异有统计学意义。
2 结果
共128例患者,其中腔镜剪刀+超声刀60例、单纯超声刀68例。各组间年龄、性别、手术范围均无统计学差异,见表1。
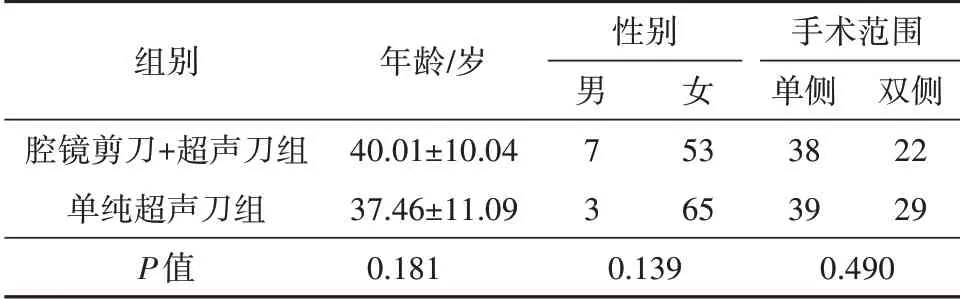
表1 患者基本临床资料Tab.1 Basic clinical data of patients
128例患者均顺利实施手术,无需中转。两组在术中出血量、术后48 h皮下引流量、1个月后局部皮瓣感觉异常中均无统计学意义,P>0.05。但在分离皮瓣耗时、气体用量均存在统计学意义,P<0.05,见表2。
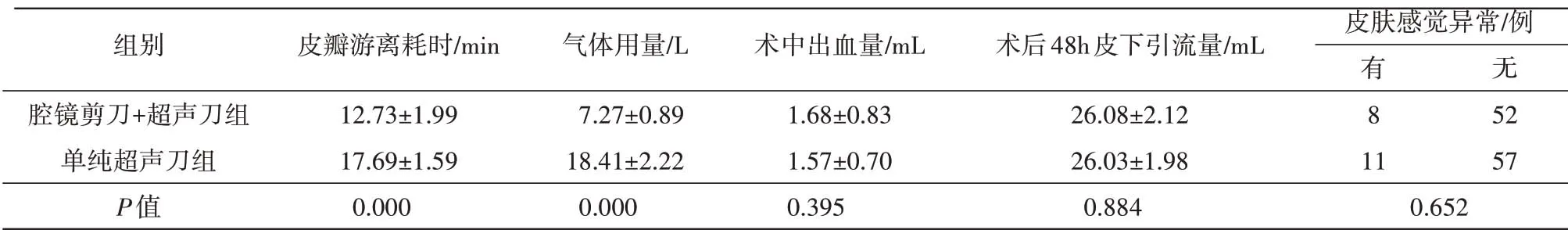
表2 各项观察指标对比Tab.2 Comparison of surgical indicators
3 讨论
腔镜甲状腺手术发展至今已出现十余种不同的手术方式,但无论何种方式均需进行皮瓣的游离。虽然手术前期已使用游离器充分游离皮下组织,协助操作空间的建立,但由于胸前区致密的结缔组织所限,刚开始进行皮瓣游离时,操作空间依然狭小[5]。同时,为了减少皮下组织术中、术后出血风险,在置入穿刺器前常常需要注入膨胀液收缩血管。此法使得手术区域存在液体残留,在使用超声刀过程中容易产生液体的溅射及增加烟雾的形成,从而造成腔镜视野的模糊,需持续排气及频发擦拭镜头才能进行手术。而在甲状腺开放手术中笔者发现颈阔肌后方结缔组织疏松,血管稀少,在钝性分离时亦无明显出血。故本研究尝试使用腔镜剪刀结合超声刀进行皮下组织的游离。
在本研究中发现腔镜剪刀联合超声刀在皮瓣游离时间及用气量为(12.73±1.99)min 和(7.27±0.89)L,相比单纯使用超声刀可缩短皮瓣游离时间及减少用气量,两者存在统计学意义。从工作原理上分析,由于超声刀是通过工作刀头的快速振动,与组织蛋白接触,造成蛋白氢键断裂和蛋白质重构,蛋白凝固闭合小管腔[6]。在这过程中会造成液体的飞溅及大量的烟雾,腔镜视野的模糊,需要反复擦拭镜头及持续排气,造成皮瓣游离时间的延长及气体用量增多。笔者发现在皮瓣游离过程中特别是在前胸壁至胸骨上窝间的区域,使用腔镜剪刀可干净利索地剪开皮下结缔组织而无明显出血,快速扩大操作空间,降低因持续使用超声刀所产生的烟雾浓度,减少擦拭镜头次数及放气时间。但此操作过程中需要薄层分离,仔细辨别血管,及时使用超声刀凝断血管及止血,减少因剪断血管造成的出血及创面血染情况。这需要丰富的手术经验及助手的配合。本研究中为减少人为因素误差,所有手术均在具有丰富腔镜经验的主任医师主刀下进行,故术中均无明显出血。但笔者单位年轻医师在进行类似操作时常常出现剪断血管造成出血及创面血染,增加皮瓣层面辨别的难度,需使用腔镜纱块或吸引器,从而造成分离时间的延长及用气量的增多。由于在腔镜剪刀皮瓣分离过程中,需要仔细的薄层分离,辨认及恰当的血管离断技巧,整个分离过程中创面常可保持干洁,而在超声刀分离过程中,由于术者对超声刀止血功能的盲目信心及操作中的轻视心理,创面常常可见细小血管的渗血。因此,在本研究中,两者皮瓣游离方式在术中出血量差异无统计学意义。而术后引流液主要由冲洗创面残留的盐水、渗液及渗血组成。本研究发现两组术后48 h 皮下引流量无统计学意义。由此可认为腔镜剪刀的应用并不增加术中及术后出血的风险。在术后1 个月局部皮肤感觉异常的研究中,两组间无统计学差异。术后瘢痕受多个因素影响,其中主要包括创伤、缺血、异物及血肿[7]。有学者研究发现腔镜甲状腺术后可引起患者颈前、胸骨区皮肤紧张或不适感[8-9]。亦有学者发现与传统开放手术相比,腔镜甲状腺并不增加术后手术区域瘢痕形成的风险[10]。本研究试图通过使用腔镜剪刀进行分离减少组织创伤、缺血风险来降低瘢痕形成可能。但在随访1个月后两组间无显著性差异。考虑既往患者随访时间短,本研究拟增长随访时间及增加行颈部彩超检查以评估颈部粘连严重程度。
综上所述,腔镜剪刀+超声刀的合理使用可快速扩大腔镜甲状腺操作空间,特别是在游离胸前区皮瓣时。同时能减少气体用量,缩短游离皮瓣时间,并不增加术中出血量、术后48 h 皮下引流量。此法安全有效,值得推广。

