灵芝多糖肽对肝癌细胞Huh7活性、迁移和细胞凋亡的影响
黄在兴,刘凌云,陈 华,翁伯琦,林占熺,刘朋虎*
(1. 福建农林大学生命科学学院/福建农林大学国家菌草工程技术研究中心,福建 福州 350002;2.福建农林大学园艺学院,福建 福州 350002;3. 福建省农业科学院,福建 福州 350002)
【研究意义】肝癌是位列世界第六大最常见的癌症,也是全球癌症死亡的第四大原因[1]。肝癌中约90 %为肝细胞型肝癌(HCC)[2], HCC的极强局部扩散和远处转移能力是其术后高复发的重要原因[3-4],也是导致癌症患者死亡的重要原因[5]。目前,HCC临床治疗主要有手术切除、化疗、化学药物治疗、分子靶向治疗等,以上治疗方式存在治疗效果不佳、价格昂贵、副作用大等缺点。近年来,因中草药具有药效明显、副作用小、价格低廉等特点,其抗肿瘤实验研究是当今的热点。【前人研究进展】灵芝为担子菌纲(Polyporales)多孔菌科(Polyporaceae)灵芝属(GanodermaKarst.),是我国法定药材之一[6]。灵芝多糖肽(Ganoderma lucidum polysaccha—rides peptide,GL-PP)作为灵芝重要活性成分之一[7-8],具有抗氧化和损失保护作用[9-12],Kim[13]从灵芝提取到一种蛋白多糖,并证明该蛋白多糖对小鼠S-180肉瘤有明显的抑制作用。目前,对灵芝抗肿瘤、调节免疫的作用多集中在灵芝多糖上[14-17],而有关灵芝多糖肽抗肿瘤作用的报道较少。【本研究切入点】本研究用GL-PP处理人肝癌细胞Huh7,分析GL-PP对离体肝癌细胞活性,细胞迁移能力和细胞凋亡的影响。【拟解决的关键问题】为揭示灵芝多糖肽抗肿瘤机制及其应用于肝癌治疗提供理论依据。

表1 主要药品与仪器
1 材料与方法
1.1 实验材料
菌草灵芝多糖肽由福建农林大学国家菌草工程技术研究中心林树钱教授提供(赤芝子实体用蛋白酶酶解后醇提取获得);肝癌细胞株Huh7由福建医科大学孟超肝胆医院提供;本实验所需其他主要药品与仪器如表1所示。
1.2 实验方法
1.2.1 GL-PP对肝癌细胞活性的影响 在96孔板中接种5000个肝癌细胞和正常的肝脏细胞,用100 μl不同浓度的GL-PP溶液(0, 50, 100, 200 μg/mL)培养基进行培养,放置在培养箱(37 ℃,5 % CO2)中过夜; 24 h后换液,向每孔加入100 μl含10 μl CCK8溶液的细胞培养基,继续培养1~4 h;培养结束后,在多功能酶标仪上测定450 nm处的吸光度。
按如下公式计算细胞活力:细胞活力(100 %)=(实验组吸光度-空白组吸光度)/(对照组吸光度-空白组吸光度)。
1.2.2 GL-PP对肝癌细胞迁移的影响 用不同浓度的GL-PP溶液(0, 100, 200 μg/mL)培养肝癌细胞,24 h后收集细胞并制备细胞悬液;在8 μm规格的Transwell小室滤膜上加入10万个细胞,用100 μl含0.5 μl BSA的DMEM细胞培养基进行培养,在下层加入600 μl含10 %胎牛血清(加相应浓度的多糖)的DMEM细胞培养基;培养24 h后,取出Transwell小室,弃孔中的培养液,用无钙的PBS缓冲液冲洗2遍,再用甲醇固定30 min,将小室适当风干。等风干后,用浓度为0.1 %的结晶紫染色20 min,用棉签轻轻擦掉上层未迁移细胞,再用PBS缓冲液冲洗3遍,最后放置在400倍显微镜下观察上室内细胞迁移情况。
1.2.3 GL-PP对肝癌细胞凋亡的影响 在24孔板中接种5万个肝癌细胞,待细胞生长到80 %汇合率时,加入不同浓度的GL-PP溶液(0、50、100、200 μg/mL)继续培养过夜;24 h后,收集细胞,用PBS缓冲液冲洗2次, 300 g 离心5 min;用100 μl 1×Annexin V binding solution重悬细胞,向细胞悬液中加入5 μl Annexin V-FITC结合物,再加入5 μl PI solution。混合均匀后,室温下避光孵育15 min并不时振荡;孵育结束后,加入200 μl 1×Annexin V binding solution并进行流式细胞仪分析。
1.2.4 数据处理 数据整理采用Microsoft Excel,差异性分析采用SPSS18.0统计软件,绘图采用GraphPad Prism,用FlowJo软件对肝癌细胞凋亡情况进行分析。
2 结果与分析
2.1 GL-PP对肝癌细胞活性的影响
本实验研究了不同浓度GL-PP(0~200 μg/mL)对肝癌细胞活性的影响(图1),实验结果显示,随培养基里的GL-PP浓度的增加,培养得到的肝癌细胞Huh7的细胞活性略微下降,且浓度越高活力下降越多,但差异性不显著,说明本试验浓度范围内,GL-PP对肝癌细胞Huh7活力影响不大。
2.2 GL-PP对肝癌细胞迁移的影响
Transwel细胞迁移实验结果如图2所示, 中浓度(100 μg/mL)的GL-PP,相比对照组(CK)的肝癌细胞迁移数量明显减少,高浓度(200 μg/mL)的GL-PP,相比中浓度(100 μg/mL)肝癌细胞的迁移数量明显下降,以上结果表明在浓度0~200 μg/mL范围内,GL-PP随着浓度的增加对肝癌细胞的迁移抑制效果越来越明显,具有一定的量效关系。
2.3 GL-PP对肝癌细胞凋亡的影响
本研究用不同浓度的GL-PP溶液处理肝癌细胞,用FlowJo软件进行分析,得到荧光双染色二维点图如图3所示, Q1表示(AnnexinV-FITC)-/PI+,此区域的细胞为坏死细胞,也可能有少数的晚期凋亡细胞在其中,甚至机械损伤的细胞也包含其中;Q2表示(AnnexinV+FITC)-/PI+,此区域的细胞为晚期凋亡细胞;Q3表示(AnnexinV-FITC)+/PI-,此区域的细胞为早期凋亡细胞;Q4表示(AnnexinV-FITC)-/PI-,此区域的细胞为活细胞。统计细胞凋亡率的方法通常采用Q2+Q3。
根据荧光染色二维点图,对凋亡率的差异性进行分析,结果如表2所示,当添加的GL-PP浓度为50和100 μg/mL时,培养得到的肝癌细胞Huh7的凋亡率和空白对照(0 μg/mL)相比没有明显的差异,显著性不差异(P>0.05);当添加GL-PP的浓度达到200 μg/mL时,肝癌细胞Huh7的凋亡率明显上升,并且差异显著(P<0.05),说明高浓度(200μg/mL)的GL-PP对肝癌细胞Huh7的凋亡有明显的诱导作用。

图1 不同浓度GL-PP对肝癌细胞Huh7活力影响Fig.1 Effects of different concentrations of GL-PP on the viability of Huh7 cells
3 讨 论
肝癌细胞的极强侵袭和转移是肝癌复发的重要原因[18],探索防止肝癌复发的有效干预策略是增加患者生存率的关键[19]。近年来,随着中草药抗肿瘤研究的深入,灵芝三萜化合物[20]、灵芝孢子粉[21]、灵芝孢子油[22]、灵芝酸[23]、灵芝多糖[24-25]、灵芝肽[26-27]等被相继报道能有效抑制肝癌细胞迁移、增殖或诱导肝癌细胞凋亡。本研究探讨了不同浓度的GL-PP对肝癌细胞Huh7的活性、迁移和凋亡的影响,发现随着GL-PP浓度的增加肝癌细胞Huh7活性越来越低,这表明GL-PP在0~200 μg/mL浓度范围内对肝癌细胞Huh7的活性有一定的影响,但差异性不显著(P>0.05)。GL-PP对肝癌细胞Huh7的迁移具有明显的抑制作用,这与曹琦珍[28]的研究结果(灵芝多糖肽处理的血清能够有效抑制人肺癌细胞的增殖)相似,而肿瘤的侵袭和迁移是一个复杂的生物学过程,每个阶段可以通过基因或者信号通路来调控[29],灵芝多糖肽抑制肝癌细胞Huh7迁移的具体机制需进一步深入研究。此外,本研究还发现低浓度(0~100 μg/mL)GL-PP对肝癌细胞Huh7的凋亡无明显诱导作用,但高浓度(200μg/mL)的GL-PP能够明显诱导肝癌细胞Huh7凋亡(P<0.05)。有研究[30]报道灵芝多糖GL-B在小鼠体内能增加肿瘤坏死因子α(TNF-α)和干扰素γ(IFN-γ)使肿瘤细胞凋亡,刘媛[14]的研究表明灵芝多糖还可通过增加NK细胞的活性来刺激TNF-α和IFN-γ的释放,最终达到抗肿瘤作用。也有报道[31]证明灵芝多糖可阻滞人肝癌HepG2细胞于G0/G1期,并可诱导其凋亡,灵芝肽可使细胞内Ca2+超载从而诱导HepG2细胞凋亡,同时还可以促使Bcl-2和survivin基因下调表达以及 p53基因上调表达,激活Caspase-3活性。因此,GL-PP在诱导肝癌细胞凋亡的机理是否与灵芝多糖或灵芝肽相同或相似也是值得深入研究的方面。
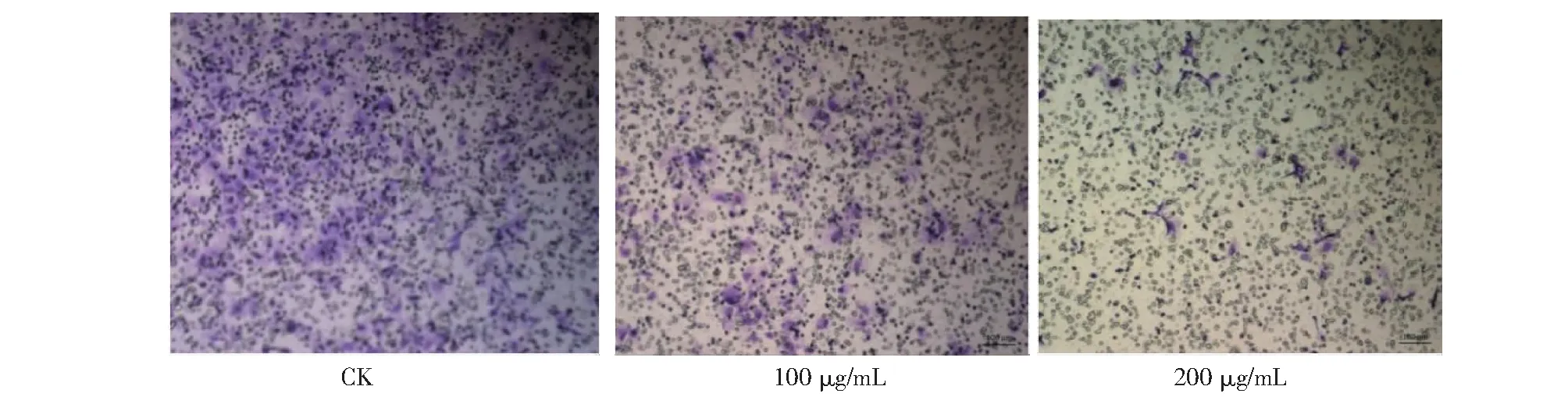
图2 不同浓度GL-PP对肝癌细胞Huh7迁移的影响Fig.2 Effects of different concentrations of GL-PP on migration of Huh7 cells

A:对照组CK; B、C、D图中GL-PP添加浓度分别为50,100,200 μg/mL图3 不同浓度的GL-PP对肝癌细胞Huh7凋亡的影响Fig.3 Effects of different concentrations of GL-PP on apoptosis of Huh7 cells

表2 不同浓度GL-PP影响下肝癌细胞Huh7凋亡率的变化
注:同列数据后不同小写字母表示不同处理之间的差异显著(P<0.05)。
综上所述,本研究证明了GL-PP能够抑制肝癌细胞Huh7的迁移,高浓度的GL-PP可明显诱导Huh7的凋亡, GL-PP对Huh7的活性影响不显著,但GL-PP 对Huh7的作用机制尚未清楚,这是今后研究的努力方向,本次研究结果可为揭示GL-PP对肝癌作用机制提供基础依据,为用于肝癌辅助治疗提供科学依据。

