阳离子瓜尔胶的制备及其助留助滤性能
陈 威,申 冉,刘传杰,李 楠
(1.曲阜师范大学工学院,山东日照 276800;2.齐鲁工业大学制浆造纸科学与技术教育部/山东省重点实验室,山东济南 250353)
瓜尔胶由半乳甘露聚糖构成[1-2],是自然界中含量丰富的可再生生物材料,具有无毒、可生物降解和特殊的物理化学性质,在水处理[3]、采矿选矿[4]、医药[5]、石油钻采[6]、纺织印染[7-9]等领域中应用广泛。瓜尔胶的结构与纤维素相似,在特定条件下可通过衍生化反应引入官能团,从而具备相应的理化特征,扩大应用范围[[10-11]]。瓜尔胶衍生物由瓜尔胶原粉(GG)经一系列化学改性引入特定官能团制备,因无毒无害且能显著改善助留助滤效果而广泛应用于造纸湿部的抄造过程。目前,阳离子瓜尔胶(CGG)的湿法制备一般采用有机溶剂(甲醇、乙醇、异丙醇等)法,制备的阳离子瓜尔胶不仅阳离子取代度低、黏度损失大,而且后处理有机溶剂回收困难,导致资源浪费和环境污染[12]。而离子液体作为一种新型的绿色溶剂,在天然多糖类化合物的化学改性中已得到广泛应用,以其作为反应介质时,瓜尔胶原粉不但能得到充分溶胀,而且反应活性也会因离子液体的催化作用而提高,从而缩短反应时间。
本课题主要研究阳离子瓜尔胶在咪唑型离子液体中的制备、表征及其在脱墨废纸浆中的助留助滤性能。在不额外添加催化剂的条件下,以离子液体为反应介质、3-氯-2-羟丙基三甲基氯化铵(CTA)为醚化剂,对瓜尔胶原粉进行醚化改性,并设计正交实验和单因素实验进一步优化CGG 的合成工艺;同时以乙醇、异丙醇为溶剂进行对照实验,制备了不同种类的CGG。利用正交实验和单因素实验考察醚化剂用量、反应温度、反应时间、碱化时间、碱用量对产物氮质量分数及黏度的影响,优化合成条件。借助傅里叶红外光谱、核磁共振波谱(1H-NMR)和扫描电镜表征产物的结构与形态,证实醚化反应的发生。
1 实验
1.1 材料和仪器
材料:瓜尔胶、3-氯-2-羟丙基三甲基氯化铵、无水乙醇(分析纯,上海阿拉丁生化科技股份有限公司),咪唑型离子液体[氯化1-烯丙基-3-甲基咪唑([AMIM]Cl)、氯化1-丁基-3-甲基咪唑([BMIM]Cl)、1-丁基-3-甲基咪唑乙酸鎓盐([BMIM]Ac)、1-烯丙基-3-甲基咪唑乙酸鎓盐([AMIM]Ac),实验室自制,真空干燥],异丙醇、氢氧化钠、盐酸(分析纯,国药集团化学试剂有限公司),脱墨废纸浆(初始打浆度55°SR,pH=6.7,山东某纸厂),聚合氯化铝(工业级,巩义腾龙化学材料厂)。
仪器:RW20 数字搅拌器(德国IKA 公司),HH-2数显恒温水浴锅(金坛市晶玻实验仪器厂),SHZ-ⅢA 型循环水式真空泵(巩义市予华仪器有限责任公司),RE52CS 型旋转蒸发仪(上海亚荣生化仪器厂),电热恒温鼓风干燥箱(上海一恒科学仪器有限公司),电子天平(上海精密科学仪器有限公司),冷凝回流装置(实验室自制),Spectrum GX 型傅里叶变换红外光谱仪(美国Perkin Elmer 公司),Brookfield 黏度计(上海尼润智能科技有限公司),AVANCE Digital 核磁共振波谱仪(德国Bruker 公司),动态保留及滤水性测试仪(DFA,德国AFG 公司),LP2000-11 浊度仪(意大利HANNA Instrument 公司),打浆度测定仪(陕西科技大学机械制造厂)。
1.2 制备方法
1.2.1 CGG 的合成原理
瓜尔胶分子上的羟基经碱催化后生成负电性氧离子,活性提高,在遇到季铵盐类醚化剂时,活化后的瓜尔胶以“亲核试剂”形式攻击季铵盐中的碳离子,进而取代卤原子发生双分子亲核取代反应,生成瓜尔胶阳离子醚。GG 和CTA 是反应物,碱是催化剂,在提高反应活性的同时也会参与反应[13],没有副反应发生。瓜尔胶以GG-OH 表示,醚化反应原理如下:

1.2.2 CGG 的制备
在离子液体中,瓜尔胶原粉与离子液体以质量比1∶6 混合并搅拌,加入40%的NaOH 溶液(NaOH 和GG 的质量比为1∶10),冰水浴碱化一段时间后加入CTA,加冷凝回流装置,升至合理温度反应一段时间,经抽滤、洗涤、旋蒸、烘干后得到CGG。为了保证反应平稳均衡地进行,NaOH 溶液分3次加入,碱化时加入1/3,加入CTA 后再加入1/3,剩余的1/3 在反应结束前0.5 h加入[14]。
在有机溶剂中,分别以乙醇、异丙醇作为介质,在碱催化下使GG 与CTA 反应,经过滤、旋蒸、干燥后得到CGG。
1.2.3 阳离子瓜尔胶的提纯
将适量CGG 溶于去离子水中,待完全溶解后用无水乙醇析出,用无水乙醇洗涤沉淀得白色絮状物,在60 ℃下干燥至恒重,即得纯化的CGG。
1.3 测试
1.3.1 氮质量分数
采用凯氏定氮法测试。以CuSO4、K2SO4作为催化剂,用浓硫酸裂解CGG,碱化后蒸馏以释放氨;用2%的硼酸溶液收集产物,以盐酸标准溶液滴定,经计算可得CGG 的氮质量分数,计算式如下:

式中,X为氮质量分数,%;c为盐酸标准溶液的浓度,mol/L;V1为测定样品时消耗的盐酸标准溶液体积,mL;V0为测定空白时消耗的盐酸标准溶液体积,mL;m为CGG 样品质量,g。
1.3.2 黏度
将CGG 配制成1%的溶液,放置2 h,用黏度计测定。转速100 r/min,测试温度25 ℃。
1.3.3 单程留着率(FPR)
(1)建立回归方程。称取5 g 绝干浆料加水配制成0.5%的溶液,搅拌均匀后倒入动态滤水仪的滤水罐,调整转速为800 r/min,收集1 L 滤液。分别取3 份200 mL 的滤液过滤后置于恒重烧杯中,烘干至恒重,测试质量分数。另取剩余滤液用不同规格容量瓶稀释至不同质量分数,用浊度计测试浊度。质量分数和浊度数据如表1所示。

表1 滤液的质量分数与浊度
将表1 中的数据进行一元线性回归分析,得到滤液质量分数与浊度的回归方程为:T=104×(1.949 5w-0.010 3),R2=0.995 36,其中,w为滤液质量分数,T为滤液浊度。
(2)计算单程留着率。将0.2%的浆料溶液搅拌均匀后倒入滤水罐,加入助留助滤剂,800 r/min 搅拌10 s 后收集100 mL 滤液,用浊度仪测试浊度,计算滤液质量分数。细小组分单程留着率指留在滤网上的细小组分占浆料总细小组分的百分数[15],计算公式为:

式中,FPR 为细小组分单程留着率,%;w为滤液质量分数,%;w0为浆料总细小组分质量分数,%。
1.3.4 打浆度
将脱墨废纸浆配制成0.5%的溶液,按需要加入各类助留助滤剂,混合均匀后用打浆度仪测定。
1.3.5 红外光谱
将纯化后的CGG、GG 分别与KBr 混合均匀后研磨压片,用傅里叶变换红外光谱仪测试,仪器分辨率4 cm-1,扫描次数8,波数范围400~4 000 cm-1。
1.3.6 核磁共振氢谱
将CGG 研磨后用核磁共振波谱仪进行测定。测试条件:正离子扫描,扫描范围m/z=100~500,氮气流速为1.5 L/min,温度为200 ℃,毛细管电压为2.5 kV,溶剂为DMSO。
2 结果与讨论
2.1 离子液体的筛选
以[AMIM]Cl、[BMIM]Cl、[AMIM]Ac 和[BMIM]Ac为反应介质,采用相同的实验条件(GG 4 g、离子液体24 g、NaOH 0.4 g、CTA 1.6 g,碱化30 min,50 ℃反应2 h)分别制备了CGG-1、CGG-2、CGG-3、CGG-4,氮质量分数和黏度结果见表2。

表2 CGG 的氮质量分数和黏度
由表2 可知,在不同离子液体中制备的CGG 黏度和氮质量分数均差别较大;在[AMIM]Ac 中制备的CGG-3 氮质量分数最高,为0.70%,表明瓜尔胶原粉在此离子液体中的醚化反应效果相对最佳。因此选取[AMIM]Ac作为后续CGG 合成实验的反应介质。
按CGG 的制备方法,改变合成条件,在[AMIM]Ac中制备了不同阳离子取代度的CGG(编号5~10),其性质如表3所示。

表3 不同阳离子取代度的CGG 性质
2.2 阳离子瓜尔胶醚化反应正交实验
因为碱化时间、m(NaOH)/m(GG)、反应温度、反应时间以及m(CTA)/m(GG)都是影响醚化反应的重要因素,所以采用L16(45)正交实验进行分析,以确定各反应条件对CGG 氮质量分数和黏度的影响大小,从而得出优化合成条件,结果见表4。
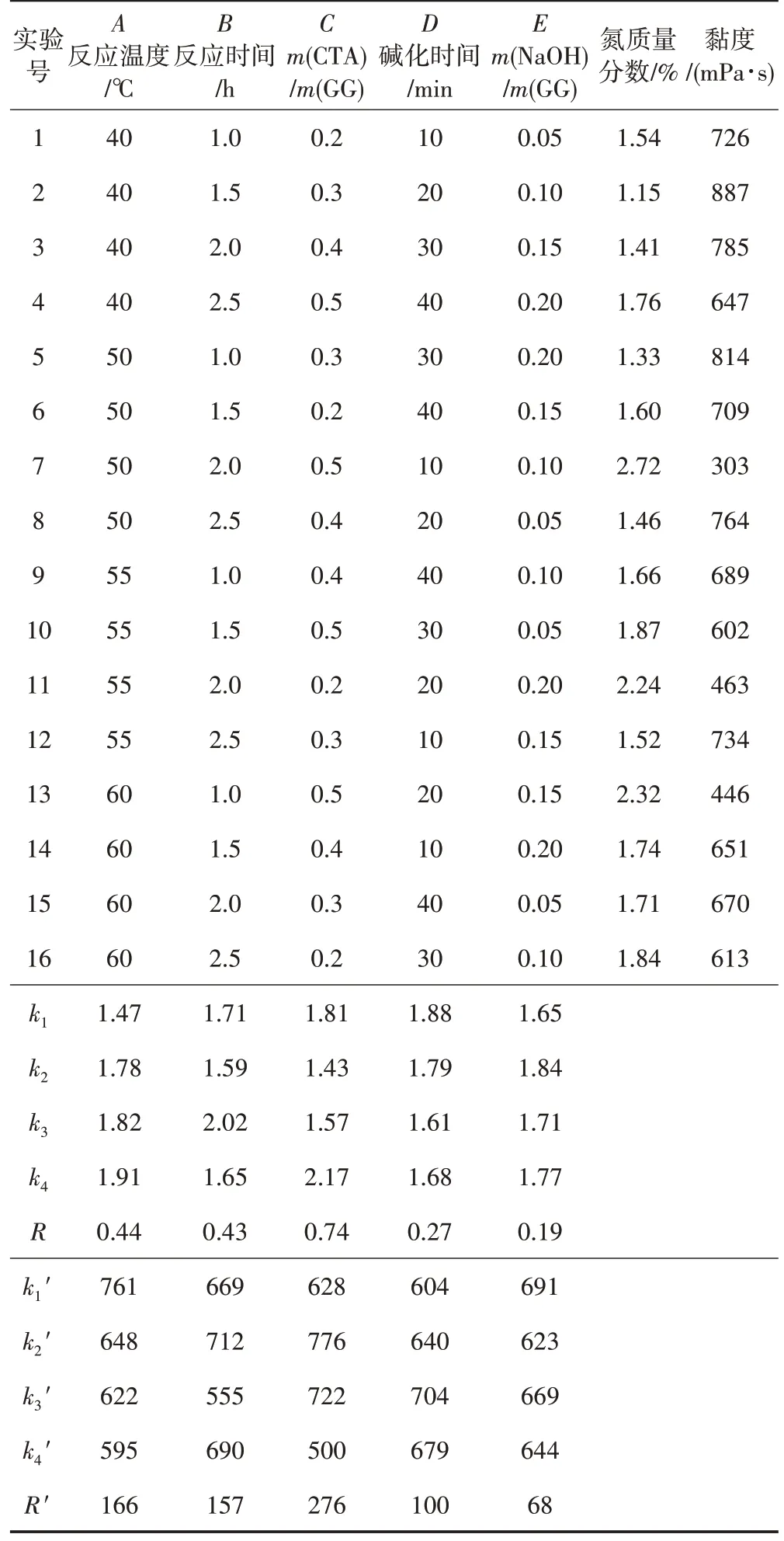
表4 阳离子瓜尔胶醚化反应正交实验结果
从表4 中可以看出,对于CGG 的氮质量分数和黏度,5 个因素的影响从大到小均为C、A、B、D、E,即m(CTA)/m(GG)影响最大,即醚化剂用量是决定CGG氮质量分数高低的直接因素;其次是反应温度,适当的温度有助于提高瓜尔胶分子的反应活性,温度过低醚化效率不足,温度过高又会导致瓜尔胶原粉热降解,进而影响醚化效率;反应时间和碱化时间其次,m(NaOH)/m(GG)的影响最小。
对于本实验而言,要制备氮质量分数(取代度)高的CGG,除了要考虑各因素对氮质量分数的影响外,还必须将黏度的影响作为辅助参考因素。综合考虑,正交实验的优化因素组合为A3B2C4D3E1,即反应温度55 ℃,反应时间1.5 h,m(CTA)/m(GG)=0.5,碱化时间30 min,m(NaOH)/m(GG)=0.1,产物的氮质量分数和黏度分别为1.87%和602 mPa∙s。
此外还应考虑离子液体用量对实验结果的影响,适量的离子液体可确保瓜尔胶原粉均匀分散并一直处于溶胀状态,从而有更多的活性羟基铺展在外侧,加速醚化反应的进行。离子液体用量过多,除了会降低瓜尔胶颗粒与碱液、醚化剂的接触面积外,还会增加生产成本和回收难度;而用量过少,自身黏度增大搅拌阻力,甚至导致瓜尔胶原粉糊化,与离子液体混合不均匀,醚化剂不能充分与活性羟基反应,降低醚化效率[4]。经多次实验后发现,瓜尔胶与离子液体质量比为1∶6时,能获得相对较佳的醚化效果。
2.3 阳离子瓜尔胶醚化反应的单因素实验
2.3.1 m(CTA)/m(GG)
由图1 可知,CGG 氮质量分数随着m(CTA)/m(GG)的增加而持续增大,当m(CTA)/m(GG)由0.2 增大至0.7 时,氮质量分数由1.15%增大至2.06%。因为CTA用量增加会加大其与瓜尔胶分子上活性羟基的接触概率,有助于醚化度的提高;当m(CTA)/m(GG)小于0.5 时,氮质量分数急剧增大;而当m(CTA)/m(GG)大于0.5 后,虽然氮质量分数继续提高,但增长趋势变缓。同时,随着醚化剂的加入,其中存在的水分、杂质等导致瓜尔胶降解,进而导致CGG 得率和黏度持续降低。因此确定m(CTA)/m(GG)=0.5。

图1 m(CTA)/m(GG)对CGG 氮质量分数和黏度的影响
2.3.2 反应温度
由图2 可知,随着反应温度的升高,氮质量分数持续增大,由1.34%增大到2.10%。因为温度升高使醚化剂分子的热运动加快,与瓜尔胶活性羟基有了更多的碰撞和接触机会,从而提高了醚化效率。但瓜尔胶原粉和CGG 也会随着温度的升高而发生降解,影响醚化反应的进行程度,导致黏度降低。尤其是温度高于55 ℃之后,氮质量分数增大趋势变缓,而黏度依旧锐减,因此确定反应温度为55 ℃。

图2 反应温度对CGG 氮质量分数和黏度的影响
2.3.3 反应时间
由图3 可知,产物氮质量分数随着反应时间的延长而增大,由1.65%增大到2.06%,而黏度却持续下降,尤其是在反应时间超过2.0 h 后,氮质量分数增大已不明显,但黏度依旧呈明显的降低趋势。因此,延长反应时间不仅对产物的黏度不利,而且会造成人力和物力的额外消耗,故确定反应时间为2.0 h。

图3 反应时间对CGG 氮质量分数和黏度的影响
2.3.4 碱化时间
碱化时间对CGG氮质量分数和黏度的影响见图4。

图4 碱化时间对CGG 氮质量分数和黏度的影响
由图4 可知,随着碱化时间的延长,氮质量分数持续增大,由1.66%增大至2.00%,碱化时间超过20 min后,氮质量分数增大不显著。预留碱化时间的目的是为了给瓜尔胶分子内的羟基进行活化及与碱反应提供足够的时间,横坐标的0 刻度代表不预留碱化时间,也就是加入反应原料和NaOH 后直接加入醚化剂进行反应。碱化过程放热会造成瓜尔胶热降解,碱化时间越长,分子降解越严重。当碱化20 min 时,氮质量分数已达1.89%,黏度也较高(562 mPa∙s)。因此,碱化时间以20 min为宜。
2.3.5 m(NaOH)/m(GG)
由图5 可以看出,随着m(NaOH)/m(GG)的增大,氮质量分数呈现增大趋势。横坐标的0 刻度代表不加NaOH,此时的氮质量分数很低(0.96%),黏度最大。m(NaOH)/m(GG)为0.05 时,氮质量分数急剧增大至1.68%,而黏度由915 mPa·s 锐减至670 mPa·s。当m(NaOH)/m(GG)超过0.10 后,氮质量分数呈现平稳增加的趋势,黏度却依旧递减。在反应过程中加入碱,一方面能与活性羟基生成醇钠,另一方面能使稳定的醚化剂转化为高活性中间体——环氧丙基三甲基氯化铵,进而与瓜尔胶原粉发生反应。综合考虑,选择m(NaOH)/m(GG)=0.10较为合适。

图5 m(NaOH)/m(GG)对CGG 氮质量分数和黏度的影响
单因素实验确定的优化合成条件:m(CTA)/m(GG)=0.5,反应温度55 ℃,反应时间2.0 h,碱化时间20 min,m(NaOH)/m(GG)=0.10。制备的CGG 氮质量分数为1.95%,黏度为583 mPa∙s。
2.4 在不同反应介质中制备的CGG 比较
由表5 可知,CGG-5 不仅具有最高的氮质量分数(1.95%),而且黏度较高(583 mPa∙s),证明离子液体对合成的CGG 起到了保护作用。在乙醇、异丙醇中合成的CGG 虽然氮质量分数较高,但黏度相对较低,因为在反应过程中瓜尔胶原粉发生了降解,同时,溶剂分子中的羟基与阳离子改性剂发生了反应,相对分子质量降低致使黏度降低,这也是其他溶剂法合成CGG 的共同缺点。

表5 在不同反应介质中制备的CGG 比较
2.5 影响FPR 的因素
2.5.1 CGG 阳离子取代度
理论认为CGG 阳离子取代度越大,也就是正电荷密度越大,通过电荷中和及架桥作用使更多带负电的细小组分凝集到纤维表面,从而有更好的助留效果。由图6 可知,在用量相同(均为0.06%)时,具有最大阳离子取代度的CGG-8 助留效果(70%)反而低于CGG-5(72.3%)。这可能是因为CGG 阳离子取代度越大,与浆料体系内微小粒子的接触点越多,而伸向溶液的链段越短,导致颗粒间的吸附架桥作用减弱,留着效果略有降低。由图6 还可知,4种CGG 对细小组分留着率的影响变化趋势一致,用量小于0.06%时,留着率都随着CGG 用量的增加而增大;用量大于0.06%之后,留着率都呈降低趋势。这是由于较大的阳离子助剂用量会使浆料体系电荷发生逆转,进而降低留着率。因此,在选择CGG 类助剂时,应根据实际需要选择合适取代度的阳离子瓜尔胶,取代度过大或过小助留效果都不理想。

图6 不同取代度CGG 对助留效果的影响
2.5.2 CGG种类
由图7 可知,CGG-5 的单程留着率优于CGG-6和CGG-7,在相同用量(均为0.06%)下,CGG-5 的留着率达到了72.3%,而CGG-6 和CGG-7 的留着率相当,均在65%左右。这是因为有机溶剂法合成的CGG在反应过程中未得到反应介质的保护而发生了碱性降解,从而导致分子链对浆料内微粒组分的吸附架桥作用减弱,进而影响了留着效果的提高。

图7 不同种类CGG 对助留效果的影响
2.6 表征
2.6.1 红外光谱
图8中,GG与CGG都有的特征吸收峰:3 289 cm-1处的O—H 伸缩振动峰,2 921 cm-1处的C—H 伸缩振动峰,1 646 cm-1处的C—O 伸缩振动峰。此外,阳离子瓜尔胶在1 560 cm-1处出现了N—H 变形振动峰,在685 cm-1处出现了N—H面外弯曲振动峰,在1 417 cm-1处出现了C—N 伸缩振动峰,在1 017 cm-1处出现了C—N 弯曲振动的中强吸收峰。以上特征峰的出现都证明CTA 与瓜尔胶原粉确实发生了醚化反应,且季铵基团(阳离子)已顺利接到瓜尔胶分子上。

图8 瓜尔胶原粉与阳离子瓜尔胶的红外光谱图
2.6.2 核磁共振氢谱
CGG 的分子结构如下:

由分子结构可知,甘露糖构成的主链呈弯曲状,有大量羟基被包覆在分子内形成了分子内氢键;半乳糖支链位于分子外侧,C6 位仲羟基的反应活性很高,故被化学改性的概率最高[3]。由图9a 可知,CGG氢谱中出现了瓜尔胶没有的峰(δ=3.33),形成了新的基团,这说明阳离子改性成功。瓜尔胶分子同时含有甘露糖和半乳糖,因两者在C1 位处连接的O 原子最多,故H 质子峰位于低场(δ=4.90~5.50)。图9b 中,δ=5.31处为瓜尔胶半乳糖侧链C1位的H 质子峰,δ=5.32处为阳离子瓜尔胶半乳糖侧链C1 位的H 质子峰,此外,δ=2.00 处为瓜尔胶分子中的羟基质子峰,δ=2.50处为DMSO 溶剂峰。

图9 CGG(a)与GG(b)的1H-NMR 谱图
3 结论
(1)在[AMIM]Ac 中合成的CGG-3 氮质量分数最大。影响醚化反应的各个因素按显著性排序由大到小依次为m(CTA)/m(GG)、反应温度、反应时间、碱化时间、m(NaOH)/m(GG)。单因素实验确定的优化合成条件为:m(CTA)/m(GG)=0.5,反应温度55 ℃,反应时间2.0 h,碱化时间20 min,m(NaOH)/m(GG)=0.10,瓜尔胶原粉与离子液体质量比为1∶6。制备的CGG 氮质量分数为1.95%,黏度为583 mPa∙s。
(2)在[AMIM]Ac 中合成的CGG-5 较在乙醇、异丙醇中合成的CGG-6、CGG-7具有更高的氮质量分数和黏度,说明离子液体对CGG 起到一定的保护作用。
(3)取代度0.26、黏度583 mPa∙s 的CGG-5 助留效果最好,用量为0.06%时单程留着率为72.3%。

