高氨氮废水短程硝化启动研究
李苏仲,薛同站,2*,李卫华,2,葛明井,程硕雅
(1.安徽建筑大学 环境与能源工程学院,安徽 合肥 230601;2.水污染控制与废水资源化安徽省重点实验室,安徽 合肥 230601)
畜禽养殖废水具有高浊度,高氨氮和高有机物浓度的特点[1]。在高有机负荷的条件下,硝化反应会被抑制[2],畜禽养殖废水往往先经过厌氧生物处理降低有机物浓度。在厌氧处理的过程中,仅有一小部分氮通过同化作用被去除。有机物的降解和氮的去除不同步导致经厌氧处理后出水的碳氮比降低。此时的污水具有高氨氮和低碳氮比的特点,碳氮比一般在0.5~2之间。
传统的生物脱氮包括全程硝化和反硝化两个步骤[3],两个阶段的反应公式分别为式(1)和(2):
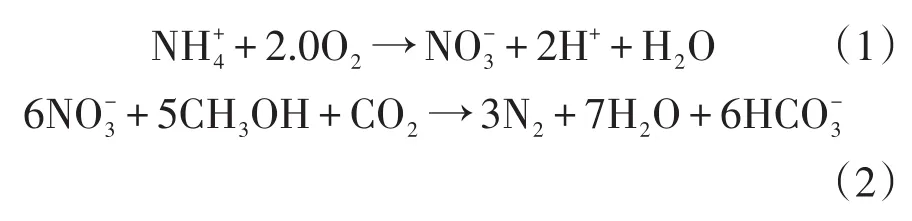
传统生物脱氮所需的大量外加碳源和能源造成脱氮成本过高。而无论是短程硝化—反硝化工艺还是短程硝化—厌氧氨氧化工艺,相较于传统的生物脱氮工艺均能节约碳源和能源。以短程硝化反硝化为例,短程硝化反硝化的两个阶段的反应公式分别为式(3)和(4)[4]:
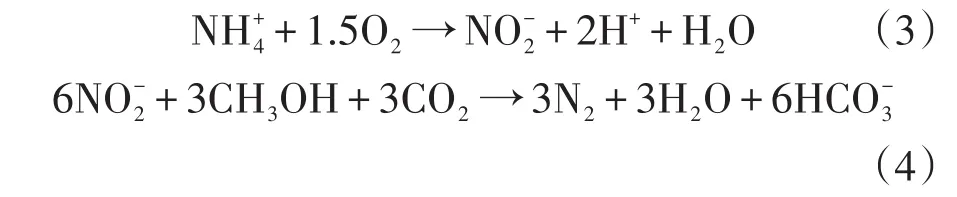
对比短程硝化反硝化工艺和全程硝化反硝化工艺可以看出,在好氧硝化阶段,相较于全程硝化,短程硝化节约了25%的供氧量,而在后续的厌氧反硝化阶段,短程硝化反硝化工艺还节省了40%的碳源,无论是曝气所需的能源还是反硝化所需的外加碳源均减少,从而节省了成本,此外还减少了反应所需时间,水力停留时间(hydraulic retention time,HRT)相应减少,进而提高脱氮效率。
如果对比短程硝化厌氧氨氧化[5]和全程硝化反硝化,则脱氮的成本进一步降低。相比于短程硝化反硝化,短程硝化厌氧氨氧化从原理上来说不需要碳源,因此可以节约100%的外加碳源。由于后续的厌氧氨氧化需要氨氮和亚硝态氮同时存在,无需将氨氮全部转化为亚硝态氮,从而进一步的降低了需氧量和HRT。
研究表明短程硝化的影响要素有温度、溶解氧(dissolved oxygen,DO)浓度、pH 值、游离氨(free ammonia,FA)浓度、游离亚硝酸(free nitrous acid,FNA)浓度、污泥龄、选择性抑制剂[9-15]等。
1 实验材料和方法
1.1 污泥接种
接种污泥取自合肥市经开区污水处理厂的好氧池,经蠕动泵输入SBR(sequencing batch reactor activated sludge process)反应器后曝气4 d。曝气后取水样测得此时MLSS(mixed liquid suspended solids)为 4 372.6 mg∙L-1。
1.2 进水配置
原水取自某养猪场,厌氧反应器处理15 d后排出,作为SBR反应器的进水。因为两个反应器间处理效率的差异过大,厌氧反应器的出水量不足以供给SBR反应器。所以在多次测量厌氧反应器出水水质之后,根据数值的平均数配置模拟水样作为替代。厌氧反应器出水部分指标如表1。
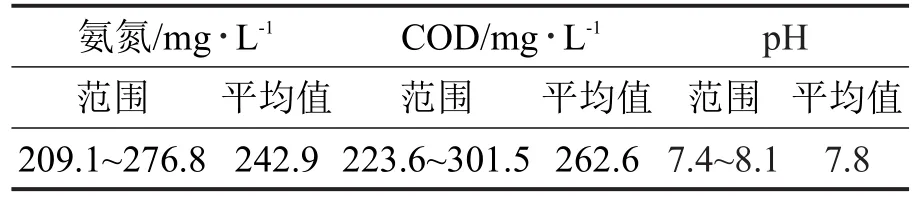
表1 厌氧反应器出水部分指标
人工模拟水样每次配置25 L,模拟水样的NH4+-N 浓度为 243 mg∙L-1,COD(chemical oxygen demand)的浓度为263 mg∙L-1。此外配制微量元素营养液,1 L进水中加入1 mL微量元素营养液,其成分及浓度如下:EDTA-2Na 18.6 g∙L-1,FeSO4∙7H2O 0.76 g∙L-1,ZnSO4∙7H2O 0.43 g∙L-1,CuSO4·5H2O 0.25 g∙L-1,CoCl2∙6H2O 0.24 g∙L-1,NaMoO4∙2H2O 0.22 g∙L-1,NaMoO4∙2H2O 0.22 g∙L-1,MnCl2∙4H2O 0.19 g∙L-1,NaSeO4∙10H2O 0.21 g∙L-1,NiCl2∙6H2O 0.19 g∙L-1。
以上药品均为分析纯。
1.3 实验设备
实验采用的SBR反应器分内外两层,有效容积为6 L。反应器结构如图1。
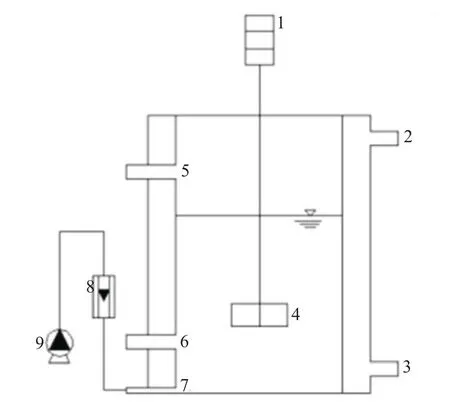
图1 SBR反应器示意图
SBR反应器一周期设定为8 h,使用KG-316T时控开关自动控制反应器的进出水,搅拌和曝气。具体时间安排如下:进水0.5 h,搅拌及曝气6 h,静置 1 h,出水 0.5 h。
本次选择我院在2017年1月~2018年接诊治疗的100例中晚期帕金森病患者作为研究对象,分析美多芭与吡贝地尔联合应用治疗中晚期帕金森病的效果及安全性。
进水和出水使用BT100-2J蠕动泵,搅拌使用D40-2F电动搅拌机及配套的调速器,曝气使用ACO-002电磁式空气泵,使用LZB-6转子流量计以达到调节曝气强度的作用。水浴加热使用MX500加热棒加热水箱中的水,温度设定为34℃,同时使用AP3100潜水泵来保证SBR外层的水循环流动。
1.4 分析测试方法
pH值使用pH计进行测量,DO使用溶解氧仪进行测量,NH4+-N采用纳氏试剂光度法测定,NO2--N使用N-(1-奈基)-乙二胺光度法测定,NO3--N采用紫外分光光度法测量[16]。COD使用重铬酸钾法测量。三维荧光扫描使用F-7000三维荧光分光光度计。
水质指标测定所使用的药品如下:酒石酸钾钠,碘化钾,碘化汞,氢氧化钠,硫酸银,硫酸汞,重铬酸钾,氨基磺酸,对-氨基苯磺酰胺,N-(1-奈基)-乙二胺二盐酸盐,盐酸,磷酸,硫酸。药品均为分析纯。
亚硝态氮积累率(nitrite accumulation ratio,NAR)计算如下[17]:
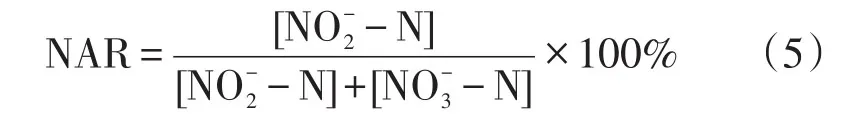
式中[NO2--N]表示反应结束后亚硝态氮的浓度,单位为mg∙L-1,[NO3--N]表示反应结束后硝态氮的浓度,单位为 mg∙L-1。
1.5 反应器的启动和运行
SBR反应器曝气4 d后,排出上清液,实验正式开始。实验总共分为三个阶段。
第一阶段:第1至第18天,此阶段为氨氮负荷提高阶段,按梯度逐步提高进水氨氮浓度,最后将进水氨氮浓度稳定在243 mg∙L-1,与厌氧反应器出水氨氮浓度保持一致。
第二阶段:第19至27天,调节进水的pH来提高氨氮去除率和NAR,然后选出最合适的进水pH浓度进行下一步实验。
第三阶段:第27至第30天,在投加Na2CO3之外还投加NaHCO3作为缓冲物质,探究在有缓冲物质的情况会对出水指标造成什么影响。
在以上阶段结束后,观测反应器内的FA和FNA变化。用三维荧光分光光度计扫描反应器出水,再用Matlab进行平行因子法分析。
2 结果与讨论
2.1 氨氮负荷提高阶段
为观测不同进水氨氮负荷下,反应器的氨氮去除率和NAR的变化,每3天提高一次进水氨氮浓度,每次提高40 mg∙L-1,持续18天,最终将进水氨氮浓度稳定在243 mg∙L-1。此阶段的出水三氮浓度见图2,氨氮去除率与NAR的变化见图3。
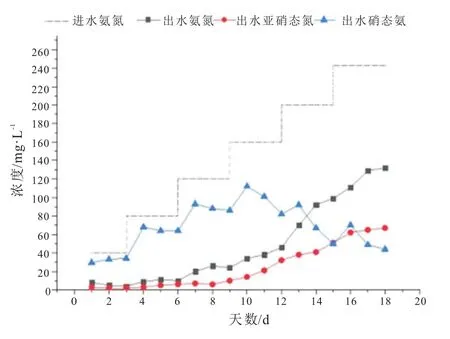
图2 氨氮负荷提高阶段出水三氮浓度变化图
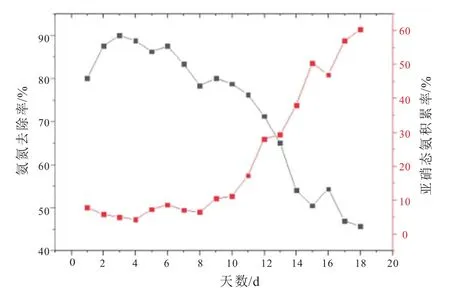
图3 氨氮负荷提高阶段的氨氮去除率与亚硝态氮积累率变化图
从污水厂接种的污泥对低氨氮浓度的进水具有很高的氨氮去除率,随着进水氨氮浓度的提高,氨氮去除率逐渐降低,尤其在进水氨氮浓度超过120 mg∙L-1后,氨氮的去除率下降更加明显。在反应器运行的前9 d,NAR均低于10%,这说明在接种污泥中,NOB占据优势地位,其不断地将亚硝态氮氧化为硝态氮。随氨氮浓度的升高,NAR不断上升,在第18 d,NAR达到了60.4%,已经满足了NO2--N占NOx--N的一半以上这一条件,此时氨氮的去除率仅有45.6%。
2.2 pH调节阶段
AOB和NOB各自生长最适合的pH不同,本阶段尝试通过调节pH的方式提高氨氮去除率与NAR。因为反应器较为封闭,在反应中途难以投加药品调节pH,因此在配置进水时就投加足够的碱性物质,不考虑中途投加。使用Na2CO3调节进水pH。根据进水的pH值,本阶段实验从进水pH=8.0开始,每3 d提高一次进水的pH。为了分析反应器内浓度随时间变化的趋势,此阶段每隔1 h取一次水样,每周期取7个水样。此阶段氨氮及亚硝态氮浓度随HRT变化如图4,不同进水pH的情况下的氨氮去除率和NAR如图5。
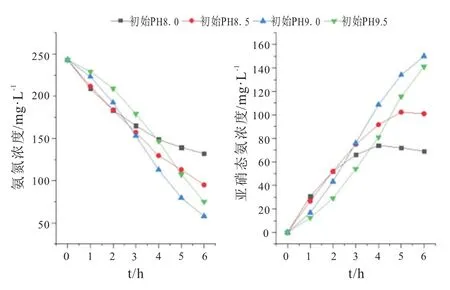
图4 不同进水pH的情况下氨氮浓度及亚硝态氮浓度随时间变化图
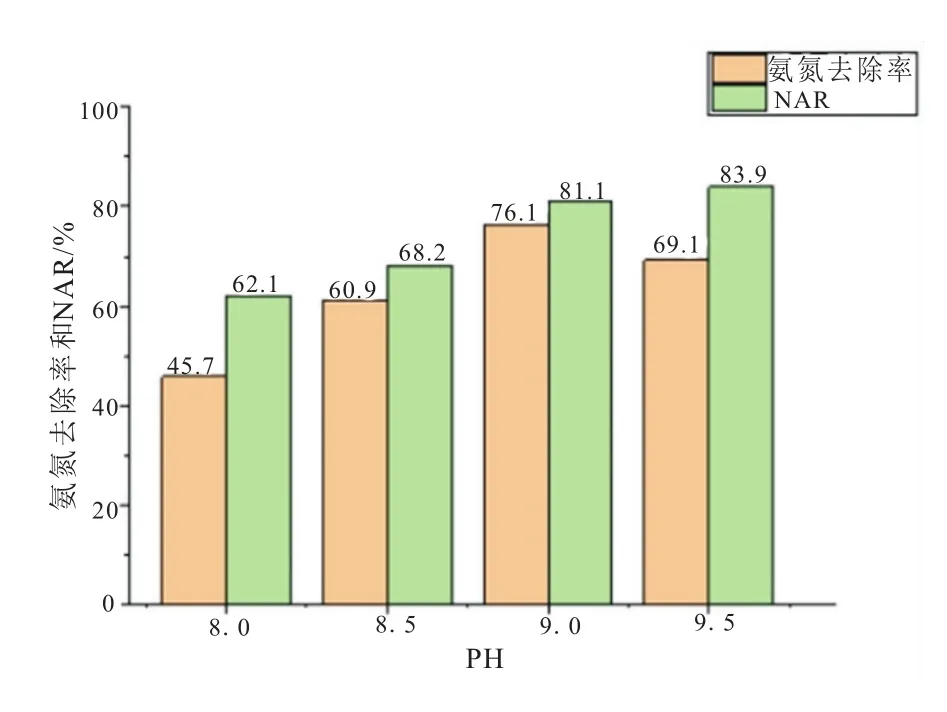
图5 不同进水pH的情况下的氨氮去除率和NAR
进水pH为8.0时,实验前期氨氮去除速度最快,但随着时间亚硝态氮的积累逐渐减慢,HRT>4 h时,由于NOB的硝化作用,亚硝态氮的浓度反而开始减少。进水pH为8.5时,同样在反应后期出现了亚硝态氮浓度降低的情况。从图5可以看出,进水pH为9.0的情况下氨氮的去除率最高;进水pH为9.5时,NAR最高。由此可知进水pH较高时更有利于亚硝态氮的积累,过高的pH会导致氨氮去除速率变慢,除此之外,进水pH为9.5的情况下,配水时有浓烈的刺激性气味,说明此时由于由于高pH,游离氨浓度高,逸出了大量氨气。综上考虑,选择将进水pH定为9.0。
2.3 投加缓冲物质对比阶段
在调节pH实验后,选择将进水pH调节为9.0进行下一步实验,此时氨氮去除率达到76.1%,出水pH为6.4。根据相关文献,AOB的最适宜 pH为 7.0~8.5,NOB的最适宜 pH更低为6.0~7.5[18]。由此可知在反应后期,反应器内的 pH值不再适合AOB。额外投加NaHCO3作为缓冲物质,观察此时的出水变化。此阶段每隔1 h取一次水样,每周期取7个水样。将投加缓冲物质前后的氨氮及亚硝态氮浓度变化曲线进行对比,结果如图6。
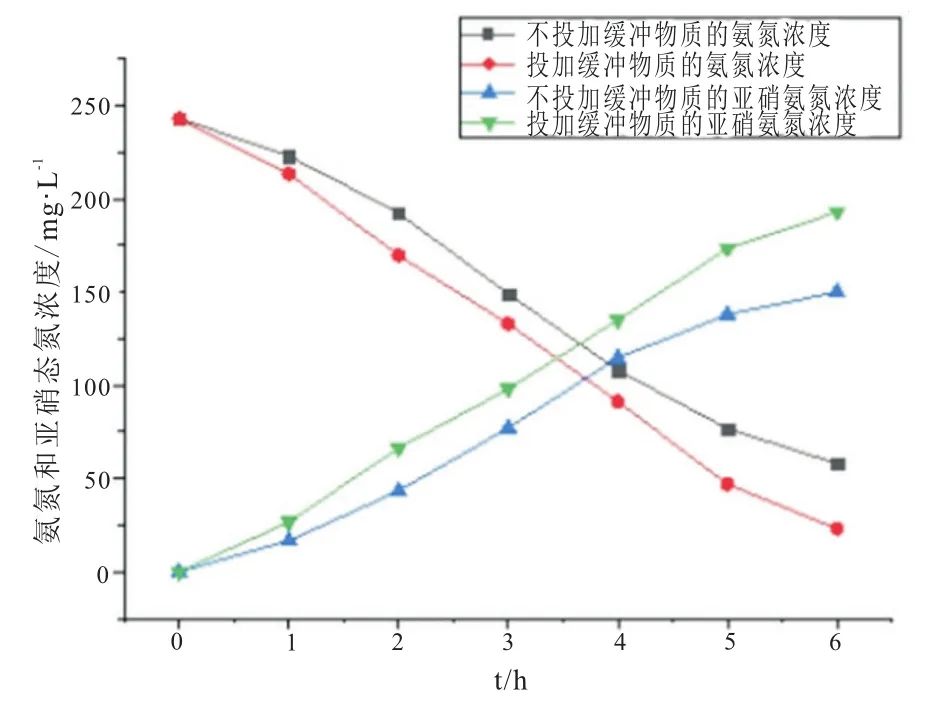
图6 添加缓冲物质前后的氨氮及亚硝态氮浓度变化对比图
投加NaHCO3后氨氮去除率和NAR均有所提高,分别达到了90.7%和88.9%。投加NaHCO3后氨氮的去除和亚硝态氮的积累曲线均变得更加线性。
2.4 反应器内的FA和FNA变化
在上述三个实验结束后,维持反应器运行,根据反应器的pH、水温、氨氮及亚硝态氮浓度,计算出反应器内FA和FNA。
FA 的计算公式[19]:
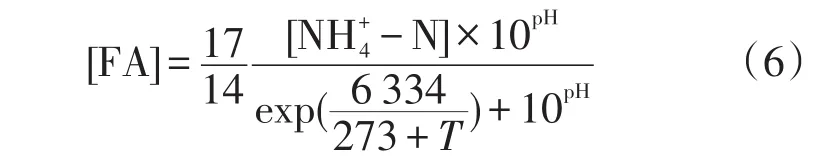
式中:FA为游离氨浓度,单位为mg∙L-1;NH4+-N为氨氮浓度,单位为mg∙L-1;T为温度,单位为℃。
FNA的计算公式[20]:
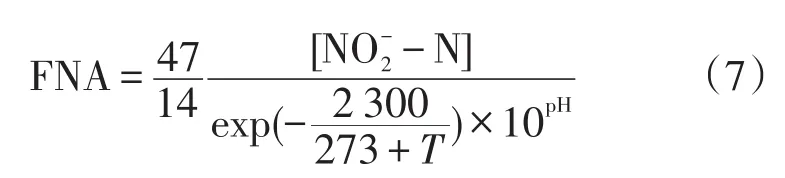
式中:FNA为游离亚硝酸浓度,单位为mg∙L-1;NO2--N为亚硝态氮浓度,单位为mg∙L-1。计算后得到FA和FNA浓度随HRT变化如图7。
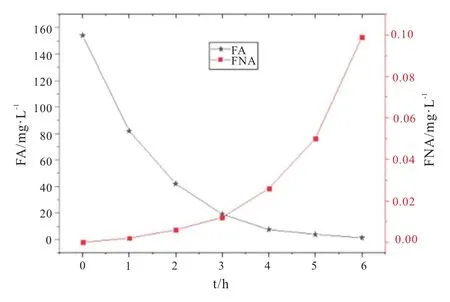
图7 FA和FNA随HRT变化图
从图7可以看出,随着HRT增加,FA与FNA急剧变化:由于氨氮浓度和pH的下降,FA浓度急剧下降,由于pH的下降和硝态氮浓度的上升,FNA浓度快速上升。反应器内FA与FNA达到一定浓度后,对AOB和NOB均能产生抑制作用[21]:FA>0.1 mg∙L-1时,FA 就会对 NOB 产生抑制作用;当FA>6 mg∙L-1时,NOB几乎被完全抑制;FNA>0.02 mg∙L-1,FNA会对NOB产生抑制作用。本实验反应器出水的FA浓度为1.04 mg∙L-1,说明反应器内的FA一直对NOB有抑制作用,反应后期FA对NOB的抑制作用减弱。反应器内FNA在HRT≥4 h时才能达到抑制浓度。综上可知,反应器内FA和FNA均对NOB产生了抑制作用,但FNA仅在反应后期起到抑制作用,而FA则全程起到抑制作用。
2.5 反应器出水的三维荧光分析
2.5.1 三维荧光分析方法
首先设定F-7000荧光分光光度计的参数:激发波长EX设为250~450 nm,发射波长EM设为300~550 nm,扫描间隔均为 5 nm[22]。使用 Matlab2018b进行数据处理时,需要消除拉曼散射和瑞利散射的影响,此外在常温条件下,不同组分的三维荧光光谱的荧光峰容易相互重叠,仅用肉眼观察荧光光谱图误差较大。
平行因子分析法是一种用于解析多维数据的化学计量学方法,常被用于分离三维荧光光谱(excitation-emission-matrix,EEM)中重叠的荧光峰,是解析EEM的常用方法[23]。在运用平行因子分析法中,为确保分离出的荧光峰准确可靠,首先便通过残差分析和核心一致度分析确定光谱组分数。
2.5.2 三维荧光分析结果
图8为出水水样的残差分析及核心一致度分析结果,可以确定出水中的可溶性有机物由2个光谱组成。
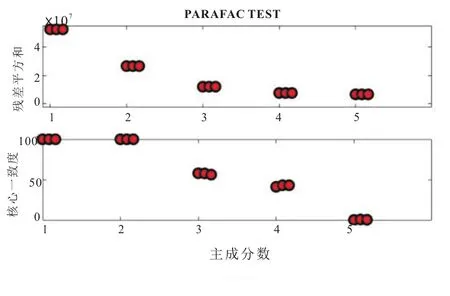
图8 残差分析及核心一致度分析图
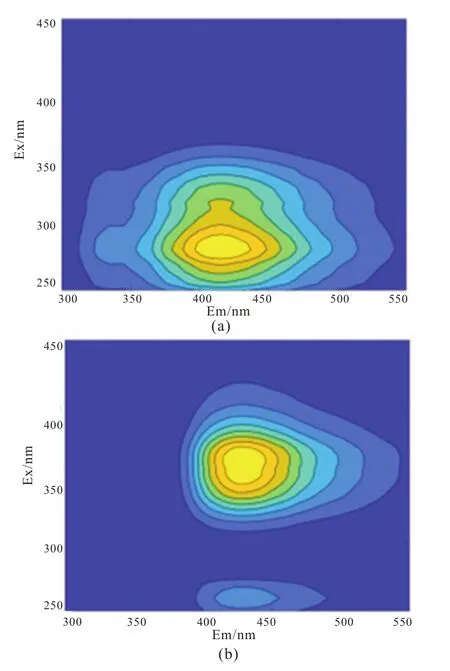
图9 平行因子法分析结果。(a)类腐殖酸荧光物质;(b)类富里酸荧光物质
在确定组分数为2后分离得到EEM中的两个荧光峰如图9,最大激发/发射波长射波长位于280 nm/420 nm的,属于类腐殖酸荧光物质,最大激发/发射波长位于355 nm/430 nm的,属于类富里酸荧光物质[24]。说明类腐殖酸和类富里酸是出水水样中的荧光主要组分。
3 小结
本文提出了一种高氨氮废水短程硝化启动的方法,对每个阶段的操作及实验结果进行了描述。在进水pH=9.0时(氨氮浓度为243 mg∙L-1),氨氮去除率和NAR均能达到较高水平,在此基础上投加NaHCO3能进一步提高氨氮去除率和NAR。平行因子法分析结果表明类腐殖酸和类富里酸是反应器出水的荧光主要组分。在反应过程中,FA急剧下降,FNA急剧上升。FA全程对NOB起到抑制作用,这就是进水高氨氮浓度更有利于AOB积累的原因,FNA仅在反应后期起到抑制作用。

