某三甲综合医院346例抗肿瘤药物致不良反应报告分析
徐伟佳,高 勇,叶美玲,蔡 林(.中国人民解放军联勤保障部队第94医院药剂科,广西 桂林 5400;.中国人民解放军联勤保障部队第94医院卫勤处,广西 桂林 5400)
抗肿瘤药物因其毒性大、安全范围窄,出现相关严重的药品不良反应(adverse drug reaction,ADR)报告的频次高于其他药物[1]。我院为一家三甲综合医院,近年来加强了对抗肿瘤药物的监测,本文提取我院抗肿瘤药物相关ADR报告进行回顾性分析,旨为临床安全用药提供参考。
1 资料与方法
基于我院2013–2018年收集的3125例ADR报告,从中提取抗肿瘤物及相关药品致ADR报告共计346例(11.07%),采用Excel软件统计数据,按国家ADR监测中心分类方法,对患者年龄及性别、药品种类、给药途径、ADR累及系统/器官及临床表现、ADR发生时间、ADR分级和转归等进行回顾性分析。
2 结果
2.1 性别与年龄分布
346例ADR报告中,女性患者212例(61.27%),男性患者134例(38.73%)。年龄最大者87岁,最小者16岁。根据世界卫生组织年龄段划分标准[2]统计,最多的为中年人(45~59岁)占43.64%,其次为年轻老人(60~74岁)占26.59%,青年(18~44岁)占23.41%。详见表1。
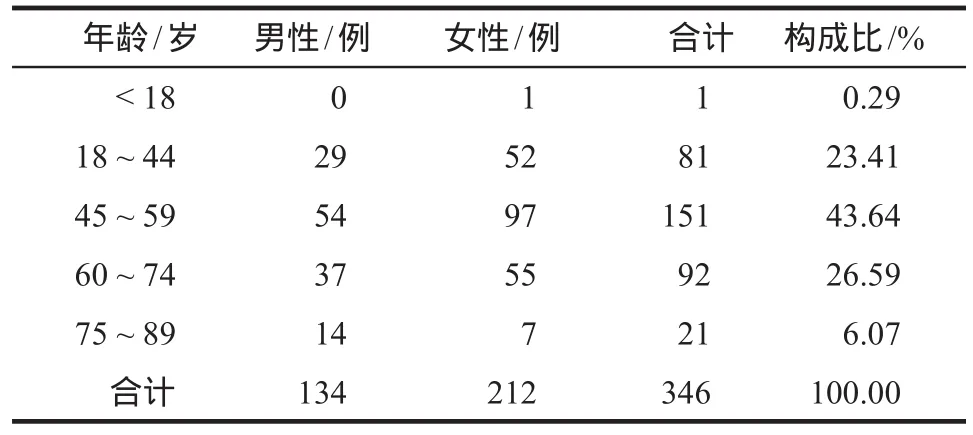
表1 患者年龄与性别分布Tab 1 Distribution of the gender and age in patients
2.2 药品种类分布
346例ADR报告中,共有429条用药记录,涉及8个类别54个品种。详见表2(“主要代表药物”列举该种类中ADR频次排名前3位的药物)。
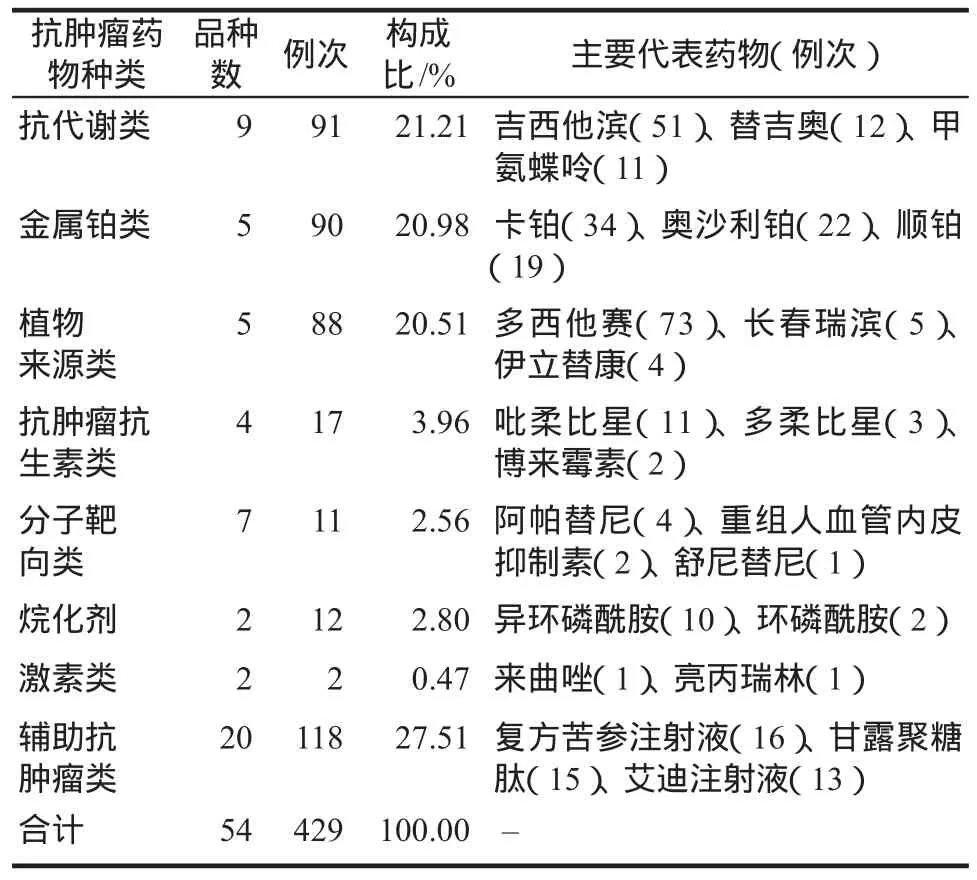
表2 引发ADR的抗肿瘤药物种类及主要代表药物Tab 2 Classification of antineoplastic drugs causing ADR and main representative drugs
2.3 ADR累及系统/器官和临床表现
部分ADR涉及2个以上系统,按临床表现出现1次为1例次计,统计出ADR具体临床表现为369例次,详见表3。
2.4 ADR给药途径与发生时间
因部分ADR有并用药品,346例ADR涉及药物429例,静脉给药占85.08%,口服给药占12.82%,其他给药途径包括腹腔注射、胸腔注射、肝动脉给药等共占2.10%。患者ADR发生时间主要在2 h内。详见表4。
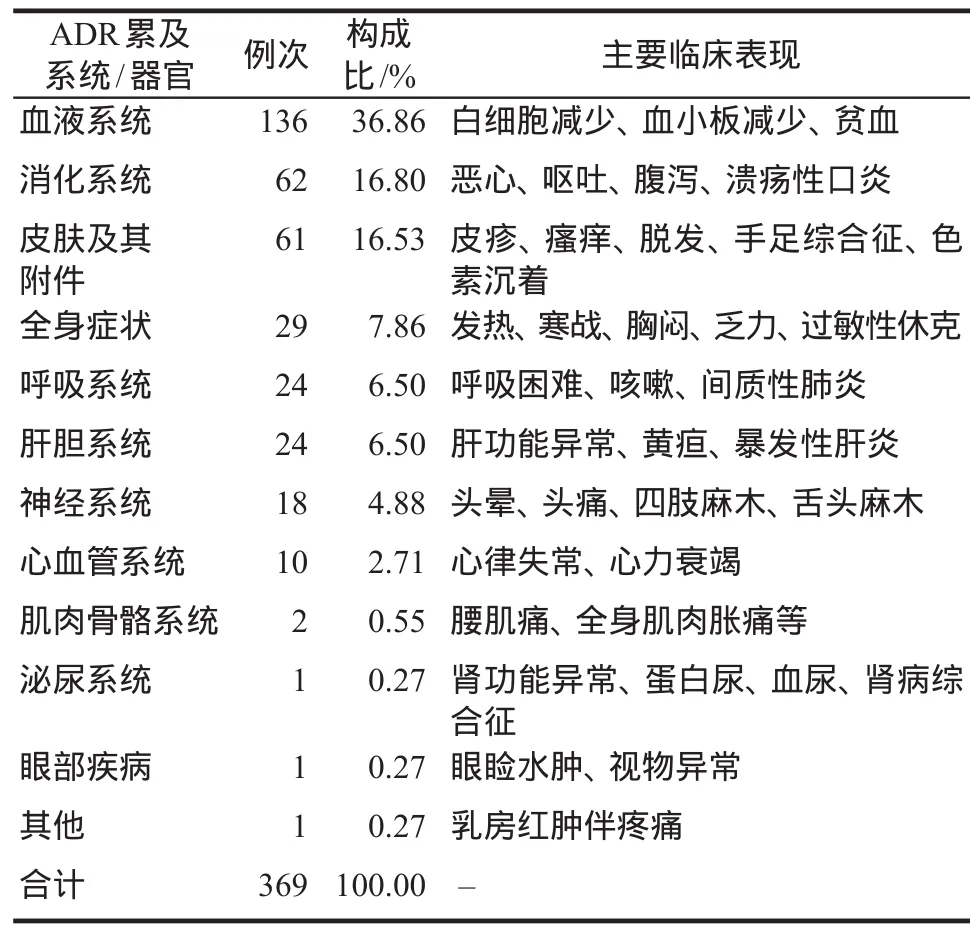
表3 ADR累及系统/器官及临床表现Tab 3 Distribution of systems/organs involved in ADR and clinical manifestations
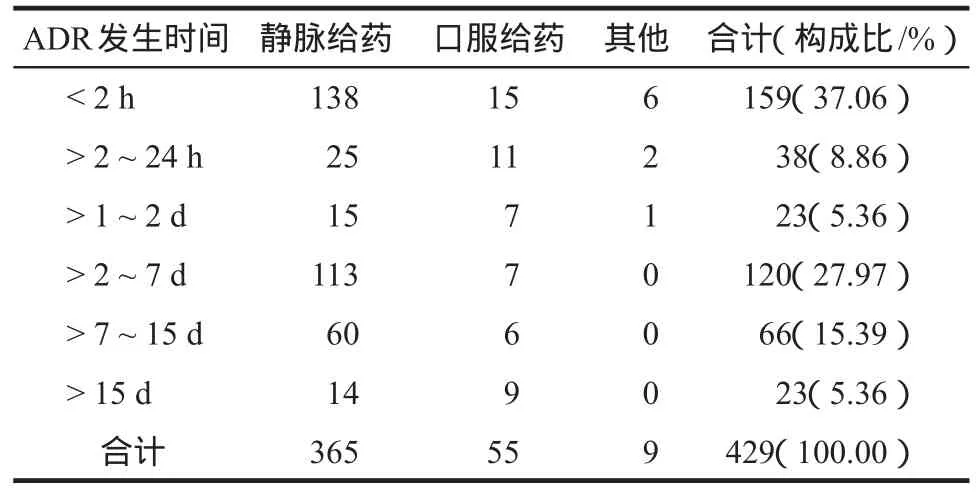
表4 ADR给药途径与发生时间分布Tab 4 Distribution of administration route and occurrence time
2.5 ADR分级与转归
346例ADR报告中,新的ADR 6例(1.73%),严重的ADR 64例(18.50%),新的且严重的ADR为1例(0.29%)。多数ADR转归较好,自愈40例(11.56%),痊愈及好转271例(78.32%),未好转33例(9.54%),有后遗症1例(0.29%),死亡1例(0.29%)。
2.6 关联性评价情况
关联性评价结果为:肯定76例(21.97%)、很可能199例(57.51%)、可能71例(20.52%)。
2.7 报告主体
346例ADR主要来源于临床医师188例(54.34%),其次为药师129例(37.28%),护士29例(8.38%)。
3 讨论
3.1 ADR与性别、年龄分布的关系
346例ADR报告中,女性比例高于男性,可能与女性体内药动学特点、生理因素以及对药物毒性更敏感有关[3]。故建议给女性患者用药时,应考虑到生理期、女性激素水平等特殊情况调整给药方案。从年龄分布看,ADR可发生于任何年龄组的患者,报告最多的年龄段为中年人。其分布特点如下:1)与肿瘤好发年龄段大致相符[4];2)由于中老年患者的器官功能退行性改变,常伴有其他基础疾病,加上肿瘤及放化疗的消耗,更易出现药物蓄积;3)中老年患者缺乏用药常识,用药依从性较差,更易发生ADR。故建议给中老年患者使用抗肿瘤药物时,应详细询问病情,根据其病理生理特点进行个体化调整。
3.2 药物种类
346例ADR报告中,抗代谢类、铂类、植物来源类基础化疗药物在临床应用广泛,药物毒性较大,故ADR发生率更高。如多西他赛的稳定微管作用比紫杉醇大2倍,有更高的生物利用度和细胞内浓度,更易发生ADR。
我院的靶向药物相关ADR涉及吉非替尼相关的皮肤破溃出血,舒尼替尼相关的严重腹泻,阿帕替尼相关的高血压,安罗替尼相关的咯血等。其他靶向药物相关的ADR也应引起药师关注并做好药学监护,如曲妥珠单抗的心脏毒性、贝伐单抗相关的栓塞性疾病,以及其他靶向药物引起的皮肤毒性等。
3.3 累及系统/器官和临床表现
346例ADR主要累及系统/器官的为血液系统、消化系统、皮肤及其附件等。抗肿瘤药物通常对高增殖细胞无选择性抑制,骨髓、消化道黏膜因其细胞增殖活跃更容易受累[5],且我院使用率较高的品种(如多西他赛、吉西他滨、卡铂)有明显骨髓抑制作用,具体表现包括白细胞减少、血小板减少、贫血等,常影响下一周期化疗,甚至危及生命。因此应注重化疗前后的血液学监测,及时对症支持治疗;对粒细胞缺乏伴发热者应参照指南及时防治感染;对既往有严重骨髓抑制的患者,应调整化疗药物剂量。
3.4 ADR的给药途径与发生时间
346例ADR的给药途径主要为静脉给药,这主要与抗肿瘤药物多以静脉给药相关。静脉给药时药物直接、迅速地进入体内循环,刺激性大,并受药物浓度、滴速、注射剂微粒、赋形剂以及药物的配制过程等因素影响[6]。建议对护士加强药物配置过程、药品贮存等方面的宣教。口服药物经肝脏首过消除后引起的ADR程度较轻,且口服化疗药的患者常带药出院,不易监测ADR,提示应加强口服抗肿瘤药的教育和监测。
ADR可发生于各时间段,但各系统对抗肿瘤药物敏感性及代偿性不同,如皮肤、胃肠道相关的ADR出现较早;而骨髓有一定的代偿能力,其ADR发生较晚[7]。总体来看ADR发生时间集中在2 h内,因部分ADR主要为静脉给药,涉及过敏反应、消化道反应、全身症状等急性反应,更易造成患者心理影响。对此,药学监护可从预处理药物的应用、药物溶媒、浓度、滴速、药物避光等方面展开。本研究中发生时间较晚的ADR包括吉非替尼引起的足趾破溃(240 d)、吡柔比星+异环磷酰胺引起的皮肤色素沉着和肝功能异常(150 d)、卡培他滨引起的恶心呕吐(90 d)等,主要与长期用药和毒性蓄积相关,又因治疗需要定期化疗不宜停药,故延长了ADR持续时间,影响患者生活质量,需要加强监护。
3.5 新的与严重的ADR
新的ADR主要有曲妥珠单抗致乳房红肿,停药4 d后缓解;奥沙利铂致大便干结难解,痔疮出血;斑蝥酸钠注射液用药后发热、寒战,予异丙嗪静滴20 min后缓解;培美曲塞致心动过速等。新的ADR数量少,一是基础抗肿瘤药物的不良反应在说明书或文献记载已较全面,二是ADR症状有时难与肿瘤疾病表现相区分,常需要药师协助临床鉴别与救治。
1例死亡患者为55岁女性,静脉滴注培美曲塞11 h后出现胸闷、呼吸困难、窦性心动过速抢救无效后死亡。其他严重的ADR还有吉西他滨致严重骨髓抑制、伊立替康致严重腹泻、阿帕替尼致血压升高等。药师建议针对发生过严重ADR的药物,应在化疗前排除相关的基础疾病,制定应急预案积极抢救。
3.6 多层次发挥药师作用
一是争取医院领导和临床科室领导的重视,发挥药学部门的主导作用,完善管理制度,优化工作流程。加强对高危品种、长期用药、严重ADR、新的ADR的监测,多方发挥药师作用。
二是调动医、药、护全员参与ADR工作的积极性。ADR上报主体大部分来自医师,其次是药师和护士。我们鼓励各岗位药师积极参与ADR工作,临床药师查房时易发现住院患者的ADR,门诊药师收集门诊ADR信息更便利,住院药房药师下科服务协助临床上报ADR。这不仅提高了ADR报告的数质量,还缓和了医患矛盾,塑造良好的药师形象[8]。
三是做好抗肿瘤药物的贮存与保管,注意控制温湿度、避光等。特别是对光不稳定的药物,如奥沙利铂、环磷酰胺、甲氨蝶呤、氟尿嘧啶、丝裂霉素、羟基喜树碱等,应使用避光的药柜存放,并注意与护士交接发药。
四是做好对临床医务人员的宣传与培训。药师收集最新药物信息,通过药讯、讲座等方式开展ADR宣教,协助临床鉴别、防治ADR。
五是协助临床制定化疗方案。药师可以从选药、剂型、滴速、浓度、溶媒、给药顺序等方面,协助医师制定个体化方案,例如:①选药:多西他赛或吉西他滨需与铂类联用时,因卡铂的骨髓抑制较强,建议改用顺铂或奈达铂;②溶媒:奥沙利铂禁用0.9%氯化钠注射液稀释;③给药顺序:紫杉醇和顺铂联用时,紫杉醇须在顺铂前输注,否则骨髓抑制加重;④滴速:输注速度宜快的药物建议控制时间为:吡柔比星30~60 min,卡铂15~60 min,吉西他滨30 min等;滴速宜慢的药物建议控制时间为:氟尿嘧啶6~8 h,紫杉醇3~5 h,奥沙利铂2~6 h等。
六是加强对患者的药学照护,促进抗肿瘤药物合理用药。加强做好口服化疗药和预处理药物(如培美曲塞、多西他赛、紫杉醇等)的用药教育,提高患者用药依从性。如多西他赛用药前1天开始口服地塞米松8 mg,bid,连用3 d;如奥沙利铂用药期间应避免冷水漱口或接触低温物品等。

