EB病毒gp350/220抗原T-B联合表位生物信息学预测
彭 菁,李 蓓,吴移谋
(1.南华大学附属第二医院,湖南 衡阳 421001;2.南华大学衡阳医学院病原生物学研究所, 湖南 衡阳 421001)
19世纪50年代,在非洲疟疾流行区域,Burkitt发现少数儿童患有B细胞淋巴瘤;在1964年,Epstein、Achong和Barr在培养的Burkitt淋巴瘤细胞中观察到一种疱疹病毒。EB病毒(Epstein-Barr virus,EBV)定殖于人的鼻咽部并且在上皮细胞内增殖,进一步感染B淋巴细胞,而B淋巴细胞通过血液循环到各个组织和器官,从而引起全身感染,而这些感染EBV的淋巴细胞潜伏于人体内,当自身免疫力低下时会引起一系列的临床症状[1]。在不同的感染时期表达的抗原不同,如潜伏期感染主要是表达潜伏膜蛋白和核抗原,而增殖期感染主要表达EBV膜抗原和EBV衣壳蛋白等。EBV感染具有地方特点,在我国南方广州及东南亚为鼻咽癌高发地区,而在其它一些地方如儿童初次感染EBV会引起急性淋巴组织增生性疾病也就是传染性单核细胞增多症,其主要的临床表现为外周血中单核细胞和异型淋巴细胞大量增多[2-5]。疫苗是预防EBV感染最有效的方法,但我国研制的基因重组疫苗正在观察中。目前对EBV感染尚缺乏肯定疗效的抗病毒药物。阿昔洛韦用药期间,能减少EBV从咽部排毒,但不能改善传染性单核细胞增多症的症状,对免疫缺陷患者中的EBV淋巴瘤治疗也无效。
防治EBV最具前景的途径是EBV疫苗[6]。最近研究发现EBV膜蛋白gp350/220抗原作为靶抗原既能刺激机体产生中和性抗体,也能起到体液免疫保护作用,同时通过研究发现gp350/220抗原能和细胞毒性T细胞发生强烈的反应[7],说明该抗原具有T细胞表位,既能产生体液免疫又能产生细胞免疫,这样对EBV的控制起重要作用,这进一步说明此抗原靶抗原在诱导特异性体液免疫保护的同时,还能通过细胞免疫途径控制EBV在体内的反复增殖。目前,EBV的预防性疫苗主要是针对gp350/220的,代表性的葛兰素史克公司研发的gp350/AS04疫苗已完成Ⅱ期临床试验,结果显示,该疫苗对预防由EBV引起的传染性单核细胞增多症的发生有显著的抑制作用,但仍未取得预期的理想效果。因而对EBV gp350/220氨基酸序列中的优势表位进行预测和筛选,将有助于研发针对EBV的高效价优势表位疫苗。本研究拟以EBV gp350/220氨基酸序列为基础,利用蛋白序列分析软件,分析gp350/220的信号肽、二级结构、B细胞表位和T细胞表位,寻找T-B联合表位,为进一步研制高价优势表位疫苗奠定基础。
1 材料与方法
1.1 EBV gp350/220氨基酸序列
EBV gp350/220氨基酸序列检索来自Gen Bank,来源于B95.8细胞株,共由291个氨基酸残基组成,蛋白质序列编号为ADN85210.1。
1.2 gp350/220氨基酸序列跨膜序列的分析
运用TMHMM Sever2.0软件对gp350/220氨基酸序列的跨膜结构进行分析。
1.3 gp350/220抗原二级结构预测
运用SOPMA Sever软件预测gp350/220的蛋白二级结构。
1.4 gp350/220抗原B细胞和T细胞表位预测
运用在线预测网站IEDB等参数对EBV gp350/220抗原的B细胞表位进行预测,运用SYFPEITHI在线预测对EBV gp350/220抗原的T细胞表位进行预测。
1.5 EBV gp350/220抗原T-B联合表位的筛选
运用DNA man软件比对筛选出EBV gp350/220抗原T-B联合表位。
2 结 果
2.1 查找Gen bank EBV gp350/220抗原的氨基酸序列
gp350/220抗原共有291个氨基酸残基编码,序列为:getspqanttnhtlggtsstpvvtsppknatsavttgqhnitssst
ssmslrpssisetlspstsdnstshmplltsahptggenitqvtpaststhhvsts
spaprpgttsqasgpgnsststkpgevnvtkgtppknatspqapsgqktavp
tvtstggkansttggkhttghgartstepttdyggdsttprtrynattylppstsse
lrprwtftsppvttaqatvpvpptsqprfsnlsmlvlqwaslavltlllllvmadc
afrrnlstshtyttppyddaetyv。
2.2 运用TMHMM Sever2.0对gp350/220的跨膜序列进行分析
gp350/220的跨膜区在247-269位区域,其中1-246位区域显示为膜外区,270-291为膜内区(图1)。
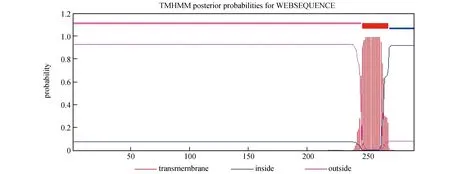
图1 TMHMM分析gp350/220的跨膜结构
2.3 gp350/220抗原蛋白质二级结构预测
利用SOPMA Sever对gp350/220抗原进行预测,发现该抗原柔性结构占氨基酸总数的87.63%(图2)。通过对gp350/220抗原的291个氨基酸各参数预测的结果,最终确定gp350/220的潜在B细胞抗原表位区域,如表1和图3。
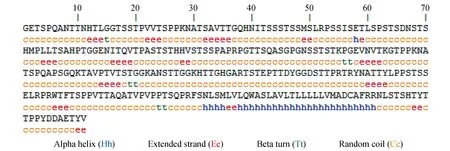
图2 SOPMA分析的gp350/220二级结构

表1 运用不同方法预测EBVgp350/220蛋白B细胞表位的肽段位置
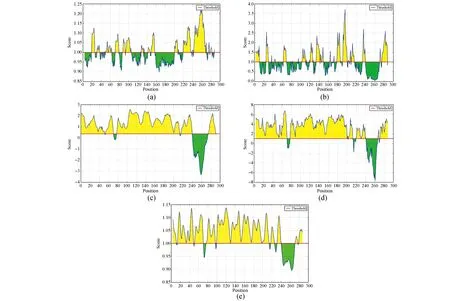
图3 IEDB分析的gp350/220的B细胞抗原表位A:Kolaskar & Tongaonkar Antigenicity Prediction Kolaskar & Tongaonkar的抗原性指数预测;B:Emini Surface Accessibility Prediction Emini表面可及性指数预测;C:Bepipred Linear Epitope Bepipred线性表位预测;D:Parker Hydrophilicity Prediction Parker亲水性指数预测;E:Karplus & Schulz Flexibility Prediction Karplus & Schulz 柔韧性区域预测
2.4 T细胞表位预测结果
运用SYFPEITHI预测gp350/220抗原T细胞表位,在进行T细胞表位的预测后,选取了分值高的12个T细胞抗原表位,预测的结果见表2。
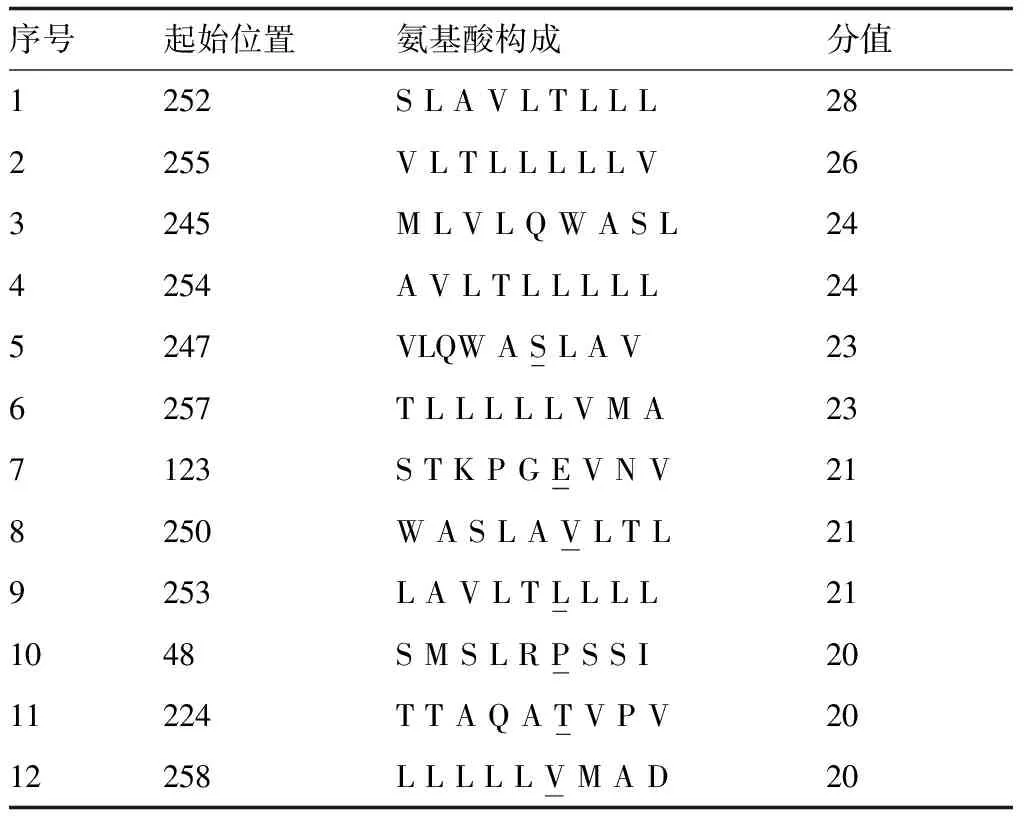
表2 SYFPEITHI预测的MHCⅠ类HLAA 0201限制性T细胞表位
2.5 运用DNAman软件中的多重序列对比T、B细胞表位
T-B联合表位为52-59 92-98 110-115,见表3。
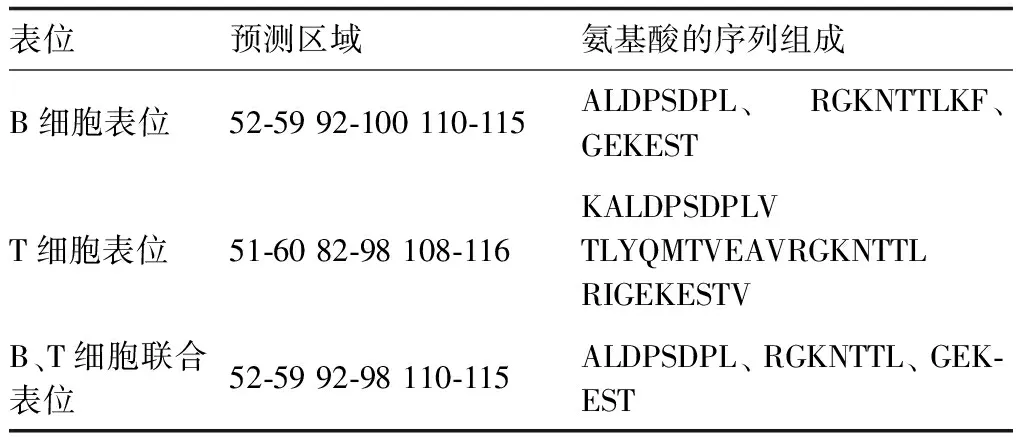
表3 B细胞与T细胞的联合表位
3 讨 论
EBV为DNA病毒,主要感染淋巴细胞,人是该病毒的宿主,主要通过唾沫传播,以儿童感染多见,感染之后基本都能产生抗体。EBV包膜上的gp350抗原可以与B淋巴细胞表面的细胞因子结合而感染B淋巴细胞[8],这些细胞大量进入血液循环而造成全身性感染,并可长期潜伏在人体淋巴组织中。
目前预防EBV感染行之有效的的方法还是使用疫苗预防为主,一种制备疫苗的新型策略,即基于已知核苷酸或氨基酸序列,利用计算机软件辅助分析,或利用噬菌体展示技术,确定和筛选可能的优势表位,然后人工合成或借助基因工程技术而制备含优势表位的多肽疫苗。
目前EBV疫苗的研究主要集中于包膜糖蛋白gp350,研究发现gp350于CD21结合而感染细胞且此蛋白是EBV和被感染细胞上最多的糖蛋白,同时能通过体液免疫产生抗体来预防EBV感染。李文姝等[9-12]制备了gp350重组疫苗应于临床研究,实验发现该疫苗有效保护率能够达到78%左右,同时能够产生EBV抗体且抗体在体内发挥保护作用时间可以长达18个月左右,说明此疫苗具有良好的抗原性和免疫原性。
近几年来新兴起来的一种重要的疫苗即重组表位疫苗[13]。本研究通过以gp350抗原的优势表位构建表位疫苗,其中包括B细胞表位和T细胞表位,B细胞表位(决定簇),是由抗原表面的亲水性氨基酸组成,易于接近B细胞受体(BCR)和抗体分子并被识别,一般由3~5个在空间上相邻的、连续的或者不连续的氨基酸残基组成。前者称线性表位或连续表位,后者为肽链折叠后形成,称为构象表位或者不连续表位。T细胞表位指被T细胞受体(T-cell receptor/TCR)识别的抗原表位,表位成分为蛋白质降解后的多肽,多存在于抗原分子内部,需要经过抗原递呈细胞(antigen presenting cells/APC)加工后与MHC分子结合成为复合物才能被TCR识别。机体的免疫应答分为细胞免疫和体液免疫应答,在免疫应答中抗原分子表面的B细胞表位和T细胞表位分别被B、T细胞表面的BCR和TCR识别,从而诱导出高度特异性的体液免疫和细胞免疫,产生特异性的免疫效应[14-15]。
本研究通过对gp350蛋白氨基酸序列等参数的预测发现膜外区域和柔性区域占该蛋白的绝大部分区域,而抗原表位的形成基本在转角及无规卷曲结构较松散,易扭曲、盘旋并展示在蛋白表面和该蛋白的膜外区域,从而有利于抗体结合,为B细胞表位提供依据。同时对gp350蛋白的T细胞表位进行预测,20分以上的T细胞表位有12个,T细胞表位,尤其是CTL表位在清除肿瘤和细胞内感染病原体的特异性免疫反应中起主要作用,而针对肿瘤抗原或感染靶细胞特定靶点的B细胞介导的体液免疫反应,则发挥如中和、调理和ADCC作用等。因此,理想的疫苗在设计上要同时考虑T细胞表位和B细胞表位。
本研究发现gp350蛋白的B细胞表位和T细胞表位的3个重叠区域为52-59、92-98、110-115。本研究目的是为开发具有较强的免疫原性的高效疫苗,作为理想的免疫原,抗原分子中应包含目的抗原的B细胞表位和自身或外源T细胞表位,可诱导出高度特异性的体液免疫和细胞免疫反应,同时从体液免疫和细胞免疫水平起到预防或治疗作用,为进一步研制高效多价疫苗奠定理论基础。

