中国汉族2型糖尿病人群体质量指数与血脂谱在糖尿病肾脏病中的交互作用
虞伟慧,胡珦,陈雄,周琦,邓慧慧,顾雪疆
(温州医科大学附属第一医院内分泌科,浙江温州325015)
糖尿病肾脏病(diabetickidneydisease,DKD)是糖尿病重要的微血管并发症之一,20%~40%糖尿病患者将进展到DKD阶段[1],它是引起终末期肾病的最常见原因[2]。随着我国糖尿病患病率的逐步上升[3],DKD的患病率也较前明显升高。研究表明血脂异常参与了DKD的发生与发展[4-7]。血浆甘油三酯(triglyceride,TG)、高密度脂蛋白胆固醇(high-densitylipoproteincholesterol,HDL-C)、TG/HDL-C比值、非高密度脂蛋白胆固醇(non-highdensitylipoproteincholesterol,nonHDL-C)/HDL-C比值与DKD相关,但未发现低密度脂蛋白胆固醇(low-densitylipoproteincholesterol,LDL-C)与DKD关联[8-11]。体质量指数(bodymassindex,BMI)不仅影响血脂水平[12],对DKD亦有影响[13-14]。目前尚未见到关于BMI和血脂谱的交互作用对DKD影响的报道。本研究旨在探讨BMI与血脂谱在DKD中的交互作用,为DKD高危人群的干预提供依据。
1 对象和方法
1.1 对象 本研究共纳入2017年3月至2019年3月温州医科大学附属第一医院收治的住院2型糖尿病患者647例,包括283例DKD患者以及364例非DKD的2型糖尿病患者。所有受试者均为汉族人。2型糖尿病的诊断依据1999年WHO标准(www.who.int/entity/diabetes/currentpublications/en)。DKD的诊断标准:估算的肾小球滤过率(estimatedglomerularfiltrationrate,eGFR)<60mL·min-1·(1.73m2)-1或24小时尿微量白蛋白≥30mg或尿白蛋白-肌酐比值(albumin-to-creatinineratio,ACR)≥30g/mg,同时排除其他肾脏疾病。本研究经医院伦理委员会批准。
1.2 方法 收集患者住院时的临床资料,包括空腹血浆葡萄糖、糖化血红蛋白(glycatedhemoglobinA1c,HbA1c)、总胆固醇(totalcholesterol,TC)、LDL-C、HDL-C、TG、肾功能、肝功能等生化指标、24小时尿微量白蛋白及ACR。同时测量患者身高、体质量、血压等人体学指标,计算BMI。nonHDL-C按弗洛斯特(Frost)公式计算:nonHDL-C=TC-HDL-C;同时计算nonHDL-C/HDL-C比值、LDL-C/HDL-C比值、TC/HDL-C比值以及TG/HDL-C比值。根据改良的MDRD公式计算eGFR[15]。
1.3 统计学处理方法 采用SPSS23.0统计软件进行数据分析。非正态分布的计量资料以M(P25,P75)表示,2组间比较采用两独立样本的非参数检验。2组间百分率的比较采用χ2检验。对各项血脂指标进行自然对数转换后进行分析。采用二分类logistic回归分析各项血脂指标与DKD的关联,同时分析BMI与血脂谱间的交互作用,交互作用的分析使用相乘模型。P<0.05为差异有统计学意义。
2 结果
2.1 基本临床性状分析 将所有受试者按照BMI分组,共包括正常体质量受试者(18.5kg/m2≤BMI<24kg/m2)265例及超重/肥胖患者(BMI≥24kg/m2)382 例。2组受试者的糖尿病病程、收缩压、舒张压、24小时尿微量白蛋白、尿酸、肌酐、TG、HDL-C、nonHDL-C、nonHDL-C/HDL-C、LDL-C/HDL-C、TC/HDL-C、TG/HDL-C差异均有统计学意义(P<0.05),此外正常体质量组与超重/肥胖组DKD的患病率差异有统计学意义(P=0.004),见表1。
2.2 血脂谱与DKD的相关性分析 采用二分类logistic回归分析血脂谱与DKD的关联,结果表明,TG、nonHDL-C、nonHDL-C/HDL-C、TC/HDL-C、TG/HDL-C均与DKD显著相关(P<0.05),OR针对各指标的自然对数计算,见表2。
2.3 BMI与血脂的交互作用分析 采用二分类logistic回归分析BMI与血脂谱的交互作用,发现BMI与TG、nonHDL-C/HDL-C、TC/HDL-C、TG/HDL-C之间的交互作用具有显著统计学意义(P 值分别为0.036、0.035、0.034、0.016),见表3。
为进一步明确血脂与DKD的关联在不同BMI人群中是否存在差异,本研究分别分析了正常体质量组及超重/肥胖组各血脂指标与DKD的相关性,结果显示血脂与DKD的关联在正常体质量组和超重/肥胖组存在异质性:TC/HDL-C与DKD在超重/肥胖组显著关联,在正常体质量组两者关联未达到显著统计学意义(见表3)。进一步以各血脂指标的四分位为界限各分为4组,结果亦显示血脂与DKD的关联在正常体质量组和超重/肥胖组存在异质性(见表4)。在超重/肥胖组,TG上四分位组DKD发生风险是下四分位组的2.131倍(95%CI:1.062~4.276,P=0.033);nonHDL-C/HDL-C上四分位组DKD发生风险是下四分位组的2.116倍(95%CI:1.050~4.265,P=0.036);LDL-C/HDL-C上四分位组DKD发生风险是下四分位组的2.284倍(95%CI:1.148~4.544,P=0.019)。但在正常体质量组,未见到上述三项血脂指标与DKD显著相关。TG/HDL-C在超重/肥胖组及正常体质量组均与DKD显著相关(P值分别为0.028及0.033)。
3 讨论
作为糖尿病的重要微血管并发症之一,DKD的患病率日趋上升,已在全球范围内造成严重的疾病负担和医疗卫生经济负担。除高血糖、高血压等传统危险因素外,血脂、肥胖等因素在DKD的发生发展中也具有重要作用。对DKD相关危险因素及其交互作用的探讨,有利于为DKD的防治提供理论依据。

表1 2组研究对象基本临床特征
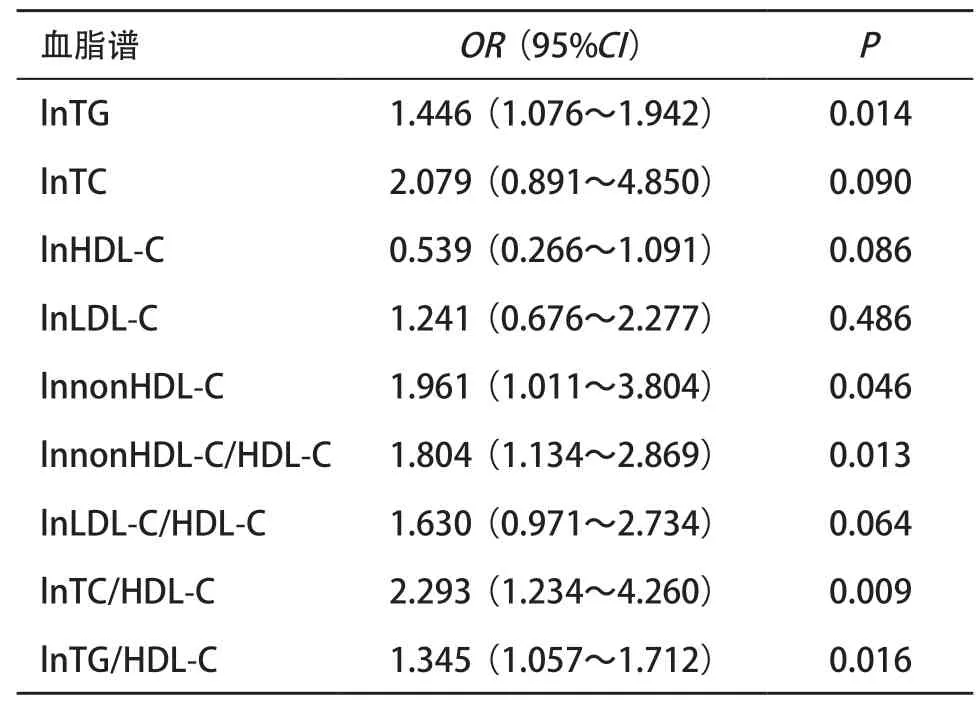
表2 血脂谱与DKD的相关性分析
既往大多数研究均提示高TG水平、低HDL-C水平与DKD风险增高相关联[8-11,16-18]。ZOPPINI等[16]对1987例门诊基线肾功能正常或接近正常的2型糖尿病患者随访5年后发现,HDL-C水平越高,患者发生慢性肾功能不全的风险越小。意大利一项大型糖尿病人群的回顾性观察研究表明,TG≥150mg/dL的糖尿病患者其低eGFR风险增加26%,白蛋白尿风险增加19%;而男性HDL-C<40mg/dL或女性<50mg/dL的糖尿病患者,低eGFR风险增加27%,白蛋白尿风险增加24%[17]。CHANG等[18]报道2型糖尿病患者中DKD的进展与高TG、低HDL-C水平相关,但是与高LDL-C水平不相关。本研究发现TG与DKD显著相关,但并未观察到HDL-C与DKD的关联。本研究亦发现nonHDL-C、nonHDL-C/HDL-C、TG/HDL-C均为DKD的危险因素,这些结果与YUN等[19]、邹健等[10]、YANG等[11]、PAN等[20]的研究结果相类似。此外,本研究发现TC/HDL-C与DKD独立相关。
BMI与血脂水平紧密相关,同时对DKD的发病风险也有一定影响[13-14]。然而,目前尚未见到有研究探讨BMI对血脂谱与DKD间关联的影响,本研究通过二分类logistic回归分析发现BMI与TG、nonHDL-C/HDL-C、TC/HDL-C、TG/HDL-C均存在显著交互作用。血脂谱与DKD的相关性在正常体质量组和超重/肥胖组间不一致:TC/HDL-C、TG、nonHDL-C/HDL-C、LDL-C/HDL-C均仅在超重/肥胖组与DKD显著关联。这说明BMI可能影响血脂谱对DKD的效应。

表3 2组血脂谱与DKD的相关性分析

表4 2组血脂谱(四分位数)与DKD的相关性分析
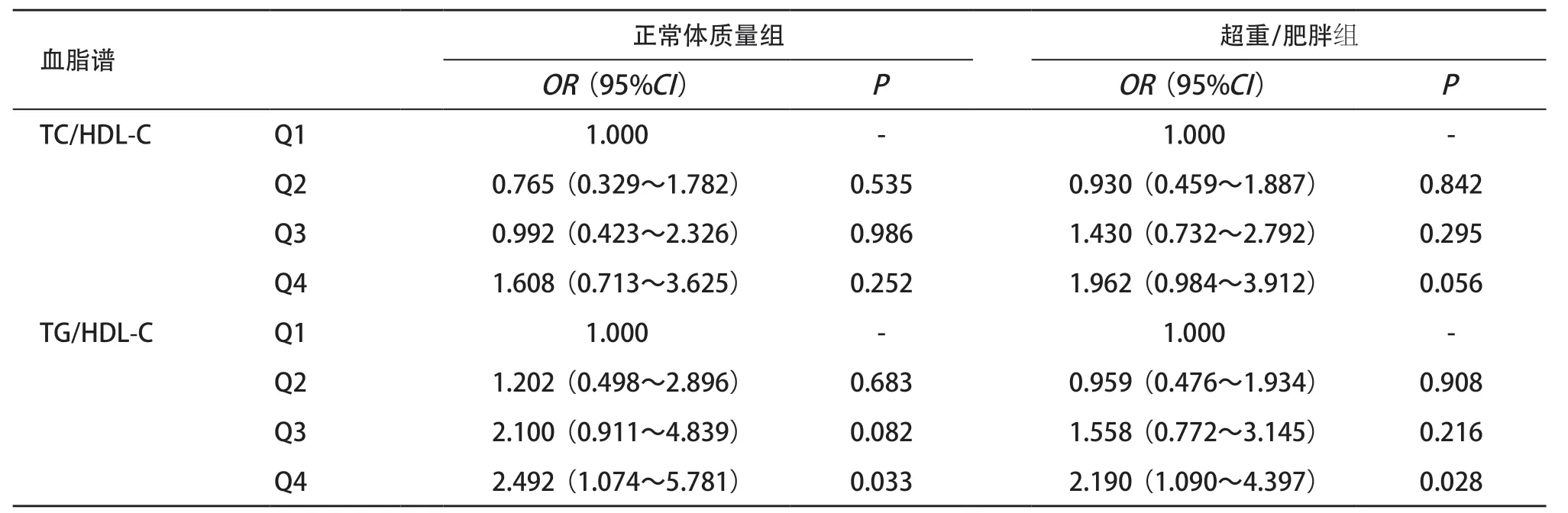
续表4
综上所述,中国汉族人群TG、nonHDL-C、nonHDL-C/HDL-C、TC/HDL-C、TG/HDL-C均为DKD的危险因素。BMI与TG、nonHDL-C/HDL-C、TC/HDL-C、TG/HDL-C之间存在交互作用,血脂谱与DKD的关联在正常体质量组与超重/肥胖组存在异质性,表明BMI可以影响两者间的关联。因此,超重/肥胖合并血脂谱异常的2型糖尿病患者更需及早预防DKD的发生发展。

