不同促排卵方案在多囊卵巢综合征患者IVF-ET 中的临床应用研究
夏怡,蒋军松
(右江民族医学院,广西 百色)
0 引言
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是女性最常见及最复杂的激素紊乱疾病之一,多囊卵巢综合征影响15% 的育龄期女性[1],也成为无排卵性不孕的主要原因。根据鹿特丹标准诊断[2],具有三种特征中的两种即为确诊:(1)稀发排卵或无排卵;(2)超声提示多囊卵巢形态;(3)临床或生物学体征雄激素过多症。卵巢过度刺激综合征(ovarian hyperstimulation syndrome,OHSS)是PCOS 患者在辅助生殖治疗过程中进行促排卵治疗时出现的最严重及可能危及生命的并发症。据报道,相比GnRH-a 激动剂方案,GnRH-a 拮抗剂方案可降低OHSS 的发生率[3]。但目前关于长卵泡期长方案的相关研究及报道较少,本文回顾性分析PCOS 患者在行IVF-ET 早卵泡期长方案、GnRH 激动剂方案及GnRH 拮抗剂方案时OHSS 的发生率及临床结局。
1 研究资料与方法
1.1 研究对象
回顾性分析2018 年1 月至2019 年9 月在人民医院生殖中心进行IVF-ET 治疗PCOS 患者121 周期。PCOS 的诊断标准:(1)稀发排卵或无排卵;(2)超声提示多囊卵巢形态;(3)临床或生物学体征雄激素过多症。排除标准:(1)一侧卵巢缺失;(2)子宫畸形、子宫腺肌病、子宫肌瘤等超声所见子宫异常;(3)患有严重内科及内分泌疾病;(4)宫腔粘连;(5)有行IVF 助孕禁忌,并排除男方不孕因素。根据不同的方案分为三组:采用早卵泡期长方案组42 周期作为实验组,同期采用长效长方案组44 周期,拮抗剂方案组35 周期为对照组。
1.2 促排卵方案
1.2.1 早卵泡期长方案
在进入刺激周期前的早卵泡期予 Gn RH-a3.75mg 降调节28-30d 后查卵泡期长效长方案比较血清激素水平(FSH、E2、P、LH) 及 B 超了解降调节情况, 在达到降调节标准(B超检测双侧卵巢无功能性囊肿,子宫内膜厚度≤ 5mm,血清FSH<5IU/I,LH<5IU/I,E2<50ng/L) 后根据卵泡生长情况血清 E2 和 LH 水平调整 Gn 用量,必要时加用外源性 LH。相应地调整Gn 用量:直至HCG 注射日止。在3 个主导卵泡直径≥17mm 或2 个主导卵泡径线≥18mm 时HCG 触发,同时应综合考虑孕酮和雌二醇水平。
1.2.2 长效长方案
排卵正常患者于超促排卵的前1 周期月经第8-10d 开始B 超检测卵泡发育,直至确定排卵日后,于黄体中期(排卵后5-7dP>5ng/ml)使用降调节药物GnRH-a;排卵障碍的患者于月经第3-5d 开始口服避孕药,每日1 片,口服避孕药余4-6片时使用GnRH-a 行双降调。使用GnRH-a 前应B 超检查若无直径≥10mm 的残余卵泡或黄素华化卵泡或其他生理性囊肿方可使用。垂体达到降调节标准LH<31U/L、E2<50ng/L、P<1ng/ml、内膜<5mm、双侧卵巢卵泡直径均<10mm、无功能性囊肿。GnRH-a 的用量,长方案使用GnRH-a1.875mg、1.25mg、1.0mg、0.8mg 甚至更少量,单次注射。垂体达到降调节标准后14-18d 达到降调节标准,开始给予Gn。当至少3个优势卵泡直径达到18mm,每个优势卵泡(直径≥14mm)E2 水 平 为200-300pg/ml 时,给 予HCG 扳 机,HCG 剂 量4000-12000IU 或rHCG250μg,36-38h 后取卵。
1.2.3 拮抗剂方案
固定给药方案:月经2-3d 启动Gn, 在给予Gn 超促排卵后的第5-6d 加拮抗剂250μg,灵活给药方案:即根据卵泡的大小和LH 水平加用拮抗剂,一般选择主导卵泡直径达14mm 或15mm 时或者LH ≥10mIU/ml,或在优势卵泡直径>12mm 且血清雌二醇>300pg/ml 时。在3 个主导卵泡直径≥17mm 或2 个主导卵泡径线≥18mm 时HCG 触发,同时应综合考虑孕酮和雌二醇水平。
1.3 体外受精及妊娠判定
行IVF 后,ET 是在体外受精后培养48-72h 进行卵裂期胚胎移植,一般选择胚胎卵裂期(第3d)阶段及囊胚阶段(第5d)进行胚胎移植。取卵后及ET 后常规行黄体支持。胚胎移植后14d 查血HCG,确定是否妊娠(生化妊娠)。移植术后30dB 超检看见孕囊再次确定妊娠(临床妊娠)[4]。
1.4 统计学处理
2 结果
2.1 三组患者基本情况的比较
早卵泡期组女方年龄、FSH 值低于拮抗剂组(P<0.05),BMI 值 高 于 长 方 案 组(P<0.05),E2 值 低 于 拮 抗 剂 组(P<0.05),LH 均高于长方案组及拮抗剂方案组(P<0.05)。不孕年限、原发性不孕例数、继发性不孕例数、PRL、P 值三组方案比较无统计学差异(P>0.05)。
2.2 三组患者卵巢刺激临床指标比较
早卵泡期组Gn 天数高于拮抗剂组(P<0.05),获卵数高于长方案组及拮抗剂组(P<0.05)。Gn 用量及OHSS 发生率三组方案比较无统计学差异(P>0.05)。见表1。
表1 三组患者卵巢刺激指标比较
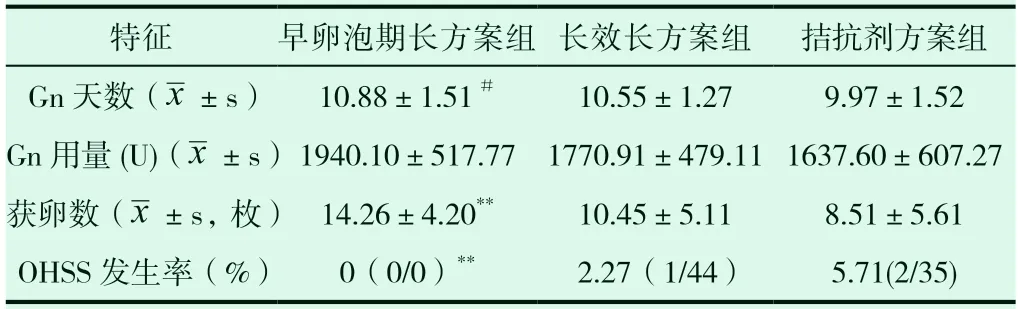
表1 三组患者卵巢刺激指标比较
注:**与长效长方案和拮抗剂方案比较,#与拮抗剂方案比较,P<0.05
特征 早卵泡期长方案组 长效长方案组 拮抗剂方案组Gn 天数(±s) 10.88±1.51# 10.55±1.27 9.97±1.52 Gn 用量(U)(±s)1940.10±517.77 1770.91±479.11 1637.60±607.27获卵数( ±s,枚) 14.26±4.20** 10.45±5.11 8.51±5.61 OHSS 发生率(%) 0(0/0)** 2.27(1/44) 5.71(2/35)
2.3 三组患者胚胎情况比较
早卵泡期组可利用胚胎枚数高于长方案组(P<0.05),优良胚胎枚数高于长方案组及拮抗剂组(P<0.05)。优胚率高于长方案组(P<0.05)。 OHSS 发生率低于长方案组及拮抗剂方案组(P<0.05)。Gn 用量三组无统计学差异。
2.4 三组患者妊娠结局的比较
早卵泡期组种植率高于长方案及拮抗剂组(P<0.05),流产率低于长方案及拮抗剂组(P<0.05),多胎率低于拮抗剂组(P<0.05),周期取消率高于拮抗剂组(P<0.05),周期总数、新鲜移植周期数、临床周期数三组方案比较无统计学差异。见表2。
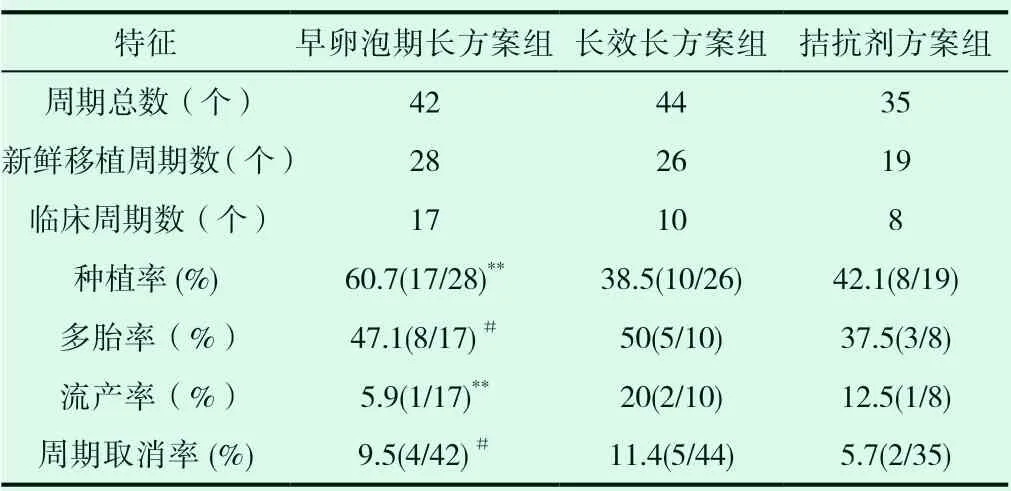
表2 三组患者妊娠结局的比较
3 讨论
多囊卵巢综合征(PCOS)是一种育龄期女性较为常见的内分泌疾病。雄激素受体和类固醇受体的共激活剂在PCOS患者的子宫内膜中过度表达及PCOS 患者常有高胰岛素血症[5]。故患有PCOS 的女性的子宫内膜容受性下降,甚至导致无法着床,移植失败。有研究认为早卵泡期长方案的应用可以改善患有PCOS 女性的子宫内膜的容受性[6],从而提高患者的着床率,从而改善妊娠结局[7]。OHSS 主要的病理特点为增加毛细血管的通透性,从而导致液体潴留在第三间隙,造成血容量的减少及血液的浓缩[8]。之前较多的研究人员使用GnRH-a 拮抗药来降低OHSS 的发生率,为预防提前排卵及黄素华的发生,较多的研究将GnRH-a 激动剂和GnRH-a 拮抗剂与Gn 研究结果表明GnRH-a 拮抗剂方案较于GnRH-a激动剂,中重度OHSS 发生率降低,但也有部分研究表明两种方案在行IVF-ET 的 PCOS 患者中OHSS 的发生率无统计学意义[9]。有实验表明早卵泡期长方案的OHSS 较低[10]。本研究显示早卵泡期长方案组的OHSS 的发生率低于长效长方案组及拮抗剂方案组。本文具有局限性,本研究的例数较少,可能影响统计结果。
综上所述,PCOS 的不孕患者在行IVF-ET 助孕治疗时,选择早卵泡期长效长方案能提高PCOS 患者子宫内膜的容受性,进而提高种植率,改善妊娠结局。另一方面,早卵泡期长方案降低了OHSS 的发生率,降低了PCOS 患者行IVF-ET的风险[11,12]。

