Zn0.2Zr0.8Ox固溶体催化剂的制备及其催化甲醇合成性能
程文强, 宋夫交, 高 佳,2b, 葛 艳,2b, 许 琦
(1. 江苏大学 化学化工学院,江苏 镇江 212013; 2. 盐城工学院 a. 环境科学与工程学院; b. 化学化工学院,江苏 盐城 224051; 3. 江苏省挥发性有机化合物控制重点建设实验室,江苏 盐城 224051)
随着经济社会的不断发展,化石能源的大量燃烧导致了大气中的CO2浓度不断增加,其引起的温室效应严重危害了人们的生存与发展。因此如何减少CO2排放以及实现对其资源化的利用,一直是各国研究人员研究的重要课题[1-3],其中CO2加氢转化为甲醇的研究最为广泛。甲醇不仅是重要的有机化工原料,还是一种清洁燃料,目前,甲醇主要由合成气(H2/CO)转化,而将CO2加氢合成甲醇不但可以减少CO2的排放量,阻止温室效应的进一步恶化,还可以将CO2转化为甲醇,因此该研究具有极其重要的经济价值和现实意义[4-7]。
Cu/ZnO/Al2O3催化剂广泛应用于低压合成气制甲醇,但铜基催化剂在CO2加氢合成甲醇反应中催化活性较低,由于逆水煤气反应(RWGS)的发生导致甲醇选择性低,且反应生成的水加速了催化剂中铜活性组分的烧结团聚[8-12]。近期,中国科学院大连化学物理研究所李灿院士课题组[13]开发了一种双金属固溶体氧化物催化剂ZnO-ZrO2,在近似工业条件下CO2单程转化率超过10%,甲醇选择性达到90%,该固溶体催化剂的合成与制备为CO2加氢制甲醇开辟了新的研究方向。
针对甲醇催化剂的制备工艺研究,房德仁等[14]研究表明了延长催化剂制备过程中老化时间有利于增大催化剂的比表面积,从而提高催化活性。国海光等[15-16]研究了不同的沉淀方法对铜基甲醇合成催化剂性能的影响,研究表明不同沉淀方法(分步沉淀法、并流沉淀法、两步沉淀法、反加沉淀法和正加沉淀法)制备的催化剂的活性不同,其中分步沉淀和并流沉淀法制备的催化剂活性最高。程鹏泽等[17]研究了不同沉淀剂(NH3·H2O、NaHCO3和Na2CO3)对CO2加氢合成甲醇催化剂Cu/ZnO/ZrO2性能的影响,通过催化剂表征证明了用NaHCO3和Na2CO3作沉淀剂,有利于形成铜锌固溶体,增强CuO-ZnO间相互作用力,从而降低催化剂的还原温度,改善催化活性。
本文对固溶体催化剂制备工艺条件作了进一步优化,以Na2CO3为沉淀剂,采用并流共沉淀法制备了一系列不同Zn/Zr摩尔比的双金属氧化物催化剂。其结构和性能经XRD、BET、Raman光谱、TEM和H2-TPR表征,并以CO2加氢制甲醇为目标反应,研究了催化剂的性能,并分析了反应温度和反应时间对催化剂活性的影响。
1 实验部分
1.1 仪器与试剂
X’Pert3Powder型X-射线衍射仪;Beckman Coulter SA3100型比表面积及孔径测定仪;2000型拉曼光谱仪;JEM-2100F型透射电子显微镜;AutoChem II 2920型化学吸附仪。
Zn(NO3)2·6H2O, Zr(NO3)4·5H2O,分析纯,国药化学试剂有限公司;其余所用试剂均为分析纯。
1.2 制备(以Zn/Zr=1/4为例)
在烧杯中依次加入Zn(NO3)2·6H2O 1.49 g、 Zr(NO3)4·5H2O 8.59 g和去离子水120~150 mL,水浴加热至70 ℃使其完全溶解;在70 ℃的反应温度下,在三口烧瓶中并流滴加0.5 mol·L-1Na2CO3溶液和金属硝酸盐溶液,用磁力搅拌促进沉淀生成,保持滴定终点pH=7.5,滴毕,继续搅拌约1 h,在70 ℃下老化3 h;冷却后在10000 r·min-1下高速离心得固体沉淀。用去离子水洗涤3次;于105 ℃干燥12 h;于500 ℃高温焙烧3 h,研磨、压片,过筛制得样品。
用类似的方法制得ZrO2、 ZnO、 Zn/Zr=1/1和Zn/Zr=1/2。
1.3 催化剂的活性评价系统
催化剂的活性测试在HP-WF51型固定床反应器上进行(不锈钢反应管内径10 mm),催化剂装填量为0.5 g,与0.5 g石英砂混合。在催化剂反应前,通入100 mL·min-1的10%H2-90%N2(体积分数)混合气,在280 ℃下常压活化4 h后冷却至反应温度250 ℃时,以空速12000 mL·g-1h-1通入H2/CO2/N2=72/24/4(体积比)的反应气,升高压力至2 MPa,待反应3 h后收集尾气,用Agilent 6820型气相色谱进行分析,用TCD检测器检测CO和CO2,用FID检测器检测甲醇,利用矫正面积归一法定量分析尾气中格组分含量。
2 结果与讨论
2.1 表征
(1) XRD
不同Zn/Zr摩尔比的XRD图谱见图1。ZnO的衍射峰出现在2θ31.8°、 34.4°、 36.2°,分别归属于ZnO的(100)、 (002)、 (101)晶面,与标准卡片JCPDS#36-1451对应。ZrO2的衍射峰出现在2θ30.1°、 35.3°、 50.3°、 60.1°,分别属于四方晶型t-ZrO2的(011)、 (110)、 (112)和(121)晶面,与标准卡片JCPDS#50-1089对应。当Zn/Zr=1/1和1/2时,ZnO衍射峰大幅度减弱,但仍然存在ZnO的衍射峰。同时,在2θ 29.4°出现了单斜型的m-ZrO2的衍射峰,当Zn/Zr=1/4时,未出现m-ZrO2和ZnO的衍射峰,其衍射峰位置与t-ZrO2对应,并伴随着小幅度的衍射峰的偏移[18]。同时,随着样品中Zr含量的增加,单斜晶型的m-ZrO2向四方晶型t-ZrO2转变。
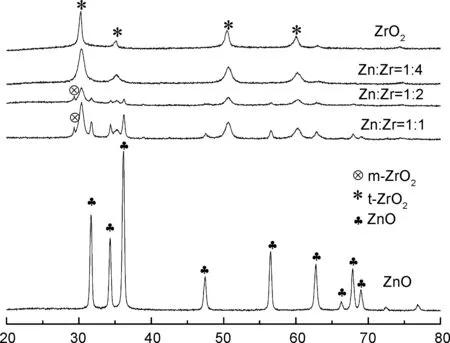
2θ/(°)图1 不同Zn/Zr摩尔比的催化剂的XRD谱图Figure 1 XRD spectra of catalysts with different Zn/Zr molar ratios
(2) BET
表1为催化剂的晶格参数与比表面积。由表1可知,当Zn/Zr=1/1、 1/2和1/4时,对比ZrO2,其最强衍射峰的出峰角度均有所增大,即向衍射角大的方向偏移。变化的原因为Zn2+的半径(0.074 nm)小于Zr4+的半径(0.082 nm), Zn2+取代了部分Zr4+进入到ZrO2的晶格中,导致晶格发生不同程度的畸变,晶面间距变小,晶格参数变小。当Zn/Zr=1/1和1/2时,由于Zn的含量很高,一部分Zn2+进入了ZrO2的晶格,一部分仍然以晶体状覆盖在ZrO2表面,因而存在ZnO的衍射峰,当Zn/Zr=1/4时,未出现ZnO的衍射峰,说明大部分Zn2+进入了ZrO2的晶格中,可能小部分以无定型形态覆盖在ZrO2表面。由表1还可知,ZnO的比表面积最小,为18.2 m2·g-1, ZrO2的比表面积较大为30.7 m2·g-1。由于ZnO本身比表面积较小,催化剂样品中Zn/Zr=1/1和1/2时,Zn含量较高导致催化剂样品比表面积较小,当Zn/Zr=1/4时,Zn摩尔含量为20%时,比表面积最大达到了46.2 m2·g-1,说明了适量的ZnO的掺杂,催化剂样品的比表面积会显著增加,有利于提高催化剂的分散度,提高更多的催化反应活性位,保证更好的催化效果[19]。
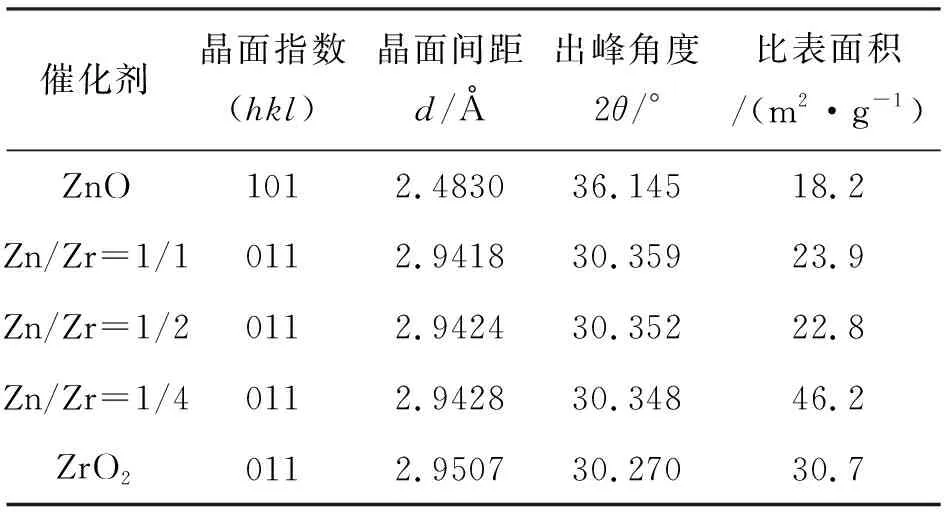
表1 催化剂的最强衍射峰的晶格参数与比表面积Table 1 The crystal parameters of the strongest diffraction peak of the catalyst and specific surface area
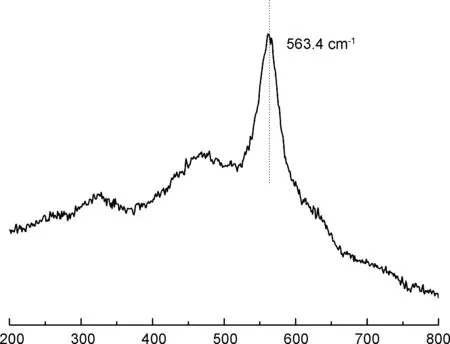
Raman shift/cm-1图2 Zn0.2Zr0.8Ox的拉曼光谱图Figure 2 Raman spectrum of Zn0.2Zr0.8Ox
(3) Raman 光谱
图2为Zn0.2Zr0.8Ox(Zn/Zr=1/4)的拉曼光谱图。由图2可知,在波长563.4 cm-1附近有尖锐的拉曼峰,证明Zn0.2Zr0.8Ox的结构为固溶体[13]。ZnO的拉曼峰位于383 cm-1、 438 cm-1和577 cm-1附近[20-21],而在该图中在这些位置拉曼特征峰的强度很弱,故认为在Zn0.2Zr0.8Ox上表面不存在晶体状的ZnO,这与XRD结果一致。
(4) TEM和HRTEM
图3(a)为Zn0.2Zr0.8Ox的TEM图。从图3(a)中可以看出,催化剂样品颗粒大小基本一致,颗粒分散较为均匀,团聚现象不明显。图3(a)右下角为根据TEM图分析得到的粒径分布图,催化剂样品的平均粒径为9.2 nm,粒径分布在7~11 nm,分布较为均匀。图3(b)为Zn0.2Zr0.8Ox的HRTEM图。由图3(b)可知,两条晶格条纹的距离为0.294 nm,与表1中t-ZrO2的(011)晶面间距一致,且没有发现ZnO的晶格条纹。
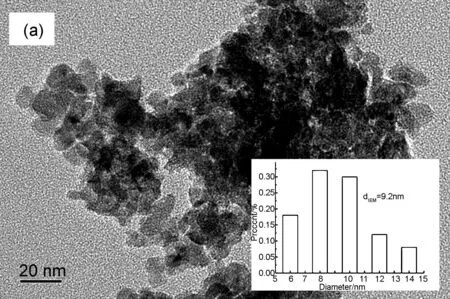

图 3 Zn0.2Zr0.8Ox的TEM图(a)和HRTEM图(b)Figure 3 TEM(a) and HRTEM(b) of Zn0.2Zr0.8Ox
(5) H2-TPR
Zn0.2Zr0.8Ox的H2-TPR谱图见图4。从图4中可以看出,在435 ℃附近有个最强的氢气消耗峰,在544 ℃附近有个微弱的氢气消耗峰,说明在Zn0.2Zr0.8Ox固溶体催化剂表面有一定的Zn活性位点被氢气还原,解释为高度分散状的Zn被还原,而高温处的则解释为体相的ZnO被还原,但被还原的量很少,这与Raman光谱图中ZnO的特征峰很弱以及XRD中几乎观察不到ZnO的衍射峰结果保持一致。ZrO2在750 ℃的高温下出现微弱的氢气还原峰[13],ZnO则在800 ℃的高温下仍然不能被氢气还原[13,22]。而当形成Zn0.2Zr0.8Ox固溶体结构时,其还原能力明显增强,证明了Zn0.2Zr0.8Ox固溶体结构中金属氧化物间存在强相互作用。
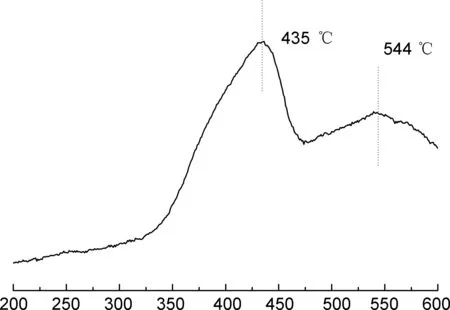
Temperature/℃图4 Zn0.2Zr0.8Ox的H2-TPR谱图Figure 4 H2-TPR pattern of Zn0.2Zr0.8Ox
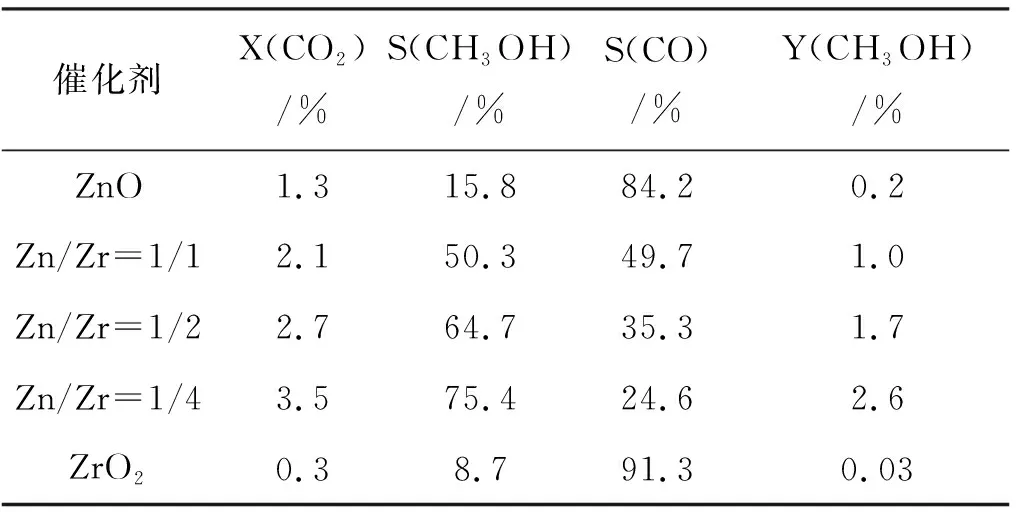
表 2不同Zn/Zr摩尔比催化剂的催化性能
2.2 催化性能
不同Zn/Zr摩尔比催化剂的催化活性测试结果如表2所示。由表2可知,纯ZnO和ZrO2基本没有催化活性,但两者形成的双金属氧化物却有着较好的催化活性,当Zn/Zr=1/4时,催化剂活性最高,CO2转化率达到了3.5%,甲醇选择性为75.4%,甲醇收率达2.6%。图5(a)为反应温度(190~310 ℃)对Zn0.2Zr0.8Ox固溶体催化剂的影响。由图5可知,随着温度升高,CO2转化率呈上升趋势,即提高温度有助于CO2转化率,而CO2加氢制甲醇是一个放热反应,即提高温度,甲醇的选择性呈下降趋势,原因为甲醇合成反应与逆水煤气反应为竞争反应,甲醇选择性下降而CO选择性升高[23]。选取催化活性最高的Zn0.2Zr0.8Ox固溶体催化剂进行了催化剂稳定性测试[图5(b)]。由图5(b)可知,催化剂在反应器中连续运行100 h, CO2转化率与甲醇选择性基本没有下降,说明催化剂具有良好的稳定性。
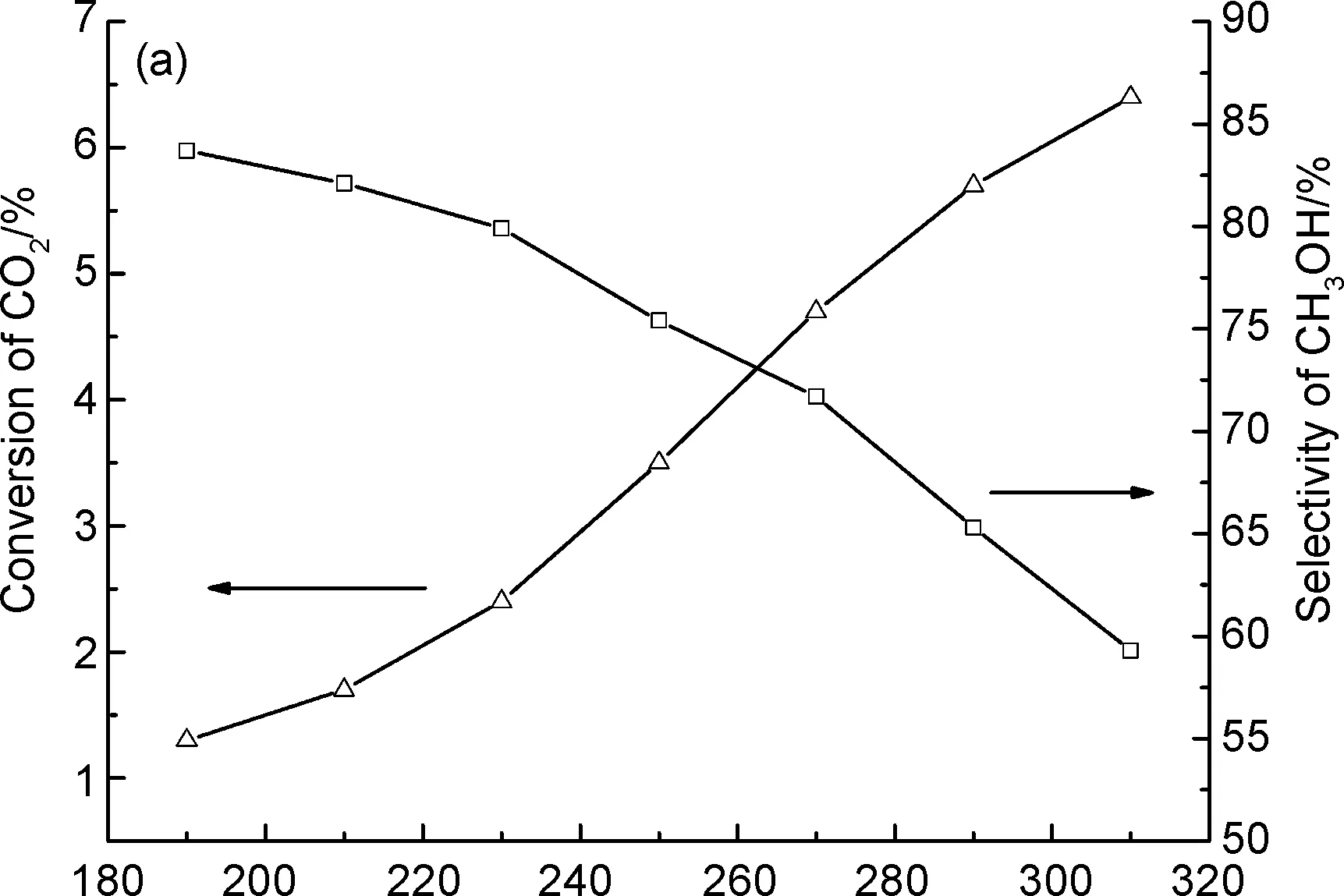
Temperature/℃
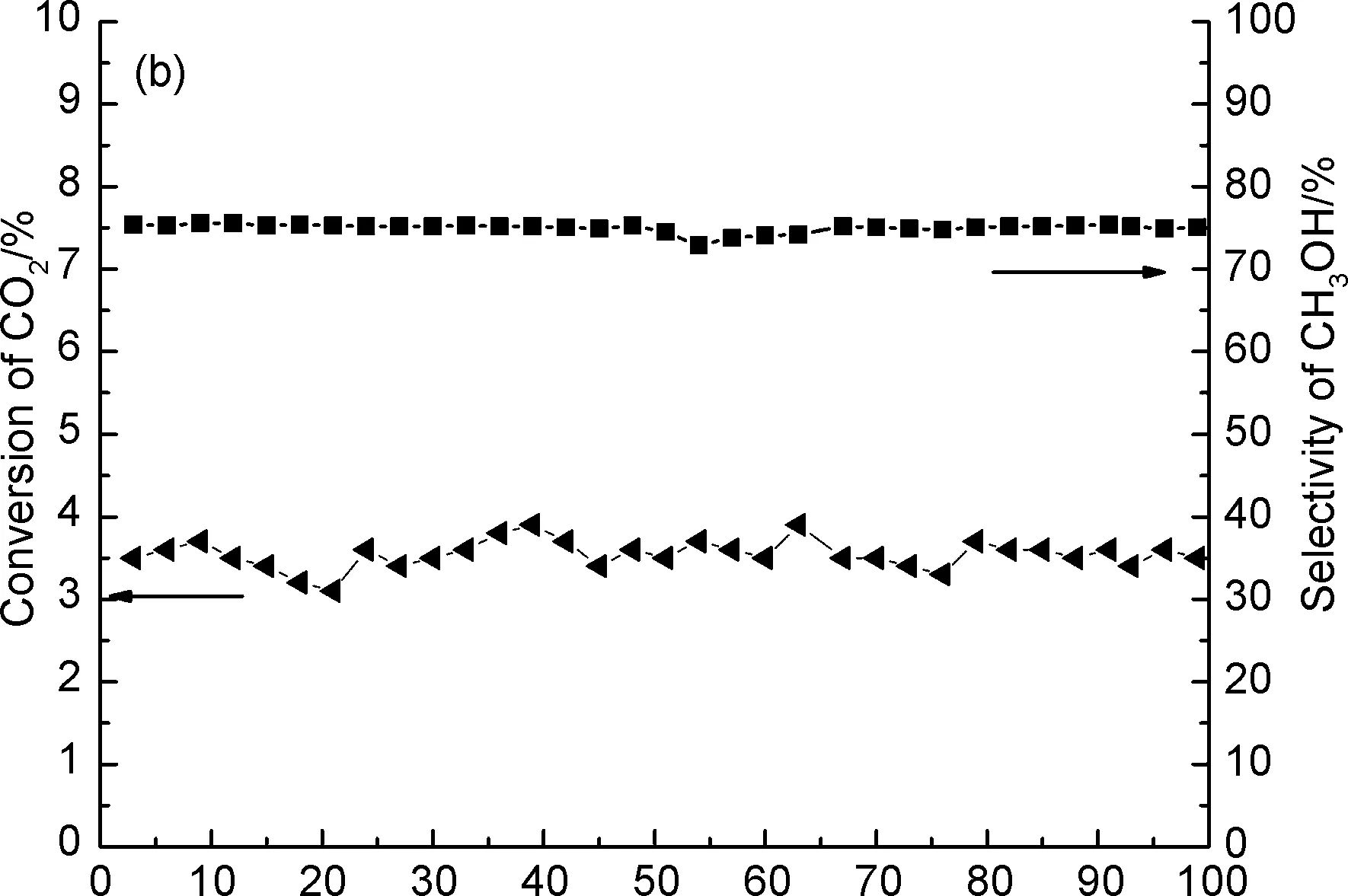
Time on stream/h图5 (a)反应温度对Zn0.2Zr0.8Ox固溶体催化剂的影响;(b)CO2转化率和甲醇选择性随反应时间的变化Figure 5 (a)Effect of reaction temperature over Zn0.2Zr0.8Ox solid solution catalyst; (b)effect of reaction time on CO2 conversion and methanol selectivity
采用并流共沉淀法制备了一系列不同摩尔比Zn/Zr催化剂,当Zn/Zr=1/4时,Zn0.2Zr0.8Ox为固溶体结构;Zn0.2Zr0.8Ox对氢气、二氧化碳合成甲醇的反应有良好的催化性能,甲醇选择性达到75.4%。催化剂的稳定性较好,在固定床反应器中稳定运行100 h未失活。

