经鼻内镜颅底肿瘤切除术后颅内感染临床特征及危险因素分析
尹丽霞 高婷 钱海鹏 刘燕 陈宝敏
神经外科术后的手术部位感染特别是颅内感染,是术后严重并发症之一。颅内感染一旦发生,需及早做出诊断,延误诊治不仅会延长患者的住院时间,增加医疗费用,严重时可致患者神经系统功能障碍,甚至死亡。据统计,颅内感染死亡率高达13%,并会产生永久性的神经系统损伤[1]。经鼻内镜颅底肿瘤切除术(endoscopic endonasal skull base surgery,EESBS)通过使用内窥镜经鼻颅底入路为颅内病变提供微创通道,但由于入路通过非无菌鼻腔,颅内感染的潜在高风险已经引起关注,成为手术部位感染监测的重点。国外相关研究显示[2-4],经鼻道内镜术后脑膜炎的发生率为1.2%~9.3%,而开放式颅骨切开术仅1.52%。但目前国内外针对EESBS术后颅内感染危险因素分析相关研究较少。本研究回顾性分析中国医学科学院北京协和医学院肿瘤医院2011年1月至2016年12月行EESBS的150例患者,深入分析颅内感染的临床特征、感染相关危险因素,筛选独立危险因素,为感染防控提供依据。
1 材料与方法
1.1 临床资料
选取2011年1月至2016年12月中国医学科学院北京协和医学院肿瘤医院行EESBS的患者150例,其中男性64例,女性86例。病理类型:垂体腺瘤84例,脊索瘤16例,Rathke's囊肿8例,颅咽管瘤8例,脑膜瘤4例,颅底肉瘤3例,复发进展鼻咽癌3例,颅底肉瘤3例,转移性肿瘤3例,复发进展鼻咽癌3例,神经鞘瘤2例,蛛网膜囊肿2例,颅底腺样囊性癌2例,颅底淋巴瘤2例,海绵状血管瘤2例,肉芽肿2例,生殖细胞瘤1例,黑色素瘤1例,鼻内翻性乳头状瘤1例。肿瘤部位:鞍区肿瘤94例,颅外蝶窦斜坡区22例,前颅底颅鼻沟通肿瘤11例,位于鞍上颅内10例,中颅底沟通肿瘤7例,颅眶沟通肿瘤4例,位于额叶1例,桥小脑角1例。
1.2 方法
1.2.1 资料收集 采用回顾性调查法,根据患者的电子病历、检验记录、检查记录、麻醉手术记录等资料逐项填写调查表,建立并录入Epidata数据库,内容包括患者年龄、性别、病史(有无合并基础疾病)、ASA评分、手术时间、手术史、手术路径、术前放化疗、术前颅内高压、围术期抗菌药物使用情况、术中颅底重建、术中脑室外/腰大池引流、术后脑脊液鼻漏等指标,分别统计感染组与非感染组的差异。
1.2.2 颅内感染诊断标准 诊断依据卫生部卫医发[2001]2 号《医院感染诊断标准》,中枢神经系统感染包括细菌性脑膜炎、脑室炎、颅内脓肿和椎管内感染。
1.3 统计学分析
采用SPSS 21.0软件进行统计学分析。计量资料采用t检验,计数资料采用χ2检验;多因素Logistic 回归分析。以P<0.05为差异具有统计学意义。
2 结果
2.1 患者特征
150例手术患者中,男性64例(42.7%),女性86例(57.3%);ASA 评分>2 分12例(8.0%);37例(24.7%)有鼻内或开颅手术史;20例(13.3%)曾接受放化疗。
2.2 感染发生率及感染患者临床特征
27例患者发生术后颅内感染(表1),感染率为18.0%,脑脊液培养结果阳性8例,阳性率为29.6%,病原体包括溶血葡萄球菌(2例)、棒状杆菌(1例)、头状葡萄球菌(1例)、弗劳地枸橼酸菌(1例)、表皮葡萄球菌(1例)、阴沟肠杆菌(1例)、浸麻类芽孢杆菌(1例)。27例颅内感染患者中18例(66.7%)发生脑脊液漏,漏发生的平均天数为9.28天。23例患者(85.2%)术中脑室外引流或腰大池引流,22例患者(81.5%)术中颅底重建。大部分患者的脑脊液常规及生化检查结果为低糖、高蛋白、高白细胞(表1)。
2.3 单因素及多因素Logistic回归分析
单因素分析结果显示(表2),术后发生脑脊液漏、未在术前0.5~1.0 h使用抗菌药物、术后脑室外引流或腰大池引流、颅底重建是发生颅内感染的危险因素(P<0.05)。筛选单因素分析中P<0.1的因素,以及文献中报道有意义的因素,纳入回归模型进行分析,结果显示BMI≥25 kg/m2、未在0.5~1.0 h内使用抗菌药物、术中进行脑室外引流或腰大池引流、术中颅底重建是术后颅内感染的独立危险因素(P<0.05,表3)。

表1 27例EESBS颅内感染患者的临床特征
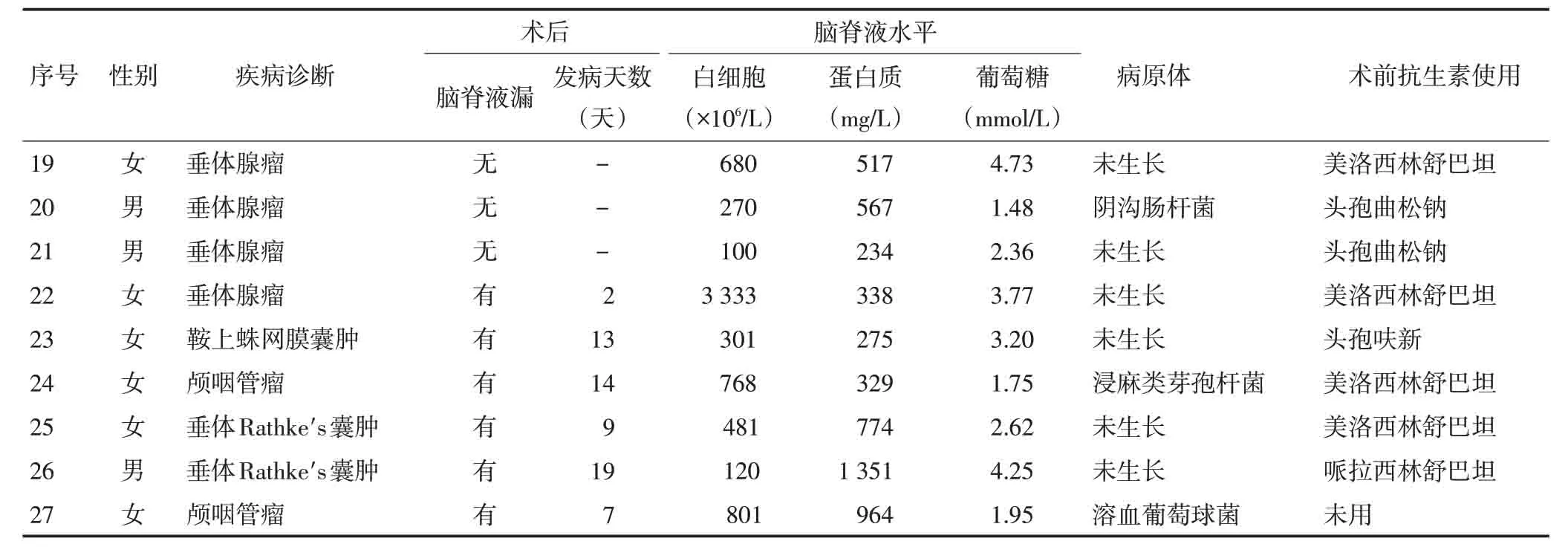
表1 27例EESBS颅内感染患者的临床特征(续表1)

表2 EESBS颅内感染危险因素单因素分析 n(%)

表2 EESBS颅内感染危险因素单因素分析 n(%)(续表2)
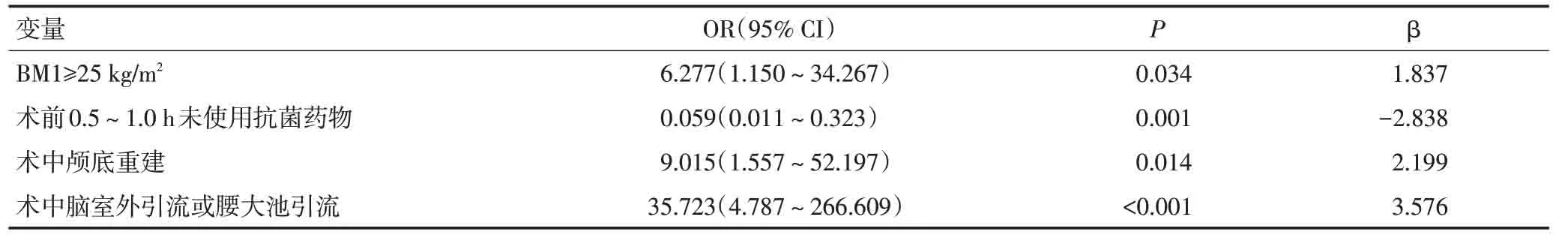
表3 EESBS颅内感染多因素回归分析
3 讨论
随着鼻内镜的发展,越来越多的颅底疾病可以通过鼻内镜微创手术解决,虽为微创,避免了传统开颅手术造成的创伤,但手术通过鼻腔鼻窦均为有菌区域,术后感染风险增大。目前,国内外报道[2-4]EESBS感染率为1.2%~9.3%。陈幼华等[5]对颅脑手术患者鼻前庭、口咽部采集拭子进行培养,200例患者鼻前庭检出条件致病菌95株,检出率为47.5%。手术中器械及植入物均需要经过鼻腔这个潜在的污染区进入术野,因此感染风险增高。Kono等[6]对1 000例EESBS患者进行分析,发现开颅或鼻内手术复杂度高,手术时进行脑室或脑室腹腔引流术,术后脑脊液漏为颅内感染的危险因素。
本研究的单因素分析显示,术后发生脑脊液漏、未在术前0.5~1.0 h 使用抗菌药物、术中脑室外引流或腰大池引流、术中颅底重建为颅内感染的危险因素。术后发生脑脊液漏通常由于颅底组织缺损或封闭不严,导致脑脊液从不完整颅底漏出。脑脊液漏发生时,颅内外出现相通,病原体可经漏口逆行进入颅内诱发感染[6-7]。患者发生颅内高压或预测颅内压增高时需进行脑室外引流或腰大池引流,可能会增加颅内感染的风险。术中颅底重建与颅内感染的关系存在一定的争议,部分研究表明颅底重建是颅内感染发生的独立危险因素[3],与本研究结果一致。颅底重建的方法有多种,分为带蒂鼻中隔瓣、游离瓣、异体材料。异体材料植入物由于缺乏血供,可能导致病原菌的附着滋生,因此单独使用可能会增加感染机率。但有研究表明使用带蒂鼻中隔瓣,无排异性,有血管蒂供血,易于存活,其用于颅底重建,可减少脑脊液漏,进而减少颅内感染[6]。
抗菌药物的预防使用对于预防颅内感染发生至关重要。Stephen等[8]对41例EESBS治疗患者抗菌药物预防进行研究,通过围手术期使用平均5天的头孢曲松抗菌药物预防,无1例发生感染。本研究在术前使用抗菌药物种类以酶抑制剂为主,虽然抗菌谱能覆盖主要病原体,但是酶抑制剂的广泛使用会增加超广谱β-内酰胺酶和KPC型碳氢霉烯酶耐药菌的产生;使用时机方面,感染组55.6%患者未在术前0.5~1.0 h 内使用抗菌药物,与未感染组差异具有统计学意义,感染组1例患者在术前未使用抗菌药物。术前0.5~1.0 h使用抗菌药物可保证在切皮时达到有效的血药浓度,成为预防手术部位感染的有效手段,但若术前抗生素使用时机不正确,会增加感染风险[9]。
本研究的多因素分析中,未在术前0.5~1.0 h使用抗菌药物、术中脑室外引流或腰大池引流、术中颅底重建、BMI≥25 kg/m2为颅内感染的独立危险因素,与单因素研究基本符合,BMI≥25 kg/m2在单因素研究中差异无统计学意义,但相关研究[10]认为其与颅内感染相关,因此在本研究中纳入多因素分析。经过回归分析认为其与颅内感染具有相关性。上述因素部分是可控的,也是今后采取防控措施的重要依据。
通过上述研究,筛选出的EESBS 颅内感染危险因素是针对性开展防控措施的重点。建议临床中应更加注重抗菌药物的规范使用,根据病原学及耐药特点结合药代动力学以及可穿透血脑屏障等特点,选择合适的抗菌药物,精准防控颅内感染。

