两种全酸蚀树脂粘接剂对正常牙本质与玻璃陶瓷粘接效果的比较研究*
司小京 李风兰 曹二弯
玻璃陶瓷因其在机械性能和美学修复方面的优势备受口腔科医生的青睐[1,2],但玻璃陶瓷修复体与牙体组织的粘接在很大程度上受粘接剂的影响[3]。树脂类粘接剂的应用使玻璃陶瓷与牙体组织的粘接取得良好效果[4],是目前临床上玻璃陶瓷类修复体常用的粘接材料。在树脂类粘接剂不同粘接系统中以全酸蚀粘接系统粘接效果最好[5],Variolink N是目前临床上常用的全酸蚀粘接剂,许多研究已表明其具有良好的粘接效果[6,7],但修复成本较高。我国登泰克公司自主研发的全酸蚀粘接剂全能酸蚀粘接套装U.link,已投入国内市场供临床使用,修复成本相对较低,但其用于玻璃陶瓷与牙本质粘接时能否具有与Variolink N相同的粘接效果,尚未明确。本实验拟研究比较Variolink N和U.link两种全酸蚀粘接剂对正常牙本质与二硅酸锂加强型玻璃陶瓷的粘接强度及粘接界面纳米微渗漏情况,评估其粘接效果,以期为口腔嵌体修复时粘接剂的选择提供实验依据。
1.材料和方法
本研究时间为2018年11月至2019年6月。
1.1 材料与仪器 选取40颗完整无龋的人磨牙(山西省人民医院口腔颌面外科门诊收集,20~30岁,患者均知情同意),去除结石及软组织、清洁牙面和消毒,置于4℃含有抑菌剂(氯氨T)的水溶液中保存,于拔牙3个月内使用。40个UP.CERA(爱尔创,中国深圳)玻璃陶瓷瓷块。全酸蚀粘接剂Variolink N(Ivoclar Vivadent,列支敦士登),全酸蚀粘接剂全能粘接套装U.link(登泰克,中国),氢氟酸凝胶IPS Ceramic Etching Gel(Ivoclar Vivadent,列支敦士登),光固化灯(LED-B,啄木鸟),速干指甲油(欧莱雅,法国),28%氨水(伟博鑫,山西),硝酸银(伟博鑫,山西),显影液(海燕,天津),定影液(kodak,美国),无水丙酮(伟博鑫,山西),CQ-6超神波清洁器(上海超声波仪器有限公司),万能实验机(英斯特朗,美国),体视显微镜(SMZ1000,尼康)电子数显卡尺(美耐特,德国),场发射扫描电子显微镜(JSM-6510,日本),能谱仪(QX200,德国布鲁克)。
1.2 方法
1.2.1 实验分组及试件制备 使用慢速切割机在喷水冷却的情况下将爱尔创全瓷块切割成大小4mm×4mm×5mm标准瓷块 40个(粘接面积4mm×4mm),体视显微镜观察排除有裂纹等缺陷的瓷块,按生产商要求,瓷块烧结结晶30min。所有全瓷试件在流动水下依次用400、600、800目碳化硅耐水磨砂纸手动打磨粘接面60s,超声清洗机中荡洗5min,干燥,备用。
40颗离体牙在流动水冷却条件下用慢速切割机沿与牙长轴垂直的方向切割,去除牙釉质及少量牙本质,暴露冠中部牙本质,磨平牙本质面;每颗离体牙制备大小为4mm×4mm×5mm的正常牙本质块一个(粘接面积4mm×4mm),使用600目碳化硅砂纸流动水下打磨粘接面30s以制备统一玷污层,超声清洗机中荡洗5min,室温下保存于蒸馏水中备用。
将牙本质块随机编号,分成2组,将两组牙本质块分别用Variolink N和U.link与瓷块按照使用说明进行粘接。试件粘接完成后,于37℃蒸馏水中储存24h。
1.2.2 粘接强度测试与断裂类型分析 水浴24小时后,试件每组随机编号选取10个进行粘接强度测试。将试件使用夹具固定好,放于万能试验机上,使加载头切端置于距粘接界面1mm处并与试件长轴相垂直,设置加载速度为1mm/min对粘接试件加力,记录粘接试件断裂的载荷值,即为粘接界面被破坏的最大载荷。剪切强度(σ)是以粘接界面被破坏的最大载荷(F)除以粘接面积(S)来计算,即 σ(MPa)=F/S(N/mm2)。
将发生断裂的各组试件分别在体视显微镜下观察并记录其断裂模式。粘接试件的基本断裂模式主要有5种[8]:①牙本质与粘接剂界面破坏;②陶瓷与粘接剂界面破坏;③粘接剂的内聚破坏;④陶瓷或牙本质内聚破坏;⑤混合破坏。
1.2.3 粘接界面纳米微渗漏观测 试件37℃水浴24小时后,根据Tay等人[9]提出的方法制备了硝酸氨银溶液50ml(pH=9.5)。避光保存。将每组剩下的10个试件依次使用400、600、800、1000、1200目碳化硅砂纸流动水下打磨,冲洗5min,干燥。在试件粘接界面1mm外区域涂布指甲油,阴凉处晾干,待指甲油干燥后置于氨化硝酸银溶液中避光保存24h。24h后取出试件,流动水冲洗5min,荧光灯下放置于显影液中8h,8h后取出试件,流动水冲洗5min,最后将试件置于定影液中定影4h。所有试件蒸馏水冲洗5min,依次用800、1200、1500、2000、2500目砂纸流动水下进行打磨,超声荡洗5min。依次用30%、50%、70%、90%、100%丙酮溶液梯度脱水,干燥。将试件喷金,热场发射扫描电镜背散射模式下观察粘接面纳米微渗漏情况。并配合X射线能谱仪(EDS)在粘接界面表进行面扫描,检测树脂牙本质粘接界面银(Ag)、铝(Al)、硅(Si)、钙(Ca)元素的分布情况。每个试件有4个粘接侧面,随机选择一个粘接侧面将其粘接线均分为4等份,选择中间的3个等分点为观察位点,即1个试件选择3个视野。3个观察位点分别取1000倍电镜图像1张进行观察,用Image J计算银染面积,以银染面积占粘接层面积的百分比作为纳米渗漏值,量化实验结果。
1.2.4 统计学方法 采用SPSS21.0统计软件进行数据的分析整理,两组剪切断裂模式分析以例数(n)进行描述,统计推断组间差异用Fisher的精确检验;两组的粘接强度和纳米微渗漏分析采用均数±标准差(x±s)描述,经Shapiro-Wilk正态性检验和Leneve方差同质性检验得P>0.05,即数据符合正态分布且方差齐性,故两组间比较用独立样本t检验分析。检验水准为双侧α=0.05。
2.结果
2.1 两组粘接强度及断裂模式的比较 见表1、表2。两组剪切强度比较,Variolink N组[(14.45±2.35)MPa]显著高于 U.link 组[(6.39±1.43)MPa],差异有统计学意义(P<0.05)。两组断裂模式差异无统计学意义(P>0.05),Variolink N组的断裂模式主要为混合断裂,而U.link组的断裂模式以牙本质与粘接剂界面断裂和混合断裂为主。两组频数最高的断裂模式的断面见图1、图2。
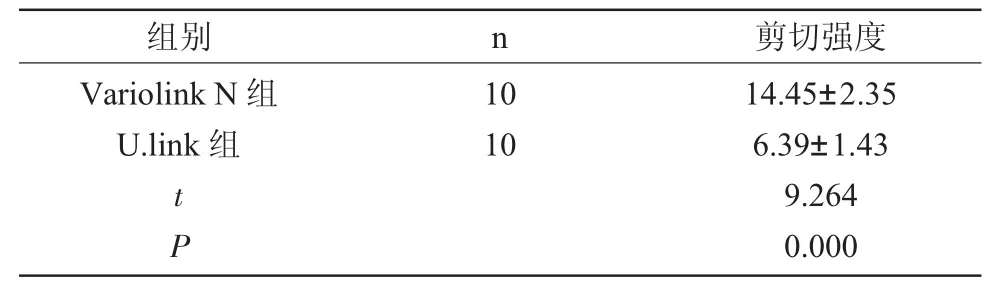
表1 两组粘接试件剪切强度比较(n,x±s)
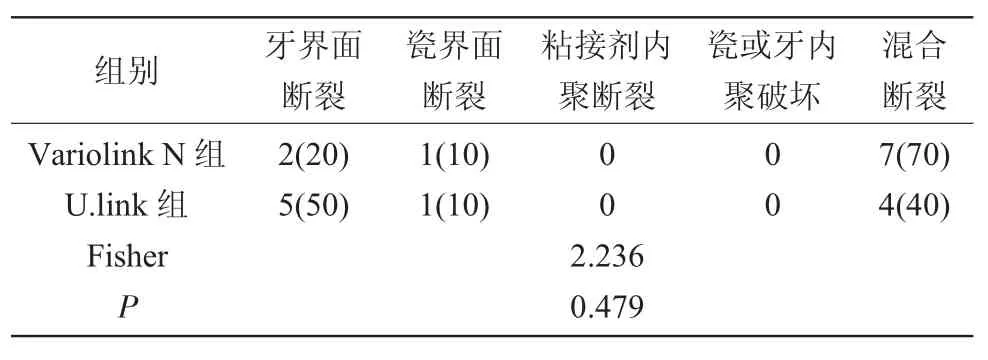
表2 两组粘接试件剪切实验后断裂模式的比较[n(%)]

图1 Variolink N组试件混合破环(体视显微镜×40)

图2 U.link组试件牙本质与粘接剂界面破坏(体视显微镜×40)
2.2粘接界面纳米微渗漏比较 见表3,图3、图4。EDS分析显示钙元素主要分布于牙本质,银元素主要分布于牙本质与粘接剂界面,而陶瓷与粘接剂界面未见银元素,硅元素和铝元素主要分布于树脂粘接剂。Variolink N组纳米渗漏值为18.02±14.07(%),U.link组为17.37±12.80(%),差异无统计学意义(P>0.05)。
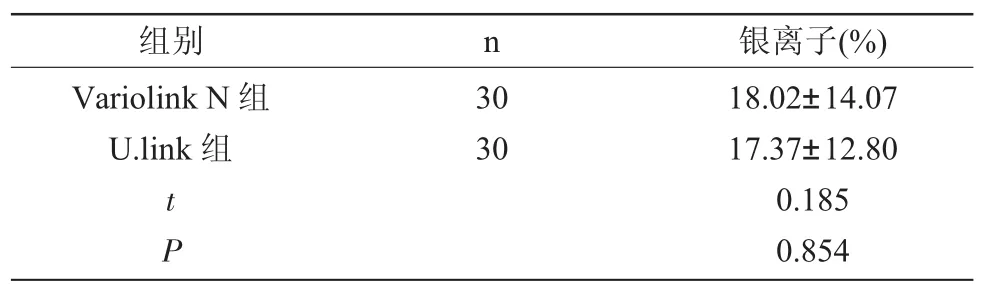
表3 两组纳米微渗漏值比较(n,x±s)
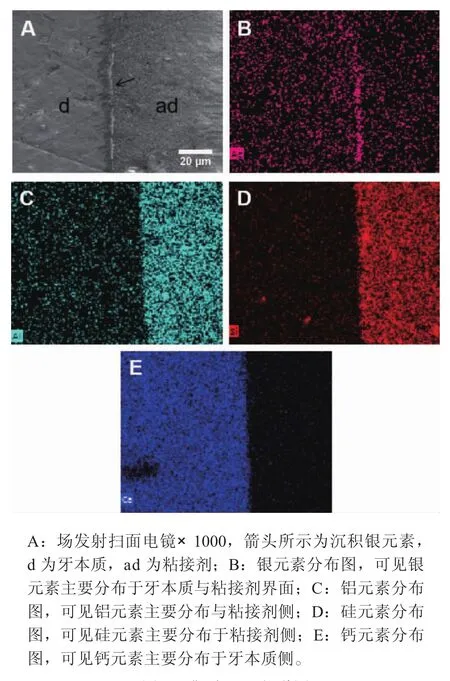
图3 典型EDS能谱图

图4 粘接界面的纳米微渗漏情况(场发射扫面电镜×1000),箭头所示为沉积银元素,d为牙本质,ad为粘接剂
3.讨论
本实验中粘接试件主要发生混合破坏和牙本质-树脂粘接剂界面破坏,仅少数发生陶瓷-树脂粘接剂界面破坏,并且两种树脂粘接剂断裂模式的频数分布差异无显著性。理论上当有两个界面时,破坏从较弱的界面开始[10]。因此说明这两种树脂粘接剂对玻璃陶瓷的粘接力优于牙本质,这也与Gundogdu M[11]的研究相一致。原因可能是HF和硅烷偶联剂的应用使树脂粘接剂和陶瓷获得微机械固位及发生化学结合[12]。两组粘接剂均未发现树脂粘接剂内聚断裂,Durmus,lar和Ölmez[13]认为内聚断裂的出现是由于测得真实粘接强度前外界所加的力已超过粘接树脂的内聚力,说明这两种树脂粘接剂的内聚力高于粘接界面结合力[13,14]。Variolink N组的断裂模式主要是混合破环,说明该粘接剂粘接强度高。U.link组主要断裂模式还有牙本质-树脂粘接剂界面破坏,且在该组拥有最高频数,说明此界面是粘接的薄弱环节。牙本质-树脂粘接剂界面破坏是临床上期望的破坏形式,因为没有破环牙本质与修复体,仅需轻微进行牙体预备即可再次修复患牙,不仅为临床操作提供便利还为患牙的保留提供很大的可能性[6]。根据两组的断裂模式及本实验中使用U.link对upcera锂瓷-牙本质粘接所得剪切强度显著低于Variolink N,可推测U.link的粘接树脂强度和对牙本质的粘接强度低于Variolink N。据Nakabayashi[15]的研究指出,用Total etch(含37%磷酸)处理牙本质面,完全去除了玷污层,树脂粘接剂渗入管间牙本质酸蚀脱矿后的胶原纤维网和牙本质小管形成混合层和树脂突,形成超微机械嵌合,是牙本质粘接中粘接力的主要来源。因此可能是U.link粘接剂的成分或是成分含量不同影响粘接树脂的强度,从而影响超微机械嵌合使得粘接强度较低以及形成牙本质-树脂粘接剂界面粘接的薄弱环节。在本实验中所测的Variolink N的粘接强度较其他研究偏低,可能是测试方法的选择、试件粘接面积等多种因素造成的[16-18]。尽管实验结果偏低,但高于自粘接树脂,自酸蚀粘接树脂粘接强度[19],因此U.link粘接剂的粘接强度可以满足临床需求。据研究,人类在咀嚼饼干、胡萝卜或肉类等食物时产生的力为70-150N[20,21],结合临床修复体的粘接面积,可知U.link粘接剂的粘接强度可以满足临床需求。也有研究指出[22],粘接强度测试结果临床相关性不高,因此本课题组又进行了可以反应粘接效果的纳米微渗漏比较实验。
Sano[23]提出的纳米渗漏理论,当粘接树脂渗透深度与酸蚀脱矿后的牙本质深度不一致时,在混合层底部存在细小的微孔(20-100nm),银离子(0.059nm)便可进入此微孔。本实验在场发射扫描电子显微镜(Field Emission Scanning Electron Microscope、FESEM)下同时显示相接的三种不同影像和两条界线,而只有一条界线上出现少量高亮影像,用EDS对此界线及界线两边影像的元素进行分析,以确定其所对应的物质[24]。分析了Ag、Al、Si、Ca四种元素,发现Al、Si主要分布于界线的一侧,Ca主要分布于界线的另一侧,Ag主要分布于界线上。因树脂粘接剂填料的主要成分为玻璃,牙本质的主要成分是羟基磷灰石,因此在元素分析中,高含量比例的Al、Si代表了树脂粘接剂的存在,高含量比例的Ca代表了牙本质的存在。而高含量比例的Ag带与扫描电镜图像中的高亮处相对应,故在扫描电镜图像中高亮处即为Ag元素的影像,代表着纳米渗漏的情况。通过EDS分析可以推出纳米渗漏只存在于牙本质与粘接剂界面。以银染面积占粘接层面积的百分比作为纳米渗漏值,定量分析实验结果,得出两组纳米渗漏无统计学意义,说明U.link和Variolink N具有相似的界面封闭性,而树脂粘接剂与瓷块的界面未发现明显的银离子沉积现象,这说明陶瓷与粘接剂界面具有良好的封闭效果,原因可能是硅烷偶联剂中含有的硅烷醇基团(-Si-OH)可与玻璃陶瓷表面的羟基(-OH)形成氢键,同时在硅烷醇和“HO-(底物)”表面经缩合反应形成-Si-O-(底物)-键,于是硅烷偶联剂与玻璃陶瓷之间形成硅氧烷网状聚合物;而含有的有机功能团与粘接树脂中的有机基质发生聚合反应。这样可以有效封闭界面,防止水分的扩散和渗漏[25]。纳米渗漏是评价粘接耐久性的一个重要指标[26],一般认为粘接界面的纳米渗漏会导致牙本质粘接剂水解[27],影响粘接的耐久性。有研究指出修复体的寿命主要受修复体材料与牙本质粘接界面微渗漏的影响[28],因此评价粘接界面纳米渗漏现象可能比粘接强度研究更具有临床相关性。因此U.link的临床粘接效果可能与Variolink N相似。
综上,本研究结果显示,U.link全酸蚀粘接剂的粘接强度低于Variolink N全酸蚀粘接剂,其界面封闭性与Variolink N全酸蚀粘接剂相似。因此临床上可根据粘接面积和牙合力的大小选择适宜的粘接剂。

