响应面法优化福林酚法测定冬枣中总酚含量
林倩,吴昊,刘芊辰,邵娟娟*
1. 河北农业大学理工学院(沧州 061100);2. 河北农业大学园艺院(保定 071000)
冬枣是一种属于鼠李科的树木果实,是一种兼具生态功能和经济功能的品种[1],与其他品种的枣在成分组成、外型等方面有较大区别。冬枣中富含多酚[2]。多酚是植物的重要组分,有助于颜色、香气的形成,同时也起到保护植物的作用[3]。多酚类化合物种类繁多,主要有黄酮、异黄酮、黄酮醇、儿茶素和酚酸的衍生物或异构体,不同的结构使多酚类化合物具有多种生物学特性,如抗氧化、抗衰老、抗癌、抗炎、保护心血管等功能,被认为是一种有效的健康保护剂以及食品天然防腐剂[4]。因此检测冬枣中这些生物活性化合物具有很大的意义。
目前,检测多酚类化合物的方法主要有高效液相色谱法和福林酚法等。其中福林酚法更适合食品组分较为简单的多酚的测定[5],该方法同时具有灵敏度高、快速和可重复性良好等特点[6],更加适合冬枣中多酚含量的测定。另外,多酚结构的多样性使得不同物质中总酚的组成不相同,被检测物质中组成成分会影响测定结果[7],并且组分含量及构成对显色反应结果的影响也有差别[8]。由于目前针对冬枣中多酚含量测定的研究主要针对多酚提取体系等方面,应用福林酚法测定冬枣中的总酚含量还未有所用试剂的定量标准[9],影响了冬枣的开发利用,因此优化福林酚法测定冬枣中总酚含量的工艺条件是十分必要的。
1 材料与方法
1.1 材料与试剂
冬枣:沧州市市售,无机械损伤,颗粒大小适中,成熟度均匀;没食子酸标品(分析纯)、福林酚试剂(生化试剂):合肥博美生物科技有限公司。
1.2 仪器与设备
超声波清洗仪(昆山市超声仪器有限公司);烘箱、电热恒温水浴锅(北京中兴伟业仪器有限公司);分析天平(奥豪斯仪器有限公司);紫外可见分光光度计(珀金埃尔默仪器有限公司)。
1.3 方法
1.3.1 最佳吸收波长的选择与标准曲线的绘制
参考张萍等[10]的方法。准确称取10 mg没食子酸标品,加水定容至100 mL,得质量浓度为0.1 mg/mL的没食子酸标准溶液。用移液枪分别移取0,0.25,0.5,0.75,1,1.25,1.5和1.75 mL于25 mL容量瓶中,加入10 mL超纯水摇匀,分别加入0.65 mL的福林试剂,避光反应后加入4 mL 20%碳酸钠溶液,用超纯水定容,于60℃水浴加热10 min,冷却后得到质量浓度为0,1,2,3,4,5,6和7 μg/mL的没食子酸系列溶液。将3 μg/mL的没食子酸溶液在全波长下扫描,并设置空白对照,确定最大吸收波长,为720 nm。
在720 nm波长下对系列溶液进行吸光度测定,以没食子酸浓度(μg/mL)作为X轴,吸光度作为Y轴,获得标准曲线,求得方程为Y=0.096 8X-0.017 8,相关系数R2=0.996 2,标准曲线见图1。
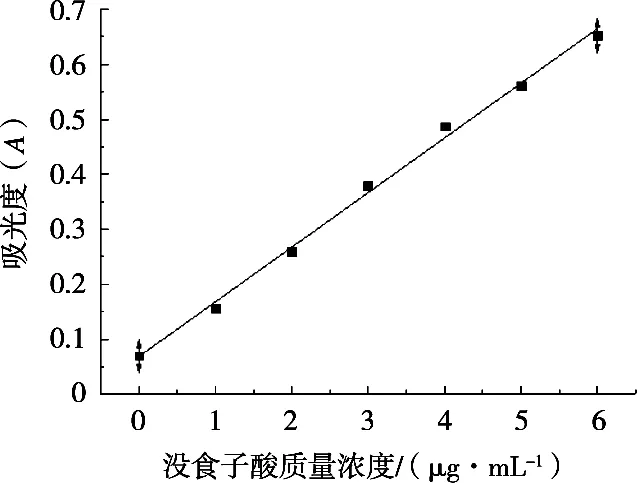
图1 没食子酸的标准曲线
1.3.2 冬枣多酚的提取
将新鲜冬枣人工去核后切片,参考杜丹丹等[11]的方法,将冬枣在烘箱内以40℃的温度恒温鼓风干燥48 h,经过加热烘干以后,冬枣干中的多酚含量会有明显上升[12-13]。用粉碎机将冬枣干粉碎为冬枣粉,然后置于不透明自封袋中低温保存。准确称取10 g冬枣粉末于锥形瓶中,加入100 mL体积分数50%的乙醇溶液,用保鲜膜封口,并将膜扎出若干小孔,放置于超声波清洗机中,在60℃条件下提取1.5 h,经过滤后的滤液以3 500 r/min离心20 min,获得冬枣多酚溶液。准确吸取1.5 mL冬枣多酚溶液于100 mL容量瓶中,用超纯水定容至刻度线并摇匀。
1.3.3 冬枣多酚的单因素试验
1.3.3.1 福林酚试剂浓度的确定
此方法通过还原福林酚试剂来形成蓝色复合物[14],因此选择福林酚试剂浓度作为考察因素。取5份1 mL冬枣多酚溶液,分别加入1 mL 0.2,0.4,0.6,0.8和1 mol/L的福林试剂,混合均匀后加入1.5 mL质量分数为20%的碳酸钠溶液,摇匀至于40℃的恒温水浴锅中,避光反应1 h,在720 nm处进行吸光度的测定,得到最佳福林酚试剂的用量,同时进行平行试验。
1.3.3.2 碳酸钠用量的确定
显色反应在碳酸钠介质中进行,碳酸钠的加入量会影响该方法,因此选择碳酸钠用量作为考察因素。取5份1 mL冬枣多酚溶液,加入1 mL 0.6 mol/L的福林试剂,混合均匀后加入分别加入0.5,1,1.5,2和2.5 mL质量分数为20%的碳酸钠溶液,摇匀至于40℃的恒温水浴锅中,避光反应1 h,在720 nm处进行吸光度的测定,得到最佳的碳酸钠用量,同时进行平行试验。
1.3.3.3 反应温度的确定
温度会影响有色物质的稳定性以及碳酸钠的溶解度,因此选择温度作为考察因素。取5份1 mL冬枣多酚溶液,加入1 mL 0.6 mol/L的福林试剂,混合均匀后加入1.5 mL 20%的碳酸钠溶液,摇匀后分别至于20,30,40,50和60℃的恒温水浴锅中,避光反应1 h,在720 nm处进行吸光度的测定,得到最佳反应温度,同时进行平行试验。
1.3.4 冬枣多酚测定方法响应面优化试验设计
根据Box-Behnken试验设计原理,在单因素的基础上,选取福林酚试剂浓度、碳酸钠用量、反应温度3个因素,进行三因素三水平的响应面分析,因素与水平设计见表1。
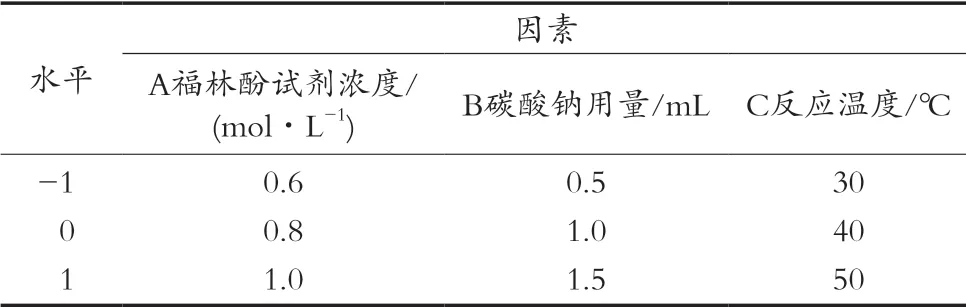
表1 响应面试验因素水平表
1.3.5 数据分析
数据分析过程中采用Origin 8软件和Excel 2010对试验数据进行整理与绘图,采用Design-Expert 8.0.6统计软件进行响应面优化分析。
2 结果与分析
2.1 单因素试验结果
2.1.1 福林酚试剂浓度的影响
如图2所示,福林酚试剂浓度对冬枣总酚测定结果的影响较大,随着福林试剂浓度的上升,反应物的含量上升,染色反应进行得愈加充分,从而使得灵敏度上升,因此所测得的总酚含量是逐步增加的。在福林酚浓度逐渐增大的过程中,多酚与福林酚的反应趋于饱和,福林酚试剂浓度继续增大,吸光度趋于平稳。当浓度为1 mol/L时所测得吸光度最大,且随着福林试剂浓度的上升,所测得的吸光度上升幅度降低,考虑到经济因素、灵敏度、线性范围,试验选择0.8 mol/mL为最佳用量。
2.1.2 碳酸钠用量的影响
如图3所示,随着碳酸钠用量的增加,所测得的吸光度先上升后下降,且当碳酸钠用量为1 mL时,测得的吸光度最高,当碳酸钠的添加量大于1 mL以后,下降的趋势会逐渐减小,且反应后的溶液中有白色沉淀的析出。因此将碳酸钠的最佳用量确定为1 mL。
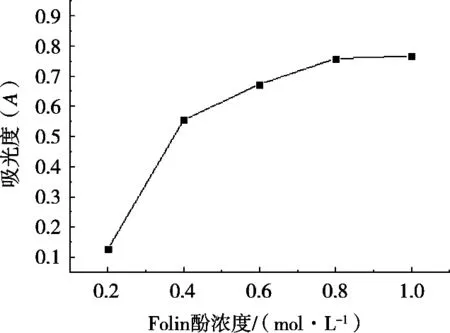
图2 福林酚试剂浓度对吸光度的影响
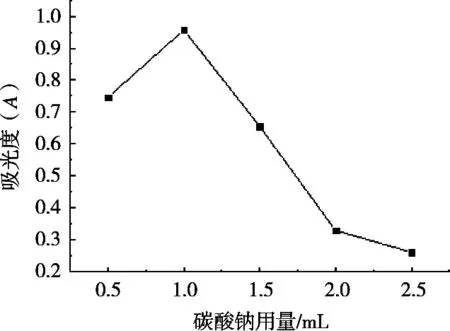
图3 碳酸钠用量对吸光度的影响
2.1.3 反应温度的影响
如图4所示,随着反应温度的上升,吸光度呈现先上升后下降的趋势,温度的上升为反应创造最佳的条件,这种急剧下降的趋势可能是50℃以上的高温会破坏生成的有色物质[15],造成吸光度下降。所以初步确定最佳反应温度为50℃。
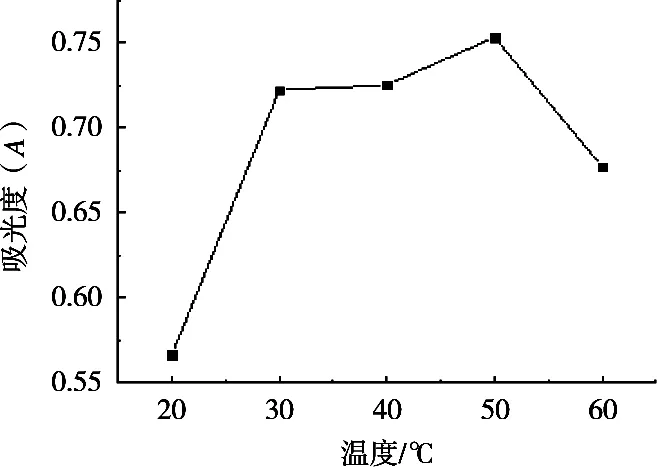
图4 温度对吸光度的影响
2.2 响应面试验结果
2.2.1 响应面结果分析
利用Design Expert 8.0.6软件对选取的3个因素进行响应面分析,响应面试验结果如表2所示。试验数据进行二次多项式回归拟合,得到总酚含量对福林酚试剂浓度(A)、碳酸钠用量(B)、显色温度(C)的回归模型方程:总酚含量(Y,μg/mL)=-71.948 75+ 83.920 00A+15.587 75B+2.034 91C-10.355 00AB-0.141 25AC-0.071 950BC-44.459 37A2-3.412 50B2-0.022 861C2。
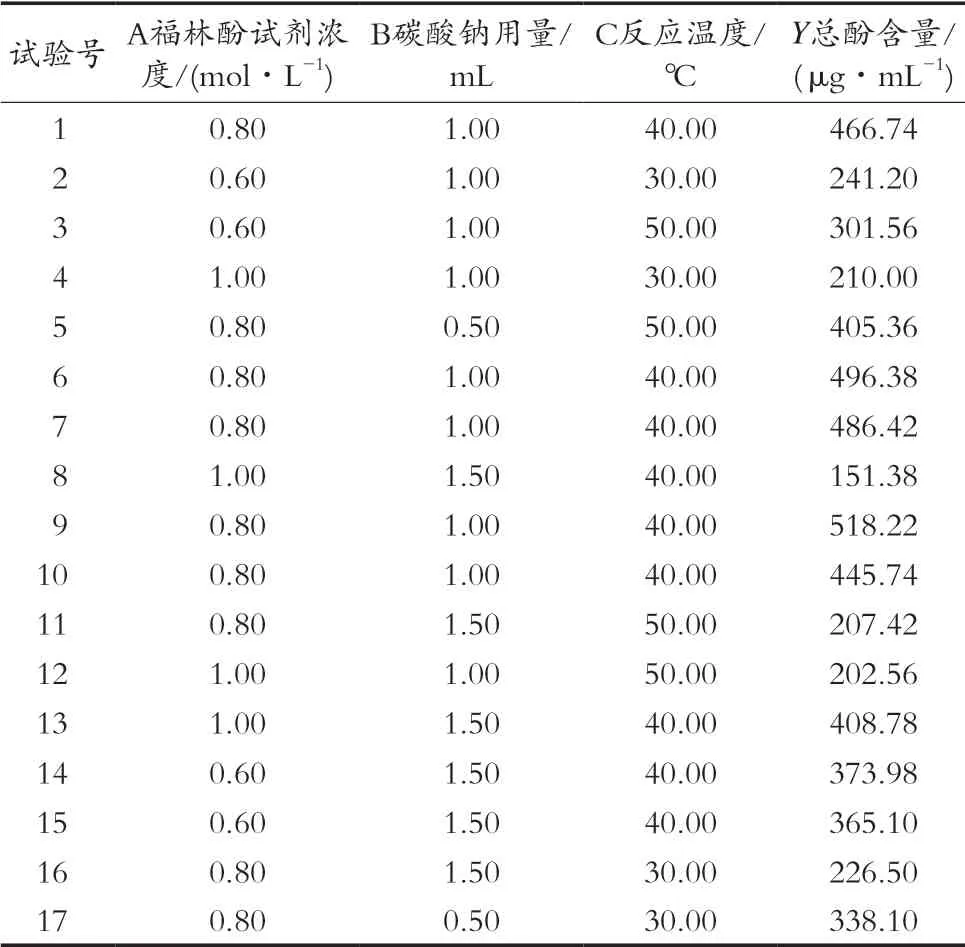
表2 响应面试验设计与结果
利用Design Expert 8.0.6软件对选取的三个因素进行响应面分析,试验结果的方差分析如表3所示。根据表3模型分析可知,二次回归模型的F=48.36,p< 0.000 1,表明该模型达到极显著水平;失拟项是模型中数据的变异,失拟项p=0.870 9,p>0.05,说明失拟项差异不显著,能充分反映实际情况,回归模型是适合的;试验模型的决定系数R2=0.941 6,说明冬枣多酚测定条件结果与模型预测结果有着良好的一致性,试验误差较小,试验模型的校正系数R2Adj=0.963 8,这也验证了该模型的可靠。回归方程各项方差分析中F值检验可以判断自变量对因变量的影响,由此可知该试验中设计的各因素对冬枣中多酚检测影响的主次顺序为B>A>C,即20%碳酸钠的用量对冬枣中总酚测定的影响最大,其次是福林酚试剂的浓度,对其影响最小的是处理温度。通过对回归方程与方差分析还可以了解到模型一次项中碳酸钠的用量对冬枣中总酚的测定结果影响极显著,福林酚试剂的浓度对试验结果的影响显著,而反应温度对试验结果的影响不显著,交互项中AB对结果的影响极显著,AC、BC对试验结果的影响不显著,二次项中A2与C2对试验结果影响极显著,B2对试验结果影响显著。
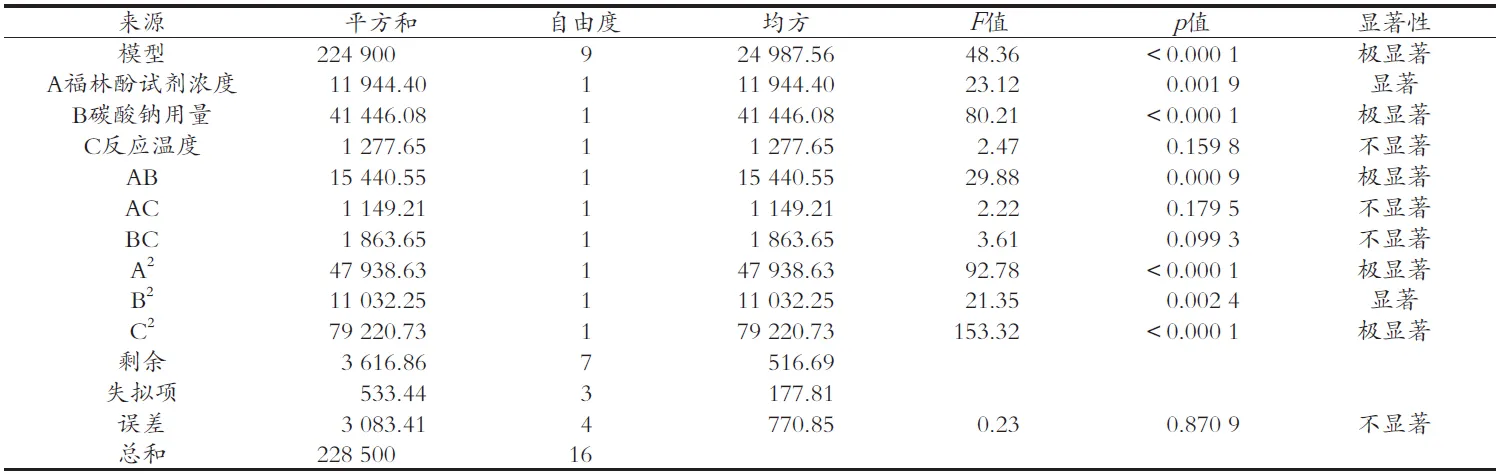
表3 回归模型方差分析表
2.2.2 响应面中交互作用及优化
多元二次回归模型所作的响应面图是通过Box- Behnken原理设计试验得到的,响应面图形反映的是各个因素之间的相互关系以及相互作用程度[16]。固定其他因素,考察交互项对冬枣中多酚测定的影响,响应面分析图可用于评价该试验中设置的试验因素对冬枣总酚测定影响的两两交互作用[17]。各因素交互作用对响应值的影响如图5~图7所示。响应面坡度越陡峭,说明改变试验条件对响应值的影响越显著,该因素对冬枣中总酚测定的影响越大;反之则表明该因素对冬枣中总酚测定的影响越不显著。在交互项对提取率的影响中,福林酚试剂浓度与碳酸钠用量的交互作用显著,其他因素之间交互作用不显著,这与方差分析的结果一致。
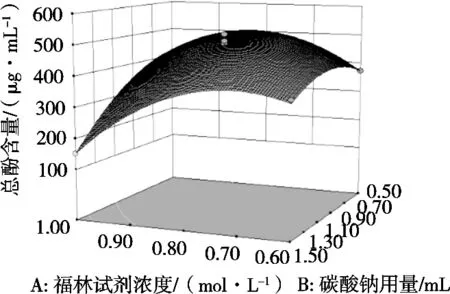
图5 福林酚试剂浓度与碳酸钠用量交互作用对总酚测定的影响
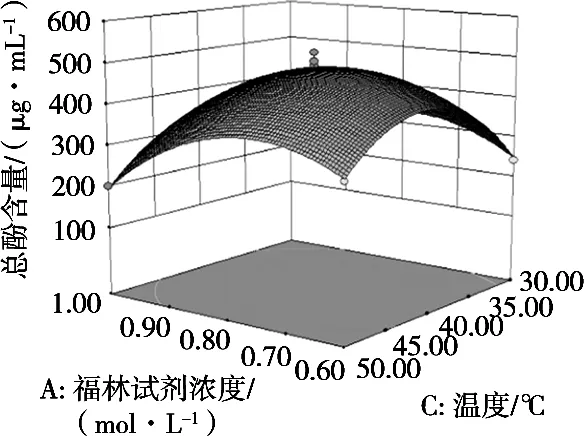
图6 福林酚试剂浓度与反应温度交互作用对总酚测定的影响
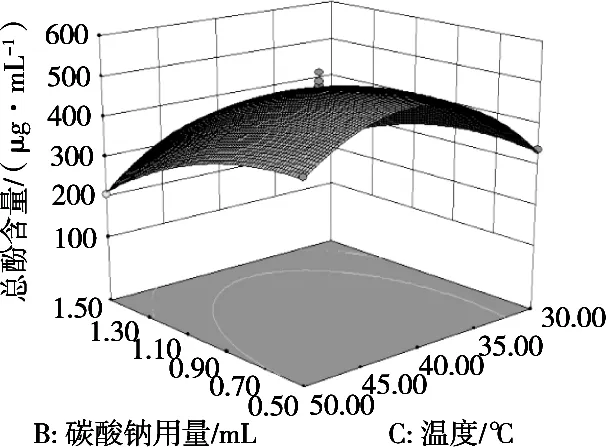
图7 碳酸钠用量与反应温度交互作用对总酚测定的影响
2.2.3 最优测定条件确定
利用Design Expert 8.0.6软件对数据进行处理,得到的最佳测定条件:福林酚试剂浓度为0.81 mol/L、20%碳酸钠溶液用量为0.63 mL、反应温度为40.03℃。得到的预估总酚测定值为509.498 μg/mL。参照最佳工艺条件,且将测定条件在实际操作中略作调整:福林酚试剂浓度为 0.8 mol/L、20%碳酸钠浓度的用量为0.6 mL、反应温度设为40℃,并进行平行试验进行验证,所测得的平均值为501±3.58 μg/mL,验证试验的结果低于表2中的最高值,但是与最佳条件下的总酚含量测定的预估值相近,且吻合度高达98.4%,这验证了该测定条件的可靠性。
3 方法学考察
3.1 稳定性试验
准确吸取1 mL冬枣多酚提取溶液,加入0.8 mol/L福林酚试剂,30 s后加入0.6 mL 20%碳酸钠浓度,置于40℃ 水浴锅中反应1 h,取出后分别放置0,1,2,3和4 h,再进行吸光度的测试,所测得的吸光度分别为0.485,0.482,0.480,0.479和0.479。吸光度呈现下降趋势,但下降的程度不大,在2 h以后趋于稳定。这验证了该方法的稳定性。
3.2 重复性试验
准确吸取1 mL冬枣多酚提取溶液,加入0.8 mol/L福林酚试剂,30 s后加入0.6 mL浓度为20%的碳酸钠,置于40℃水浴锅中反应1 h,并进行5次平行试验,所测得的冬枣多酚含量分别为501,497.42,504.35,495.60,492.94和502.20 μg/mL,根据上述测得的多酚含量计算出标准偏差,为4.33%,说明该方法重复性良好,获得的数据可靠。
3.3 加标回收率试验
准确吸取1 mL冬枣多酚提取溶液,分别加入质量浓度为1,2和3 μg/mL的没食子酸标品,按照响应面分析获得的最佳工艺条件进行试验,每一个没食子酸标品的浓度均进行3次平行试验,获得的加标回收率的平均值分别为98.6%,100.2%和100.5%,平均加标回收率为99.7%,这进一步证明了该工艺条件的稳定。
4 结论与讨论
参照响应面分析得到的结果,将测定条件在实际操作中略作调整,获得的最佳工艺条件为福林酚试剂浓度 0.8 mol/L、20%碳酸钠浓度的用量为0.6 mL、反应温度40℃。在此条件下测得的冬枣总酚平均值为501±3.58 μg/mL,与预估值509.498 μg/mL的吻合度高达98.4%。所得冬枣总酚的测定结果稳定,数据可靠。
由于福林酚法也是测定蛋白质的方法[18-19],冬枣中的蛋白质会干扰试验结果,但是潘莹[20]证明冬枣中的蛋白质含量极少,这种干扰不会对试验结果造成太大影响。由于所用碳酸钠溶液中溶质的溶解度随温度变化较明显[21],所以该方法在使用时建议在温度适宜且恒定的条件下使用。

