参麦注射液联合EPOCH 化疗方案对非霍奇金淋巴瘤患者疗效及生活质量的影响
张畅英,匡跃敏,黄 黎,王 莉,蒋志勇(金华市人民医院血液内科,浙江 金华 321000)
恶性淋巴瘤是一种原发于淋巴样器官的实体瘤,可将其分为霍奇金氏淋巴瘤、非霍奇金氏淋巴瘤两种类型[1-2],它是临床常见肿瘤之一,可发生在任何年龄阶段,以青少年为好发人群[3]。流行病研究显示,非霍奇金氏淋巴瘤发病率约为霍奇金氏淋巴瘤的7 倍左右,而且在世界范围内仍呈逐年上升趋势[4-5]。本研究探讨参麦注射液联合依托泊苷+泼尼松+长春新碱+环磷酰胺+多柔比星(EPOCH)化疗方案对非霍奇金淋巴瘤患者疗效及生活质量的影响,为相关临床治疗提供依据,现报道如下。
1 资料与方法
1.1 一般资料 2017 年3 月至2018 年5 月收治于金华市人民医院的78 例中度非霍奇金氏恶性淋巴瘤患者,随机数字表法分为观察组(40 例)和对照组(38 例)。其中,观察组男性29 例,女性11 例;年龄23~71 岁,平均年龄(43.85±5.38)岁;临床分期Ⅱ期6 例,Ⅲ期29 例,Ⅳ期5 例,而对照组男性30 例,女性8 例;年龄21~70 岁,平均年龄(44.27±6.31)岁;临床分期Ⅱ期7 例,Ⅲ期28例,Ⅳ期3 例。2 组一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 纳入、排除标准
1.2.1 纳入标准 ①经临床病理学/细胞学诊断确诊为非霍奇金淋巴瘤;②临床分期Ⅱ~Ⅳ期;③预计生存期≥3 个月;④KPS 评分≥60 分;⑤年龄20~75 岁;⑥可评价病灶≥1 个;⑦研究经医院伦理委员会批准,患者自愿签署知情同意书;⑧初治患者。
1.2.2 排除标准 ①复发性非霍奇金淋巴瘤;②合并心、肝、肾等严重疾病;③合并其他恶性肿瘤;④合并精神疾病。
1.3 治疗手段 对照组给予EPOCH 化疗方案,包括50 mg/m2依 托 泊 苷、10 mg/m2多柔比 星或吡 柔比星、0.4 mg/m2长春新碱静脉滴注,持续1~4 d;750 mg/m2环磷酰胺静脉滴注,第5 天;60 mg/m2波尼松口服,1~5 d,21 d 为1 个疗程。观察组在对照组基础上加用参麦注射液(云南个旧生物药业有限公司,国药准字Z53021721),取50 mL,加到500 mL 5% 葡萄糖注射液中静脉滴注,每天1 次,连续14 d,间歇7 d 后进行下一个疗程。2 组均治疗2 个疗程。在疗程开始的第1~2 天,化疗前30 min 给予患者5-HT3 拮抗剂盐酸格拉司琼以预防呕吐,化疗期间若患者白细胞计数<1.5×109/L 则皮下注射粒细胞集落刺激因子(G-CSF)至1.0×1010/L。
1.4 指标检测 根据WHO 及美国国立综合癌症网络(NCCN)指南建立相关疗效评价标准[6]。(1)缓解,临床症状及影像学上异常病灶消失,病理症状、相关异常生化指标恢复正常;(2)部分缓解,在全身选取6 个较大淋巴结或肿块SPD 较治疗前范围减小≥50%,而且去除上述所选的6 个淋巴结外无其他淋巴结异常增大,或者肝、脾病灶SPD 缩小≥50%;(3)稳定,不符合(1)(2)或(4);(4)进展,治疗后原有淋巴结或肿块增大,或出现新增肿块病灶。有效率=缓解率+部分缓解率。
患者化疗毒性反应发生情况采用WHO 抗癌药物常见毒副反应分级标准[7],分为0 度、Ⅰ度、Ⅱ度、Ⅲ度、Ⅳ度,Ⅱ度+Ⅲ度+Ⅳ度为不良反应。
患者生活质量评价采用国际公认的生存质量测定量表简表(WHOQOL-BREF)问卷[8],包含26 个计分条目,分别从生理、心理、社会关系、环境4 个领域进行考察。
1.5 统计学处理 通过SPSS 22.0 软件进行处理,计量资料以(±s)表示,组间比较采用t检验;计数资料以百分率表示,组间比较采用卡方检验。以P<0.05 为差异具有统计学意义。
2 结果
2.1 临床疗效 观察组总有效率高于对照组(P<0.05),见表1。

表1 2 组临床疗效比较[例(%)]
2.2 化疗毒性反应 观察组消化道反应、肝功能损害、肾功能损害发生率低于对照组(P<0.05),但2 组白细胞减少发生率比较,差异无统计学意义(P>0.05),见表2。
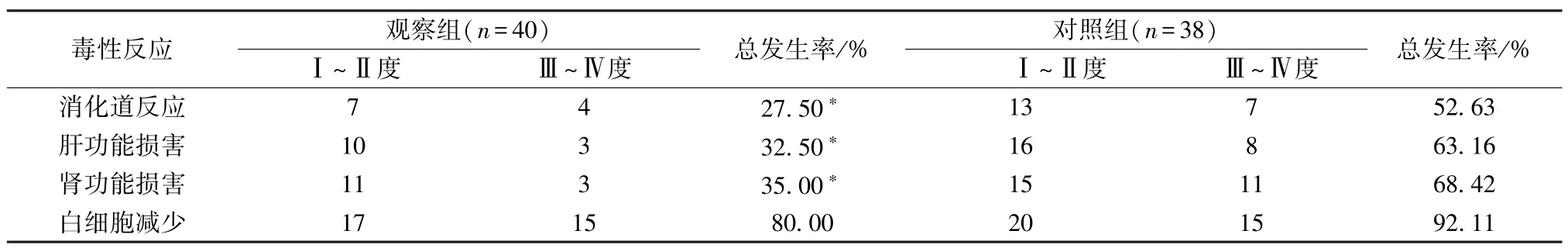
表2 2 组化疗毒性反应比较(例)
2.3 生活质量 治疗后,2 组生理领域、心理领域、社会关系领域、生活环境领域评分降低(P<0.05),以对照组更明显(P<0.05),见表3。
表3 2 组生活质量比较(±s)

表3 2 组生活质量比较(±s)
注:与同组治疗前比较,∗P<0.05;与对照组治疗后比较,#P<0.05。
3 讨论
对于中高度恶性非霍奇金淋巴瘤患者而言,其治疗方案以化疗为主,环磷酰胺+阿霉素+长春新碱+泼尼松(CHOP)化疗方案是目前公认的一线方法,远期生存率可达40%,但仍有50%~60%的患者出现复发或耐药[9-10],也是死亡的主要原因。EPOCH 化疗方案是以CHOP 为基础,由长春新碱、足叶乙苷、阿霉素等药物组成,可逆转肿瘤细胞耐药,增加对抗耐药瘤株的杀伤作用,增强其抗肿瘤作用,但仍存在不良反应,如造血功能受抑、感染、胃肠反应、黏膜炎、肝脏、心脏毒性等,从而降低患者生存质量,影响治疗效果[11],这也成为目前非霍奇金淋巴瘤的研究热点。
中医药在提高化疗疗效、改善化疗不良反应等方面发挥了良好的作用,通过提高机体免疫功能来增强患者耐受性,使其生活质量得到提高[12-13]。参麦注射液组方人参、麦冬,具有益气固脱、养阴生津、生脉功效,与化疗药物联合使用时具有一定增效作用,同时有助于减少后者所引起的毒性反应[14-15]。药理研究表明[16-17],人参可有效刺激机体造血器官,从而促进机体造血功能旺盛,提高免疫力,促进血细胞生成,避免多种原因所导致的血细胞减少,提高网状内皮系统功能;麦冬可显著增加外周血细胞数量,促进血细胞的生成。
本研究发现,观察组患者近期治疗临床疗效显著高于对照组,消化道反应、肝功能损害、肾功能损害发生率也显著降低,与文献[18]报道相似,提示参麦注射液联合EPOCH 化疗方案可有效提高临床疗效,同时降低不良反应发生率。前期报道显示,参麦注射液可有效提高患者白细胞计数,从而降低白细胞减少发生率[19],而本研究中虽然观察组白细胞减少发生率较对照组有所降低,但无显著性差异,可能是由于纳入样本量较小所引起。此外,治疗后2 组患者生理、心理、社会关系、生活环境领域评分均显著降低,以对照组更明显,与文献[20]报道相似,表明患者化疗后生活质量有所降低,而联合给药后其降低程度较小,可能与参麦注射液可降低化疗毒性反应、提升化疗耐受性等因素有关。
综上所述,参麦注射液联合EPOCH 化疗方案可有效提高非霍奇金淋巴瘤患者临床疗效,降低毒性反应,同时有助于生活质量提高。

