煤矿酸性废水对喀斯特稻田环境污染的实验研究*
王 虎 吴永贵 覃远翠 刘桂华 罗有发 付天岭# 何 照
(1.贵州大学资源与环境工程学院,贵州 贵阳 550025;2.贵州雏阳生态环保科技有限公司,贵州 贵阳 550025;3.贵州省土壤肥料研究所,贵州 贵阳 550006)
煤矿酸性废水(AMD)的污染问题已在世界范围内引起人们的广泛关注[1-4]。大量调查性污染评价工作在AMD污染造成周边及下游地区的稻田土壤酸化[5-6],土壤、作物重金属污染[7-8]等方面开展,相对深入的研究工作主要是关于重金属形态及生物有效性分析方面[9-10]。但这些工作主要针对红壤、酸性硫酸盐土等非岩溶区土壤,而针对喀斯特地区土壤的研究较少。而且,这些工作大都单独针对土壤开展,对于水-土体系整体水平,特别是对脆弱喀斯特地区的稻田土壤系统方面的研究尚未见报道。
同时,土壤微生物量及土壤酶活性作为土壤质量及肥力水平的关键影响因素[11-15],显著影响着土壤系统中养分的转化、持续供给及对有害物质的抗性,密切关系着土壤生产力及作物品质[16-18]。AMD污染对稻田土壤酶活性的研究主要有许超等[19]、申万暾等[20]开展的AMD污染地调查性分析研究,但对不同程度AMD污染的稻田土壤环境中酶活性等微生物的变化特征尚缺乏系统研究。
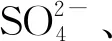
1 材料与方法
1.1 样品采集与制备

1.2 试验设计与方法
分别取2 g(干样计)过5 mm筛的新鲜水稻土壤,参照刘桂华等[24]244的试验方法用已知酚酞酸度的AMD滴定绘制土壤酸碱滴定曲线,并根据滴定曲线,设置7个AMD污染倍数梯度。称取200 g(干样计)新鲜稻田土壤样品于5 L PP级圆柱形塑料桶底部,上层添加不同AMD污染的田面水,模拟AMD污染的稻田土壤系统,每个AMD污染倍数梯度设置3个平行,20~25 ℃下稳定1周。


1.3 数据统计与分析
采用DPS2000统计分析软件包进行数据的统计与分析。
2 结果与分析
2.1 AMD污染对岩溶地区稻田pH、EC、Eh的影响
如表1所示,当AMD污染倍数为0~5.0时,田面水pH虽下降,但都维持在7.5以上,10.0时pH迅速下降到4.5以下,15.0~20.0时pH下降相对减缓,20.0时pH为3.00;当AMD污染倍数较低时,土壤pH下降相对不明显,0~10.0时pH仍能维持在7左右,其后开始直线下降,20.0时pH降至3.56。这表明,稻田田面水和土壤中均有较强的缓冲作用,但AMD污染倍数为15.0~20.0时也均呈极显著下降的趋势(p<0.01)。当AMD污染倍数为0~5.0时,田面水及土壤的EC均急剧升高;10.0时EC趋于平缓甚至轻微下降;15.0~20.0时EC又明显升高,且田面水比土壤变化明显。当AMD污染倍数为0~10.0时,田面水Eh有一定的波动性,从起始的217.70 mV逐渐升高到5.0时的242.70 mV,10.0时Eh有一个最低点,下降到204.70 mV,其后Eh则迅速增加至20.0时的331.30 mV,比未污染时升高50%以上;土壤Eh从起始的196.66 mV逐步增加到20.0时的336.66 mV。综上,AMD的持续污染可极显著地改变稻田水水体系统的pH环境、盐度及氧化还原环境(p<0.01)。
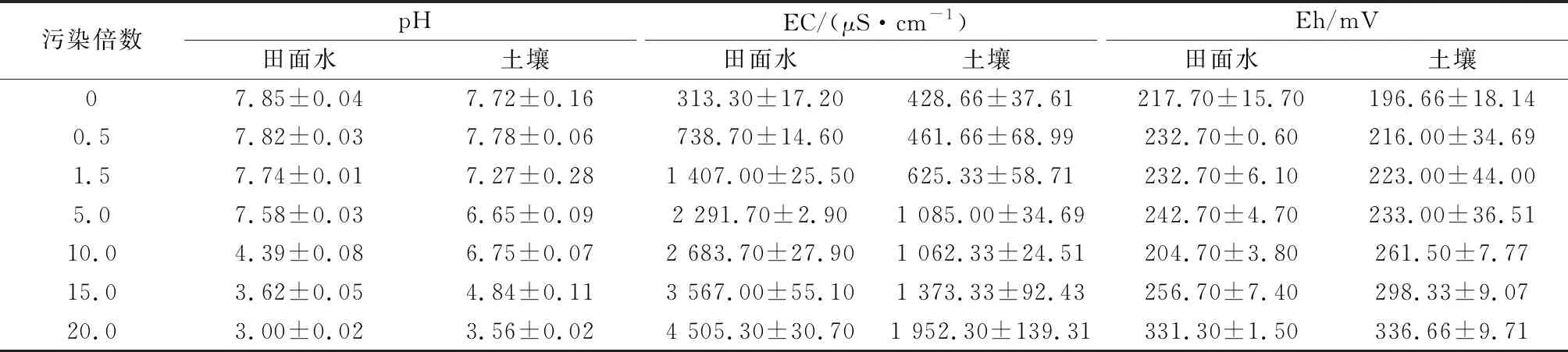
表1 不同AMD污染倍数下喀斯特稻田田面水和土壤pH、Eh和EC的变化趋势
2.2 AMD污染下喀斯特稻田中特征污染组分的变化
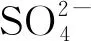
当AMD污染倍数为0~15.0时,田面水中铁均维持在50 mg/L以下明显较低的水平,仅20.0时才显著增加(p<0.05),达到630.14 mg/L(见表3),此时田面水及土壤pH已接近甚至低于3.5(见表1),但仍远低于AMD中铁初始值(3.11 g/L)。随着AMD污染程度的持续增加,土壤中铁均呈显著增加的趋势(p<0.05),风干土壤的颜色更加呈现铁污染的典型赭色特征,这也与VAN ROTTERDAM LOS等[29]288、BLECKER等[30]对矿业活动或废水灌溉对土壤影响的研究结果相一致。当AMD污染倍数为0~5.0时,田面水中锰维持在1 mg/L以下的较低水平,10.0~15.0时急剧升高,20.0时趋于平缓,维持在明显较高的水平,已明显高于AMD中锰初始值(61.00 mg/L)。当AMD污染倍数为0~5.0时,土壤中锰呈逐步增加的趋势,其后显著降低(p<0.05),10.0~20.0时已明显低于原土中锰初始值(约675 mg/kg)。田面水中铜、锌在较低污染倍数下均维持在明显较低的水平,后随着AMD污染程度的增加,铜、锌显著升高(p<0.05)。整体上,随着AMD污染程度的增加,土壤中铜、锌与锰呈现基本一致的变化趋势。综上,在较低污染程度下稻田土壤系统有较好的缓冲性能,田面水中重金属污染水平较低;但在较高污染程度下将丧失缓冲性能,同时导致土壤已有组分的溶出,明显增加锰、铜、锌在田面水中的含量。

表2 不同AMD污染倍数下喀斯特稻田中酸碱度及的变化趋势

表3 不同AMD污染倍数下喀斯特稻田田面水和土壤中铁、锰、铜和锌的变化趋势
2.3 AMD污染下喀斯特稻田中微生物学指标的变化
如表4所示,AMD污染可显著降低稻田土壤微生物量(p<0.05)。未污染的稻田土壤微生物量可达51.91 nmol/g,随着AMD污染倍数的持续增加,土壤微生物量先急剧下降,当AMD污染倍数为10.0时达到最低值(30.48 nmol/g),降低程度达40%之多,之后又呈持续增加的趋势,但最终仍明显低于未污染土壤。随着AMD的持续污染,土壤脲酶活性整体呈极显著降低的趋势(p<0.01),从未污染土壤的1.08 mg/(g·h)急剧下降到当AMD污染倍数为20.0时的0.14 mg/(g·h)。AMD污染对磷酸酶活性的影响不明显,当AMD污染倍数为0~15.0时一直维持在1.60~1.98 mg/(g·h),直到20.0时才下降到0.77 mg/(g·h)。当AMD污染倍数为0~1.5时,过氧化氢酶活性急剧增加,之后增幅明显变缓,但仍呈总体增加的趋势。本研究中过氧化氢酶活性随着AMD污染程度的增加呈极显著增加的趋势(p<0.01),与诸多研究的规律不同。同时,关松荫等[31]表明,过氧化氢酶活性在显碱性的褐土、栗钙土、潮土、紫色土、石灰岩土、水稻土中较高,而在微酸性的白浆土、棕壤、黄壤和红壤中较低;万忠梅等[32]指出,pH<5时,过氧化氢酶活性几乎丧失。本研究明显与他们相悖。
3 讨 论
AMD持续污染影响稻田pH、EC、Eh等综合性能指标。污染前期较低污染倍数下,喀斯特稻田对酸污染有较好的缓冲性能,但长期高强度的持续污染下可导致田面水及土壤的明显酸化;增加田面水及土壤的EC和Eh。AMD中极低的pH能引入的大量H+,势必会降低稻田pH环境[33],但喀斯特稻田土壤中含有较丰富的碳酸盐岩矿物的岩溶组分[34],可有效缓冲H+污染[35];但高浓度AMD持续污染1周后,稻田土壤pH由原来的7.72降到3.56,将会使缓冲体系失效,导致稻田体系的严重酸化。AMD中丰富阴阳离子含量,体现在明显较高的EC(6 361.00 μS/cm),可直接增加田面水和土壤盐度,较低的pH也可明显促进土壤中矿物组分的溶解释放;同时,结合AMD中高浓度的氧化性铁锰离子,将会提高稻田的Eh,AMD污染倍数为10.0时田面水出现一个最低点主要是由于田面水pH急剧下降到4.39,破坏了土壤原有岩溶环境,致使微生物等有机体死亡与腐解,土壤淋出液中有机质增加,降低了田面水Eh(204.70 mV)。


表4 不同AMD污染倍数下喀斯特稻田土壤微生物量和过氧化氢酶、脲酶、磷酸酶活性的变化趋势
AMD污染可对稻田土壤的微生物及其酶活性产生影响。AMD灌溉会引入大量的酸、盐及有害重金属等污染组分,导致pH、盐度、氧化还原环境等变化,将会直接杀死体系中原有的微生物或明显抑制其活性[39-40],进而降低稻田土壤中的微生物含量,同时明显降低土壤中多种酶活性[41-42]。由于AMD中含有丰富的嗜酸性微生物[43],随着污染程度的增加,逐渐适合酸性微生物的存活和生长,进而使得土壤微生物量又逐步增加,但AMD持续污染过程中稻田原有微生物类群及AMD嗜酸微生物类群的变化及演替过程有待进一步研究。除酸、盐、重金属等引入外,土壤中的矿物养分和团粒结构改变对土壤微生物量和酶活性也有重要影响。研究表明:脲酶、磷酸酶、转化酶、过氧化氢酶等主要土壤酶活性与土壤中的有机质、全氮、全磷及有效态氮磷的含量呈正相关关系[44];土壤酶主要以酶-无机矿物胶体复合体、酶-腐殖质复合体和酶-有机无机复合体等形式存在于土壤中,黏粒和腐殖质含量较高的土壤中酶活性的持续期相对较长、活性相对较高[45-47]。稻田养分指标的分析结果表明,随着AMD污染程度的增加,土壤有机质、全氮、全磷、有效氮及有效磷均呈极显著降低的趋势(p<0.01);AMD污染条件下土壤中铁铝氧化膜的大量溶出使团粒中矿物的连接变得疏松分散,导致土壤团粒结构发生变化,并出现孔洞,使土壤变得较蓬松。综上,AMD的持续污染明显改变了土壤的物理结构、化学特性、矿物组分及养分含量,引入了大量外来有害组分,将导致土壤微生物数量及酶活性等土壤微生物特性的退化。
本研究中过氧化氢酶活性随着AMD污染程度的增加总体呈极显著增加的趋势(p<0.01),与现有诸多研究结论不符,造成以上趋势主要是因为AMD污染引入丰富的H+和铁锰等氧化物质。298.15 K、酸性介质中,O2/H2O2、Fe3+/Fe2+、H2O2/H2O标准电极电势分别为0.682、0.771、1.776 V,Fe3+/Fe2+可在酸性条件下作为催化剂将H2O2分解为O2和H2O。AMD污染引入大量H+,将营造一个酸性环境,引入丰富的铁离子将会促进H2O2的分解,进而造成过氧化氢酶活性的假阳性。因此,具体改进方法可做进一步研究。
4 结 论
(1) 在污染前期较低污染倍数下,喀斯特稻田水-土系统对AMD污染有较好的缓冲性能,但高浓度持续污染1周以上可导致稻田田面水及土壤的明显酸化,增加体系的EC和Eh。

(3) AMD污染可降低稻田土壤微生物量、脲酶活性,但对磷酸酶活性的影响不明显;由于AMD引入大量H+及丰富的铁离子将会促进H2O2的分解,进而造成过氧化氢酶活性总体升高的假阳性趋势。
——以长江中游单季稻田为例

