NH4-N氮源下海洋酸化对东海原甲藻和米氏凯伦藻生长的影响❋
贺云凤, 逄 凯, 李克强, 梁生康, 王修林
(中国海洋大学海洋化学理论与工程技术教育部重点实验室,山东 青岛 266100)

氮是海洋生物生长和繁殖的重要元素之一,且已成为海洋生物生长和生物群落演替的限制因素, 此外,溶解无机氮(DIN)是浮游植物生长的必需营养物质[5-7]。NH4-N作为一种还原态氮形式,可被浮游植物直接吸收利用而不需消耗较多能量,而其它两种DIN—NO3-N和NO2-N,则需要被硝酸还原酶(NR)还原成氨氮等还原态氮才能被浮游植物利用,所以在三种DIN中,浮游植物优先吸收利用NH4-N[8-9]。
在过去的几十年里,有害藻华(HABs)对世界沿海地区的海洋渔业、公共卫生和水生环境造成巨大损害[10-12],已经成为全世界沿海地区的主要环境问题之一[13]。东海原甲藻(Prorocentrumdonghaiense)和米氏凯伦藻(Kareniamikimotoi)是中国东南沿海地区HABs的主要优势藻种且二者存在演替现象[14-15]。近年来,东海原甲藻是中国东海海域大规模HABs的主要种类,常见于浙江沿岸和长江口的表层和次表层水域[16-19]。米氏凯伦藻是一种在全球广泛分布的甲藻,它常在太平洋沿岸[20-25]、大西洋[26-28]和印度洋[29]以及中国东海发生形成HABs。米氏凯伦藻是一种典型的鱼类毒性物种,其毒性对野生鱼和养殖鱼都是致命的[30-31],除此之外,它还与贝类和其它无脊椎动物的死亡有关[32-36]。
浮游植物是主要的初级生产者,并在全球范围内影响海洋的碳循环。不同浮游植物的CO2浓缩效率和调节机制不同,则其对海洋酸化的响应就不同。研究表明,海洋酸化对海洋原甲藻(Prorocentrummicans)、亚历山大藻(Alexandriumsp.)和短孢角毛藻(Chaetocerosbrevis)的生长并无明显影响[37-39],而三角褐指藻(Phaeodactylumtricornutum)、牟氏角毛藻(Chaetocerosmuelleri)和塔玛亚历山大藻(Alexandriumtamarense)的生长却受到了海洋酸化的抑制[40-42]。
为此,本文选取东海原甲藻和米氏凯伦藻,在室温、模拟光照条件下,以NH4-N为氮源, 通过增加pCO2改变海水的酸化程度,研究海洋酸化对米氏凯伦藻和东海原甲藻生长的影响,并分析两种甲藻对NH4-N的吸收动力学和生物酶活性,探讨其环境适应性。
1 材料与方法
1.1 实验藻种的培养
为了模拟海洋酸化对东海原甲藻和米氏凯伦藻生长的影响,培养实验设置3个pH梯度:8.10(当前海水pH值)、7.81(21世纪末海水pH值)和7.45(高酸化海水pH值),分别对应通入CO2浓度为380、800和1 500 μatm的混合空气。培养实验中使用的CO2混合空气采用称量法配置,即将纯原料气定量地从原料气瓶转移到混合气气瓶来制备,组分气体的添加量通过称量充装前后的标准气瓶来确定。同时,每个pH值设置两个平行样。
培养实验所用东海原甲藻接种于中国海洋大学海洋化学理论与工程技术教育部重点实验室藻种室,米氏凯伦藻接种于中国科学院海洋研究所海洋生态与环境科学重点实验室藻种室,将藻种均保存于f/2培养液并置于光照培养箱中(光照强度191 μmol·m-2·s-1,光暗比为12 h∶12 h,温度为(20±1)℃)。将培养实验所用海水(胶州湾近海海域,36°5′42″N, 120°15′41″E, PO4-P:0.946 μmol·L-1;NO2-N:0.561 μmol·L-1;NO3-N:0.842 μmol·L-1;NH4-N:1.453 μmol·L-1)经孔径0.45 μm的醋酸纤维膜过滤以除去颗粒物,再将过滤海水置于高压灭菌锅中120 ℃下高温高压灭菌20 min。实验采用5 L锥形瓶进行培养,向培养瓶中加入3.5 L灭菌海水,以锡纸(实验前450 ℃下灼烧4 h)为盖,分别通入不同CO2浓度的混合空气,待三个pH梯度的海水碳酸盐系统平衡后添加藻种,取100 mL东海原甲藻藻液和200 mL米氏凯伦藻藻液加入到3.5 L灭菌海水中,使藻密度达到2 000 cell/mL左右,再加入NH4-N(30 μmol·L-1,NH4Cl;国药集团化学试剂有限公司(SCRC))和PO4-P(1.5 μmol·L-1,KH2PO4;国药集团化学试剂有限公司(SCRC)),微量元素和维生素浓度按照f/2培养液浓度比例添加(上海光语生物科技有限公司)(见表1)。东海原甲藻培养实验周期为10天,米氏凯伦藻培养实验周期为20天,取样频次为1~2次/d,具体取样频次根据两种藻的生长规律而定。取样前将培养体系摇匀,取200 mL藻液经0.7 μm的 GF/F玻璃纤维膜(Whatman 公司,450 ℃下灼烧4 h)过滤,滤膜用于测定SOD酶、CAT酶活性和叶绿素,将滤液装入60 mL的棕色玻璃瓶中,用于测定水体中的NH4-N,并将样品置于-20 ℃下保存。
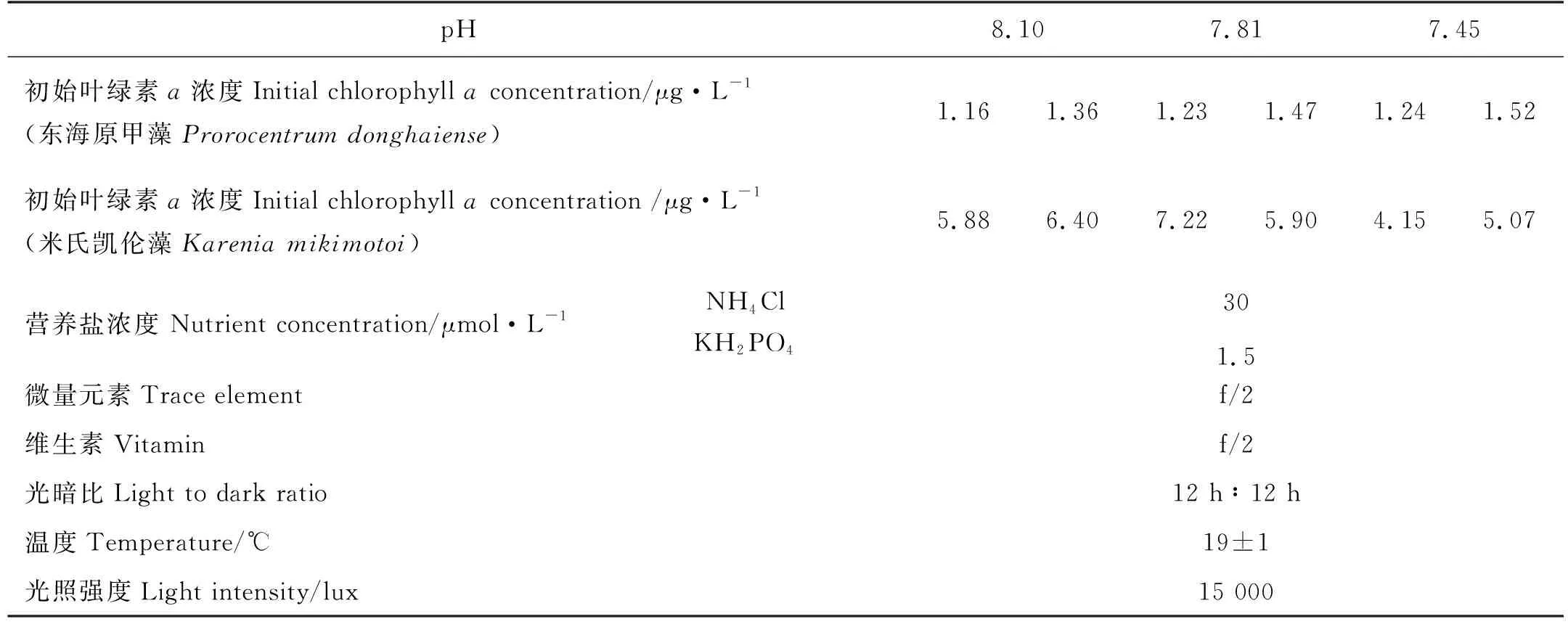
表1 东海原甲藻和米氏凯伦藻培养实验条件Table 1 Experimental conditions of Prorocentrum donghaiense and Karenia mikimotoi
1.2 pH的调节与测定
为维持培养体系pH环境的稳定,在体系中加入生物缓冲剂HEPES[43-44](~0.04或~0.05 g·L-1),并采用以间甲酚紫为指示剂的分光光度法测定体系的pH值[45]。为观测pH的变化幅度,前期取样较密集,观测结果发现pH的波动范围不大,即在培养后期减少了对pH的观测次数。测得培养体系的pH值在整个生长周期内变化范围为:0.1±0.05(见图1)。
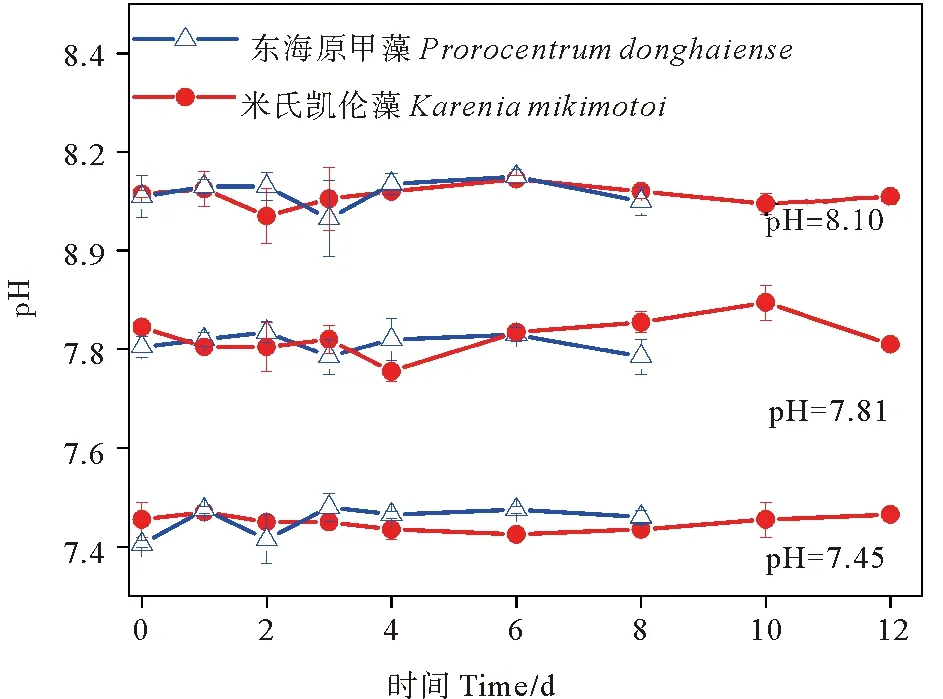
图1 东海原甲藻和米氏凯伦藻培养期的pH波动Fig. 1 pH fluctuations in the culture seawater of Prorocentrum donghaiense and Karenia mikimotoi under experimental processes
1.3 分析方法
叶绿素a的测定[46]:滤膜经8 mL 90%的丙酮溶液在4 °C下避光提取24 h,离心10 min后取其上清液,以90%的丙酮溶液作为空白,采用紫外分光光度计测定630、647、664 nm波长下的吸光度。

SOD酶的测定[48]:依据SOD酶在光下对抑制氮蓝四唑(NBT)的还原作用来确定SOD酶的活性,测定560 nm下的吸光度。
CAT酶的测定[48]:依据CAT酶可在磷酸缓冲液中催化H2O2,在240 nm波长下,可用H2O2的减少速率来确定CAT的活性。即以A240nm每分钟减少0.01为1个CAT酶活性单位(U·mg-1·min-1)。
1.4 数据处理
采用Slogistic2生长模型计算东海原甲藻和米氏凯伦藻的终止生物量和最大生长速率,通过Origin8.5软件(The Microcal Inc.)拟合生长曲线,公式如下[49]:
其中:Bt为t时刻的生物量(chla,μg·L-1);Bf为终止生物量(chla,μg·L-1);B0为初始生物量(chla,μg·L-1);μmax为最大生长速率(μg·L-1·h-1)。
氮摄取通常用Michaelis-Menten方程计算,而为了覆盖摄取和生长情况,本文采用Monod方程[50]并将其修改为:

本文通过SPSS 22.0软件(SPSS Inc)对结果进行T检验来判断数据是否存在显著性差异,并设置显著性差异水平为α=0.05。
2 结果
2.1 生长状况
图2为东海原甲藻和米氏凯伦藻在NH4-N和不同pH条件下的生长曲线。东海原甲藻和米氏凯伦藻分别于第2天和第3天开始快速生长进入指数生长期,并分别于第5天和第7天进入稳定生长期,此期间,东海原甲藻和米氏凯伦藻的chla浓度达到峰值,在pH=8.10条件下出现最大值(15.64和46.77 μg·L-1),其次是pH=7.81处(9.75和43.17 μg·L-1),在pH=7.45处chla浓度有最小值(7.45和8.62 μg·L-1)。随后,东海原甲藻和米氏凯伦藻分别于第8天和第11天开始死亡,进入死亡期。在高酸化条件(pH=7.45)下,米氏凯伦藻的生长受到极大限制。
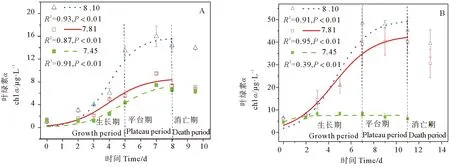
图2 不同pH条件下东海原甲藻(A)和米氏凯伦藻(B)的生长曲线Fig. 2 Growth curve of Prorocentrum donghaiense (A) and Karenia mikimotoi (B) under different pH conditions
Slogistic2生长模型拟合结果表明,在NH4-N条件下,东海原甲藻和米氏凯伦藻的终止生物量和最大生长速率均随pH的下降而降低(见图3)。具体表现为,在pH=8.10处,东海原甲藻和米氏凯伦藻的终止生物量分别为15.76和49.76 μg·L-1,最大生长速率分别为0.182和0.357 μg·L-1·h-1;在pH=7.81处,东海原甲藻和米氏凯伦藻的终止生物量分别为8.66和43.17 μg·L-1,最大生长速率分别为0.076和0.250 μg·L-1·h-1;pH值为7.45时,藻类生长受到极大的限制,东海原甲藻和米氏凯伦藻的终止生物量分别为7.67和7.56 μg·L-1,最大生长速率分别为0.067和0.093 μg·L-1·h-1(见表2)。与自然条件下(pH=8.10)相比,东海原甲藻在pH=7.81处的终止生物量和最大生长速率分别下降了45.0%和58.2%,在pH=7.45处下降了51.3%和63.2%;米氏凯伦藻在pH=7.81处的终止生物量和最大生长速率分别下降了13.2%和30.0%,在pH=7.45分别下降了84.8%和73.9%。显著性分析表明,东海原甲藻在pH=7.81和pH=7.45处的终止生物量和最大生长速率显著低于(p<0.05)pH=8.10处,米氏凯伦藻在pH=7.45处的终止生物量和最大生长速率均显著低于(p=<0.05)pH=8.10处的两个参数,且米氏凯伦藻的终止生物量和最大生长速率显著高于(p<0.05)东海原甲藻。

图3 不同pH条件下东海原甲藻和米氏凯伦藻的终止生物量(A)和最大生长速率(B)Fig. 3 Terminative biomass (A) and maximum growth rate (B) of Prorocentrum donghaiense and Karenia mikimotoi under different pH conditions
2.2 氮吸收动力学
图4为东海原甲藻和米氏凯伦藻在不同pH条件下对NH4-N的吸收曲线,NH4-N分别在96和168 h内被快速吸收。Monod方程拟合结果表明,东海原甲藻和米氏凯伦藻的最大氮吸收速率随pH的下降而降低,半饱和常数和最小浓度阈值随pH的下降而升高。具体表现为,在pH=8.10处东海原甲藻和米氏凯伦藻的最大氮吸收速率有最大值(0.59和0.39 μmol·L-1·h-1),其次为pH=7.81处(0.46和0.34 μmol·L-1·h-1),在pH=7.45处东海原甲藻的最大氮吸收速率有最小值(0.38和0.24 μmol·L-1·h-1)(见图5(A))。显著性分析表明,东海原甲藻和米氏凯伦藻在酸化(pH=7.81和pH=7.45)条件下的最大氮吸收速率显著低于(p<0.05)正常海水条件下,且东海原甲藻的最大氮吸收速率显著高于(p<0.05)米氏凯伦藻。
在pH=7.45处东海原甲藻和米氏凯伦藻的半饱和常数有最大值(1.36和7.81 μmol·L-1),其次为pH=7.81处(0.39和2.31 μmol·L-1),在pH=8.10处有最小值(0.24和1.57 μmol·L-1)(见图5(B))。显著性分析表明,米氏凯伦藻在pH=7.81和pH=7.45处的半饱和常数显著高于(p<0.05)pH=8.10处,且其在pH=7.45处的半饱和常数显著高于(p<0.05)东海原甲藻。
在pH=8.10处东海原甲藻和米氏凯伦藻的最小浓度阈值有最小值(1.10和1.30μmol·L-1),其次为pH=7.81处(2.10和2.17 μmol·L-1),在pH=7.45处有最大值(2.10和7.37 μmol·L-1)(见图5(C))。

表2 不同pH条件下东海原甲藻和米氏凯伦藻的生长和氮吸收动力学参数Table 2 Growth and nitrogen uptake kinetics parameters for Prorocentrum donghaiense and Karenia mikimotoi under different pH conditions
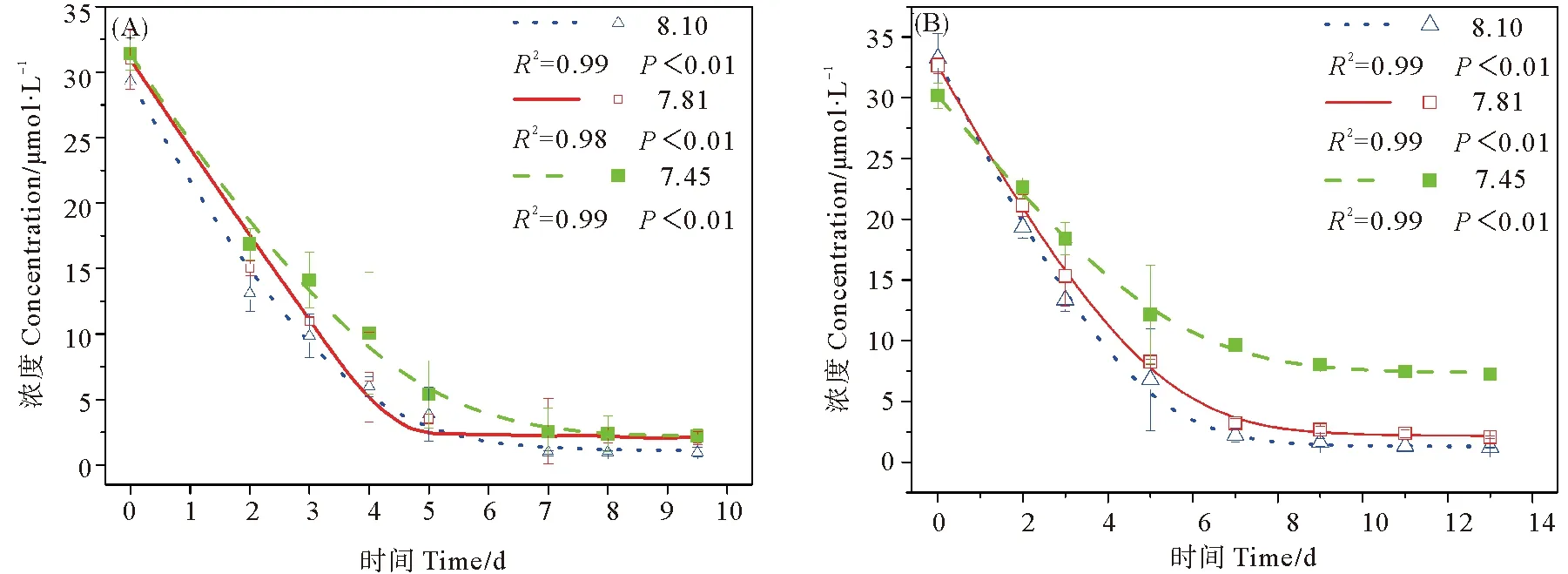
图4 不同pH条件下东海原甲藻(A)和米氏凯伦藻(B)的氮吸收曲线Fig. 4 Nitrogen uptake curve of Prorocentrum donghaiense (A) and Karenia mikimotoi (B) under different pH conditions
Vmax/Ks比率可代表所有养分吸收位点的总亲和力之和,涉及单一藻类和不同条件下特定过程的比率,Vmax/Ks比率越高表明竞争能力越高,可用来表征藻类在竞争生长中的地位。随着酸化程度加深,东海原甲藻和米氏凯伦藻的Vmax/Ks比率均呈现下降趋势。在pH=8.10处东海原甲藻和米氏凯伦藻的Vmax/Ks比率有最大值(2.46和0.25 h-1),其次为pH=7.81处(1.18和0.15 h-1),在pH=7.45处东海原甲藻和米氏凯伦藻的Vmax/Ks比率有最小值(0.28和0.03 h-1)(见图5(D))。与自然条件下(pH=8.10)相比,东海原甲藻在pH=7.81处的最大氮吸收速率和Vmax/Ks比率分别下降了22.0%和52.0%,在pH=7.45处下降了35.6%和88.6%;同样,米氏凯伦藻在pH=7.81处的最大氮吸收速率和Vmax/Ks比率分别下降了12.8%和40.0%,在pH=7.45处分别下降了38.5%和84.0%。显著性分析表明,东海原甲藻在pH=7.45处的Vmax/Ks比率显著低于(p<0.05)pH=8.10处,且东海原甲藻在三个pH条件下的Vmax/Ks比率均显著高于(p<0.05)米氏凯伦藻。
2.3 SOD和CAT酶活性
受酸化条件的影响,东海原甲藻和米氏凯伦藻的SOD和CAT最大酶活性均随pH的下降而升高。东海原甲藻和米氏凯伦藻SOD的最大酶活性在pH=8.10处分别为1.40和2.51 U·μg-1,随着pH值的降低,在pH=7.81处SOD的最大酶活性分别升高至2.12和4.90 U·μg-1,在pH=7.45处,东海原甲藻和米氏凯伦藻的SOD最大酶活性分别升高至2.26和5.76 U·μg-1(见图6(A))。同样,东海原甲藻和米氏凯伦藻的CAT最大酶活性在pH=7.45处最高(5.09和4.40 U·mg-1·min-1),其次是pH=7.81处(4.29和3.63 U·mg-1·min-1)和pH=8.10处(4.06和3.61 U·mg-1·min-1)(见图6(B))。显著性分析表明,在pH=7.81和pH=7.45处,米氏凯伦藻SOD的最大酶活性显著高于(p<0.05)pH=8.10处,且米氏凯伦藻SOD的最大酶活性显著高于(p<0.05)东海原甲藻。

图5 不同pH条件下东海原甲藻和米氏凯伦藻的最大氮吸收速率(A)、半饱和常数(B)、最小浓度阈值(C)和Vmax/Ks比率(D)Fig.5 Maximum nitrogen uptake rate (A), half-saturation constant (B), min-concentration threshold (C) and the Vmax/Ks ratio (D) of Prorocentrum donghaiense and Karenia mikimotoi under different pH conditions

图6 不同pH条件下东海原甲藻和米氏凯伦藻的SOD(A)和CAT(B)最大酶活性Fig. 6 SOD (A) and CAT (B) maximum activity of Prorocentrum donghaiense and Karenia mikimotoi under different pH conditions
3 讨论
海洋浮游植物是世界生态系统的基础,它们对全球变化的响应将影响海洋食物网和全球养分的循环。这些单细胞初级生产者随着潮汐和水流漂移,占据全球碳固定的一半左右,并成为将固定碳汇入到深海生物碳泵的基础[51]。高强度的人为活动导致大气CO2浓度升高,表层海水的pCO2上升、pH下降,从而影响了海洋初级生产者的生长[52-53]。甲藻作为一个世界性的浮游植物群体,具有大量繁殖形成有害藻华的能力,其细胞内的RubisCO酶对CO2的亲和力较低,光合作用易受碳浓度的限制,因此甲藻的生长更易受酸化的影响[54]。在本研究中,东海原甲藻和米氏凯伦藻的生长均受到酸化条件的抑制。随着酸化程度的加深,东海原甲藻和米氏凯伦藻的最大生长速率和终止生物量均呈下降趋势,这是因为酸化程度的加深导致浮游植物需消耗更多的能量以适应这种变化,从而减少了用于浮游植物生长的能量而受到负面影响。
在海洋系统中,氮元素通常是限制浮游植物生长的营养物质,人类活动导致的氮元素输入的增加可以显著改变许多陆地、海洋以及一些淡水环境中的藻类和微生物的生产[55]。受海洋酸化的影响,东海原甲藻和米氏凯伦藻的最大氮吸收速率和Vmax/Ks比率均随pH值的降低而下降。米氏凯伦藻在同等条件下的最大氮吸收速率和Vmax/Ks比率均低于东海原甲藻,表现为较低的竞争能力,酸化过程加剧了这种影响。研究表明,当海水中存在多种形式的氮时,浮游植物将优先使用还原形式氮(NH4-N),因为浮游植物可以通过GS / GAGOT酶直接吸收NH4-N而合成氨基酸[56],且甲藻能够在低NO3-N、高NH4-N的海域大量繁殖[57]。酸化条件会降低能量在细胞内的流通,进而降低细胞对氮的吸收,即在酸化条件下会降低细胞内蛋白质的合成效率[58]。维持细胞内外的离子浓度平衡对浮游植物的生长至关重要,酸化强度加深,细胞内外的pH平衡受到破坏,浮游植物需要消耗大量的能量去维持平衡,进而抑制了浮游植物的生长[59]。在本研究中,pH=7.81和pH=7.45的酸化条件打破了东海原甲藻和米氏凯伦藻正常的细胞内外离子浓度的动态平衡,两种藻必须对酸化条件作出响应并建立适应pH值变化的酸碱平衡,从而影响了藻细胞内正常的代谢速率,所以两种藻对NH4-N的吸收随酸化程度的加深而减少。由Monod方程拟合得到的最小浓度阈值均随pH的降低而增大,由此可见,酸化强度越大,米氏凯伦藻和东海原甲藻对氮的吸收利用率就越低。
在正常情况下,浮游植物体内存在一套完整的抗氧化系统,且ROS的产生和清除始终处于动态的平衡状态[58]。当浮游植物处于海洋酸化条件下,低pH值会导致浮游植物细胞的内外酸碱失衡,进而可激活抗氧化系统,消除过量产生的氧自由基,从而维持正常的浮游植物生理活动[60-61],SOD酶和CAT酶是这个过程中主要的抗氧化酶。研究发现东海原甲藻的生长在受亚麻酸胁迫时,藻细胞内的SOD和CAT活性随着亚麻酸的浓度升高而升高[62]。同样,受氧化作用的胁迫,米氏凯伦藻细胞内SOD和CAT的活性也随之升高[63]。在本研究中,酸化条件下,海水pH值的变化打破了东海原甲藻和米氏凯伦藻细胞内外的酸碱平衡,导致细胞内SOD和CAT的酶活性升高,以此消除过量的ROS对藻细胞的影响,即通过自身的生理调控机制来维持浮游植物正常的代谢活动。当海水pH值低于一定阈值时,浮游植物体内的调控系统达到极限,会导致浮游植物细胞酸中毒进而影响其生长和对氮的吸收,比如在pH=7.45条件下,米氏凯伦藻的生长受到了极大限制。
4 结论
通过实验室藻类培养实验研究了海洋酸化对东海原甲藻和米氏凯伦藻生长、氮吸收和生物酶的影响,实验结论如下:
(1)海洋酸化对东海原甲藻和米氏凯伦藻的生长均有抑制作用。随着酸化程度的加深,两种藻的终止生物量和最大生长速率均呈现下降的趋势。在高酸化(pH=7.45)条件下,米氏凯伦藻的生长受到的抑制更大,显著低于正常海水条件(P<0.05)。
(2)海洋酸化抑制了东海原甲藻和米氏凯伦藻对NH4-N的吸收。随着酸化程度的加深,两种藻的最大氮吸收速率和Vmax/Ks比率均呈现下降的趋势。米氏凯伦藻在同等条件下的最大氮吸收速率和Vmax/Ks比率均低于东海原甲藻,表现为较低的竞争能力,酸化过程加剧了这种影响。
(3)海洋酸化诱导了米氏凯伦藻和东海原甲藻的ROS升高,随着酸化程度加深,抗氧化生物酶(SOD和CAT)的活性升高。海洋酸化对两种甲藻生长的影响,通过抗氧化酶的活性变化从生理层面对外界环境的变化作出响应,与生长和氮吸收过程相对应。

