曲妥珠单抗联合不同化疗方案治疗人表皮生长因子受体-2阳性晚期胃癌患者的回顾性研究
邹 黎,钱 军
(江苏省盐城市第一人民医院,1.肿瘤内科;2.心胸外科,江苏 盐城,224001)
In the trastuzumab-SOX group,RR,DCR and PFS were 47.4%,84.2% and 8.2 months,respectively.
There were no significant differences in short- and long-term efficacy between two groups(P>0.05).Grade 3 or 4 hand-foot syndrome was more frequently observed in the trastuzumab-XELOX group than in the trastuzumab-SOX group,there was no significant difference in the incidence of other adverse reactions (P>0.05).ConclusionTrastumuzab-SOX therapy has the equal efficacy versus trastumuzab-XELOX therapy,but the former has better safety,and can be used interchangeably for patients with Her2-positive advanced gastric cancer.
KEYWORDS:chemotherapy;human epidermal growth factor receptor-2;gastric cancer;gimeracil;tratuzumab;capecitabine
口服氟尿嘧啶类联合铂类药物如卡培他滨联合奥沙利铂(XELOX)或替吉奥联合奥沙利铂(SOX)的方案是不能切除、复发或晚期胃癌(AGC)的治疗方案之一[1]。曲妥珠单抗是一种能结合人表皮生长因子受体-2(Her-2)的特异性单克隆抗体,相关研究[2]证实了曲妥珠单抗加入化疗方案中治疗Her-2阳性AGC患者的有效性。但Her-2阳性胃癌患者比例较低[3],关于这部分人群的研究[4-5]较少,故关于曲妥珠单抗联合SOX方案的有效性和安全性的证据有限。本研究回顾性比较Her-2阳性AGC患者接受曲妥珠单抗联合XELOX与曲妥珠单抗联合SOX方案的治疗疗效及不良反应,现将结果报告如下。
1 资料与方法
1.1 一般资料
Her-2阳性的标准是免疫组化(IHC) 3+,或者IHC 2+并且荧光原位杂交(FISH)阳性。筛选2014年1月—2018年12月本院肿瘤内科收治的符合入选标准的Her-2阳性AGC患者40例,回顾性调查其医疗记录。将曾经接受过曲妥珠单抗联合XELOX方案或曲妥珠单抗联合SOX方案作为一线化疗方案的患者分别纳入曲妥珠单抗-XELOX组(n=21)或曲妥珠单抗-SOX组(n=19)。本研究通过本院伦理委员会审核批准。
1.2 治疗方案
曲妥珠单抗-XELOX组、曲妥珠单抗-SOX组分别采用卡培他滨(850 mg/m2,第1~14天每天2次,每3周为1个周期)、替吉奥(40 mg/m2,第1~14天每天2次,每3周为1个周期)口服,2组中奥沙利铂(130 mg/m2)在每周期第1天静脉滴注。曲妥珠单抗在第1周期第1天以8 mg/kg首剂,随后6 mg/kg静脉滴注。这些程序与相关研究[2]一致。剂量调整方案由主治医生根据患者的一般状况和不良反应决定。
1.3 观察指标
客观疗效根据实体瘤疗效评价标准1.1版评价[6]:客观缓解率(RR),为达到完全和部分缓解的患者比例;疾病控制率(DCR),为达到完全缓解(CR)、部分缓解(PR)和稳定(SD)的患者比例;无进展生存期(PFS),指从治疗开始至疾病进展(PD)或死亡的时间。所有不良反应回顾医疗记录根据不良事件通用术语标准进行评价[7]。患者一般状况参照美国东部肿瘤协作组体力状况评估。
1.4 统计学分析
RR、DCR和毒性反应用双侧Fisher确切概率法进行分析。采用Kaplan-Meier法绘制PFS曲线,两亚组间的比较采用Log-rank检验。用STATA 12.0软件进行分析,P<0.05为差异有统计学意义。
2 结 果
2.1 一般资料
曲妥珠单抗-XELOX组患者年龄45~66岁,曲妥珠单抗-SOX组患者年龄42~60岁,曲妥珠单抗-XELOX组的中位年龄大于曲妥珠单抗-SOX组,差异有统计学意义(P<0.05),2组性别、原发部位、体力状况评分、Her-2状态、转移部位比较,差异无统计学意义(P>0.05)。见表1。
2.2 近期疗效
本研究所有患者的RR、DCR分别为42.5%、85.0%,2组患者RR、DCR比较,差异无统计学意义(P>0.05),见表2。
2.3 远期疗效
采用Kaplan-Meier法绘制2组患者PFS曲线,本研究中所有受试者的中位PFS为7.9个月(95%可信区间为6.7~9.2)。曲妥珠单抗-XELOX组的中位PFS为7.6个月(95%可信区间为5.7~9.4),曲妥珠单抗-SOX组的中位PFS为8.2个月(95%可信区间为6.6~9.9),风险比为0.92(95%可信区间为0.43~1.93),2组间差异无统计学意义(P>0.05)。见图1。

表1 2组患者一般资料比较
Her-2:人表皮生长因子受体-2;IHC:免疫组化;
FISH:荧光原位杂交。
2.4 不良反应
本研究中,患者最常见的严重血液学不良反应是中性粒细胞减少,曲妥珠单抗-XELOX组3~4度中性粒细胞减少的发生率为28.6%,曲妥珠单抗-SOX组为26.3%。只有1例曲妥珠单抗-SOX组患者发生粒缺性发热(3度)。2组均未见4度粒缺性发热或粒缺性发热导致死亡的病例。最常见的3~4度非血液学不良反应是手足综合征,曲妥珠单抗-XELOX组3~4度手足综合征发生率高于曲妥珠单抗-SOX组,差异有统计学意义(P<0.05),2组其他非血液学不良反应如恶心、呕吐、腹泻、周围神经病变、黏膜炎等的发生率比较,差异无统计学意义(P>0.05)。见表3。
3 讨 论
胃癌是世界范围内第3大癌症相关死因,大多数患者在确诊时已失去进行根治性手术的机会[8]。虽然系统性治疗的疗效在不断提高,但不可切除、复发胃癌或AGC患者的中位生存期依然在13.1~16.6个月,预后并不乐观[9-10]。目前胃癌的化疗尚无统一的金标准,提高化疗效果,降低药物不良反应发生率,是肿瘤治疗的研究方向。
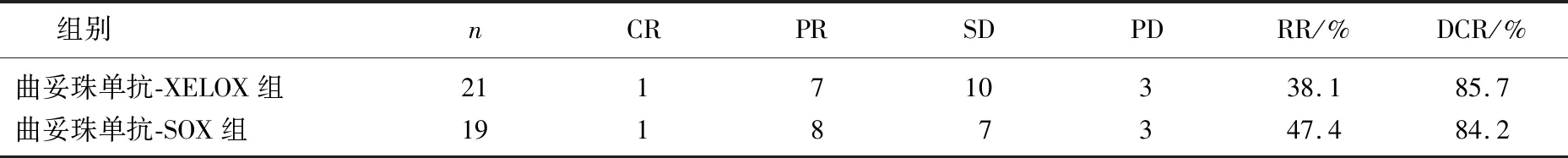
表2 2组患者近期疗效比较
CR:完全缓解;PR:部分缓解;SD:稳定;PD:疾病进展;RR:客观缓解率;DCR:疾病控制率。

AGC的全球标准一线化疗方案是氟尿嘧啶类联合铂类方案。奥沙利铂是第3代铂类药物,不仅抗癌谱广、活性高,而且与顺铂、卡铂等药物不存在交叉耐药[11]。替吉奥是氟尿嘧啶的减毒增效改良制剂,可以减少化疗不良反应。Bodoky等[12]发现,使用替吉奥治疗胃癌的临床疗效优于氟尿嘧啶,且不良反应更轻,替吉奥联合铂类方案也被列入一线化疗方案。
国际性Ⅲ期试验ToGA研究[2]选择将氟尿嘧啶联合铂类(FP)或卡培他滨联合铂类(XP)方案与曲妥珠单抗联合使用,证实了曲妥珠单抗联合化疗方案对Her-2阳性AGC有效。一项日本的Ⅱ期临床研究(HERBIS-1研究)[13]分析了曲妥珠单抗-替吉奥联合铂类方案的安全性和有效性。虽然HERBIS-1研究证明曲妥珠单抗-替吉奥联合铂类方案是有效并安全的,但由于患者数量较少,积累的证据并不充分。本研究探讨曲妥珠单抗-SOX方案治疗Her-2阳性AGC患者的效果是否劣于曲妥珠单抗-XELOX方案,结果发现,曲妥珠单抗-SOX组与曲妥珠单抗-XELOX组的RR、DCR、中位PFS无显著差异。此外,ToGA研究[2]中RR、DCR、中位PFS分别为47%、79%、6.7个月,HERBIS-1研究[13]中分别为68%、94%、7.8个月,与本研究结论相似,提示本研究中曲妥珠单抗联合化疗方案是有效的,且曲妥珠单抗-SOX方案的临床疗效不亚于曲妥珠单抗-XELOX方案。

表3 2组患者不良反应比较[n(%)]
与曲妥珠单抗-SOX组比较,*P<0.05。
卡培他滨的一种典型非血液学不良反应是手足综合征[14]。本研究中,曲妥珠单抗-XELOX组3~4度手足综合征的发生率显著高于曲妥珠单抗-SOX组,其他血液学及非血液学不良反应则无显著差异,与既往比较卡培他滨和替吉奥的研究[15]结果相似。由此表明,曲妥珠单抗-SOX方案的安全性优于曲妥珠单抗-XELOX方案,对于无法耐受手足综合征的Her-2阳性AGC患者而言,曲妥珠单抗-SOX方案不失为一种好的选择。
本研究结果显示,曲妥珠单抗联合SOX方案与曲妥珠单抗联合XELOX方案的疗效相当,但具有更好的安全性,曲妥珠单抗联合SOX方案可与曲妥珠单抗联合XELOX方案互换用于治疗Her-2阳性AGC。但本研究为回顾性分析,无法避免入组年龄存在的差异,且样本量小,随访时间短,远期疗效评价仅分析了中位PFS,不及分析中位总生存期精确,这些均可能造成主观偏倚,故以后还需开展高质量的前瞻性随机对照研究,以提供更多的循证医学证据指导临床实践。

