抗流感药的研发进展及市场情况
张建忠 柯樱 戴厚玲
摘 要 流感是由流感病毒引起的一种急性呼吸道传染病,具有流行面广、传染性强等特点,严重危害人类健康。目前,应对流感病毒感染的主要措施是疫苗接种和药物治疗。本文就抗流感药的国外上市和开发现状以及国内、外销售情况作一简要介绍。
关键词 抗流感药 研发 市场
中图分类号:R978.7 文献标志码:C 文章编号:1006-1533(2020)05-0024-04
Recent progress in research and development of anti-influenza drugs and their situation on market
ZHANG Jianzhong*, KE Ying, DAI Houling
(Department of R&D Management, Shanghai Pharmaceuticals Holding Co., Ltd., Shanghai 200020, China)
ABSTRACT Influenza is an acute respiratory infectious disease caused by influenza virus and is characterized by wide spread and strong infectivity and can seriously endanger human health. At present, the main therapies for influenza virus infection are vaccination and drug treatment. The foreign development status, domestic and foreign sales of anti-influenza drugs are outlined.
KEY WORDS anti-influenza drugs; research and development; market
流行性感冒(以下簡称流感)是由流感病毒引起的一种急性病毒性呼吸道感染疾病[1]。流感病毒属于正黏病毒科成员,分为甲型流感(IVA)、乙型流感(IVB)、丙型流感(IVC)和丁型流感(IVD)4种类型。甲型流感和乙型流感是人类流感的主要病原体。甲、乙型流感病毒的基因组为负链RNA,分为HA、NA、M、NP、PBl、PB2、PA和NS等8个节段。结构蛋白血凝素(hemagglutinin, HA)、神经氨酸酶(neuraminidase, NA)和M2蛋白嵌合在病毒包膜上,M1基质蛋白位于病毒包膜以下,病毒核心是由核蛋白(nuclear protein, NP)包裹病毒基因组RNA构成的核蛋白体[2]。流感在全球的感染范围比较广,每年约有500万人会感染流感,其中造成50万人死亡[1]。当前,对流感的预防手段主要就是疫苗预防及药物防治,而由于流感病毒变异性较强,所以疫苗预防有一定的滞后性,因此,流感治疗主要依靠抗流感病毒药物防治。本文就抗流感药的国外上市和开发现状以及国内、外销售情况等作一简要介绍。
1 国外抗流感药的研发现状和市场情况
1.1 目前常用的几种抗流感药
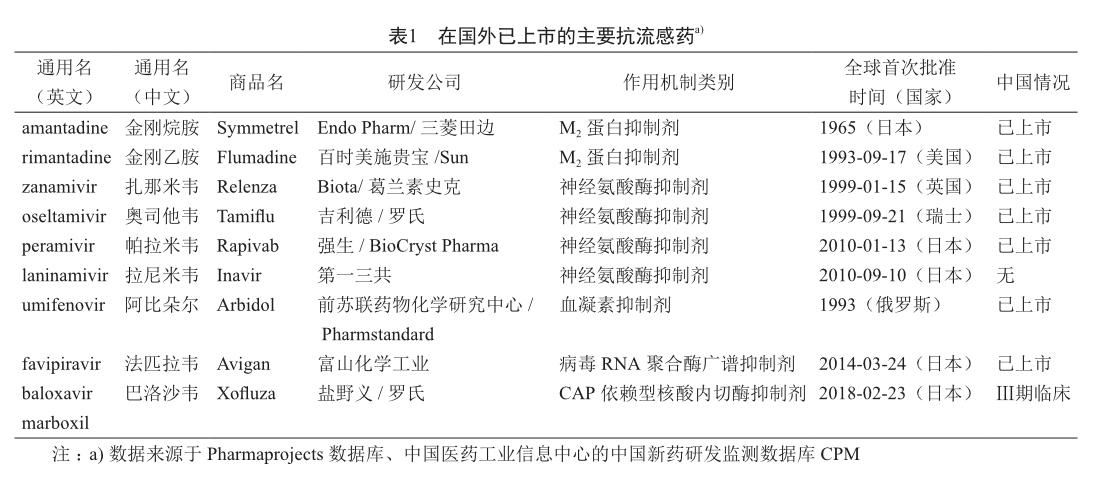
目前在国外已上市的主要抗流感药见表1。
金刚烷胺和金刚乙胺是M2蛋白抑制剂,作用于甲型流感病毒M2蛋白,该蛋白可形成病毒复制所必需的蛋白通道[3]。该类药物曾被批准用于≥1岁儿童和成人的甲型流感病毒感染的预防和治疗[4]。金刚烷胺最初在日本是用于帕金森疾病的治疗,后于1966年被批准作为亚洲感冒流行的预防药,1976年在预防的基础上确认为治疗药[2]。
扎那米韦、奥司他韦、帕拉米韦和拉尼米韦是神经氨酸酶抑制剂(nueraminidase inhibitors, NAIs,又称唾液酸酶抑制剂),可抑制流感病毒表面神经氨酸酶的活性,阻止病毒由被感染细胞释放从而阻止感染新的宿主细胞,有抗甲型流感病毒和乙型流感病毒的活性[5]。美国疾病预防控制中心(Centers for Disease Control and Prevention, CDC)推荐NAIs作为流感抗病毒药物的一线治疗,可用于儿童[4]。
阿比朵尔是非核苷类抗病毒药物,通过抑制流感病毒脂膜与宿主细胞融合阻止流感病毒进入宿主细胞而发挥抗病毒作用,用于>2岁儿童及成人的治疗和预防[4]。阿比朵尔仅在俄罗斯和我国批准上市。
法匹拉韦是RNA聚合酶抑制剂,可以特异性地抑制病毒RNA聚合酶阻断病毒RNA的合成,从而起到抗病毒的作用。法匹拉韦对甲型、乙型流感病毒均有活性,用于治疗新型和复发型流感的成人患者[4]。
巴洛沙韦是RNA聚合酶复合物PA亚单位抑制剂药物——CAP依赖型核酸内切酶抑制剂,抑制流感病毒从宿主细胞中夺取宿主mRNA 5端的CAP结构用于自身mRNA转录,从而达到抑制病毒复制的作用。用于治疗≥12岁的急性、无并发症流感患者,是首个口服单剂抗病毒药物,同时也是近20年来首个具有创新作用机制的抗流感药物[4]。
1.2 研发概况
截至2020年1月,目前处于临床3期的全球抗流感药物有吡莫地韦、DAS181和硝唑尼特。
吡莫地韦(pimodivir)是全球首创的RNA聚合酶复合物PB2亚单位抑制剂药物,通过竞争结合流感病毒的PB2亚单位上的5甲基帽结合位点,从而抑制流感病毒复制,但因为甲型和乙型流感病毒的PB2帽状结合口袋结构不同,因此仅对甲型流感病毒有效[6]。强生公司在2014年从vertex pharmaceuticals获得了药物的全球开发权益。Ⅱb期临床试验表明,吡莫地韦与奥司他韦联用可以将患者的病毒载量降到更低水平,因其显著的治疗潜力,已在2017年3月获得了FDA快速通道,正在进行纳入青少年的3期临床研究中[4]。
DAS181(Fludase,流感酶)是针对宿主细胞的广谱抗病毒药物,DAS181通过切断呼吸道上皮细胞表面的唾液酸受体来阻断流感病毒入侵宿主细胞。根据作用机理可知DAS181对奥司他韦耐药的流感病毒亦有活性。由于唾液酸受体可以与多种呼吸道病毒结合,DAS181对多种呼吸道病毒均有抑制活性,包括流感病毒、副流感病毒、偏肺病毒等[7]。一项双盲安慰剂对照Ⅱ期临床证实DAS181可以有效降低流感病毒载量,并且耐受性良好。
硝唑尼特(nitazoxanide,NT-300)也是针对宿主细胞的广谱抗病毒药物。硝唑尼特是一类噻嗪类广谱抗病毒药物,最初作为治疗隐孢子虫的药物被批准上市,通过抑制流感病毒HA蛋白翻译后细胞内转运从而抑制流感病毒复制。硝唑尼特对于甲型、乙型流感病毒均有活性,包括奥司他韦耐药的病毒株。两项随机双盲安慰剂对照Ⅱ期临床试验显示,硝唑尼特能够减少流感症状的持续时间,但不能缩短流感的住院时间[8]。
另外一个很有可能上市的是MEDI8852,2016年3月,FDA授予阿斯利康旗下全球生物制剂研发部门MedImmune研发的单克隆抗体MEDI8852用于治疗甲型流感病毒住院患者的快速通道地位。MEDI8852是一种实验性人IgG1κ单克隆抗体(monoclonal antibody, mAb),通过输液给药,MEDI8852能够结合至血凝素蛋白(hemagglutinin)茎部的一个区域,这在甲型流感病毒所有亚型中均高度保守。目前,MEDI8852正处于Ⅱ期临床开发,调查单剂量静脉注射MEDI8852作为单药疗法或联合奥司他韦,用于由甲型流感病毒导致的急性、无并发症流感成人患者的疗效和安全性[9]。Evaluate Pharma预测其2023年底上市。
1.3 销售情况
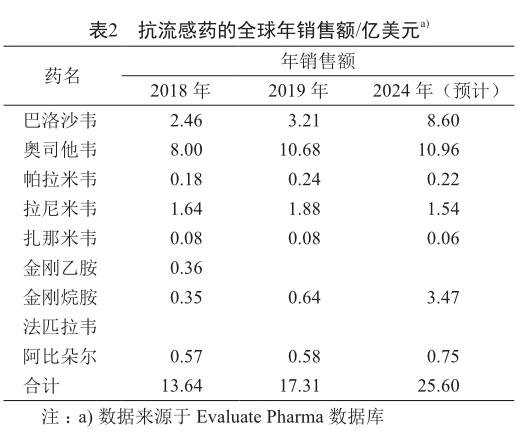
主要抗流感药的全球年销售额见表2。
从全球年销售额可以看出,今后几年主要抗流感药的销售额还是有较大的增长,Evaluate Pharma预测到2024年,销售额基本上是2018年的1倍,销售额主要是排前两位的奥司他韦和巴洛沙韦。
2 国内抗流感药的生产、研发和市场情况
2.1 生产情况
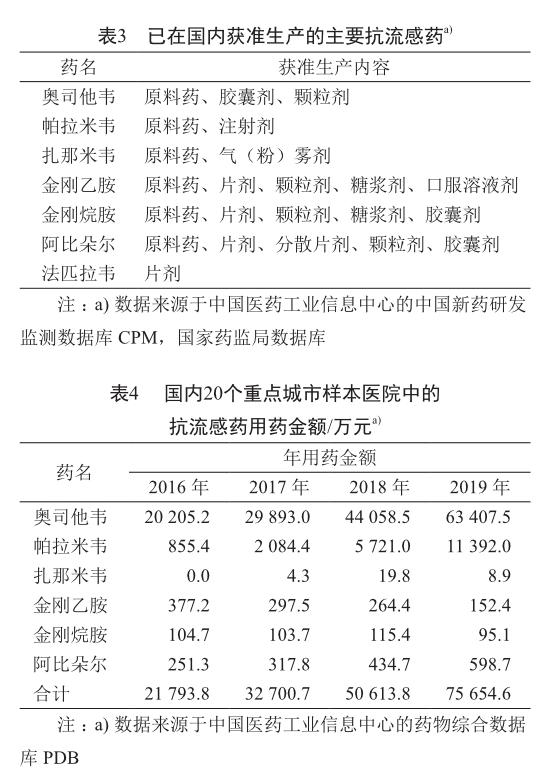
国外制药公司在抗流感药的研究、生产上一直处于领先优势,但是国内科研机构和制药公司的研发和生产能力已经有了很大的提升。同时流感属于易感传染病,在处于紧急的公共卫生事件的面前,国外公司也会出于世界卫生组织和国际社会压力,授权给国内有研发和生产能力的药企生产上市,比如2003年,在禽流感蔓延之际,罗氏授权了上海医药和东阳光两家来生产还处在化合物专利期内的达菲(奥司他韦)。今后随着国内药企走向国际,所以不管是授权还是合作将会更多。已在國内获准生产的主要抗流感药见表3。
2.2 市场情况
国内20个重点城市样本医院中的抗流感药用药金额见表4。
从表中可以看出,近几年国内20个重点城市样本医院中的抗流感药用药金额曾增长态势,2019年相比2016年增长了约3.5倍,说明了流感的易发和市场急剧扩增,同时奥司他韦占绝对的市场地位。从东阳光的年报也可以看出,仅东阳光的奥司他韦制剂2019年销售已经超过了60亿元。
2.3 研发、注册情况
目前,国内药企对新药的抢仿速度非常快,申报竞争程度也十分激烈。国内企业对国外常用的抗流感药基本都有仿制。国内有奥司他韦仿制药的1个原料药、2个胶囊剂和2个颗粒剂生产批文,2个原料药批文因未完成再注册而被取消;帕拉米韦仿制药的1个原料药和2个注射液生产批文;扎那米韦仿制药的2个原料药和1个吸入粉雾剂生产批文;金刚乙胺仿制药的2个原料药、2个片剂、3个颗粒剂、1个糖浆剂和1个口服溶液剂生产批文;金刚烷胺仿制药的5个原料药、45个片剂、20个颗粒剂、12个糖浆剂和4个胶囊剂生产批文,另有多个含金刚烷胺的复方制剂的生产批文;阿比朵尔仿制药的2个原料药、2个片剂、1个分散片剂、1个颗粒剂和1个胶囊剂生产批文。
法匹拉韦在中国获得授权仿制,2016年6月22日海正药业与原研厂家日本富山化学工业株式会社签订了化合物专利独家授权协议[4],于2020年2月16日在中国获批上市,用于治疗成人新型或再次流行的流感(仅限于其它抗流感病毒药物治疗无效或效果不佳时使用),同时获得新型冠状病毒肺炎的临床试验批件。法匹拉韦是一种嘌呤核苷类似物,除流感病毒外,法匹拉韦对其它RNA病毒也有部分抑制活性,因此是一种极有前景的广谱抗病毒药物[10]。由于其广谱的抗病毒特性以及不易出现耐药,法匹拉韦可能会成为应对突发新发传染病和耐药流感患者的重要应对手段。
巴洛沙韦2018年已经率先在日本、美国、泰国和中国香港上市,并已进入我国药品审评中心快速审评通道,罗氏的巴洛沙韦混悬颗粒剂已获批临床,目前在上海市徐汇区中心医院完成了Ⅰ期临床试验,Ⅲ期临床已有登记号,2019年11月20日试验公示,主要适应证是甲型或乙型流感,在中日友好医院开展,试验状态显示尚未招募。
在国际上处于Ⅲ期的吡莫地韦同时也进入了中国,西安杨森为主申请的吡莫地韦Ⅲ期临床已有登记号,2019年11月25日试验公示,主要适应证是甲型流感,在中日友好医院开展,试验状态显示尚未招募。
3 结语
流感病毒引起的流行性感冒是一种传染性强、传播速度快的疾病,极易发生大范围流行。虽然目前抗流感药物上市品种较多,但随着各个一线药物耐药形势的恶化,对新型抗流感药物的需求也更加迫切。值得欣慰的是,随着法匹拉韦、硝唑尼特、DAS181等品种的陆续上市,一线药物的耐药威胁有望在近年内得到缓解。但面对流感病毒的快速变异,新的耐药株也将逐步出现,因此在研发上如能建立一个有不同机制或不同抗药特征的药物库,对流感病毒的预防及治疗有很大帮助。
参考文献
[1] Dawood FS, Iuliano AD, Reed C, et al. Estimated global mortality associated with the first 12 months of 2009 pandemic influenza A H1N1 virus circulation: a modelling study[J/OL]. Lancet Infect Dis, 2012, 12(9): 687-695. doi: 10.1016/S1473-3099(12)70121-4.
[2] 曹瑞源, 趙磊, 钟武. 抗流感小分子药物研究进展[J]. 临床药物治疗杂志, 2018, 16(1): 1-5.
[3] 艾则孜·图尔荪尼亚孜. 流行性感冒防治药物的研究进展[J]. 药物与临床, 2019, 28(1): 208-209.
[4] 刘心悦, 蒋荣猛. 儿童流行性感冒抗病毒药物研究进展[J]. 中华儿科杂志, 2019, 57(4): 313-316.
[5] 梁媛, 赵江云, 龙朋伟, 等. 流行性感冒防治药物研究进展[J]. 国际药学研究杂志, 2017, 44(3): 220-228.
[6] Trevejo JM, Asmal M, Vingerhoets J, et al. Pimodivir treatment in adult volunteers experimentally inoculated with live influenza virus: a phase IIa, randomized, double-blind, placebo-controlled study [J]. Antivir Ther, 2018, 23(4): 335-344.
[7] Koszalka P, Tilmanis D, Hurt AC. Influenza antivirals currently in late-phase clinical trial[J/OL]. Influenza Other Respir Viruses, 2017, 11(3): 240-246. doi: 10.1111/irv.12446.
[8] Rossignol JF. Nitazoxanide: a first-in-class broad-spectrum antiviral agent[J]. Antiviral Res, 2014, 110: 94-103.
[9] 佚名. FDA授予阿斯利康单抗MEDI8852治疗A型流感感染的快车道地位[EB/OL]. (2016-03-10)[2020-02-20]. https://www.instrument.com.cn/news/20160310/186003. shtml.
[10] Furuta Y, Komeno T, Nakamura T. Favipiravir (T-705), a broad spectrum inhibitor of viral RNA polymerase[J]. Proc Jpn Acad Ser B Phys Biol Sci, 2017, 93(7): 449-463.

