15例COVID-19患者治疗后痰、粪便标本新型冠状病毒核酸检测结果比较
李宝林,李 芹,吴 刚,曾章锐,黄富礼,詹小亭,唐 敏,刘靳波
(西南医科大学附属医院 1. 医学检验部; 2. 传染科,四川 泸州 646000)
2019年12月在中国湖北省武汉市出现新型冠状病毒肺炎病例,被发现人传人,疫情迅速向其他省份蔓延[1-2]。新型冠状病毒感染的暴发已经成为一个公共卫生问题[3],对新型冠状病毒的检测也迫在眉睫。促进公共卫生干预的首要优先事项之一是可靠的实验室诊断,RT-PCR是目前已经证明最可靠、最成熟的技术[4-6]。2020年2月11日国际病毒分类委员会将新型冠状病毒正式命名为SARS-CoV-2,并认定这种病毒是SARS冠状病毒的姊妹病毒。目前针对SARS-CoV-2的检测试剂主要有两种,一种是基于免疫检测患者血液中的IgG与IgM,另一种是检测患者呼吸道标本中SARS-CoV-2核酸。在《新型冠状病毒肺炎诊疗方案(试行第五版)》[7]中阐述病例诊断需具备病原学特征之一:(1)呼吸道标本或血液标本实时荧光定量 PCR 检测 SARS-CoV-2 核酸阳性;(2)呼吸道标本或血液标本病毒基因测序,与已知的 SARS-CoV-2 高度同源。因此,准确、及时的病原学核酸检测已成为诊断 SARS-CoV-2感染的重要环节。
目前临床上常用的标本来源有:上呼吸道标本最常见的有口咽拭子和鼻咽拭子等,其中以口咽拭子为主;下呼吸道标本有深咳痰、呼吸道抽取物、支气管灌洗液、肺泡灌洗液和肺组织活检标本等,其中以深咳痰为主。据不同检测机构及已开展SARS-CoV-2核酸检测情况来看,口咽拭子检出率最低,深咳痰检出率相对较高,但是取样相对困难。为更好的平衡取样便捷性与阳性检出率,同时考虑患者容易接受的样本来源,本研究对已经确诊治疗后的15例新型冠状病毒肺炎(COVID-19)患者深咳痰和粪便标本进行核酸检测,探讨粪便标本作为其疑似或确诊患者筛查的可行性。
1 材料与方法
1.1 标本来源 收集2020年2月11—13日送至西南医科大学附属医院医学检验部的15例COVID-19患者治疗后的痰、粪便标本。
1.2 SARS-CoV-2 RNA的提取
1.2.1 痰SARS-CoV-2 RNA的提取 取3倍于痰体积的4% NaOH溶液,加入痰采集管中液化30 min,液化过程中每10 min振荡一次,直至样本无拉丝。取1 mL液化后样本13 000 rpm离心10 min,弃上清后用生理盐水洗涤,13 000 rpm离心10 min,留取300 μL上清,弃除多余的上清后将剩余的300 μL上清与沉淀混匀,将混合物吸入到EX3600核酸自动提取仪配套的核酸提取预装板A孔中(一次性可以提取36个标本),将预装版置于设备固定位置,启动核酸提取程序提取核酸(上海之江)。
1.2.2 粪便SARS-CoV-2 RNA的提取 利用PowerMicrobiomeTM RNA Isolation Kit粪便RNA提取试剂盒(凯杰,德国,货号:26000-50),提取粪便中SARS-CoV-2核酸。
1.3 SARS-CoV-2基因扩增 采用湖南圣湘新型冠状病毒(2019-nCoV)核酸检测试剂盒检测痰、粪便标本中SARS-CoV-2核酸。SARS-CoV-2扩增的基因为ORF 1ab基因和N基因,对应扩增通道为FAM和ROX,内标通道VIC检测人体细胞RNase P。
1.4 核酸扩增设备及结果判读 采用ABI7500扩增SARS-CoV-2靶基因核酸,扩增程序如下:逆转录,50℃ 30 min;预变性,95℃ 1 min;变性,95℃ 15 s;退火、延伸及荧光检测,60℃ 31 s,45个循环;仪器冷却,25℃ 10 s。判断标准:FAM或ROX通道检测到典型的S型扩增曲线,Ct≤40,内标Ct≤40的样本可判读为阳性;FAM和ROX通道均未检测到典型的S型扩增曲线,或Ct>40,VIC通道有扩增曲线,且Ct≤40的样本,结果判读为阴性。
2 结果
2.1 标本人体细胞RNase P扩增情况 15例COVID-19患者治疗后痰、粪便标本中,人体细胞RNase P均呈典型的明显的扩增曲线,但痰标本中RNase P基因扩增曲线信号明显强于粪便标本,Ct值也均低于粪便标本。见图1、表1。
2.2 不同标本来源SARS-CoV-2核酸的扩增曲线 15例患者治疗后,痰、粪便标本中均有6例SARS-CoV-2核酸检测阳性。病例1、5、10、11、12的痰、粪便标本SARS-CoV-2核酸扩增均为阴性,病例6、8的痰、粪便标本SARS-CoV-2核酸检测均为阳性,病例3、4、7、13的痰标本SARS-CoV-2核酸检测为阳性,病例2、9、14、15的粪便标本SARS-CoV-2核酸检测为阳性,见表2。患者痰、粪便阳性标本SARS-CoV-2核酸扩增曲线见图2、3,6例患者痰阳性标本中有2例同时扩增出ORF 1ab基因与N基因(见图2),6例患者粪便阳性标本中有4例同时扩增出ORF 1ab基因与N基因,见图3。

A:痰标本;B:粪便标本。
图115例COVID-19患者治疗后痰、粪便中管家基因RNase P的扩增曲线图
Figure1Amplification curve of RNase P gene in sputum and feces of 15 patients with COVID-19 after treatment
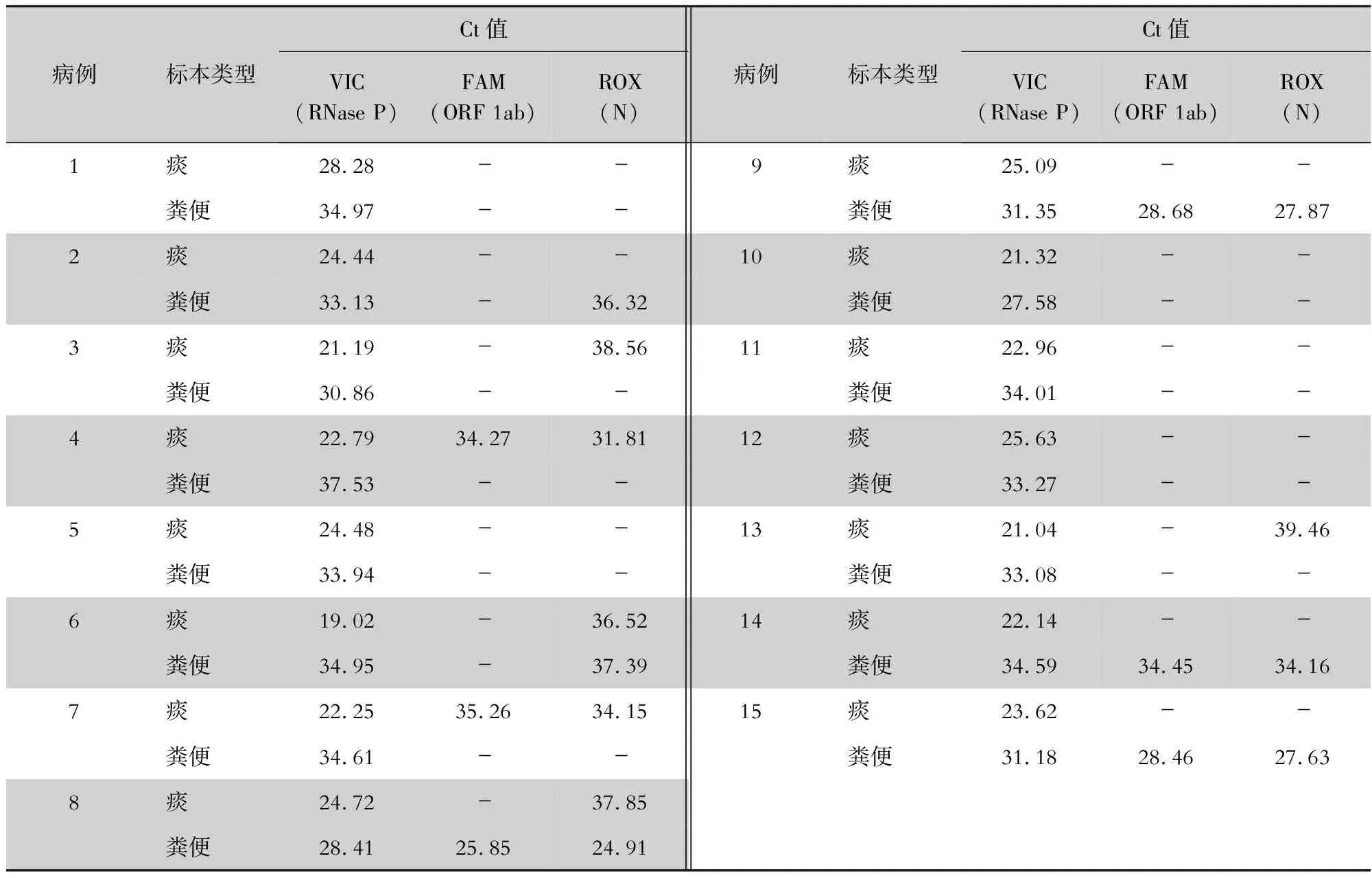
表1 15例COVID-19患者治疗后痰、粪便标本中相关基因检测Ct值
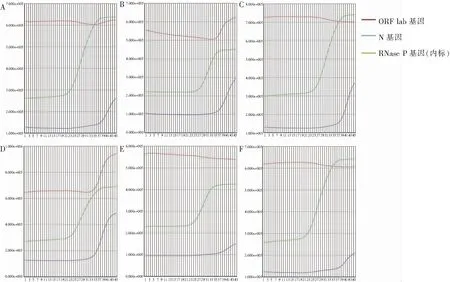
A~F:分别为病例3、4、6、7、8、13痰标本。
图26例SARS-CoV-2感染患者痰标本SARS-CoV-2基因扩增曲线
Figure2Amplification curve of SARS-CoV-2 gene in sputum specimens of 6 patients infected with SARS-CoV-2
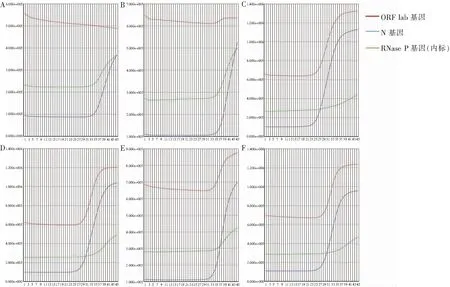
A~F:分别为病例2、6、8、9、14、15粪便标本。
图36例SARS-CoV-2感染患者粪便标本SARS-CoV-2基因扩增曲线
Figure3Amplification curve of SARS-CoV-2 gene in fecal specimens of 6 patients infected with SARS-CoV-2
2.3 不同住院、发病时长患者痰、粪便标本SARS-CoV-2核酸检测阳性情况 患者发病时间确定来源于微信公众号“泸州发布”中发布的确诊患者病例通报,患者发病后被收入传染病医院,15例患者中,治疗>5 d的患者中痰、粪便标本均有SARS-CoV-2核酸检测阳性。由于病例较少,未收集到治疗5 d以内患者标本,但患者粪便标本SARS-CoV-2核酸检测阳性与患者治疗周期没有必然联系。对不同发病时长患者痰、粪便标本进行SARS-CoV-2核酸检测,不同发病时长患者的粪便中都有SARS-CoV-2核酸检测阳性,发病时间5~10 d内的患者有4例,其中有1例仅粪便标本中检出病毒核酸,其余3例粪便与痰标本均未检出病毒核酸。见表2。
表2不同治疗、发病周期痰、粪便标本SARS-CoV-2核酸检测阳性情况
Table2Positive detection result of SARS-CoV-2 nucleic acid in sputum and fecal specimens during different treatment and disease course
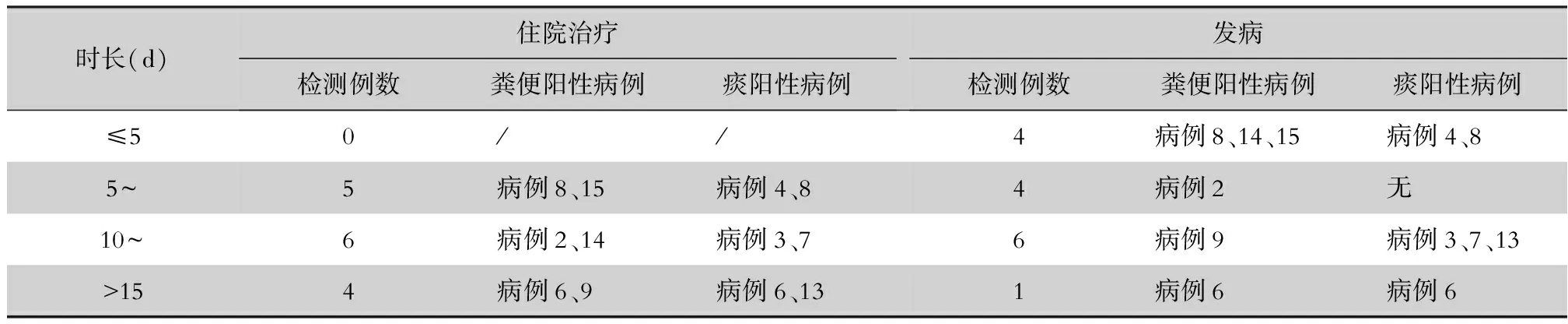
时长(d)住院治疗检测例数粪便阳性病例痰阳性病例发病检测例数粪便阳性病例痰阳性病例≤50//4病例8、14、15病例4、85~5病例8、15病例4、84病例2无10~6病例2、14病例3、76病例9病例3、7、13>154病例6、9病例6、131病例6病例6
3 讨论
本研究对15例COVID-19患者治疗后痰、粪便标本进行了SARS-CoV-2核酸扩增分析。2020年2月1日深圳市第三人民医院在COVID-19患者粪便中检出SARS-CoV-2核酸阳性[8],至此,从粪便标本检测SARS-CoV-2核酸开始引起人们的重视。在国家卫生健康委发布的COVID-19预防指南中也明确提出,部分患者有消化道症状,如腹泻[9],2020年2月10日钟南山团队从一例COVID-19患者的粪便标本中分离到一株SARS-CoV-2[10]。本研究发现随着病程进展,有患者下呼吸道标本SARS-CoV-2核酸检测为阴性,但其粪便标本检测为阳性,提示在病程发展过程中,SARS-CoV-2会进入消化道。李萍等[11]认为可以在疾病的早期或轻症患者中选择粪便标本进行核酸检测,而在本研究中由于缺乏早期患者标本,结合李萍的研究认为,在疑似病例有消化道症状者、经治疗出院时均应采集粪便标本进行SARS-CoV-2核酸检测。2020年2月21日成都市公卫中心通过微博发布“新型肺炎疫情防控”:一例出院患者复查核酸阳性[12]。提示可能对于COVID-19患者出院标准不应限于当前指南,可以尝试纳入粪便标本SARS-CoV-2核酸检测;以呼吸道标本SARS-CoV-2核酸检测阴性作为排除COVID-19及治愈标准在实施过程中需谨慎,应考虑是否将粪便标本SARS-CoV-2核酸检测阴性也纳入其中。
粪便标本中检出SARS-CoV-2核酸阳性,同时有活的病毒存在,因此,防止生态环境的污染也应引起重视,应对患者排泄物进行彻底消毒[13]。SARS-CoV-2是SARS冠状病毒的姊妹病毒,2003年,我国学者首先评估了SARS-CoV在外界环境物品中生存的能力,结果显示,SARS-CoV在模拟污染的玻璃片、不锈钢片、塑料片上可以存活至少2 d,在模拟污染的滤纸片、木片、棉布片、土壤上至少可存活4~6 h,随后又有多个实验室进行了验证[14-16]。目前还缺少SARS-CoV-2对环境污染的评估数据,但对患者排泄物进行定时清洁与消毒处理,是非常必要的。
研究探讨COVID-19患者在不同标本,如咽拭子、痰、血、尿、粪便中的病毒含量及存在时间,对实验室诊断COVID-19尤为重要。由于纳入病例较少,尚不具有代表性,尤其缺乏治疗早期患者标本。期待在后续研究中纳入更多的标本类型,进行进一步的数据分析,为疾病防控措施提供一些建议。同时也希望相关部门积极制定环境消毒策略,从不同的方面对SARS-CoV-2传播做好防控。

