改性锯末生物炭对水中As(III)和Cd(II)吸附机制的研究
解攀,张言,王雪梅,张萌,季宏兵
(北京科技大学 能源与环境工程学院,北京 100083)
大量的矿石开采和能源的利用使砷(As)和镉(Cd)过量的释放到自然水体中,造成了大面积的水污染[1],水体中砷和镉污染治理已经迫在眉睫。生物炭是一种新型环保吸附材料,具备材料来源广泛、含碳量大、比表面积大、孔径发达、官能团数量多等优点,被广泛应用于水体和土壤中的重金属去除[2]。锯末是一种来源广泛的工业副产物[3],本文将锯末在缺氧的状态下500 ℃热解制备生物炭,并对其进行铁、锰氧化物改性[4],探究其对水中砷和镉的去除效果以及吸附机制。
1 实验部分
1.1 试剂与仪器
锯末;高锰酸钾、三氯化铁、氯化镉、亚砷酸钠均为分析纯。
HH-6恒温振荡器;DFG801恒温干燥箱;YFX7/10Q-GC马弗炉;NexION300X电感耦合等离子体发射光谱仪;ASAP2020全自动比表面及孔隙度分析仪。
1.2 生物炭的制备及改性
锯末用去离子水(18.2 MΩ·cm)清洗数遍,去除表面的杂质及灰尘,90 ℃烘干,过60目筛。放入马弗炉内,通入氮气,以10 ℃/min的升温速率,升温到500 ℃,恒温热解2 h,制备锯末生物炭,记为SB,干燥储存。
取等体积(40 mL)0.1 mol/L FeCl3和0.3 mol/L KMnO4溶液混合,制备改性溶液[5]。准确称量SB浸入改性溶液中,超声2 h。95 ℃干燥12 h。再于管式炉内通入氮气,以10 ℃/min的升温速率加热至500 ℃,维持0.5 h。取出后使用去离子水清洗3次,干燥,制得改性后生物炭,记为FMSB。制备3种比例改性生物炭,铁∶锰∶生物炭的质量比分别为1∶3∶15,1∶3∶25,1∶3∶35,分别记为F1M3SB15、F1M3SB25、F1M3SB35。
1.3 吸附实验
在25 ℃时,50 mL离心管中,分别加入浓度50 mg/L的Cd2+和As3+溶液30 mL,以0.1 mol/L HCl和0.1 mol/L NaOH调节溶液pH,加入0.1 g原始生物炭及3种比例改性生物炭,以250 r/min在恒温摇床中振荡24 h后取样,通过0.45 μm滤膜过滤,用ICP-OES测定[6]Cd2+和As3+浓度。生物炭对砷和镉的吸附量qt(mg/g)、吸附率X分别通过公式(1)和公式(2)进行计算[7]:
(1)
(2)
式中C0,Ct——分别代表溶液初始和t时刻的离子浓度,mg/L;
V——溶液的体积,mL;
m——吸附剂的质量,g。
2 结果与讨论
2.1 生物炭表征
2.1.1 FTIR分析 原始生物炭以及改性生物炭的红外谱图见图1。
由图1可知,4种材料均含有相同的锯末化学结构[8],尽管在改性后出现了一些不同,但是吸收峰仍然十分相似。吸附剂材料在3 000,3 700,1 420 cm-1处有较强的吸收峰出现,3 700 cm-1是O—H的伸缩振动[8];3 000 cm-1是 —CH3不对称伸缩性振动[9-10];1 420 cm-1为 —CH3伸缩振动引起的,在改性材料中,600~700 cm-1可能是Fe—O特征吸收峰,500 cm-1可能是Mn—O特征吸收峰,证明在改性后引入了铁、锰氧化物。引入铁、锰氧化物可以与砷镉形成络合物,提高重金属去除能力[11]。

图1 吸附材料傅里叶红外光谱图
2.1.2 XRD分析 吸附材料的XRD图谱见图2。
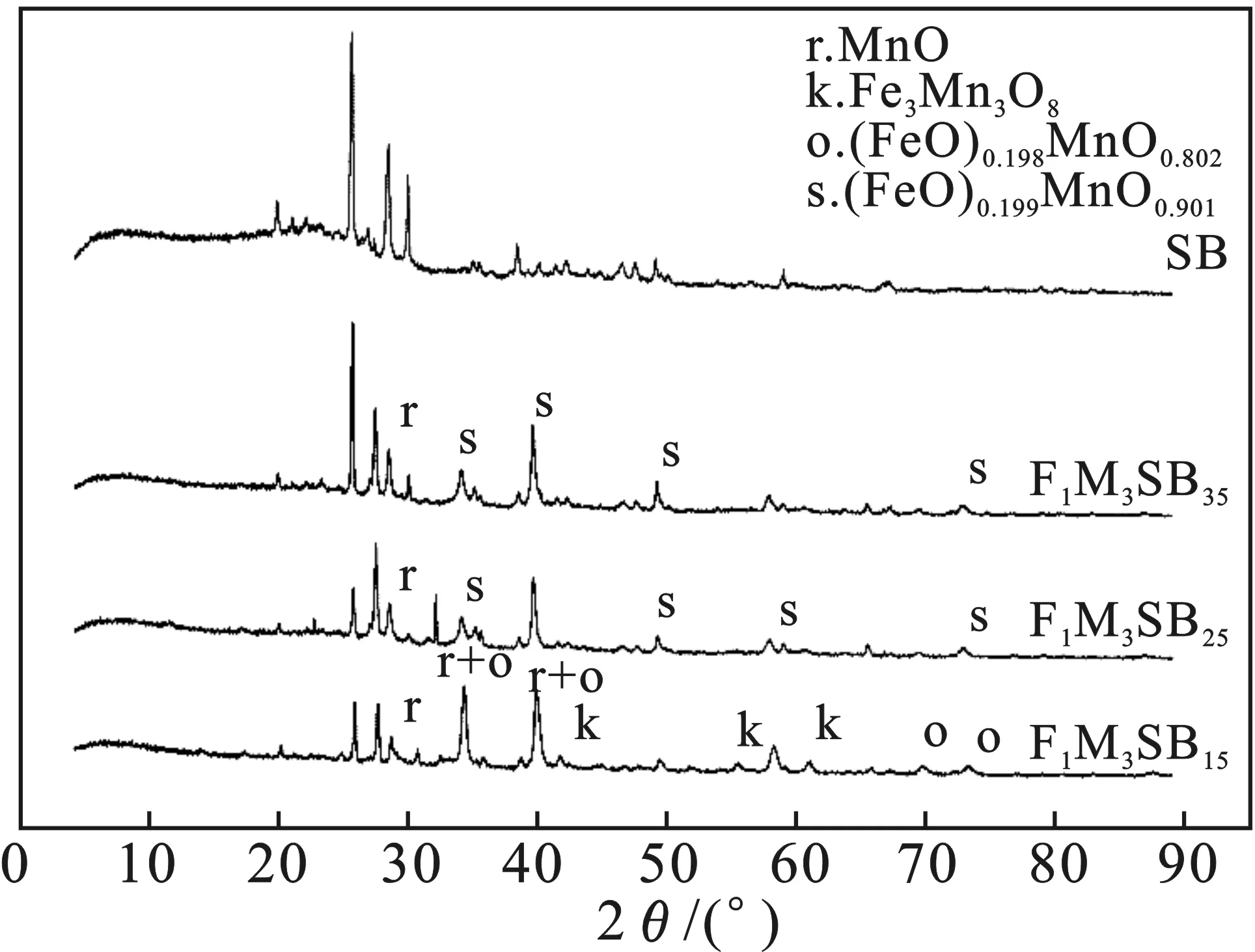
图2 吸附材料的XRD图谱
由图2可知,3种改性材料中出现了铁、锰氧化物的特征衍射峰[12],包括MnO(PDF75-0527)、(FeO)0.198(MnO)0.802(PDF77-2361)、Fe3Mn3O8(PDF75-0034)、(FeO)0.099(MnO)0.901(PDF77-2362),证明了经过改性合成了铁、锰氧化物,这与FTIR结果一致。
2.1.3 孔径与形貌分析 4种吸附剂材料的孔径、总孔体积、比表面积见表1。
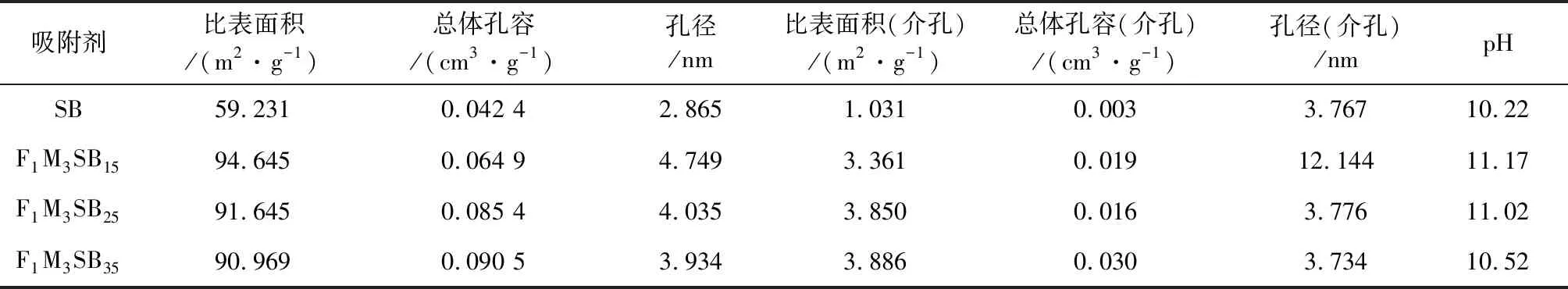
表1 吸附材料的比表面积和pH值分析
由表1可知,经过改性,吸附剂材料的比表面积和孔径增大,随着铁、锰投加比例的增加,比表面积和平均孔径增大,总体孔容缩小,可能是孔径内附着了铁、锰氧化物,造成了部分孔结构堵塞[13],改性材料F1M3SB15的孔径及比表面积大于F1M3SB25和F1M3SB35,因此其物理吸附效果优于其余两种比例改性材料[14]。由于改性溶液的pH值为12.21,因此材料的pH值随着改性溶液的投加量增加而增大,较大的pH值使得吸附剂材料更加适用于酸性废水的治理中[15]。
图3展示了4种吸附剂材料的SEM-EDS谱图。
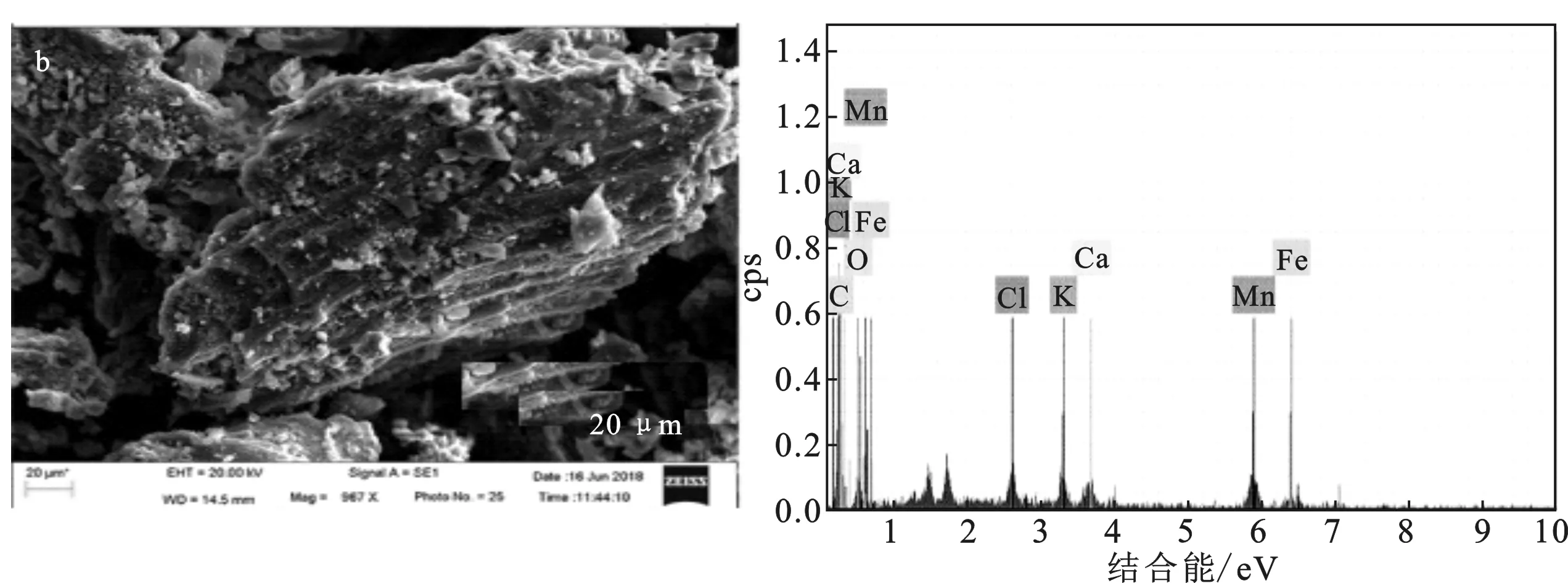
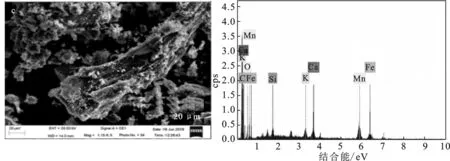
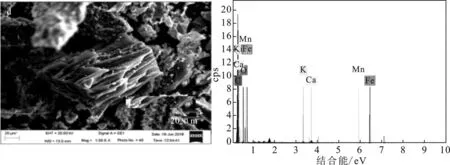
由图3可知,锯末生物炭材料表面分布着大量的管状孔结构,随着铁、锰投加量的增加,孔变得更为密集。同时由EDS分析可知,改性后,生物炭材料中的Fe、Mn、K、Ca、Cl等元素含量大量增加,同时铁、锰含量比为1∶3,这与改性溶液的配比数据吻合[16]。
2.2 吸附动力学
分别量取30 mL浓度为50 mg/L Cd(II)溶液、As(III)溶液以及Cd(II)和As(III)混合溶液于50 mL 离心管中[17],准确加入0.1 g原始生物炭以及3种比例改性生物炭材料,使用0.1 mol/L HCl以及0.1 mol/L NaOH溶液调节溶液pH值至5,在摇床上以250 r/min速度室温下振荡24 h。同时设置空白试验,排除离子沉淀影响。分别在0,5,10,20,40,60,120,240,480,960,1 440 min时取样。测定Cd2+和As3+含量,用准一级动力学模型(3)和准二级动力学模型(4)来分析吸附过程和计算数据,结果见图4和表2、表3。
log(qe-qt)=logqe-(k1/2.303)t
(3)
(4)
式中,k1和k2分别为准一级吸附模型和准二级吸附模型的反应速率常数min-1和g/(mg·min);qe和qt分别表示平衡吸附量和t时刻的吸附量。
由图4可知,①随着时间的增长,吸附逐渐达到稳定平衡。在吸附初始阶段,Cd2+和As3+的去除速率非常快,这是由于此时吸附主要发生在吸附剂表面,属于物理吸附。当吸附质逐渐达到吸附剂内部,此时吸附剂的官能团开始参与反应,反应速率下降,当吸附点位逐渐饱和时,吸附反应达到平衡;②改性后的吸附剂材料吸附效果远优于原始生物炭,其中F1M3SB15的吸附效果最好,这与孔径分析的结论一致。在竞争吸附实验中,当Cd2+存在时,会促进As3+的吸附,这是由于Cd2+非常容易被其他吸附质离子取代[17]。


图4 吸附动力学
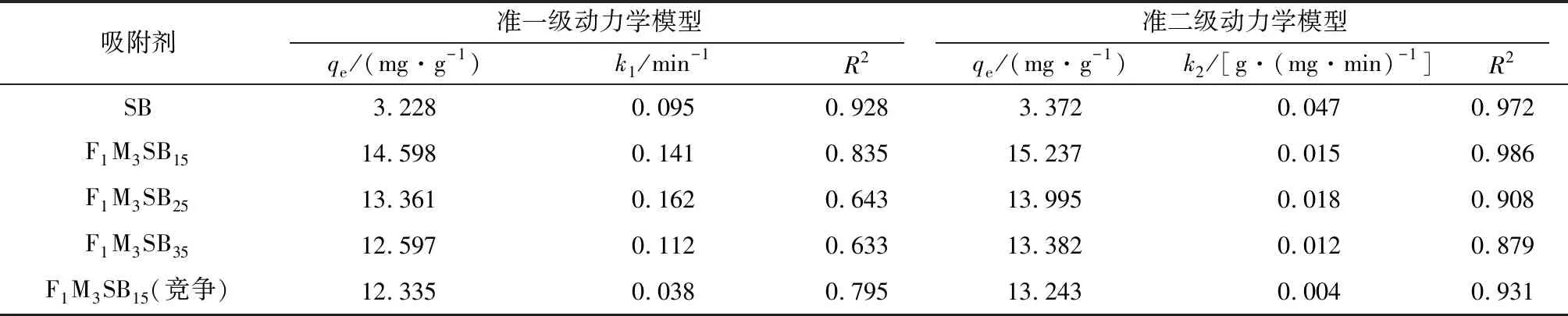
表2 镉吸附动力学参数

表3 砷吸附动力学参数
由表2和表3可知,Cd和As吸附更符合准二级吸附动力学模型。
2.3 吸附热力学
以吸附效果最好的F1M3SB15作为吸附剂进行吸附等温实验。分别取30 mL浓度为10,20,30,40,50,60,80,90,100 mg/L Cd2+溶液、As3+溶液以及Cd2+和As3+混合溶液,加入0.1 g F1M3SB15,调节pH值至5,在摇床上以250 r/min速度室温下振荡5 h(Cd2+和As3+混合溶液振荡8 h)。用Langmuir和Freundlich模型(其中Langmuir模型基于吸附质在吸附剂表面发生单分子层吸附,Freundlich 基于多相不均匀表面上的吸附[18]),进行拟合,结果见图5和表4、表5。
LangmuirQ=(qe×k×C)/(1+k×C)
(5)
(6)
式中,qe是Langmuir最大吸附量(mg/g);k是Langmuir 常数(L/mg);C是平衡时离子浓度;kF是吸附容量(mg/g);n是Freundlich常数。


图5 吸附等温图
由图5可知,As的热力学曲线比Cd的热力学曲线更加平滑,增长速度较慢,这可能是由于吸附剂吸附As更多的是化学吸附。由表4和表5可知,As和Cd的吸附热力学更加符合Langmuir模型,这表明离子吸附过程为单层吸附。

表4 镉吸附热力学参数

表5 砷吸附热力学参数
2.4 溶液初始pH对吸附的影响
溶液初始pH值梯度从2~9,准确称量F1M3SB150.1 g投加到30 mL浓度为50 mg/L的Cd2+溶液、As3+溶液以及Cd2+和As3+混合溶液中,在摇床上以250 r/min速度室温下振荡5 h(Cd2+和As3+混合溶液振荡8 h)。图6展示了溶液初始pH对As和Cd吸附效率的影响。
由图6可知,随着pH值的增加,Cd的去除效率迅速增加,这是由于前期H+离子浓度较高,抢占了Cd2+的吸附点位。而pH的增加对砷去除的影响相对较小,随着pH的改变,单一砷离子的去除效率并没有显著变化[19]。在砷镉竞争吸附实验中,混合溶液中Cd2+的去除效率低于单一Cd2+,这是由于As3+抢占了Cd2+的吸附点位,这与吸附动力学的数据一致,随着pH的增加,As3+的去除效率持续增加,这是由于在高pH环境下,As3+与Cd2+形成了Cd3(AsO4)2沉淀[20],本次实验确定5为吸附最佳pH[21]。


图6 溶液初始pH对吸附的影响
2.5 解吸附实验
吸附试验完成后,将上清液替换为0.01 mol/L CaCl2溶液,调节pH为5,在摇床上以250 r/min速度室温下振荡5 h(Cd2+和As3+混合溶液振荡8 h),样品过滤后通过ICP-OES测定。解吸附试验完成后,进行再吸附实验,步骤与第一步实验相同[22]。
在单一离子解吸附实验中,F1M3SB15吸附剂对于As和Cd的解吸率分别为18%和17%,吸附剂再生能力较差,在竞争吸附中,As和Cd的解吸附率分别为8%和7%,低于单一离子吸附实验,这可能是由于吸附过程中,有化学沉淀反应参加,降低了解吸附能力[23]。
在再吸附实验中,F1M3SB15吸附剂展示出了较强的再吸附能力,对于As和Cd的去除效率达到了55%和79%,这说明第1次吸附完成后,吸附剂仍然有未占用的吸附点位[23]。
3 结论
(1)经过改性后,锯末生物炭对于As和Cd的去除效率显著增加,其中F1M3SB15去除效果最好,对于As和Cd的最大吸附量达到了7.452,17.053 mg/g。
(2)pH对于Cd2+的去除有较大影响,低pH环境不利于Cd2+的去除,而As3+去除受pH影响较小。
(3)吸附剂材料的物理性质对于Cd2+去除影响较大,物理吸附在Cd2+吸附中占主要地位,而与官能团的络合在As3+去除中起重要作用[24]。

