响应曲面法优化曼尼希碱缓蚀剂的合成工艺
岳 泉
响应曲面法优化曼尼希碱缓蚀剂的合成工艺
岳 泉
(中国石油化工股份有限公司江汉油田分公司石油工程技术研究院, 湖北 武汉 430035)
采用响应曲面分析法对一种曼尼希碱的合成工艺进行优化。该曼尼希碱由曼尼希反应和季胺化反应合成得到。以Box-Behnken设计评价胺酮比、醛酮比、反应温度、pH和时间5个因素的显著性和交互作用分析,得出一种曼尼希碱的最佳合成条件为:胺酮比1.02,醛酮比1.066,反应温度67.2 ℃,pH为3.46和时间2.96 h,该条件下将这种曼尼希碱添加到腐蚀介质中后的腐蚀速率为0.02 g/(m2·h)。本文采用响应曲面法建立的模型较准确,可以较准确的得出一种曼尼希碱在合成过程中5个因素的交互作用及其最高效的合成条件,为曼尼希碱合成效率的提高提供一定参考价值。
曼尼希碱;腐蚀速率;合成条件;响应曲面法
油田开采方面,随着油气井往更深的地层发展,开采的条件日益复杂,因此常采用高浓度盐酸对油气井进行酸化,提高油气井的采收率,同时也面临着盐酸带来的对金属设备的腐蚀问题。通常采用添加缓蚀剂来来减缓浓酸对设备的腐蚀[1-2]。近年来,在油田开发领域,国内主要使用的缓蚀剂种类有曼尼希碱、季铵盐和咪唑啉等,其中以曼尼希碱的合成工艺简单,综合性能优良而受到广泛应用[3-4]。曼尼希碱加入到酸性介质后在金属表面形成致密的氧化膜,形成较强的疏水和覆盖效果,从而减缓腐蚀[5]。以响应曲面法优化曼尼希碱的合成工艺的研究还鲜有报道。本文先开展单因素试验,后采用响应曲面法优化曼尼希碱的合成工艺,为曼尼希碱的工业化生产提供参考。
1 实验部分
1.1 试剂和仪器
硫脲、苯乙酮、乙醇(98%),分析纯,国药;有机胺(BT),分析纯,天津市科密欧化学试剂开发中心;甲醛,分析纯,国药;浓盐酸(98%),天津市科密欧化学试剂开发中心;NICOLET6700型红外光谱仪,美国;CS350H电化学工作站,武汉科思特仪器股份有限公司。
N80钢试片,N80钢为油井油管钢,含碳0.22%~0.28%,硅≤0.25%,锰0.30%~0.60%,铬0.30%~0.50%,钼0.30%~0.50%,镍3.00%~3.50%,钒0.05%~0.15%。
1.2 实验方法
1.2.1 曼尼希碱季铵盐缓蚀剂的合成方法

图1 曼尼希碱季铵盐缓蚀剂的合成路线
采用一锅法来合成Mannich碱。将一定量的苯乙酮、甲醛、二甲胺溶于无水乙醇中,加至装有搅拌器、球形冷凝管、温度计的三口烧瓶中,置于恒温水浴锅搅拌5 min,用15%盐酸调节溶液至相应pH,升温至相应温度,反应一定时间后,即得醛酮胺缩合的曼尼希碱;调节反应温度至75 ℃后,向烧瓶中加入氯化苄进行季铵化,即得曼尼希碱季铵盐。
1.2.2 产物表征
将曼尼希碱季铵盐溶液于60~80 ℃进行减压蒸馏。粗产品在丙酮中重结晶两次得到橙黄色纯固体,并将其用红外光谱进行表征。
1.2.3 腐蚀速度评价方法
采用静态挂片失重法测定N80钢试片在15%盐酸水溶液中的腐蚀情况,如未作说明,缓蚀剂添加量(质量分数)为1.0%,温度为40 ℃,腐蚀时间为4 h。其腐蚀速率的测定参照中华人民共和国石油与天然气行业标准SY5405-1996《酸化用缓蚀剂性能试验方法及评价指标》[4]。
1.2.4 电化学方法
腐蚀和缓蚀都属于电化学现象,因此缓蚀剂的缓蚀效率可以用电化学方法进行测定[5]。室温下,采用CS350H电化学工作站测定缓蚀剂的极化曲线。工作电极为待测钢片,参比电极Ag/AgCl,辅助电极为铂电极,扫描范围相对开路电位为-250~+250 mV,扫描速率为0.01 V/s。在15%HCl体系中加入1%的缓蚀剂,另以15%HCl作为对照,分别测其极化曲线。
1.2.5 响应面试验设计
基于单因素试验的结果,以腐蚀速率为响应值,选取曼尼希碱制备过程中的(二甲胺)/(苯乙酮)、(甲醛)/(苯乙酮)、反应温度、反应pH和反应时间5个因素为响应变量,采用5因素4水平的Box-behnken中心组合试验设计,对各反应条件进行优化。具体实验因素水平和编码见表1。

表1 响应面设计试验因素水平和编码
2 结果与分析
2.1 单因素试验结果
2.1.1 反应温度对腐蚀速率的影响
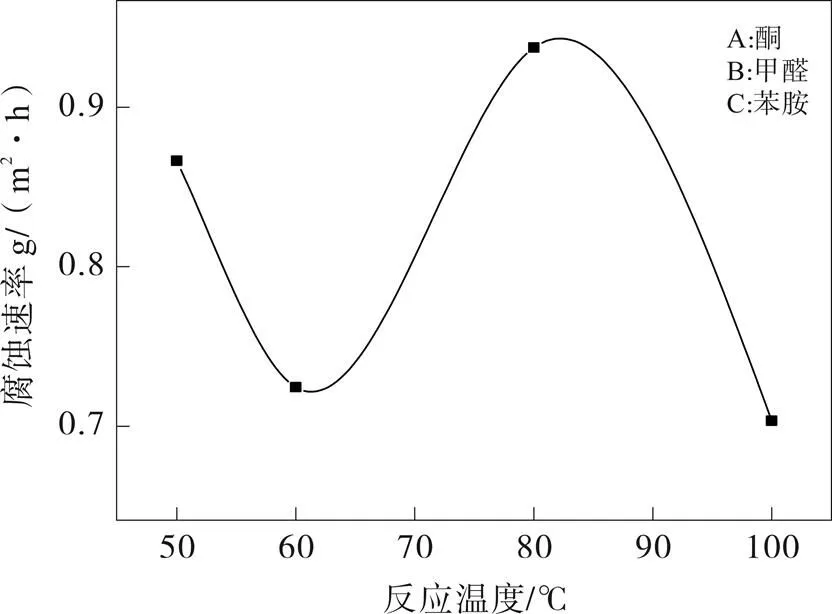
图2 反应温度对腐蚀速率的影响
如图2所示,随着反应温度的增加,钢片的腐蚀速率呈现无规律状态。腐蚀体系温度为100 ℃时,缓蚀速率最大,即其腐蚀速率最小,因此选反应温度为100 ℃为最佳反应温度。
2.1.2(二甲胺)/(苯乙酮)对腐蚀速率的影响
如图3所示,(二甲胺)/(苯乙酮)的增加,钢片的腐蚀速率先增加后减少。当(二甲胺)/(苯乙酮)为1.0时,钢片的腐蚀速率最小,因此选(二甲胺)/(苯乙酮)为1.0。
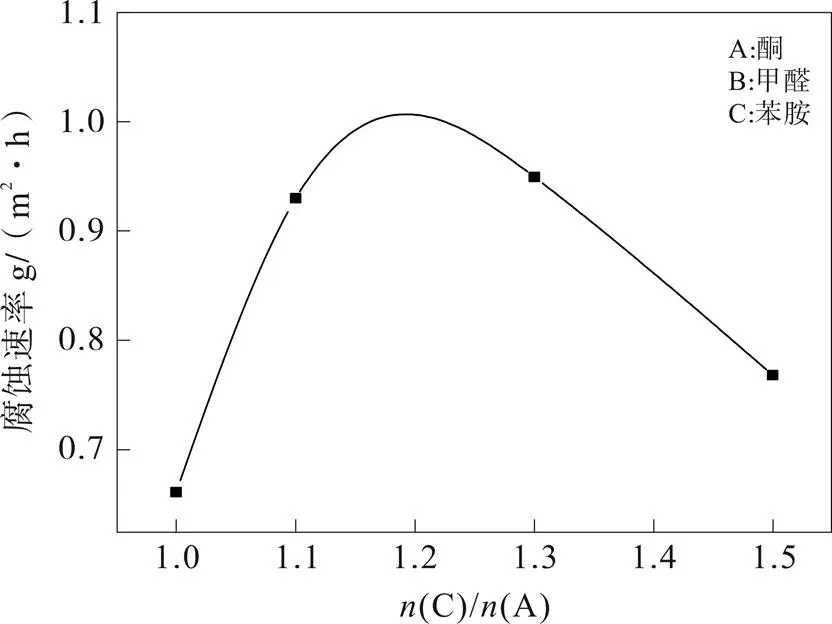
图3 n(二甲胺)/n(苯乙酮)对腐蚀速率的影响
2.1.3(甲醛)/(苯乙酮)对腐蚀速率的影响
如图4所示,(二甲胺)/(苯乙酮)的增加,钢片的腐蚀速率呈现无规律变化。当(甲醛)/(苯乙酮)为1.3时,钢片的腐蚀速率最小,因此选(甲醛)/(苯乙酮)为1.3。
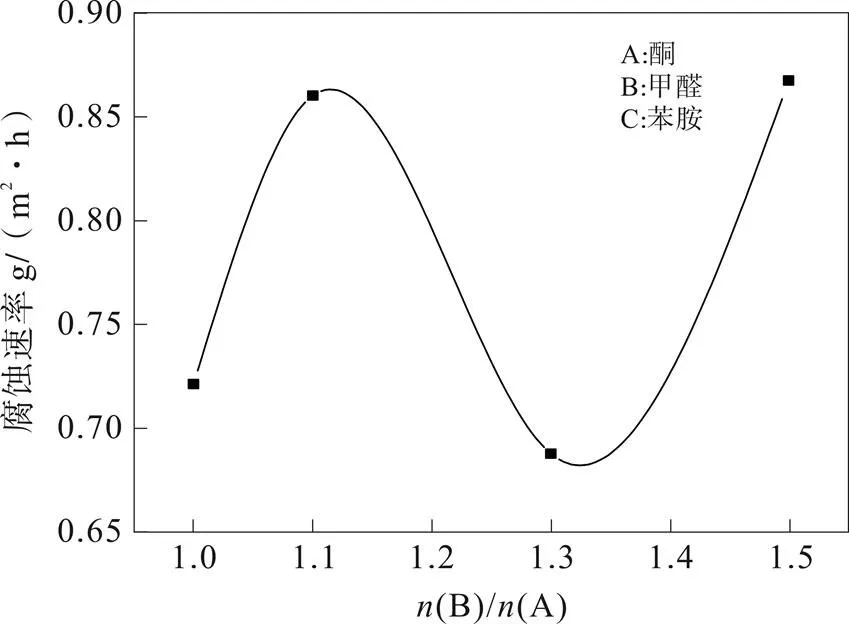
图4 n(甲醛)/n(苯乙酮)对腐蚀速率的影响
2.1.4 反应体系pH对腐蚀速率的影响
如图5所示,反应体系pH的增加,钢片的腐蚀速率先增加后减少。当反应体系pH超过5时,合成反应停止,因此选反应体系pH为5。
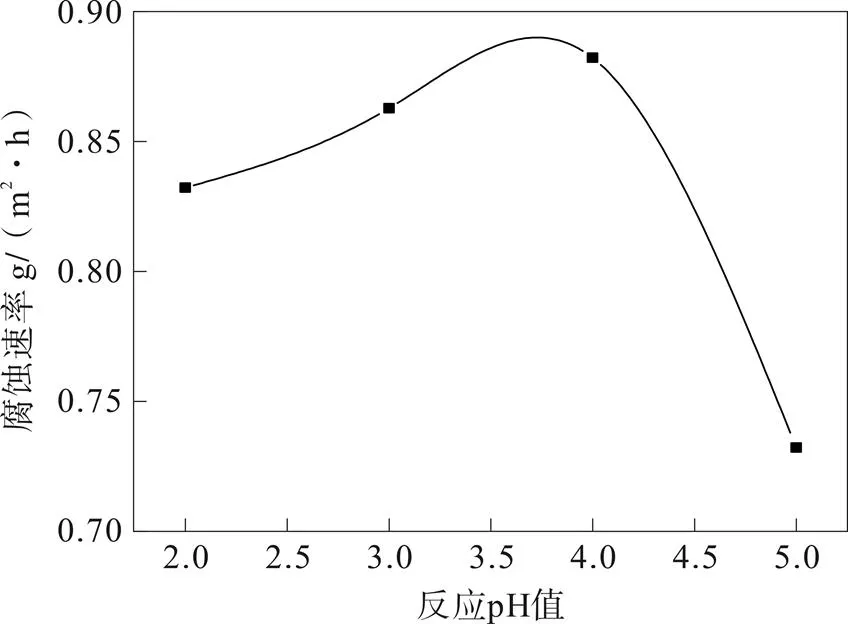
图5 反应体系pH值对腐蚀速率的影响
2.1.5 反应时间对腐蚀速率的影响
如图6所示,反应时间的增加,钢片的腐蚀速率先减小后增加,因此选反应时间选为6 h。
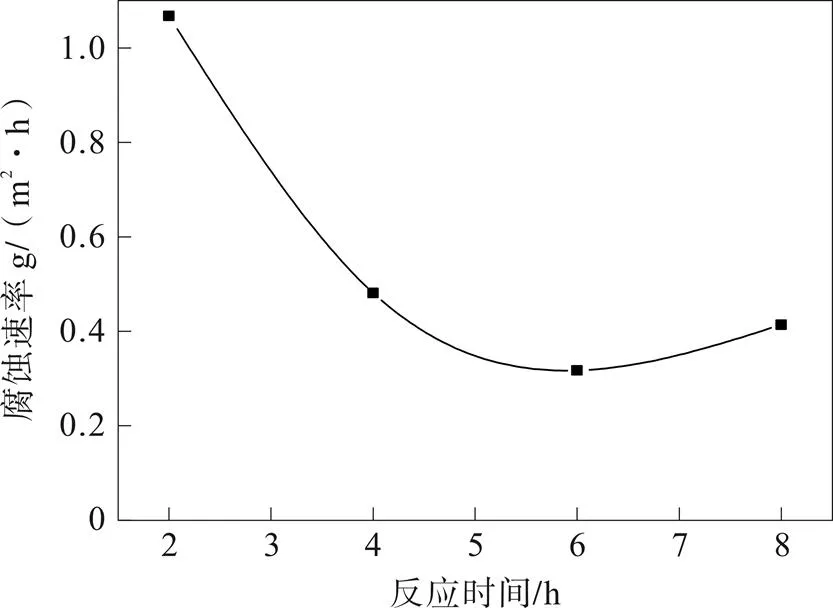
图6 反应时间对腐蚀速率的影响
2.2 响应面设计结果与分析
2.2.1 模型的建立及显著性检验
运用Design-Expert软件,使用Box-behnken响应曲面法设计数学模型,试验结果见表2,运算后得到合成条件与腐蚀速率之间的多项式模型为:
=0.57+0.21-0.28B-0.29-0.48-0.14-0.79-0.38-0.39+0.46-0.52+0.15
式中:为腐蚀速率,、、、、分表代表(二甲胺)/(苯乙酮)、(甲醛)/(苯乙酮)、反应温度、pH和时间的编码值。
从表3的方差结果可以看出,方程的复相关系数其平方2为0.992 9,可以认为该模型极显著(<0.05)。Radj2为0.973 4,证明该模型可以解释响应值变化比例达97.34%,该回归方程具有较高的拟合度和可信度,试验误差相对较小,此模型可以用来分析和预测曼尼希碱的合成条件及其产物的腐蚀速率。
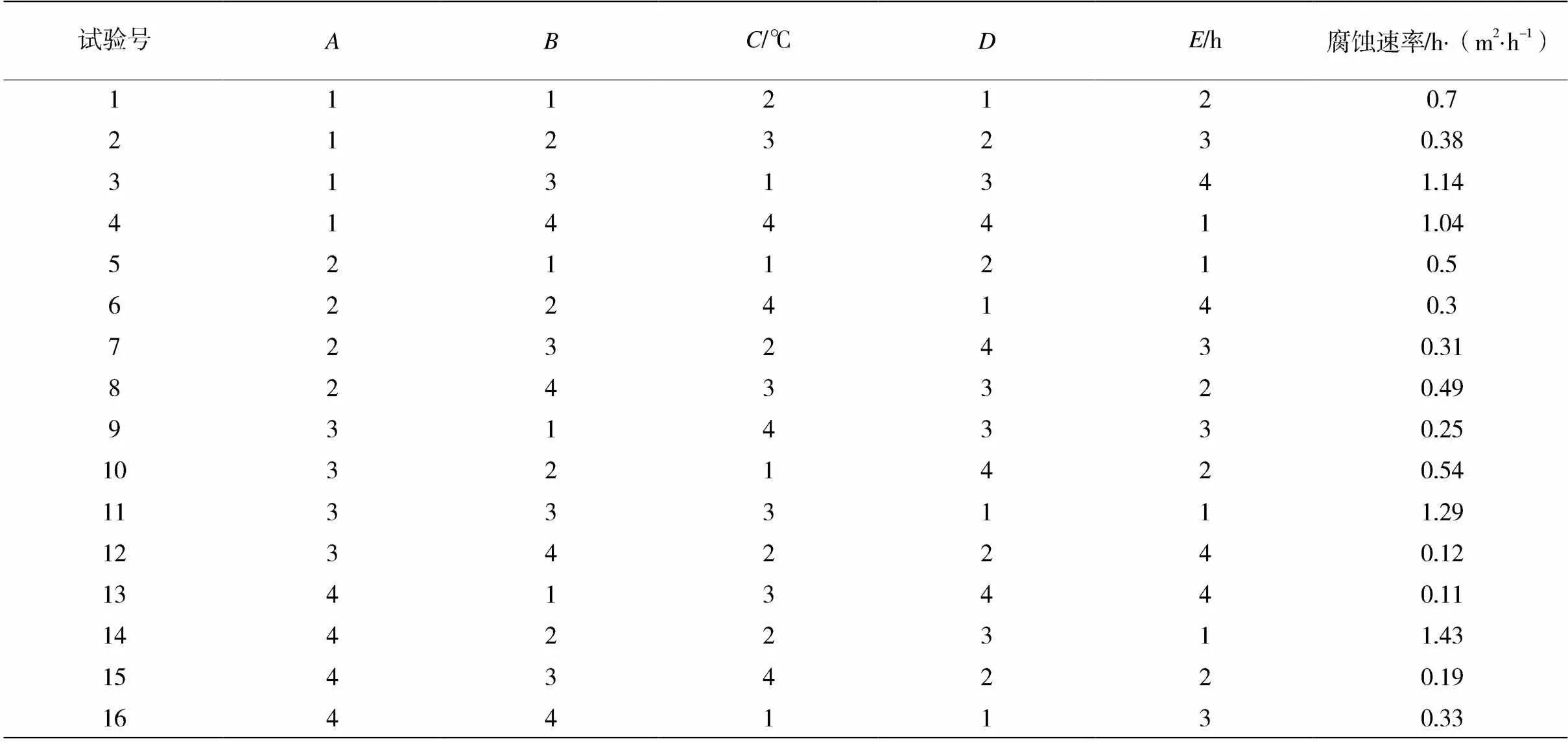
表2 响应面试验设计和结果
2.2.2 响应面的分析与优化
根据试验的回归方程,利用软件Design-Expert得到其响应曲面图形,对拟合得到的响应曲面形状进行分析,考察曼尼希碱合成的各个反应条件对其腐蚀速率的影响。其响应曲面图如图7所示,6组图较为直观反应了各个因素对于响应值造成的影响。

表3 回归模型的方差分析
注:*差异不显著(>0.05);**差异显著(<0.05);***差异极显著(<0.01)。
分析并对比6组图和表3中的值可知,模型的一次项、和影响极显著(<0.01),影响显著(<0.05),影响不显著(>0.05),根据值大小可推断各因素对腐蚀速率的影响程度为:(pH)>(温度)>(醛酮比)>(时间)>(胺酮比);交互项中、、、和影响极显著(<0.01),而影响不显著(>0.05)。此结果说明曼尼希碱的合成过程中的各个条件对腐蚀速率的影响均不能用线性关系来描述,因此采用回归方程可获得最佳的合成条件。

2.2.3 模型的优化和验证
为了检验模型结果的准确性,获得合成曼尼希碱的最佳工艺条件,分析回归方程,得到曼尼希碱的最佳合成条件为胺酮比()为1.02,醛酮比()为1.066,反应温度()为67.2 ℃,pH()为3.46和时间()为2.96 h,该条件下将这种曼尼希碱添加到腐蚀介质中后的腐蚀速率为0.02 g·(m2·h-1)。结合实际生产的情况,最终选取合成条件为胺酮比()为1.0,醛酮比()为1.1,反应温度()为67 ℃,pH()为3.5和时间()为3 h。
2.3 曼尼希碱季铵盐的表征及性能评价
2.3.1 曼尼希碱季铵盐的表征
采用响应曲面法优化的最优合成工艺条件,对曼尼希碱季铵盐进行红外表征,如图8所示。
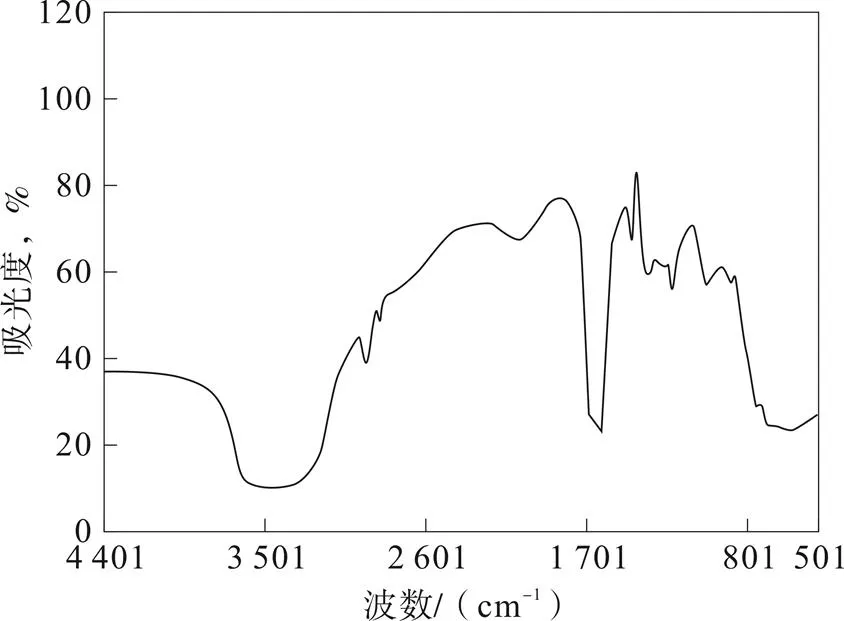
图8 曼尼希碱季铵盐缓蚀剂的红外光谱
由图8可以看出:波数在1 639 cm-1处出现羰基的特征吸收峰;在2 862 cm-1处出现C-N键伸缩振动峰;在1 524 cm-1处出现了特征吸收峰[C-N]+,说明产物分子中有季铵结构存在;在692 cm-1和748 cm-1处出现苯环的弯曲振动双峰。从红外图谱可以看出,证明该物质即为所获的目标产物。
2.3.2 抗温性与抗酸性
抗温性与抗酸性是评价缓蚀剂的重要指标之一。向体系添加2%的曼尼希碱季铵盐缓蚀剂,改变腐蚀体系的温度和HCl浓度,对N80钢片进行静态刮片腐蚀试验,测定结果如图9所示。
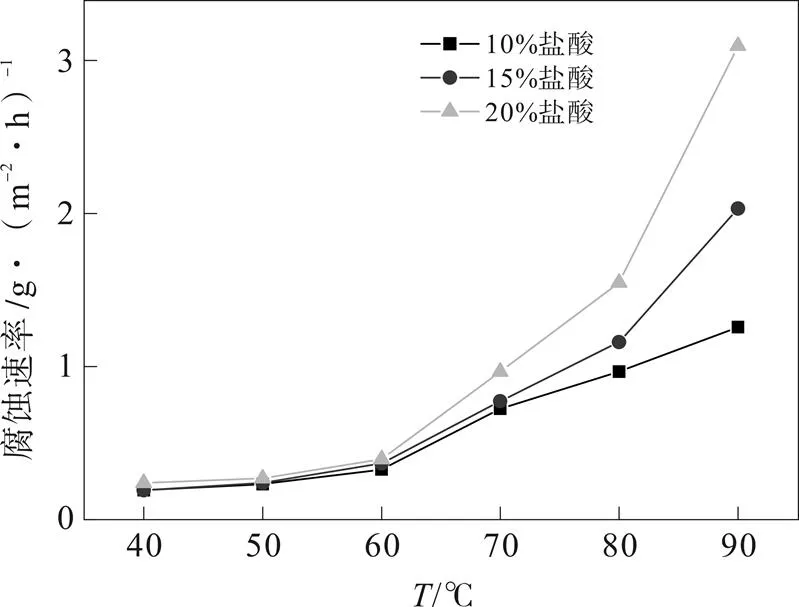
图9 腐蚀温度和HCl浓度对腐蚀速率的影响
由图9可知,N80钢片的腐蚀速率随着温度的升高而变大,当腐蚀试验温度超过80 ℃时,腐蚀速率急剧加快。但在腐蚀试验温度为40~60 ℃时,其腐蚀速率较低,说明该缓蚀剂的缓蚀效果良好。在90 ℃时,N80钢片在15%HCl体系中腐蚀速率降为2.01 g/(m2·h),表明缓蚀剂具有一定抗温性、抗酸性。
2.4 极化曲线
采用CS350H电化学工作站测定缓蚀剂TS-13的极化曲线,见图10。

图10 极化曲线图
由图10可以看出,将5%的曼尼希碱季铵盐缓蚀剂加入至15%的HCl体系中,N80钢的自腐蚀电位明显增大,阴极、阳极极化曲线均向低电流方向移动,自腐蚀电流明显减小,阴极、阳极极化曲线的Tafel斜率均变大,但阳极极化曲线的变化趋势更加明显。由此看出,该曼尼希碱季铵盐碱缓蚀剂是以抑制阳极过程为主的混合控制型缓蚀剂。
3 结论
在单因素试验的基础上,利用Design Expert 7.0.0设计软件,建立了关于缓蚀速率和各合成条件因素之间的数学模型,并验证了该模型,获得了曼尼希碱季铵盐的最佳合成条件及理论响应值。获得的最佳合成工艺为:胺酮比为1.0,醛酮比为1.1,反应温度为67 ℃,反应pH为3.5和反应时间为3 h。采用最佳工艺合成曼尼希碱,在90 ℃的盐酸体系内加入2%缓蚀剂,N80钢片的腐蚀速率降为2.01 g/(m2·h)。极化曲线测试的结果表明:该季铵盐缓蚀剂TS-13主要是以抑制阳极腐蚀过程为主的混合型缓蚀剂。
[1]何新快,陈白珍,张钦发. 缓蚀剂的研究现状与展望[J]. 材料保护,2003, 36(8):1-3.
[2]周生杰,郭学辉,杜素珍,宋宇,胡百顺,石茂才. 油井酸化腐蚀剂的开发研究进展[J]. 2014, 26(5): 469-472.
[3]刘朝霞,张贵才,孙铭勤,何小娟,刘国良. 120℃高温酸化缓蚀体系的研究与评价[J]. 钻采工艺,2005, 28(2): 81-83.
[4]刘志辉,王霞,吴艺琛. 曼尼希碱型酸化缓蚀剂研究进展[J]. 应用化工,2014, 43(1): 148-150.
[5]刘德新,邱广敏,赵修太. 高温酸化缓蚀剂的合成与筛选[J]. 钻采工艺,2007,30(4):l19-120.
Optimization of the Synthesis Process of Mannich Base by Response Surface Method
(Petroleum Engineering Technology Research Institute of Sinopec Jianghan Oilfield Company, Hubei Wuhan 430035, China)
A Mannich base synthesis process was optimized by response surface analysis. The Mannich base was obtained via Mannich reaction and quaternary amination reaction. Taking amine-ketone ratio, aldehyde-ketone ratio, reaction temperature, pH and reaction time as experimental factors, based on the analysis of significance and interaction among different factors, the optimal condition of synthesis process was obtained as followed: the ratio of amine to ketone 1.02, the ratio of aldehyde to ketone 1.066, the reaction temperature 67.2 ℃, the pH 3.46 and the time 2.96 h. Mannich base was obtained under the optimal condition and its corrosion rate was 0.02 g·(m2·h-1) in corrosion medium. The model established by response surface methodology is accurate after model verification. The synthesis process of Mannich base and established model can provide reference value for synthesis of Mannich base.
Mannich base; corrosion rate; synthesis; response surface methodology
2020-02-04
岳泉(1984-),男,湖北省武汉人,工程师,硕士研究生,2009毕业于长江大学油气田开发工程专业,研究方向:页岩气压裂工艺、化学品研发、提高采收率、水处理、防腐防垢。
TG 174.42
A
1004-0935(2020)03-0233-05

