酚类天然产物Buxifoximes A的合成及生物活性
钟上勇, 李星毅, 王艳红, 胡志勇, 白云丽, 荀苗苗, 袁长春
(中北大学化学工程与技术学院 化工综合国家级实验教学示范中心, 太原 030000)
1 引 言
酚类化合物是一类非常重要的化学物质[1],不仅广泛存在于活性药物分子[2]、天然产物[3]、农用化学品[1]和功能材料[4]中,还常常作为起始原料和中间体广泛应用于化学工业生产[5]和有机合成化学研究中[6]. 因此,酚类化合物的化学合成研究一直是有机合成研究中的热点问题之一[7],那些具有良好生物活性的酚类天然产物更是引起了天然产物全合成化学家们的广泛关注[3,8].
酒饼簕(Atalantia buxifolia)是一类多分布于东南亚沿海地区的茴香科常绿灌木植物,同时它还是一味被中国海南黎族人民广为应用的传统中药,具有止咳化痰、消肿止痛、除湿、抗疟等多种功效[9]. 关于此类植物化学成分的研究也十分广泛,并分离鉴定了生物碱类、香豆素类、柠檬苦素类、倍半萜类等多种类型的天然产物,具有抗菌、抗过敏、昆虫拒食、细胞毒等多样的生物活性[10-15].

图1 目标化合物1与2的结构Fig.1 Structures of target compounds 1 and 2
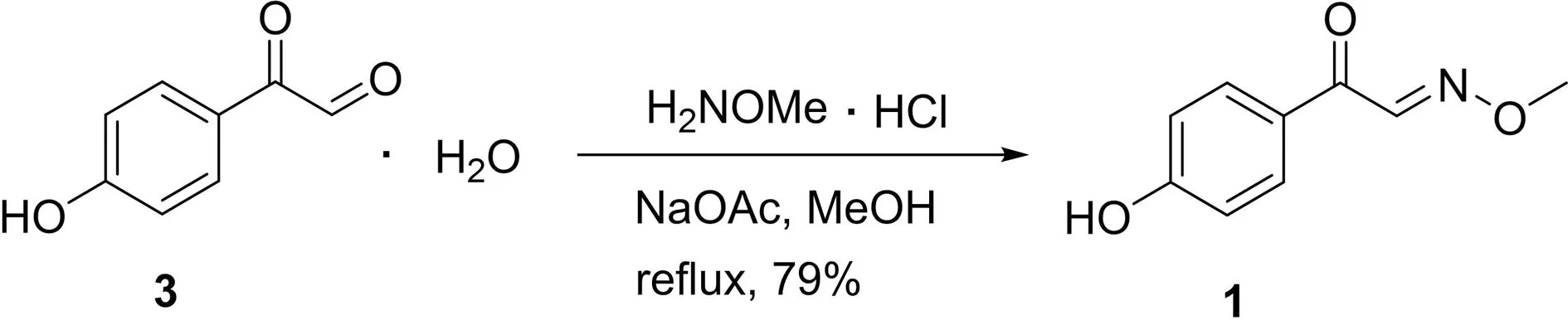
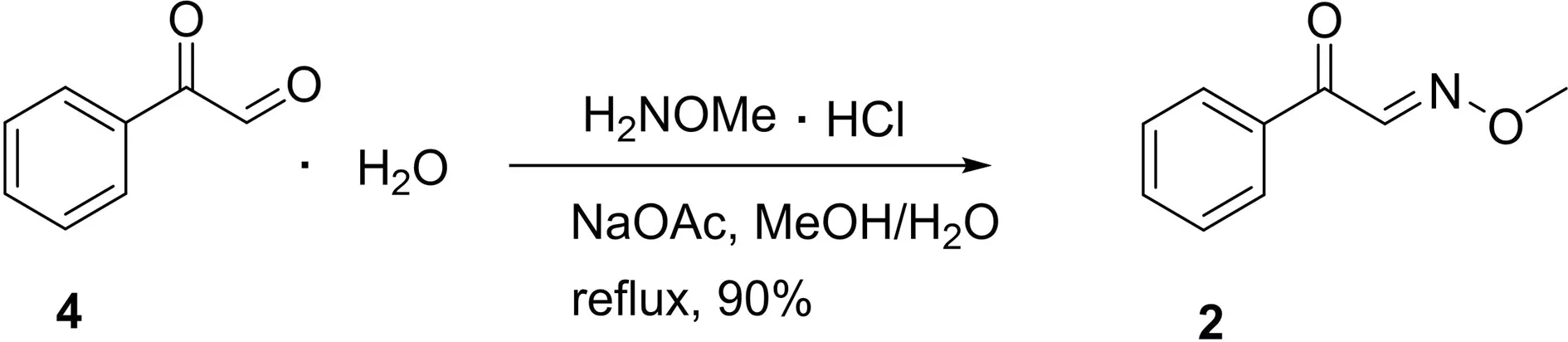
图2 目标化合物1与2的合成Fig.2 Syntheses of target compounds 1 and 2
2017年, Cheng课题组从该植物的树枝中提取分离了一系列酚类及其酚类衍生天然产物[16],其中化合物1被命名为Buxifoximes A(图1),该化合物含有苯酚和醛肟两个结构单元. Buxifoximes A具有显著的抗炎活性,可以有效抑制超氧阴离子的生成,其IC50值为4.8 ± 0.7 μmol/L. 与化合物1一同被Cheng课题组分离鉴定的还有已知化合物2,结构上二者只是有无酚羟基的差别. Buxifoximes A独特的结构以及潜在的生物活性,引起了我们的合成兴趣. 本文以商品化试剂4-羟基苯甲酰甲醛水合物为起始原料,与甲氧基胺盐酸盐经一步肟化反应合成了Buxifoximes A,同时还经已知步骤合成了化合物2 (图2),并初步研究了化合物1和2的抗肿瘤活性.
2 实验部分
2.1 仪器与试剂
瑞士Bruker公司Advance Ⅲ HD 600 MHz型核磁共振波谱仪(CDCl3为溶剂,TMS为内标);美国Thermo Fisher Exactive Plus型高分辨质谱仪;安捷伦Gemini 型X-射线单晶衍射仪;恒温培养箱、移液枪、离心机均购自美国Thermo Fisher公司;96孔细胞培养板、multilabel reader酶标仪均购自美国PerkinElmer公司.
4-羟基苯甲酰甲醛水合物、乙酸钠、甲氧基胺盐酸盐、二甲基亚砜均购自百灵威科技有限公司;苯甲酰甲醛水合物、三乙胺均购自萨恩化学技术(上海)有限公司;四氢呋喃、无水甲醇均为分析纯,用前未经处理;Z-138和MV4-11细胞均购自美国模式培养物集存库(ATCC);FBS、抗生素、RPMI1640培养基均购自购自美国Gibco生命科技公司;CellTiter-Glo试剂购自普洛麦格(Promega)生物技术公司.
2.2 合 成
2.2.1 化合物 1的合成 室温下,向装有回流冷凝管的三口烧瓶中依次加入4-羟基苯甲酰甲醛水合物(化合物3,100.9 mg, 0.6 mmol)、乙酸钠(49.2 mg, 0.6 mmol),并用注射器加入10.0 mL无水甲醇,最后加入甲氧基胺盐酸盐(50.1 mg, 0.6 mmol).将反应液加热至回流,反应4 h后停止加热并冷却至室温.然后室温搅拌下,向反应体系加入30.0 mL饱和碳酸氢钠,旋转蒸发仪减压除去甲醇.水相使用乙酸乙酯萃取(100 mL×3次),合并有机相并用无水硫酸钠干燥除去水分,过滤除去硫酸钠,在旋转蒸发仪上减压浓缩后经硅胶层析柱 [洗脱剂:A=V(石油醚)∶V(乙酸乙酯)=4∶1] 纯化后得白色固体1,共84.9 mg,收率79%,1H NMR (600 MHz, CDCl3)δ4.09 (s, 3H), 5.42 (s, 1H) 6.90 (d, J = 9.0 Hz, 1H),7.9 (s, 1H), 8.09 (d, J = 8.4 Hz, 1H);13C NMR (150 MHz, CDCl3)δ63.5(s), 115.5(s), 129.2(s), 133.0(s), 147.3(s), 160.5(s), 186.4(s);HRMS (ESI):m/zcalcd for C9H8NO3{[M+H]+}178.0510 , found 178.0500.
2.2.1 化合物 2的合成 根据已知步骤可合成化合物2[17],路线如图2所示. 室温下,向装有回流冷凝管的三口瓶中依次加入苯甲酰甲醛水合物(化合物4,760.8 mg, 5.0 mmol)、乙酸钠(410.2 mg, 5.0 mmol),并用注射器依次加入7.5 mL无水甲醇以及2.5 mL蒸馏水,最后加入甲氧基胺盐酸盐(417.6 mg, 5.0 mmol). 将反应液加热至回流,反应30 min后停止加热并冷却至室温.然后室温搅拌下,向反应体系加入50.0 mL饱和碳酸氢钠,旋转蒸发仪减压除去甲醇.水相使用乙酸乙酯萃取(150 mL×3次),合并有机相并用无水硫酸钠干燥除去水分,过滤除去硫酸钠,在旋转蒸发仪上减压浓缩后经硅胶层析柱 [洗脱剂:A=V(石油醚)∶V(乙酸乙酯)=60∶1] 纯化后得淡黄色油状体2,共734.4 mg,收率90%,1H NMR (600 MHz, CDCl3)δ4.08 (s, 3H, CH3O), 7.44~7.48 (m, 2H), 7.58~7.64 (m, 1H), 7.95 (s, 1H), 8.07~8.10 (m, 2H);13C NMR (150 MHz, CDCl3)δ63.5(s), 128.4(s), 130.3(s), 133.5(s), 135.9(s), 147.3(s), 188.2(s).
2.2 化合物1与化合物2的细胞生长抑制试验
分别将处于对数生长期的套细胞淋巴瘤细胞Z-138、急性单核白血病细胞MV4-11于1 000 rpm下离心3 min后,用含有10% FBS,1% 抗生素(青霉素/链霉素)的RPMI1640培养基重悬上述离心后的细胞,使用细胞计数仪计数并分别调整细胞个数为50 000/mL(Z-138细胞)和30 000/mL(MV4-11细胞). 用移液枪轻吹混匀,以100 μL/孔的体积将细胞接种于96孔细胞培养板中,于5% CO2、37 ℃恒温培养箱中静置孵育1 h. 以DMSO为阴性对照组,实验组加入稀释于培养基中的不同浓度的化合物1或化合物2,以100 μL/孔的体积转移至含有细胞的96孔板,并分别保持DMSO的终浓度为1‰(Z-138细胞)和2‰(MV4-11细胞). 化合物处理细胞的最终浓度为200,100,50,25,12.5,6.25,3.125,1.562 5和0.781 25 μmol/L.
培养4 d后检测细胞的存活率:每孔加入20 μL的CellTiter-Glo试剂,室温环境下摇床孵育10 min,使其充分混匀并反应,而后使用移液枪吸取100 μL混悬液转移到96孔细胞培养板. 上机读板,在multilabel reader酶标仪上于400~700 nm波长下进行检测,全程避光处理. 检测结果通过GraphPad Prism 7.0软件分析,拟合得到IC50值.
3 结果与讨论
3.1 表 征
3.1.1 化合物1和化合物2的合成与结构表征 以4-羟基苯甲酰甲醛水合物为起始原料,首先对肟化反应进行了条件优化(表1). 首先考虑溶剂因素,分别选取四氢呋喃和无水甲醇作为反应溶剂,发现溶剂效应对该反应的收率影响不大(表1, entries 1和3). 随后的研究发现,添加剂的加入对该反应的收率有较大影响:以三乙胺作为添加剂,无论是在四氢呋喃还是无水甲醇中反应,均没有目标产物生成;以乙酸钠作为添加剂,选取无水甲醇作为反应溶剂,可以以79%的收率得到目标产物1. 合成的Buxifoximes A通过1H NMR、13C NMR谱及高分辨质谱表征,表征数据与分离提取的天然Buxifoximes A完全吻合. 此外,通过已知步骤合成了Buxifoximes A的天然类似物2,并通过1H NMR、13C NMR谱表征了该化合物,表征数据与已知文献[17]一致.
表1合成化合物1的最佳反应条件
Tab.1Optimizationofthereactionconditionstopreparecompound1a
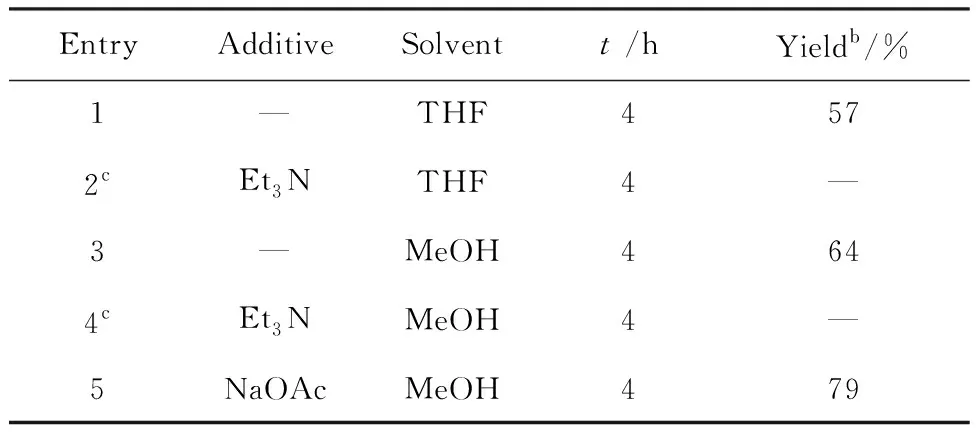
EntryAdditiveSolventt /hYieldb/%1—THF4572cEt3NTHF4—3—MeOH4644cEt3NMeOH4—5NaOAcMeOH479
aUnless other specified, the reaction was carried out with 3 (1.0 mmol) and the N-methoxylamine hydrochloride (1.0 mmol) in solvent (10.0 mL) and was monitored by TLC.bIsolated yield.cDesired product could not be obtained in this entry.
3.1.2 化合物1与化合物2的细胞生长抑制试验 利用体外细胞生长速率测定法[18],选取了两株肿瘤细胞Z-138和MV4-11对化合物1和化合物2进行了细胞生长抑制试验(表2). 结果表明,化合物1和化合物2对MV4-11细胞系有优秀的抑制作用,而对Z-138细胞系基本无抑制效果. 化合物1较之于化合物2表现了更强的增长抑制能力,构效关系上表明酚羟基是影响抗肿瘤活性的重要因素. 两个化合物的量效曲线见图3.
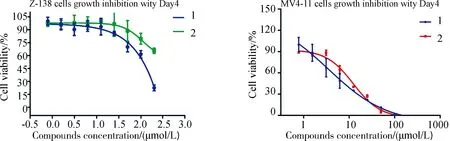
图3 化合物1与化合物2对两种肿瘤细胞抑制作用的量效曲线
Fig.3 Dose response curves for the synthesized compounds against two cancer cell lines
3 结 论
以商品化试剂4-羟基苯甲酰甲醛水合物、甲氧基胺盐酸盐为主要反应物,经一步肟化反应合成了天然产物Buxifoximes A (1),同时还经已知步骤合成了天然类似物2. 初步的抗肿瘤生物活性研究结果表明,两个化合物均对急性单核白血病细胞MV4-11显示出较好的离体抑制活性,具有深入研究的价值.

