多系统萎缩患者直立性低血压的临床特点及相关因素分析
刘 丽 李丽霞 张铁梅 张 巍
多系统萎缩(multiple system atrophy,MSA)是一组成年期散发的进行性神经变性疾病,临床表现为不同程度的自主神经功能障碍、对左旋多巴类药物反应不良的帕金森综合征、小脑性共济失调和锥体束征等临床症状和体征。临床上将MSA分为以帕金森样症状为突出表现的(MSA parkinsonism variant,MSA-P)亚型和以小脑型共济失调症状为突出表现的(MSA cerebellar variant,MSA-C)亚型[1]。各型MSA均有不同程度的自主神经功能障碍,泌尿生殖功能障碍是其最常见的症状,其次为直立性低血压(orthostatic hypotension,OH)[2,3]。目前认为,严重、全面的自主神经功能衰竭是MSA患者不良预后的最重要因素[4,5]。研究MSA患者自主神经功能障碍的危险因素可能是探索MSA发病机制的潜在突破口。本研究通过分析MSA患者OH的相关因素,旨在为明确MSA的发病机制提供线索。
对象与方法
1.研究对象:(1)纳入MSA患者:按照2008年Gilman等[1]提出的第2版诊断标准将MSA分为可能、很可能和确诊3个等级的诊断。本研究纳入的所有患者均未行病理检查,为临床很可能的MSA患者。排除标准:排除原发性帕金森病、继发性帕金森综合征、遗传性帕金森综合征;排除家族性高脂血症、甲状腺功能异常、服用降脂药物者;排除肿瘤、感染、自身免疫病、重要脏器功能不全者;排除糖尿病植物神经病变、药物、脱水等其他因素引起OH者。回顾性选择2014年1月~2019年1月在笔者医院住院的MSA患者327例,其中男性174例(53.2%),女性153例(46.8%)。患者年龄36~83岁,平均年龄59.7±8.1岁,平均发病年龄56.5±8.2岁。病程1个月~10年,平均病程3.1±2.0年。MSA-P型148例(45.3%),MSA-C型179例(54.7%)。(2)研究分组:根据卧立位血压试验或直立倾斜试验结果判定患者有无OH,将纳入的患者分为MSA伴OH组和MSA不伴OH组。
2.收集临床资料:(1)收集一般资料:收集整理所有患者临床病历资料及化验、检查,包括住院次数、年龄、性别、起病年龄、病程、主诉、现病史、既往史、用药情况等。(2)记录实验室指标:血常规、肝肾功能、血糖、血脂4项[包括甘油三酯(TG)、总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)]、糖化血红蛋白、血尿酸、血浆白蛋白、血浆球蛋白、红细胞沉降率等。(3)记录卧立位血压试验结果:患者至少卧床30min以上,首先测定卧位基础血压和心率,然后迅速站立,立即测血压和心率,此后每隔1min测量1次立位血压和心率,5min测量最后1次。评定标准:仰卧位变为站立位后3min内收缩压下降至少30mmHg或者舒张压下降至少15mmHg,即为卧立位血压试验阳性。未达到OH诊断标准者择日复测[1]。(4)记录直立倾斜试验检查结果。

结 果
1.MSA伴OH患者临床特点:327例MSA患者中,195例有OH,占59.6%;其中,190例因卧立位血压试验阳性而诊断,5例因直立倾斜试验阳性而诊断。不伴OH者132例,占40.4%。MSA伴OH的患者中,有头晕症状者103例(52.8%),其中4例患者有反复晕厥发作;卧立位收缩压差值≥50mmHg共16例,最大差值为88mmHg;立位收缩压≤80mmHg者15例,立位收缩压≤70mmHg者5例,最低立位血压为65/44mmHg。
2.MSA伴OH组和MSA不伴OH组一般资料及实验室指标的比较:在MSA伴OH患者中,男性107例,女性88例,两组OH发生率比较差异无统计学意义(107/174 vs 88/153,P>0.05);MSA-P型患者90例,MSA-C型患者105例,两型OH发生率比较差异无统计学意义(90/148 vs 105/179,P>0.05)。与MSA不伴OH组比较,MSA伴OH组TG水平更低(1.26±0.62mmol/L vs 1.54±0.87mmol/L,P<0.05);两组在年龄、病程、TC、HDL-C及LDL-C水平等方面比较差异无统计学意义(P>0.05,表1)。
3.MSA患者OH影响因素的Pearson相关性分析:笔者将性别、年龄、病程、MSA分型及实验室指标进行Pearson相关性分析,结果显示OH与TG呈负相关(r=-0.184,P<0.05),与性别、年龄、病程、MSA分型、TC、HDL-C、LDL-C等实验室指标的相关性比较,差异无统计学意义(表2)。

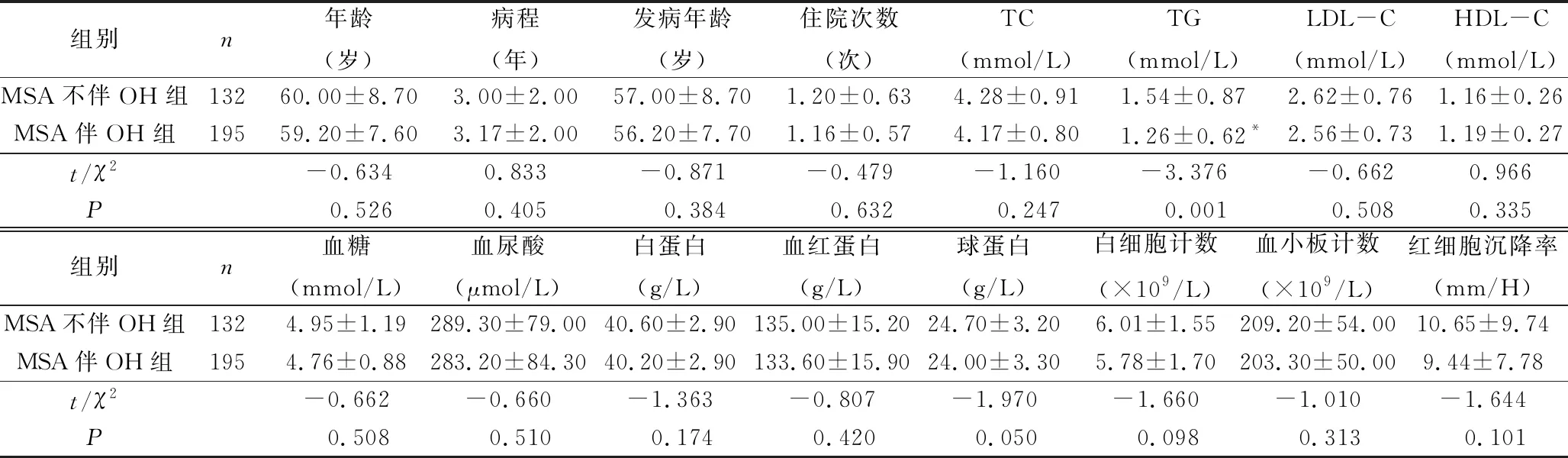
组别n年龄(岁)病程(年)发病年龄(岁)住院次数(次)TC(mmol/L)TG(mmol/L)LDL-C(mmol/L)HDL-C(mmol/L)MSA不伴OH组13260.00±8.703.00±2.0057.00±8.701.20±0.634.28±0.911.54±0.872.62±0.761.16±0.26MSA伴OH组19559.20±7.603.17±2.0056.20±7.701.16±0.574.17±0.801.26±0.62*2.56±0.731.19±0.27t/χ2-0.6340.833-0.871-0.479-1.160-3.376-0.6620.966P0.5260.4050.3840.6320.2470.0010.5080.335组别n血糖(mmol/L)血尿酸(μmol/L)白蛋白(g/L)血红蛋白(g/L)球蛋白(g/L)白细胞计数(×109/L)血小板计数(×109/L)红细胞沉降率(mm/H)MSA不伴OH组1324.95±1.19289.30±79.0040.60±2.90135.00±15.2024.70±3.206.01±1.55209.20±54.0010.65±9.74MSA伴OH组1954.76±0.88283.20±84.3040.20±2.90133.60±15.9024.00±3.305.78±1.70203.30±50.009.44±7.78t/χ2-0.662-0.660-1.363-0.807-1.970-1.660-1.010-1.644P0.5080.5100.1740.4200.0500.0980.3130.101
与MSA不伴OH组比较,*P<0.05
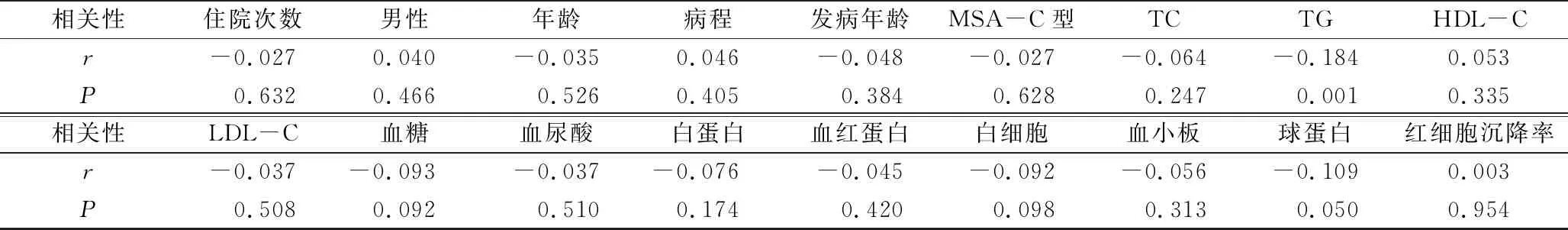
表2 MSA患者伴OH与一般资料及实验室指标的Pearson相关性分析
讨 论
MSA是一种少见的、原因不明的、进展相对快速的神经系统变性疾病,临床表现为多系统受累,少突胶质细胞内包涵体形成是此病的特征性病理改变。MSA与帕金森病、路易体痴呆等同属于α-突触核蛋白病的神经变性病,有相似的临床表现,但近期研究表明,MSA关键性特征是早期出现严重的自主神经功能衰竭,自主神经功能障碍严重程度还是可能MSA和很可能MSA诊断之间最重要的区分点[6]。MSA病变主要累及初级运动皮质、锥体和锥体外系、脑干的自主神经中枢等,病变部位主要在黑质纹状体系统、橄榄体-脑桥-小脑系统和脊髓中间内外侧细胞柱和Onuf′s核。这些部位的少突胶质细胞胞体内形成包涵体和神经元包涵体,破坏了髓鞘的完整性导致脱髓鞘,神经元受损导致自主神经功能损害症状的发生。
在MSA诊断标准中,OH被定义为由仰卧位变为站立位3min内收缩压下降至少30mmHg或者舒张压下降至少15mmHg[1]。既往研究报道OH在MSA中的发生率为43%~75%[3,7,8]。本研究中MSA患者OH发生率为59.6%,与既往研究结果较为相符。OH患者临床可表现在体位变动时出现头晕、视物模糊、行走不稳,严重者甚至出现晕厥。本研究中,52.8%的MSA伴OH患者有头晕症状,4例患者反复出现体位性晕厥,16例患者卧立位血压差值>50mmHg,立位血压<80mmHg者15例,提示OH严重影响MSA患者生活质量、工作及生存。
人体大部分血管平滑肌仅受交感缩血管神经纤维的支配,只有部分血管除接受交感缩血管神经纤维支配外,还接受某些舒血管神经纤维的支配。交感缩血管神经纤维的节前神经元位于胸、腰段脊髓的中间外侧柱内,末梢释放乙酰胆碱,作用于椎旁神经节和椎前神经内的节后神经元胞体,引起节后神经元兴奋,节后神经元末梢释放的递质为去甲肾上腺素,与血管平滑肌α受体结合引起血管收缩。正常情况下,压力感受器介导的交感神经兴奋引起血管收缩维持立位血压,而这种血管收缩的代偿功能在MSA患者中是减弱或缺失的。神经病理研究认为下丘脑室旁核血管加压素神经元缺失及胸、腰髓侧角节前交感神经元变性均可能导致MSA患者出现OH[9]。
MSA的病因及发病机制尚不清楚,既往研究显示MSA患者的血脂水平明显低于正常人群,并且,血脂降低在MSA早期即出现,与MSA病程无关,提示血脂变化可能是MSA的发病因素,而非继发性改变。MSA发病机制可能与血脂代谢异常有关,尤其是TG和HDL-C[10,11]。已有研究指出,TG和HDL-C水平减低可能与MSA发病相关[12]。本研究结果显示TG水平减低是MSA伴OH的独立危险因素,提示TG水平减低可能与MSA发病相关,TG可能在下丘脑室旁核血管加压素神经元缺失或胸、腰髓侧角节前交感神经元变性中发挥作用,有待进一步研究来证实。
少突胶质细胞是中枢神经系统的髓鞘形成细胞,髓鞘的主要成分是脂蛋白,称髓磷脂,包括髓鞘蛋白脂蛋白和髓鞘碱性蛋白等。适当的血脂成分及水平对维持髓鞘的正常结构和功能具有重要作用,脂质稳态的失衡可能导致髓鞘结构和功能异常,造成髓鞘不稳定、进而溶解和脱失[13]。目前认为髓鞘的形态和功能异常是MSA的发病核心,尸检研究发现,髓鞘溶解可能是MSA早期的发病机制之一。髓鞘异常涉及α-突触核蛋白、脂质转运体ABCA8及血脂稳态的破坏等多种因素。血清脂质水平下降可能是MSA发病的一个早期信号,即脂质稳态的失衡可能是MSA发病的始动因素,对MSA发病具有重要的预测作用。
本研究未发现OH与性别、病程、MSA类型有明显相关性,提示OH在不同性别、不同类型和不同疾病阶段的MSA患者中广泛存在。
综上所述,MSA的病因和发病机制尚不明确,治疗手段有限,研究MSA发生、进展和预后的生物学标志物可为明确其发病机制和治疗策略提供依据。本研究发现TG是MSA伴OH的独立危险因素,可能与MSA发病机制和预后有关,需继续进行论证研究。本研究为单中心的回顾性研究,病例数有限,未来需扩大样本量进行前瞻性研究,以证实本研究的结果。

