布地奈德联合噻托溴铵治疗对ACOS患者肺功能、免疫功能和炎性因子的影响
刘 莉,张红梅,韩 雪,陈国强,王志华
(邯郸市第一医院急诊科,河北邯郸 056001)
哮喘和慢性阻塞性肺疾病(COPD)是临床上常见的以气道炎症和气流受限为特征的慢性疾病。哮喘的典型特征是可逆性气流受限,而COPD的特征主要是不可逆的气流受限[1]。然而,这两种疾病之间可能存在重叠,同时具备哮喘和COPD的特征时,可界定为哮喘-COPD重叠综合征(ACOS)[2]。ACOS发病人群以老年人为主,其发病机制可能与机体免疫功能降低后患者肺部感染风险增加继发肺功能下降有关,而支气管哮喘及COPD均可激发全身炎性反应,进一步加重ACOS患者病情[3]。研究表明,近四分之一的COPD患者存在哮喘史,与单纯哮喘或COPD患者相比,ACOS患者的生活质量更差、肺功能下降更快、病死率更高,使用的医疗资源更多[4]。目前,ACOS的定义尚不完善,主要诊断标准包括支气管扩张试验阳性[第1秒用力呼气容积(FEV1)增加≥15%或≥400 mL],痰液中嗜酸性粒细胞增多和哮喘病史;次要标准包括两次或多次总IgE升高、个体特应性病史和支气管扩张试验阳性(FEV1增加≥12%或≥200 mL)[5]。临床用药尚未达成共识,大多是采用糖皮质激素、β2肾上腺受体激动剂及抗胆碱能药物等治疗[6]。布地奈德是一种糖皮质激素,可改善患者肺功能缓解临床症状,大剂量下具有良好的局部抗炎作用;噻托溴铵是一种支气管扩张剂,促进呼吸功能恢复,适用于COPD的维持治疗。为进一步探讨ACOS的治疗方法,本研究观察了布地奈德联合噻托溴铵对ACOS患者肺功能、免疫功能和炎性因子的影响,旨在为临床提供依据。
1 资料与方法
1.1一般资料 将2015年6月至2018年6月间河北省邯郸市第一医院收治的ACOS患者132例纳入研究。采用随机数表法将纳入研究者分为研究组和对照组,各66例。研究组中男38例、女28例,年龄38~75岁,平均(55.79±11.76)岁,病程3~8年,平均(5.38±7.63)年,有吸烟史的42例;临床症状:咳痰32例,呼吸困难41例,喘息29例,胸闷28例;合并症:气胸36例,支气管扩张29例,呼吸衰竭14例;存在哮喘家族史18例。对照组中男39例,女27例,年龄39~78岁,平均(56.02±12.12)岁,病程3~9年,平均(5.47±7.74)年,吸烟史44例;临床症状:咳痰34例,呼吸困难42例,喘息33例,胸闷31例;合并症:气胸34例,支气管扩张26例,呼吸衰竭16例;有哮喘家族史16例。本研究经患者知情同意并签署知情同意书,得到本院伦理委员会核准后进行。两组患者的一般资料比较差异无统计学意义(P>0.05),具有可比性,见表1。
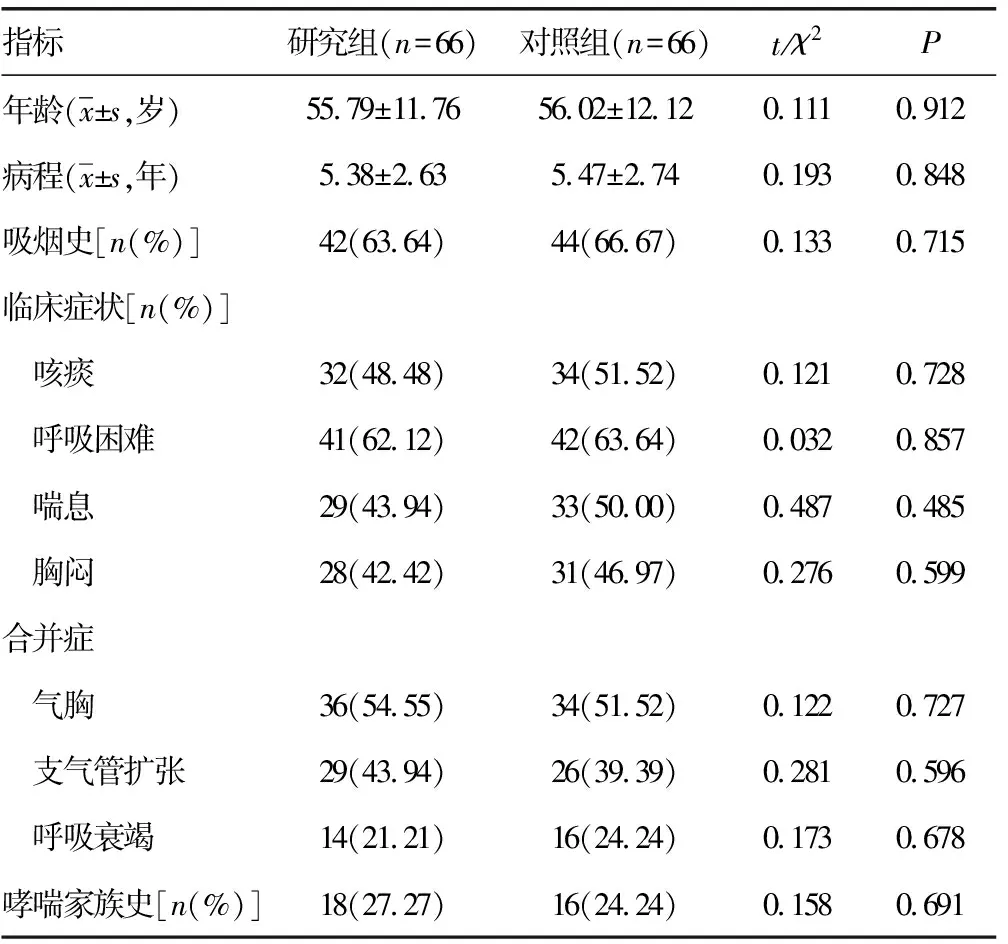
表1 两组患者的一般资料比较
1.2纳入标准与排除标准 纳入标准:(1)符合2014年全球倡议(GINA)和GOLD科学委员会联合制定的ACOS诊断标准[7];(2)入院前1月内未接受全身糖皮质激素及可能影响本研究结果的药物治疗者;(3)对本研究所用药物无过敏;(4)同时具有哮喘和COPD症状者;(5)认知功能正常可配合研究者。排除标准:(1)合并肺部、呼吸道感染性疾病者;(2)合并其他脏器器质性病变者;(3)合并免疫系统、血液系统疾病者;(4)存在肺功能检查禁忌证者;(5)哺乳或妊娠期妇女;(6)合并恶性肿瘤者。
1.3仪器与试剂 (1)Masterscreen型肺功能测试仪购自德国CareFusion公司;(2)DD-5M型号医用离心机购自湖南迈克尔实验仪器有限公司;(3)Attune NxT流式细胞仪购自赛默飞世尔科技(中国)有限公司。
1.4方法
1.4.1治疗方法 两组患者入院后均给予减少运动负荷、止咳平喘、吸氧、抗感染及机械辅助呼吸等常规治疗。然后对照组给予布地奈德粉剂(生产厂家:瑞典AstraZeneca AB公司,规格:0.1 mg×200吸/支,批号:20150522)吸入治疗,1吸/次,2次/天。研究组在对照组的基础上加用噻托溴铵干粉雾剂(生产厂家:正大天晴药业集团股份有限公司,规格:18 μg×10粒/盒,批号:20150428)吸入治疗,1粒/次,1次/天,4周为1疗程,两组患者均治疗3个疗程。治疗过程中依据患者临床症状、病情危险程度给予相应的对症治疗。
1.4.2检测方法 两组患者治疗前后均进行如下指标检测:(1)肺功能测试仪测定两组患者的肺通气及肺容量指标,包括FEV1、用力肺活量(FVC)、第1秒用力呼气容积占用力肺活量百分比(FEV1/FVC)、一氧化碳弥散量(DLCO)、吸气分数(IC/TLC)、残气量/肺总量(RV/TLC)、峰值流速(PEF)及呼出气一氧化氮(FeNO);(2)于入院第2天清晨空腹静脉采血5 mL,分2份,医用离心机3 000 r/min离心10 min后,收集血清置于-20 ℃冰箱保存待测。采用酶联免疫吸附试验(ELISA)测定白细胞介素17(IL-17)、白细胞介素4(IL-4)、白细胞介素6(IL-6)及肿瘤坏死因子(TNF-α)水平,试剂盒均购自上海酶联生物科技有限公司(批号:20150218、20170623),速率散射比浊法测定超敏C反应蛋白(hs-CRP)水平,免疫荧光法测定IgE水平,自赛默飞世尔科技(中国)有限公司(批号20150523、2017817);(3)采用流式细胞仪测定患者的Th1、Th2细胞百分比、Th1/Th2比值、CD3+细胞百分比、CD4+/CD8+比值;(4)治疗前后采用哮喘控制测试(ACT量表)、COPD自我评估测试问卷(CAT)进行评分,统计治疗期间的急性加重频次和不良反应。所有检验操作严格按照试剂盒及仪器说明书进行操作。
1.5判定标准 疗效判定标准[8],显效:治疗后患者临床症状、肺功能显著改善,哮喘连续1周未发作;好转:治疗后患者临床症状得到控制,肺功能明显改善,1周内哮喘发作次数减少50%以上;无效:患者临床症状、体征、肺功能无改善或病情恶化。有效率=显效率+好转率。
1.6统计学处理 本研究采用SPSS22.0软件进行数据分析。肺功能指标、免疫功能指标、炎性因子指标以及ACT、CAT评分和急性发作/加重频次等计量资料的比较采用t检验或配对t检验;计数资料的组间比较采用χ2检验;等级资料的组间比较采用秩和检验;均为双侧检验,P<0.05表示差异有统计学意义。
2 结 果
2.1两组ACOS患者疗效比较 研究组有效率为92.42%,高于对照组的77.27%,差异有统计学意义(P<0.05),见表2。

表2 两组ACOS患者疗效的比较
2.2两组患者治疗前后的肺功能指标的比较 治疗前两组患者的FEV1、FVC、FEV1/FVC、DLCO、IC/TLC、RV/TLC、PEF及FeNO比较,差异均无统计学意义(P>0.05);治疗后,两组患者的FEV1、FVC、FEV1/FVC、DLCO、IC/TLC及PEF均明显升高且研究组高于对照组,而RV/TLC、FeNO明显降低且研究组低于对照组,差异均有统计学意义(P<0.05)。见表3。
2.3两组患者治疗前后免疫功能指标比较 治疗前,两组患者的Th1、Th2细胞百分比、Th1/Th2比值、CD3+细胞百分比、CD4+/CD8+比值及IgE水平比较,差异无统计学意义(P>0.05);治疗后,两组患者的Th1、Th2细胞百分比、Th1/Th2比值、CD3+细胞百分比、CD4+/CD8+比值均明显升高,而且研究组高于对照组,IgE水平明显降低且研究组低于对照组,差异均有统计学意义(P<0.05)。见表4。
2.4两组患者治疗前后的炎性因子水平比较 治疗前,两组患者的IL-17、Hs-CRP、IL-4、IL-6及TNF-α水平比较,差异无统计学意义(P>0.05);治疗后,两组患者的IL-17、Hs-CRP、IL-4、IL-6及TNF-α水平均明显降低且研究组低于对照组,差异均有统计学意义(P<0.05)。见表5。
2.5两组患者治疗前后ACT、CAT评分及急性发作/加重频次比较 治疗前,两组患者的ACT、CAT评分及急性发作/加重频次比较,差异无统计学意义(P>0.05);治疗后,两组患者的ACT评分均明显升高,CAT评分及急性发作/加重频次均明显降低且研究组ACT评分高于对照组,CAT评分及急性发作/加重频次低于对照组,差异均有统计学意义(P<0.05)。见表6。
2.6两组患者治疗后的不良反应发生情况比较 研究组治疗期间发生口干2例、心悸2例、排尿困难2例、口腔假丝酵母菌感染3例,总发生率为13.64%(9/66);对照组治疗期间发生口干2例、心悸1例、排尿困难1例、口腔假丝酵母菌感染1例,总发生率7.58%(5/66)。均未处理就自行好转。两组不良反应发生率比较,差异无统计学意义(χ2=1.278,P=0.258)。

表3 两组患者治疗前后肺功能指标的比较

表4 两组患者治疗前后的免疫功能指标比较

表5 两组患者治疗前后的炎性因子各指标比较

表6 两组患者治疗前后的ACT、CAT评分及急性发作/加重频次比较
3 讨 论
ACOS在阻塞性气道疾病患者中很常见,特别是在老年人群中,并且其患病率随着年龄的增长而持续增加[9]。据研究统计,50岁以上的阻塞性气道疾病患者中,约65%为ACOS患者,19%为单纯COPD患者,16%为单纯哮喘患者[10-11]。ACOS兼有哮喘和COPD的相关症状,而且均以持续性气流受限为主要特征慢性气道炎性病变,其发病机制复杂,是遗传、基因和环境等多因素相互作用的结果。哮喘和COPD均存在不同程度的气道重塑、呼吸困难、肺功能下降及支气管痉挛等症状,部分患者也具有气道高反应性和可逆性气流受限。既往研究表明,哮喘和COPD均可激发机体氧化应激[12],白细胞活化及免疫功能紊乱,继而出现全身炎性反应,炎性因子的大量释放可导致ACOS病情加重。
ACOS与哮喘、COPD的治疗比较,病情更重、预后更差,消耗的医疗资源也更多,其临床治疗方法尚未统一,治疗方案的制订通常综合了现行的哮喘和COPD治疗指南。糖皮质激素是临床治疗持续性气道炎性反应的一线药物,其局部抗炎效果显著,不良反应轻微,在哮喘和COPD的治疗过程中被广泛应用。研究也证实,吸入糖皮质激素可有效降低哮喘和COPD患者的气道高反应性,延缓气道重塑,抑制炎性反应,提高肺功能及减少急性发作频次[13-14]。但单纯使用糖皮质激素类药物效果欠佳,且大剂量使用糖皮质激素会导致不良反应增加,患者不耐受,因此需要联合用药以提高疗效和减少不良反应。
布地奈德为糖皮质激素的一种,可作用于气道炎性反应的多个环节中,抑制炎性因子的分泌合成,降低机体炎性反应,从而改善支气管黏膜上皮细胞功能,延缓气道重塑,进而改善患者肺功能。噻托溴铵为季铵衍生物,是一种特异性长效抗胆碱药,对毒蕈碱受体具有较高亲和力,可特异性作用于M1、M3受体,能长时间、持久地扩张支气管,改善肺功能,不良反应相对较小。在临床试验和动物实验中均发现,噻托溴铵可显著提高哮喘的治疗效果[15-17]。本研究采用布地奈德联合噻托溴铵治疗ACOS患者,通过多靶点、多途径给药,结果显示治疗后研究组的FEV1、FVC、FEV1/FVC、DLCO、IC/TLC及PEF均高于对照组,而RV/TLC、FeNO低于对照组,炎性因子(包括IL-17、Hs-CRP、IL-4、IL-6及TNF-α)水平均低于对照组。这提示,布地奈德联合噻托溴铵可明显改善患者的肺功能,降低机体炎性因子水平,效果优于对照组,与相关研究结果一致[18-19]。炎性反应在ACOS患者疾病的发生、发展中起着重要作用,而T淋巴细胞亚群在气道炎性反应中作用明显,T淋巴细胞亚群失衡是哮喘的重要发病机制之一[20]。本研究中发现,治疗后研究的Th1、Th2细胞百分比、Th1/Th2比值、CD3+细胞百分比、CD4+/CD8+比值均高于对照组,而IgE低于对照组,ACT评分高于对照组,CAT评分及急性发作/加重频次低于对照组。这提示,布地奈德联合噻托溴铵可显著改善患者的免疫功能,减轻患者临床症状和急性发作频次,提高患者生活质量。此外,研究的临床疗效显著高于对照组,而不良反应发生情况两组间比较无明显差异。这提示,布地奈德联合噻托溴铵治疗ACOS患者在提高疗效的同时并未明显增加不良反应。
4 结 论
布地奈德联合噻托溴铵治疗ACOS患者安全有效,可明显缓解患者临床症状、改善肺功能,提高患者免疫功能,降低炎性因子水平。

