重复性经颅磁刺激治疗功能性消化不良伴失眠20例
柳 慧,梅应兵,2*,黄乜瑞,吴静洁
1.湖北中医药大学(湖北 武汉 430061)2.湖北省中医院、湖北中医药大学附属医院老年病科、湖北省中医药研究院(湖北 武汉 430061)
功能性消化不良(Functional Dyspepsia,FD)是临床上常见的消化系统疾病之一,临床上以上腹痛、餐后不适为主要症状。FD全球发病率为5%~11%[1],我国FD发病率为18%~45%,占消化门诊的20%~40%[2]。研究表明[3]FD与焦虑、抑郁、失眠关系密切,FD多伴有睡眠质量下降及睡眠障碍。失眠是一种以入睡困难和(或)睡眠持续困难为主的睡眠障碍,2002年“世界睡眠日”对全球10个国家的研究发现[4]一般人群中失眠人数占12.1%(DSM-IV标准),我国有45.4%在过去1个月内经历过不同程度的失眠,10%患有失眠症。失眠不仅会影响工作和生活,增加交通事故风险,还会浪费医疗资源。研究显示[5]伴有明显功能损害的失眠症患者每人每年造成的经济负担为5 010美元。失眠的治疗,临床多采用镇静催眠类药物,而这些药物多具有明显的不良反应,同时长期服用还有一定的依赖性、成瘾性。重复性经颅磁刺激术(Repetitive Transcranial Magnetic Stimulation,rTMS)是一种无痛、无创的绿色治疗方法,可以有效改善抑郁、焦虑、失眠。本研究发现rTMS治疗在改善睡眠的同时,对FD症状也起到改善作用,现报道如下。
1 资料与方法
1.1一般资料选取2018年10月-2019年3月在湖北省中医院确诊为FD合并失眠患者40例,以抛硬币的方式随机分为对照组和治疗组,每组各20例,所有患者均符合中华医学会神经病学分会睡眠障碍学组失眠诊断标准[6]和罗马Ⅳ功能性消化不良诊断标准[7]。纳入标准:①年龄18~70岁;②无严重肝肾功能损害及心脑血管疾病;③签署知情同意。排除标准:①有rTMS治疗禁忌症如安装心脏起搏器、心脏支架者,耳蜗植入物者,颅内置有金属异物者,颅内压明显增高者,有严重出血倾向者,有癫痫病史或家族史者;②胃镜检查有器质性改变者,有器质性疾病导致的失眠如甲亢、癫痫等;③过敏体质,对安眠药、促胃动力药等药物不能耐受者。两组患者在性别、年龄、病程等一般资料比较,差异无统计学意义(P>0.05),具有可比性,见表1。
1.2治疗方法对照组采用西药治疗,根据症状给予抑酸、促胃肠蠕动药物及安定类药物等治疗,治疗组在西医常规治疗基础上予以rTMS治疗,重复经颅磁刺激仪(武汉依瑞德医疗设备新技术有限公司,YRDCCY型),刺激鼻枕线与颞顶线交叉点(Cz)后1 cm处,刺激频率1 Hz,刺激个数10个,间歇时间5 s,重复60次,15 min/次,1次/d,连续治疗14 d。

表1 两组患者一般资料比较
1.3检测指标治疗前,治疗结束后采用相关量表进行评分。随访3个月,观察并记录患者出现的不良反应及应对措施。
1.3.1 FD总体症状积分 FD症状积分=∑(症状严重程度×发作频率),餐后饱胀不适、早饱感、中上腹疼痛、中上腹烧灼感4个症状,严重程度:从未有过计0分;轻度,不影响生活计1分;中度,尚能忍受,已经部分影响生活计2分;重度,难以忍受,明显影响日常生活计3分。发作频率计分:无计0分;每周3 d计1分;每周4~5 d计2分;每周6~7 d计3分[8]。
1.3.2 匹兹堡睡眠量表(PSQI) 分别从主观睡眠质量、入睡时间、睡眠时间、睡眠效率、睡眠障碍、催眠药物、日间功能障碍7个方面评定其睡眠质量,评分范围0~21分,分数越高,睡眠质量越差[9]。
1.3.3 汉密尔顿焦虑量表(HAMA) 14~21分提示有焦虑;21~29分提示明显焦虑;≥29分提示严重焦虑[10]。
1.3.4 汉密尔顿抑郁量表(HAMD) 8~20分,提示可能有抑郁症状;20~35分提示有轻或中度抑郁;≥35分提示严重抑郁[11]。

2 结果
2.1治疗前后FD总体症状积分和PSQI积分比较治疗前两组FD总体症状积分、PSQI积分比较,差异无统计学意义(P>0.05),治疗后两组FD总体症状积分、PSQI积分均低于治疗前(P<0.05),治疗组FD总体症状积分、PSQI积分低于对照组(P<0.05),见表2。
2.2治疗前后HAMA、HAMD积分比较治疗前两组HAMA、HAMD积分比较,差异无统计学意义(P>0.05),治疗后两组HAMA、HAMD积分均低于治疗前(P<0.05),治疗组HAMA积分低于对照组(P<0.05),见表3。
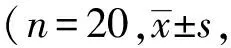
表2 两组治疗前后FD的总体症状积分、PSQI积分比较分)
注:与治疗前比较,*:P<0.05;与对照组比较,#:P<0.05。
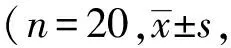
表3 两组治疗前后HAMA、HAMD比较分)
注:与治疗前比较,*:P<0.05;与对照组比较,#:P<0.05。
2.3不良反应对照组无明显不良反应,治疗组仅1例患者出现头痛,未予特殊处理,症状自行消失。
3 讨论
FD是临床常见的消化疾病,具有反复发作,迁延难愈的特点,患者反复就诊,浪费大量医疗资源。目前西医主要采用HP根除治疗、促进胃肠动力、抑酸护胃、抗焦虑抑郁等方法,但效果不尽如意。2016年Rome Ⅳ将FD改为脑-肠轴互动异常,新定义强调脑-肠轴对于FD的重要性,认为FD主要是肠道内微生物失调、黏膜免疫功能改变、肠道信号改变(内脏过敏症)和中枢神经系统调节肠道信号和运动功能失调等因素失调导致[12]。脑-肠互动主要通过分泌神经递质(脑肠肽)在中枢神经系统、肠神经系统及胃肠道效应细胞间传递而实现[13]。很多神经递质不仅在胃肠系统中发挥重要作用,还参与了睡眠和觉醒生理周期的调控[14],如肠道细胞产生的5羟色胺(5-HT)[15],是一种重要的中枢神经递质,不仅在FD中发挥重要作用,还参与多种行为、情绪活动和睡眠的调节,在睡眠—觉醒调节中起重要作用。褪黑素除在消化系统发挥作用外,还具有显著的催眠作用。一氧化氮(NO)是胃肠运动的主要抑制性递质,可能具有促进觉醒的作用[16]。如今随着生活各种压力的增加,精神心理因素和应激因素对于FD和失眠的影响越来越明显。De La Roca-Chaipas等[17]认为应激、焦虑、抑郁能延缓胃排空,从而导致FD。研究显示[18]70%~80%精神障碍患者均伴有失眠症状,而50%失眠患者同时患有1种或1种以上的精神障碍。
rTMS在临床精神病、神经疾病及康复领域获得越来越多的认可。rTMS是时变磁场作用于大脑皮质产生感应电流来改变皮质神经细胞的动作电位,从而影响脑内代谢和神经电活动。2017年中国失眠症诊断及治疗指南中明确提到了rTMS,其治疗失眠的机理目前尚不十分明确。李冬等[19]认为rTMS可促进入睡并增强睡眠深度,影响睡眠障碍者的免疫系统,影响大脑皮质可塑性相关基因及分子的表达水平,影响大脑神经网络及神经递质水平,影响褪黑激素的分泌过程和影响机体的神经内分泌活动。罗京等[20]认为rTMS主要通过诱导加深睡眠深度和入睡时间,影响局部脑代谢功能和神经递质水平,影响褪黑素的分泌,影响心理因素4个方面来改善睡眠质量。基于此研究,rTMS治疗对于FD的影响可能与以下几个方面有关:①通过改变神经递质的水平;②影响褪黑素分泌;③影响神经内分泌的调节和心理因素。
rTMS频率不同,作用也不同,高频(15~25 Hz)会使刺激部位兴奋,引起局部脑血流量、葡萄糖代谢率增加,脑源性神经营养因子分泌增加,基因表达增加等。低频(1~5 Hz)会使刺激部位抑制。睡眠障碍患者多采用低频刺激顶叶Cz后1 cm,或者右侧额叶背外侧,抑郁症患者多采用低频刺激右侧额叶背外侧,高频刺激左侧额叶背外侧。
综上所述,rTMS用于FD伴有失眠患者,是比较安全有效的方法,但rTMS是否可以代替其常规治疗,还有待于以后进一步研究。

