单左室起搏实现心脏再同步化治疗对左房结构及功能的影响
李皓晗 赵青 郭洁 蔡尚郎
传统心脏再同步化治疗(CRT)起搏模式为双室起搏(BVP),一般设置固定的房室延迟(AVD),舍弃了房室结生理延迟功能,加重二尖瓣及三尖瓣返流从而影响左室血流动力学。随后有研究提出长期右室起搏会导致新的室间及室内失同步,使CRT效果及应答率降低[1]。因此,新的起搏模式——单左室起搏(LUVP)应运而生。
CRT通过改善左室的收缩功能及同步性而改善整体心功能得到认可[1-2],但具有储存、管道及辅泵功能的左房没有得到有效评价。有临床研究证实CRT可改善左房重构及减少房性心律失常[3-4],其中心房颤动发生风险降低50%,但报道的CRT起搏模式大多为BVP,尚无大规模临床研究提出LUVP对左房结构、功能的影响。笔者通过分析LUVP及BVP两种起搏方式术后心脏超声及心功能,初步探讨LUVP对左房结构及功能的影响。
1 资料与方法
1.1研究对象 选取2017年1月至2018年12月于青岛大学附属医院接受CRT治疗的患者30例,其中男19例,女11例。心功能NYHA分级Ⅲ级18例,Ⅳ级12例。缺血性心肌病7例,均行冠状动脉(简称冠脉)造影,其中1例行冠脉支架植入术;扩张型心肌病23例。将研究对象随机分成两组,其中LUVP组15例,BVP组15例,术前随机选择起搏器型号。本研究通过医院伦理委员会审核批准。患者及家属签署手术知情同意书,并自愿参与本研究。
1.2入选及排除标准 入选标准:①窦性心律;②左室射血分数(LVEF)≤0.35;③QRS波时限≥130 ms;④左束支传导阻滞;⑤经正规药物治疗至少1年,NYHA分级仍为Ⅱ级及以上;⑥排除恶性肿瘤等预后差疾病,预期生存期超过1年。排除标准:①心房颤动;②房室传导阻滞;③右束支传导阻滞;④肥厚型梗阻性心肌病;⑤未行外科治疗的心脏瓣膜病;⑥预期生存期<1年。
1.3起搏器及导线植入 患者取平卧位,消毒双侧锁骨上下区。穿刺左锁骨下静脉,将3根指引导丝送至下腔静脉。作横切口并制作起搏器囊袋后填塞纱布压迫止血。沿导丝置入冠状窦长鞘及电极至冠状窦,完成冠状窦造影寻找合适的靶静脉。置入PTCA导丝至靶静脉远端。沿导丝送左室电极至理想位置,将左室电极固定在靶静脉内。术中测起搏阈值、阻抗、感知,要求起搏阈值≤3.0 V,阻抗400~1 000 Ω,感知>5 mV。顺剩余2根导丝置入血管鞘。沿鞘管分别送心房电极、心室电极至右心耳及右室心尖部,固定电极至肌小梁。测试心房阈值<1.5 V,感知>2 mV,心室阈值<1.0 V,感知>5 mV,阻抗400~1 000 Ω。将电极连接到脉冲发射器,一并置于囊袋内,缝合包扎。本研究应用的起搏器型号为Boston Scientific G148、Boston Scientific W173、Medtronic VIVATMXT、Medtronic C2TR01。
1.4术中起搏程控优化 根据术前分组通过程控起搏模式为LUVP和BVP。应用Boston Scientific G148、Boston Scientific W173型号的起搏器术后可直接选择起搏模式为BVP,也可以通过Smart delay算法一键程控,同时满足心房-右室间期<270 ms、左右心室起搏间期(VVD)>20 ms可程控为LUVP模式。Medtronic VIVATMXT型号的起搏器术后可直接选择起搏模式为BVP,也可通过AdaptivCRT算法一键程控,满足心律规整、自身心率<100次/分时为LUVP,每分钟起搏器自动监测心率及自身心房-右室间期变化,自动切换LUVP和BVP模式,通过药物及生活方式干预,术后随访可达到较高的LUVP比例。Medtronic C2TR01无一键优化功能,根据分组程控起搏模式为BVP:首先根据心房起搏与感知情况,设置基础的心房感知-BVP间期(SAV)或心房起搏-BVP间期(PAV),以10 ms为步长逐渐延长SAV/PAV,每次程控5 min后行心脏超声,当E、A峰分离,左室充盈时间占心动周期比例(LVFT/RR)最大时,则此时SAV/PAV优化为最佳AVD;设定初始左右心室起搏间期(VVD)为0 ms(即左右心室同时起搏),以10 ms为步长,使左室提前起搏,完善心电图及心脏超声,当QRS波最窄、心室间机械延迟时间(IVMD)最小时优化为最佳VVD。程控起搏模式LUVP:逐渐滴定延长AVD,直到腔内心电图提示心房感知-心室感知(AS-VS)状态,以AS-VS间期-感知补偿(ASC)为基础,以10 ms为步长缩短AVD,相当于左室早于右室起搏,每次程控5 min后完善心脏超声,当E、A峰分离,IVMD、LVEF、LVFT/RR最大, QRS波时限最短时对应的AVD为优化的AVD。根据术前24 h动态心电图,可得到下限跟踪频率(LLR)和上限跟踪频率(UTR)对应的PR间期。根据频率适应性房室延迟(RAAVD)相关公式:起始频率的SAV=优化的AVD+(起始频率的PR间期-优化时的PR间期),终止频率的SAV=优化的AVD-(优化时的PR间期-终止频率的PR间期)。将计算出的个体化AVD程控入起搏器,并打开RAAVD功能,使左侧的房室延迟跟随右侧生理性房室延迟[5]。
1.5心电图及心功能评价 所有研究对象均在术前及术后1、3、6个月完善十二导联心电图检查,记录QRS波时限。由2名心血管内科医师评估研究对象NYHA心功能分级。由2名心脏超声科医师采用PHILIPS EPIQ 7C彩色多普勒超声诊断仪进行超声心动图检查,采用S5-1探头应用心尖四腔心和心尖两腔心面积-长度法测定左房容积指数(LAVI)、左房射血分数(LAEF)、二尖瓣返流面积(MRA);基于改良的Simpson法获取四心腔切面测试LVEF;于左室及右室流出道监测血流,标测出IVMD、室间隔与左室后壁收缩期轴向应变达峰时间差(SPWMD);于胸骨旁左室长轴切面测量出左室舒张末期内径(LVEED)。

2 结果
2.1两组一般临床资料的比较 两组年龄、性别、病因、左室导线位置、起搏器型号选择一般临床资料无差异(P>0.05),具体数据见表1。
2.2两组术前及术后1、3、6个月检测指标比较 两组术后心功能改善,NYHA心功能分级降低,LVEF增加,QRS波时限(图1)、IVMD、SPWMD、MRA(图2)减小,术后1、3、6个月差异有统计学意义(P<0.05);LAVI、LVEED仅术后6个月较术前减小有差异(P<0.05);LAEF术后3、6个月较术前增加有差异(P<0.05)。见表2。
术后LUVP组QRS波时限较BVP组缩短,术后1、3、6个月有差异(P<0.05),见图1;LUVP组MRA相对减小,术后3、6个月有差异(P<0.05)。见表2,图2。

表1 两组一般临床资料的比较
注:前/后:前侧静脉/后侧静脉,起搏器型号按顺序分:Boston Scientific G148、Boston Scientific W173、Medtronic VIVATMXT、Medtronic C2TR01。括号内为百分数

两组术前QRS波宽大畸形,术后6个月QRS波时限较术前明显缩短,且LUVP组较BVP组缩短更明显
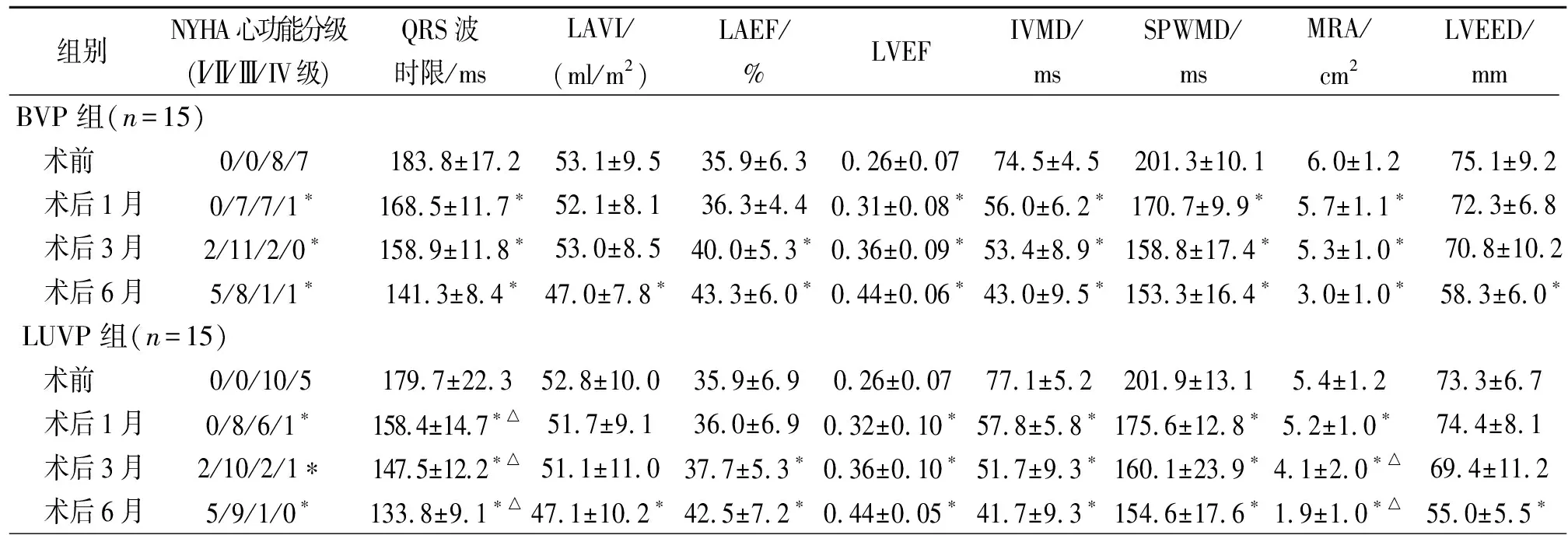
表2 两组术前、术后1、3、6个月检测指标比较
注:LAVI:左房容积指数;LAEF:左房射血分数;LVEF:左室射血分数;IVMD:心室间机械延迟时间;SPWMD:室间隔与左室后壁收缩期轴向应变达峰时间差;MRA:二尖瓣返流面积;LVEED:左室舒张末期内径。与术前相比,*P<0.05;与BVP组相应时间比较,△P<0.05
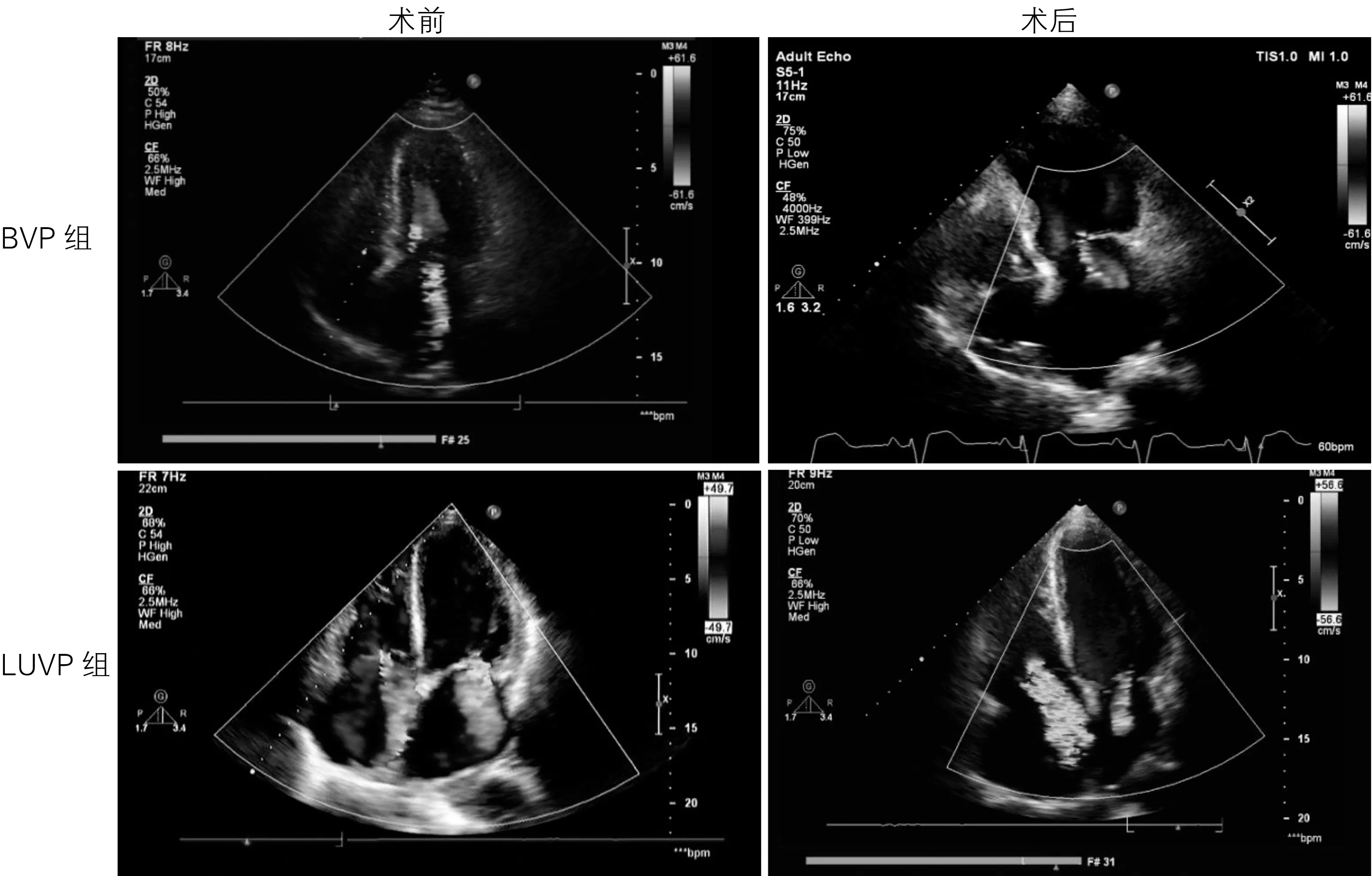
两组术后返流均减轻,LUVP组减轻更多
3 讨论
CRT通过如下机制改善心功能[6]:①优化AV间期,延长心室舒张期,增加心脏前负荷以提高心功能;②优化 VV间期,获得最大的左室每搏输出量;③改善房室不同步,减少二尖瓣返流;④改善心室内不同步,减少左室内分流,逆转左室重构。虽然大部分人群获益,但CRT高达30%无应答率及高昂的手术费用限制了CRT的广泛应用,这是心血管内科临床工作中毋须解决的问题。影响CRT应答率的因素众多[2],例如:设定短而固定的AV间期,较高的右室起搏率,不适合的左室导线位置,合并心律失常[如心房颤动(简称房颤)],心力衰竭(简称心衰)合并窄QRS波群,不合理药物治疗及术后并发症未得到合理的解决等。慢性心衰患者多合并左束支传导阻滞,这些患者中右室电活动大多是正常的[7],而右室心尖部或流出道起搏电激动希-浦系统传导,与生理性电活动方向相反,从而导致了新的室内及室间电活动不同步,以至心功能改善受限。有研究表明,设置LUVP模式,使左室起搏与生理性房室传导激动融合,可以改善室间同步性,在保留了房室结生理功能的同时,避免了不必要的右室起搏。因此对于右室电活动正常(不合并右束支阻滞)的患者,应用LUVP技术可能一定程度提高CRT应答率,或者至少可以作为BVP无应答的替代方案,已有ESC指南建议,LUVP实现CRT的效果不劣于标准BVP[8]。
另一方面,左房的辅助泵功能在心功能不全患者中发挥着至关重要的作用[9],无论何种类型的慢性心衰大多存在左房容积增大,排空能力减退,进一步加重慢性心衰。考虑左房可通过以下方面影响心功能:左房辅助泵功能的减退,使心衰患者丧失25%甚至40%的心室充盈量;左房受左室舒张、收缩功能影响,慢性心衰患者左室充盈压升高,致心房前负荷增加,左房代偿性压力升高,最终导致左房结构改变,与心衰形成恶性循环。同时,左房结构改变与房颤的发生互为因果[10],交感神经过度兴奋、炎症因子与氧化应激等多种致房颤的因素同时引起心房电、机械重构。左房重构是房颤维持的主要机制,扩大后的心房肌发出子波,使房颤不依赖触发灶的异常电活动维持,从而形成持续性房颤,扩大的左房经射频消融难以完全消除心房多处折返,导致窦性心律难以维持,增加了房颤治疗的难度。同时,房颤发病率从心功能Ⅰ级的5%增长到心功能Ⅳ级的50%,即心功能越差越多合并房颤。CRT作为慢性心衰有效的手段,与房颤发生及左房重构被广泛关注,已有研究提出,CRT可以提高左房顺应性及收缩功能,逆转左房结构改变[11-12]。但研究局限于BVP与左房结构的关系,暂无大规模临床研究涉及LUVP。本研究证实,两种起搏模式的CRT术后在改善心功能及逆重构心肌有明确的作用。与BVP组相比,LUVP组的QRS波时限较短,MRA较小。在改善左房功能的原因考虑有以下几点:①CRT通过改善左室结构功能,减少了二尖瓣返流,降低左室充盈压,从而降低左房前后负荷;②LUVP减少了不必要的右室起搏,改善右室内收缩不同步,不会诱发右室功能减退,减轻左房前后负荷;③心室收缩延迟致舒张期缩短,导致心室舒张早中期与心房收缩期重合,此时心室高于心房内压,导致心房前负荷增加,使心房扩大。LUVP通过优化房室延迟时间,更有利于改善慢性心衰房室不同步,使心房收缩落在心室舒张期末,心房压力高于心室,降低了左房前负荷,有利于改善左房功能及结构。综上认为LUVP术后较短的QRS波时限提示更好地改善了心室间同步性,同时优化较长的房室延迟,致左室起搏激动与右房-右室自身生理性传导激动融合,减少了不必要的右室起搏,有利于心室及左房逆重构,因此,LUVP更生理,对LUVP的应用及发展提供了有力证据支持。

