痛风性关节炎的影像学研究进展
朱聪聪,杨青
1.青岛市市立医院西院区(青岛市第九人民医院)放射科,山东青岛 266002;2.青岛大学附属医院放射科,山东青岛 266061;*通讯作者 杨青 yq9799@126.com
痛风是体内嘌呤代谢紊乱,血尿酸增多所致的一种代谢性风湿病。高尿酸血症导致尿酸盐结晶沉积于关节内及关节外组织,从而形成痛风性关节炎。痛风流行于世界各地,我国痛风的患病率约为0.34%~2.84%,呈升高趋势[1],其防治任务更加艰巨,早诊断、早治疗对痛风患者至关重要。目前痛风诊断多采用1977年美国风湿病学会(American college of rheumatology,ACR)制订的痛风分类标准,即:①关节液中有特异度尿酸盐结晶,或②用化学方法或偏振光显微镜证实痛风石中含尿酸盐结晶,或③具备以下12 项(临床、实验室、X线表现)中6 项,A.急性关节炎发作>1次;B.炎症反应在1 d 内达到高峰;C.单关节炎发作;D.可见关节发红;E.第一跖趾关节疼痛或肿胀;F.单侧第一跖趾关节受累;G.单侧跗骨关节受累;H.可疑痛风石;I.高尿酸血症;J.不对称关节内肿胀(X线证实);K.无骨侵蚀的骨皮质下囊肿(X线证实);L.关节炎发作时关节液微生物培养阴性。该标准纳入了X线平片辅助临床诊断痛风。近年来,双能CT、MRI和超声等先进的影像学检查在痛风诊断中发挥了重要作用,这在美国风湿病学会和欧 洲 抗 风 湿 联 盟 (American college of rheumatology/European league against rheumatism,ACR/EULAR)联合制订的2015 痛风分类标准中有所体现:该标准采用更多的影像学检查方法,如利用双能CT和超声识别关节或滑囊的尿酸盐沉积,以及X线平片鉴定痛风性骨损害[2]。先进的影像学检查在痛风诊断中发挥越来越重要的作用,风湿病疗效观察痛风工作组确定了痛风影像学研究的3个领域:尿酸盐沉积、关节炎症和关节结构的损害[3]。总之,实验研究和医学实践表明影像学检查不仅有助于诊断痛风,还能作为监测方法评估病情及降尿酸治疗的效果。
本文拟对X线平片、CT、MRI、超声和核医学检查在痛风临床和科研中的应用进展作一综述。
1 X线平片
X线平片具有方便、快捷及较高的诊断特异度等优势,曾是诊断痛风性关节炎的首选影像学检查方法。X线平片显示痛风异常好发于手、足小关节,尤其是第一趾跖关节,其次可累及踝、膝、腕、肘等关节,多表现为非对称性的关节病变。痛风早期的X线表现可以仅有关节周围软组织肿胀,而无骨质异常,但随着疾病进展,尿酸盐沉积积累引起关节周围软组织密度增高。在慢性痛风石性关节炎期,典型的X线表现为:边界清楚的偏心性骨质破坏,呈穿凿状或囊状,可见硬化边,骨质破坏边缘可见悬挂的骨质,呈外翘状突向痛风石,严重者可见多个骨质破坏区相互融合(图1)。这种表现可能是由于沉积在关节内及关节旁的尿酸盐结晶激活了炎症细胞,进而导致邻近骨组织的退变及破坏,双能CT 显示骨质缺损区有尿酸盐结晶沉积证实了这一点[4]。痛风X线平片的另一个典型表现为早期关节间隙不变窄,晚期反复发作后才会变窄。
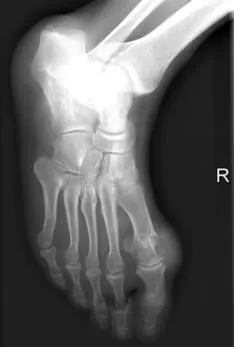
图1 男,50岁,痛风性关节炎。X线平片示右足第一跖趾关节穿凿状骨质破坏,边缘呈外翘状,邻近软组织肿胀,呈团块状高密度影
ACR/EULAR 联合制订的2015 痛风分类标准指出,手、足X线平片中“伴硬化边和悬挂边缘的骨质破坏”这种表现可以有力地支持临床诊断痛风石[2]。然而,X线平片对无痛风石的早期病变难以做出正确诊断,这需要新的能有效提高早期痛风诊断敏感度和特异度的影像学检查。
2 CT
CT 诊断痛风石具有高度特异度,能检测痛风石的数量、体积等,且具有很好的可重复性。痛风石可以沉积在骨内、关节周围、肌腱及软组织等处。在踝跗关节,痛风石最常累及的关节为楔骨间关节,韧带为距腓前韧带,肌腱为跟腱,这可能与相应部位的解剖特点及生物力学改变有关[5]。痛风石表现为结节状或团块状高密度影,高于周围软组织密度。Dalbeth 等[6]通过对存在骨质破坏的关节内痛风石和沉积于皮下但无邻近骨质破坏的痛风石进行CT值测量,发现沉积于关节内的痛风石CT值为191.1 Hu,沉积于皮下的痛风石CT值为189.9 Hu,两者差异无统计学意义;该研究发现,在有骨质破坏的区域,82%可见明显的痛风石,而在较大的骨质破坏区域均可发现痛风石。胡亚彬等[7]通过分析沉积于踝关节及膝关节韧带和肌腱处的痛风石,发现沉积于该区域的痛风石多呈条块状,且邻近骨质呈弧形或波浪状破坏,周围软组织多肿胀;因此,痛风石可能是导致骨质破坏的一个重要因素(图2),为及早降尿酸治疗提供了有力的支持,从而防止骨关节进一步损害。
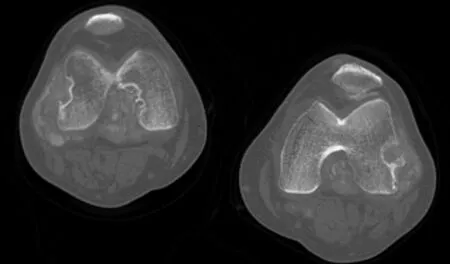
图2 男,58岁,痛风性关节炎。CT 横轴位示双膝关节周围软组织肿胀,内见多发团片状高密度影,邻近骨质呈不规则囊状破坏,可见硬化边
双能CT是痛风影像学研究领域的新技术,它通过80 kV和140 kV 两个不同能级水平的X线球管进行同步扫描,根据尿酸盐结晶表现出的两种不同能量衰减,可得到两种能级下尿酸盐晶体CT值的变化,通过工作站后处理软件进行数据分析及颜色编码,最后可以较好地识别尿酸盐沉积(图3)。双能CT 对痛风石的识别效果取决于其尿酸盐的含量,有研究认为双能CT 对特定密度的痛风石(约15%~20%尿酸盐含量)显示效果最佳,而相对低密度的痛风石在颜色编码图像上不能显示[8]。然而,该研究样本量较少,其可靠性尚需进一步探索。
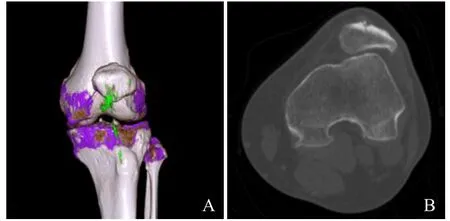
图3 男,37岁,痛风性关节炎。双能CT VR图像示左膝髌韧带走行区、左侧胫骨平台内侧面见尿酸盐沉积(绿色,A);CT横轴位示左侧髌骨前下部局限性骨质缺损,周围见结节状高密度影(B)
双能CT 有助于无创性诊断痛风。Baer 等[9]通过对10例有痛风石和11例无痛风石的痛风患者行双能CT检查,在7例无痛风石患者的多个关节区域检测到尿酸盐沉积,而所有痛风石患者均可检测到尿酸盐沉积。Zhu 等[10]研究发现,双能CT 在检测上肢和下肢尿酸盐沉积上均有较高的敏感度,Bongartz 等[11]报道在诊断痛风上双能CT的敏感度为90%,特异度为83%。Wu 等[12]报道双能CT 诊断痛风的敏感度和特异度分别高达97.9%和87.5%,阳性预测值和阴性预测值分别为95.9%和93.3%。此外,Chhana 等[13]通过对实验标本的双能CT、常规CT及MRI图像与病理解剖学进行对照研究,发现双能CT和病理解剖学评估尿酸盐沉积具有高度一致性;在评估痛风石和骨质破坏方面,常规CT、双能CT均与病理解剖学高度一致,进一步验证了双能CT 诊断痛风的可靠性。总之,双能CT 有助于临床明确诊断痛风,尤其是对于无法实施关节腔穿刺术的痛风患者;双能CT 诊断痛风有较高的敏感度和特异度,但如在足趾指甲和足垫周围等部位容易产生与尿酸盐结晶衰减特性相似的伪影,干扰检查结果,因此需要特别注意,以便做出正确诊断[14]。
双能CT可用于研究尿酸盐沉积。Dalbeth 等[15]研究发现,尿酸盐最常累及的肌腱是跟腱,其次是腓骨肌腱,而在胫骨前肌腱和伸肌腱等负重少的肌腱很少见到尿酸盐沉积,该研究认为生物力学因素可能在疾病进程中具有重要作用。Carr 等[16]纳入22例处于发作间歇期的痛风石性痛风患者和10例性别、年龄匹配的对照患者,结果发现双能CT 在实验组肋软骨处探测到广泛的尿酸盐沉积,部分男性的椎间盘也有沉积,而对照组也有类似的尿酸盐沉积情况,推测中年男性中轴骨的尿酸盐沉积可能是一种生理特征。双能CT 还可用于观察其他类型风湿病患者尿酸盐结晶的沉积情况。Petsch 等[17]报道在类风湿性关节炎和高尿酸血症患者中,约20%的患者存在尿酸盐异常沉积。
双能CT可用于阐明痛风侵蚀性病变的机制。Sapsford 等[18]研究发现痛风石中的尿酸盐和软组织成分与骨质破坏直接相关。Dalbeth 等[6]研究发现,双能CT 检测到尿酸盐结晶沉积的区域存在关节结构的损害,表明尿酸盐结晶可能通过直接影响骨表面而对骨质造成侵蚀与破坏。Towiwat 等[19]的研究未发现骨皮质完整而骨内有尿酸盐沉积,即尿酸盐沉积在关节内、骨表面和骨内均伴有邻近骨皮质破坏,表明尿酸盐晶体沉积在骨表面,并通过“由外而内”的机制造成骨质的侵蚀破坏。
上述研究显示了双能CT 在诊断痛风中的潜在价值,实际上,其已在痛风诊断与疗效监测应用中发挥着重要作用。ACR/EULAR 联合制订的2015 痛风分类标准确定总评分≥8 分即可诊断痛风,其中双能CT 发现存在尿酸盐沉积记4 分[2],与体格检查发现痛风石、高尿酸血症≥100 mg/L、超声发现双边征及X线平片发现骨关节损害具有相同的权重。风湿关节炎临床试验结果测量小组OMERACT 已将尿酸盐沉积减少作为痛风研究中的转归指标,而双能CT 在监测降尿酸治疗后痛风石的转归方面发挥重要作用。Araujo 等[20]采用双能CT 评估聚乙二醇重组尿酸酶治疗难治性痛风患者,结果显示,在治疗有效果的患者中(80%以上治疗期内血尿酸降到低于60 mg/L),94.8%的患者痛风石总量减少;在治疗无效的患者中(即血尿酸水平未降低),治疗后48%的患者痛风石总量减少;另外,该研究表明位于关节区域的痛风石治疗效果优于位于肌腱区域的痛风石。
CT 在痛风领域应用广泛,其中双能CT 有助于准确地诊断痛风,并可用于监测、评估痛风患者降尿酸治疗的效果和研究痛风的病理生理机制。
3 MRI
MRI 在诊断风湿病中具有重要作用,尽管其不能像双能CT 一样特异度地识别尿酸盐结晶,但能提供滑膜炎、骨质破坏和骨髓水肿等重要信息[21-22]。
痛风石的MRI 信号具有一定的特征。痛风石在T1WI图像上呈等或低信号,在T2WI上信号表现多样,常为混杂信号(图4),这是由于痛风石含水量及内部成分如钙质、蛋白成分等含量不同所致。对比增强扫描,痛风石多表现为边缘强化。

图4 男,59岁,痛风性关节炎。MRI 平扫矢状位T1WI(A)和PDWI-FS(B)示右跟腱外侧皮下、外踝后下方、跗骨间、跖骨周围见多发团块状长T1、混杂PD-FS 信号影,邻近骨质呈不同程度破坏
MRI可用于诊断痛风性关节炎。Poh 等[23]研究报道,痛风性关节炎的MRI 征象包括痛风石(71%)、骨质破坏(69%)、骨髓水肿(53%)、滑膜炎(29%)、腱鞘炎(16%)和肌腱变性(4%),在无合并症的痛风患者中骨髓水肿并不常见。Popovich 等[24]确立了一套痛风性关节炎软骨损伤的MRI 评分系统,指出在痛风性关节炎中,软骨往往表现为局灶性损伤,且与骨质破坏、滑膜炎、痛风石有关,而与骨髓水肿无关。Carter 等[25]利用MRI 研究痛风发作间歇期慢性滑膜炎的存在情况,并探讨其与血尿酸水平的相关性,结果发现87.5%的患者存在滑膜血管翳,其是否存在及严重程度与血尿酸水平无显著相关性。胡亚彬等[22]通过对33例痛风患者共累及54个下肢关节进行MRI、X线及CT检查,发现MRI 在诊断早期痛风所表现的滑膜增厚、软组织肿胀和骨髓水肿方面优于X线平片和CT。另外,Carter 等[26]研究表明,痛风所致骨关节损害在病程早期即已出现,MRI可能是发现早期侵蚀性改变的最佳方法。因此,MRI 在指导临床及时有效地治疗痛风、阻止病情进展方面发挥重要作用;MRI 应用于痛风领域,有助于阐释痛风的疾病进程[24]。
4 超声
超声是影像学常规检查设备,临床应用普遍,其优点是无辐射、检查时间短、价格低廉、快速诊断,可实时提供影像信息。
超声传感器向组织发射声波,由于物理特性不同,这些声波一部分反射回来,一部分传向更深部的组织。这些组织或内容物如果对超声波反射效应低,如滑液,则表现为无回声或低回声,而富含钙质的组织如骨皮质,对超声波反射效应高而表现为强回声。痛风石在超声上多表现为高或强回声(图5)。超声能探测沉积在关节、滑囊、肌腱等组织的痛风石。Ventura-Ríos 等[27]报道,超声识别肌腱处痛风石的敏感度和特异度分别为69.6%和92.0%。
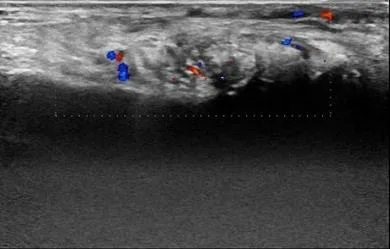
图5 男,54岁,痛风性关节炎。超声示右侧第一跖趾关节腔见多发团块状不均质高回声,内见多发点状强回声,边界不清,后方伴声影,彩色多普勒血流显像示其内血流信号增多
尿酸盐结晶体沉积于透明软骨表面,这种沉积形成一种高回声或强回声平行于强回声的软骨下骨质,即“双边征”,位于中间的透明软骨则呈无回声或低回声。Ogdie 等[28]研究认为,超声发现双边征的敏感度为83%,特异度为76%。ACR/EULAR 联合制订的2015 痛风分类标准纳入了超声的双边征作为一项评分标准[2]。
超声在评估尿酸盐或痛风石沉积所致侵蚀性病变方面具有优势。Ogdie 等[29]对824例受检者(包括416例病例组和408例对照组)进行超声检查,结果显示在痛风侵蚀性病变的检出上,超声的敏感度、特异度分别为76.9%和84.3%,阳性预测值、阴性预测值分别为83.3%和78.2%,病程≥2年和有皮下结节(可疑痛风石)的病例组敏感度更高。超声还可用于阐释痛风侵蚀所致关节功能障碍的机制。Stewart 等[30]研究认为在痛风及无症状高尿酸血症患者中,足机能减退相关的临床表现与尿酸盐的沉积有关,而与骨质破坏和软组织炎症无关。
超声检查安全、方便重复操作,适用于评估痛风的治疗效果。超声在疗效评价中可明确显示双边征消失、痛风石减小或消失等转归信息。超声还可发现亚临床状态的痛风石相关的充血性改变,这一改变经有效治疗后可以好转[31]。
5 核医学
核医学在痛风领域的研究较少,多见于个案报道。痛风可导致核素摄取值增加,但这种摄取表现是非特异性的。在PET/CT 融合显像中,痛风可表现为FDG 摄取值增加,增加的幅度在良性病变范围内。Ito 等[32]报道1例双膝关节疼痛伴发热的痛风患者,其膝关节、跖趾关节及肘关节旁的软组织肿块可见FDG 高摄取,推测FDG 高摄取与巨噬细胞的活动有关,巨噬细胞在痛风的病理生理机制中发挥保护作用,通过吞噬尿酸盐结晶对抗急性痛风。Qiu 等[33]报道1例全身多关节肿痛的痛风患者,PET/CT图像显示沉积在四肢关节处软组织结节的最大标准化摄取值值为5.1~7.2。研究认为PET/CT可用于评估痛风患者的严重程度,指导临床决策。
与有创性诊断痛风尿酸盐晶体的“金标准”相比,通过影像学检查明确尿酸盐或痛风石的沉积,进而无创性地诊断痛风是目前影像学研究的热点之一。双能CT、MRI和超声等影像学检查为研究痛风提供了新方法。双能CT和超声能直观地观察尿酸盐结晶的沉积情况,有助于监测和评估治疗效果。MRI 在显示痛风所致软组织炎性病变方面更有优势,可能是诊断和评估滑膜炎的理想方法。总之,各种影像学检查的综合应用有助于探讨痛风的发病机制,协助痛风的诊断与治疗。

