经食道心脏超声在肝移植手术中的应用
吉晓琳, 张欢, 黄佳鹏
(1 清华大学附属北京清华长庚医院麻醉科, 清华大学临床医学院, 北京 102218; 2路易维尔大学麻醉暨围术期医学科, 美国 肯塔基州 40202)
肝移植手术因其患者术前合并症多, 术中血流动力学波动剧烈以及围术期可能发生不可预测的心血管事件, 给麻醉管理带来巨大挑战。 对于高危患者, 推荐术中使用经食道心脏超声(transesophageal echocardiography, TEE), TEE可对术中心脏结构和功能以及容量状态提供实时连续的监测[1]。 美国心脏超声协会(American Society of Echocardiography, ASE)/心血管麻醉医师学会(Society of Cardiovascular Anesthesiologists, SCA)的TEE指南提出, 对于可能会出现严重血流动力学波动的非心脏手术或当出现难以矫正且无法解释的威胁生命的循环不稳定时, TEE是有效的辅助检查手段[2]。 美国肝病研究协会建议肝移植手术使用TEE, 用于术中评估心脏各房室大小, 心室肥厚程度, 收缩舒张功能, 瓣膜功能以及左室流出道梗阻(left ventricular outflow tract obstruction, LVOTO)情况。 因此, 很多麻醉医生支持在肝移植手术中常规应用TEE[3]。 本文将从TEE用于肝移植手术的普遍性、 有效性及安全性等方面进行综述。
1 TEE用于肝移植手术的普遍性
对10年前美国肝移植中心的调查显示, 大多数麻醉医生已经在肝移植手术术中应用TEE。 Wax等[4]在2008年针对术中TEE的应用, 调查了40个肝移植中心(年肝移植手术50例), 在217名被调查的麻醉医生中, 86%会在部分或全部肝移植术中应用TEE; 而2003年发表的一篇对99个肝移植中心的调查也报道了相似结果[5]。 但麻醉医生在应用TEE的全面性上差异很大, 只有27%的麻醉医生会按照ASE/SCA指南定义做全面检查, 73%的麻醉医生仅进行了有限的检查。 完成检查的差异性间接反映了TEE培训的水平, 在被调查的麻醉医生中, 只有12%是通过心脏麻醉培训或完成心脏麻醉进修来获得TEE能力, 并取得国家专业认证; 而其他绝大多数是通过自学或继续教育项目课程[4]完成。
2014年发表的一篇对79个肝移植中心(代表全美83%的肝移植手术)的调查显示[6], 肝移植术中TEE的使用率为94.9%, 不应用TEE的最主要原因是认为TEE“没有必要”和缺乏TEE培训; 在被调查的598名麻醉医生中, 38%在全部肝移植中常规应用TEE, 57%在特殊情况或抢救时应用; 28.4%经过心脏麻醉培训; 31.6%拥有国家基础或高级TEE认证。
2 TEE用于肝移植手术的有效性
肝移植手术的各个时期——“无肝前期, 无肝期, 新肝期”, 都对麻醉管理形成了特殊的挑战。 术中应用TEE可以提高容量监测质量和指导患者复苏, 这两点对于肝移植患者术中存活至关重要。 Shillcutt等[7]报道了肝移植各时期常见的TEE发现, 包括血栓栓塞, 容量不足, 心室高动力, 轻度左心室功能减低, 左、 右双心室功能障碍, 经卵圆孔左向右/右向左分流等。 根据查阅的文献和协会指南, 所有肝移植手术应用TEE是可行的; 至少在发生紧急情况时, 比如持续低血压, 无法解释的低氧或者恶性心律失常, TEE是非常有效的手段。
2.1 无肝前期: 从麻醉诱导到夹闭门静脉
诱导后, 即可进行初次全面的TEE评估, 评价和确认心脏结构和功能的基础状态。 患者可能存在的TEE基础发现包括: (1)右心室扩张/功能障碍; (2)左心室扩张/功能障碍; (3)瓣膜返流/狭窄; (4)卵圆孔未闭; (5)肺动脉高压(右心室收缩压上升); (6)心包积液压迫/未压迫心脏; (7)胸腔积液; (8)左心室室间隔上部肥厚; (9)舒张功能障碍等[3]。 终末期肝病患者通常血流动力学呈高动力状态, 左心室射血分数增加(图1)。 另外, TEE还可用于确认中心静脉导管和肺动脉导管位置。
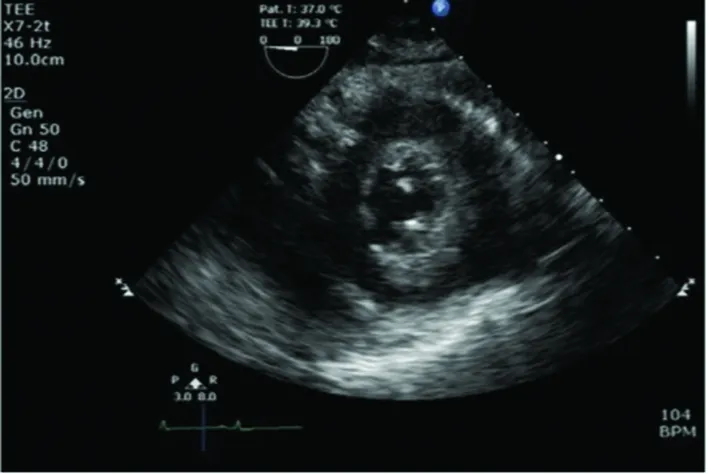
图1 经胃中部短轴切面显示左心室呈高动力状态,收缩期左心室腔几乎消失[3]
手术开始后, 由于腹水引流、 出血和下腔静脉受压, 会出现前负荷的改变(图2)。 关于左心室射血分数的测量, 熟练掌握TEE的医生能够通过观察图像主观合理估计, 较为准确; 客观的测量方法包括Simpson法, 面积改变分数和缩短分数。 心输出量和每搏量可以通过连续方程和多普勒计算出来, 但相对比较耗时。 右心室功能也可以通过面积改变分数和三尖瓣环收缩期位移评估, 但其正常值是基于经胸心脏超声的研究。 尽管这些方法各有各的缺陷, 但通过它们可以发现术中心室功能的变化趋势。 通过观察TEE图像及测量相关参数, 可以帮助医生鉴别是心室收缩功能障碍, 需要正性肌力药的支持; 还是心室充盈不足, 需要补充液体或白蛋白。 另外, 识别哪些患者具有LVOTO高危因素, 包括左心室小, 室间隔上部肥厚以及二尖瓣收缩期前向运动(systolic anterior motion, SAM), 这样麻醉医生才能做好准备以应对新肝开放初期可能出现的血流动力学急剧波动[2]。
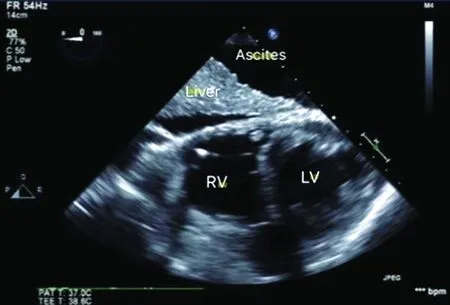
RV: 右心室; LV: 左心室; Liver: 肝脏; Ascites: 腹水.
图2 经胃中部短轴切面可见环绕肝脏的大量腹水[2]
2.2 无肝期: 从夹闭门静脉到供肝再灌注
无肝期期间, 由于门静脉和下腔静脉(inferior vena cava, IVC)的夹闭, 回心血量通常会减少。 部分夹闭IVC或者采用“背驮式”术式可以保证IVC有持续的静脉回流, 但患者收益有差异。 一个单中心的回顾性研究[7]报道了56%的患者在无肝期也有异常TEE发现, 包括低血容量, 右心室功能障碍, 双心室功能障碍, 肺栓塞和心内血栓。 TEE有助于快速鉴别以上情况并在再灌注之前给予恰当的治疗。
2.3 新肝期: 从门静脉重新开放开始
门静脉开放后, 低温、 酸中毒、 高钾和含有扩血管物质及炎症介质的血液突然进入循环, 再灌注开始即刻就会出现低血压。 所谓“再灌注综合征(postreperfusion syndrome, PRS)”, 是指再灌注后5 min内, 血压下降>30%且持续至少1 min, 心动过缓和肺血管阻力增加。 12%~77%的患者出现肺动脉压增高。 PRS的危险因素包括供体年龄、 冷缺血时间、 血钾水平、 血钙水平、 终末期肝病评分和贫血[8]。 下面分析几种新肝开放后即刻可能发生的危急事件以及TEE在这些事件中的作用。
2.3.1 心源性休克 肝移植或双器官联合移植中出现对药物治疗无反应的心源性休克, 很可能是发生了肺栓塞(pulmonary emboli, PE)或心肌梗死, 可通过TEE观察右心功能异常, 肺动脉栓塞及节段性室壁运动异常以明确原因。 另外, 这类极端情况, 体外膜肺氧合可以提供暂时的循环和呼吸支持, TEE可用于指导导丝和动静脉管路的放置。
2.3.2 急性右心衰 急性右心衰的特点是右心室扩张, 新发三尖瓣返流和房室间隔左移(图3)。 右心衰竭可能是PRS的一个表现, 但也可能是已存在的右室功能障碍的恶化, TEE可用于鉴别右心室功能障碍的原因, 如果是收缩功能障碍, 立即使用正性肌力药(泵注米力农或肾上腺素), 如果是肺血管阻力增加, 则吸入肺血管扩张剂(吸入NO或依前列醇)。
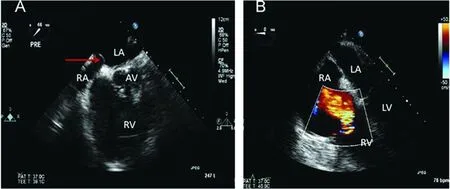
RA: 右心房; LA: 左心房; RV: 右心室; LV: 左心室; AV: 主动脉瓣.图3 食管中段四腔心切面显示房室间隔左移, 右心室扩张及重度三尖瓣返流[9]
2.3.3 血栓和栓塞 由于无肝期血液停滞在IVC, 血栓可能会形成栓子进入心脏和肺脏(图4)。 如TEE直接看到血栓, 可立即采取相应措施, 包括正性肌力药支持和给予溶栓药(组织纤溶酶原激活剂)或肝素抗凝以减小血栓和减慢血栓生长。 如进行溶栓或抗凝治疗, 是需要TEE的高度怀疑或确认血栓存在的, 因为这类治疗可能导致威胁生命的出血。 心脏超声除了是诊断心内血栓(intracardiac thrombi, ICT)的工具, 还可以帮助调整取栓导管位置和监测溶栓治疗后ICT的变化。 一个单中心的回顾性研究, 回顾了3年495名患者, 发现肝移植期间肺PE或ICT的发生率是4%[10]。 还有一些小的病例系列报道, ICT的发生率是1.2%~6.2%, 但死亡率接近50%[11]。
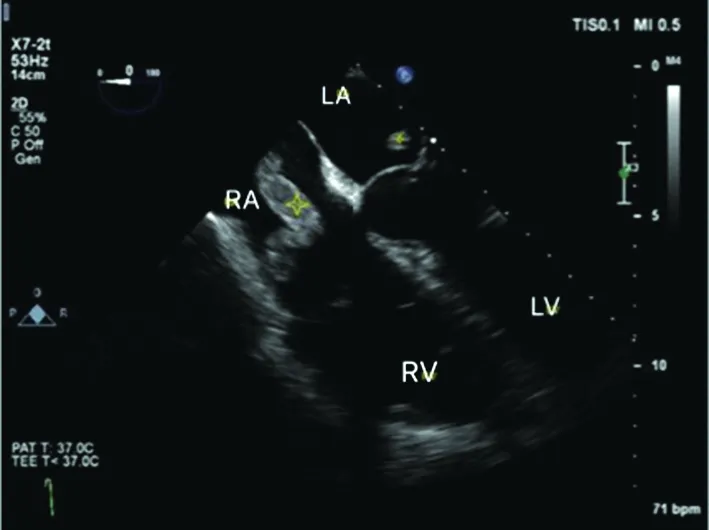
RA: 右心房; LA: 左心房; RV: 右心室; LV: 左心室.
图4 食管中段四腔心切面可见弥散于左右心腔的血栓(星标)[2]
2.3.4 经心内缺损的右向左分流 当右心压力增加时, 右向左分流可使血液或血凝块进入体循环。 空气进入左心房和左心室, 再移动到右冠状动脉, 引起冠脉缺血和痉挛导致心室下壁运动减弱[9](图5)。 心肌顿抑可导致低血压甚至心源性休克, 尤其是低温、 高钾、 酸性血液进入心脏后[12]。 血凝块或空气移动到脑循环会引起神经功能损害。 如TEE观察到空气, 应立即经中心静脉导管吸出, 调成头低脚高位和给予药物支持循环。
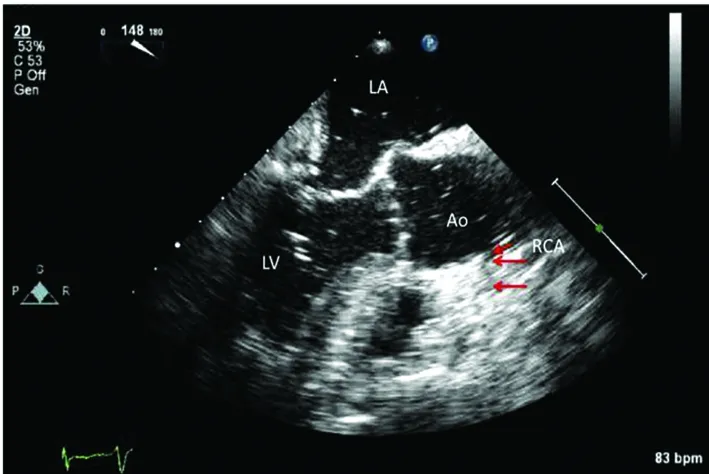
LV: 左心室; LA: 左心房; AO: 主动脉; RCA: 右冠状动脉.
图5 食管中段左心室长轴切面可见空气进入右冠状动脉[9]
2.3.5 LVOTO 低血容量, 室间隔肥厚, 已存在SAM和心动过速使患者更容易出现LVOTO和SAM。 Essandoh等[13]报道TEE发现LVOTO后, 应立即采取措施降低心肌收缩力, 容量复苏和增加后负荷来改善这种病理状态。 反之, 如果LVOTO是因为右心室衰竭导致左心室充盈不足产生的, 那么治疗的焦点就是增强右心室收缩以增加前向血流来提高左心室前负荷。
除以上情况外, 新肝期还可能出现心包填塞, 胸腔积液, 新发的严重三尖瓣返流和室性心律失常[2]。 术中TEE鉴别出这些病理改变也有助于指导术后的管理, 由于这些情况产生的双心室功能障碍, 会导致患者死亡率增加5倍[7]。
3 TEE用于肝移植手术的安全性
食道静脉曲张被认为是放置TEE的相对禁忌证, 而等待肝移植的患者73%有食道静脉曲张。 食道损伤和食道静脉曲张破裂是肝移植术中应用TEE最值得关注的安全问题[14]。 食道静脉曲张严重程度的分级见表1[15]。
表1 食道静脉曲张分级[15]

分级表现1级曲张静脉小且直, 食道内注气加压不会消失2级曲张静脉中等大小, 小于1/3的食道管腔被侵犯占据3级曲张静脉大且盘绕, 占据大于1/3的食道管腔
Markin等[16]回顾了116名患者肝移植术中应用TEE的安全性, TEE相关并发症发生率为1.7%(2/116), 而严重并发症(上消化道出血)发生率为0.82%(1/116)。 一项来自梅奥诊所的回顾性研究, 回顾了10年232名术中应用TEE的肝移植患者, 其中230名患者术前进行了食道胃镜检查, 70%的患者存在食道-胃底静脉曲张; 但只有1名患者由于术中应用TEE出现了曲张静脉出血[17]。 有研究系列观察了肝移植术中应用TEE的安全性, 共纳入了287名存在1级或者2级食道静脉曲张的患者, 只有1名患者出血, 危险发生率是0.3%[18]。 表2对以上3个研究进行了总结。
TEE的并发症可以发生在置入探头和操作探头获取图像时。 可降低患者损伤风险的方法包括润滑探头, 使用喉镜, 使用小型号探头, 限制探头在食道的前进和操作以及减少探头在患者体内的停留时间[17]。 无肝期夹闭IVC会增加肝静脉压力, 导致曲张静脉充血肿胀。 静脉曲张出血最可能的原因是曲张静脉壁张力增加, 静脉壁张力主要是由肝静脉压力梯度和血管直径决定, 术中钳夹肝静脉会恶化静脉曲张。 因此, 无肝期应尽量限制操作探头。 对于高危食道损伤风险患者(3级食道静脉曲张或上消化道出血史), 应避免经胃和经胃深切面, 因为位于胃食道连接处附近的曲张静脉往往最为表浅且最易受损伤。
表2 关于TEE用于晚期肝病患者肝移植手术安全性的研究
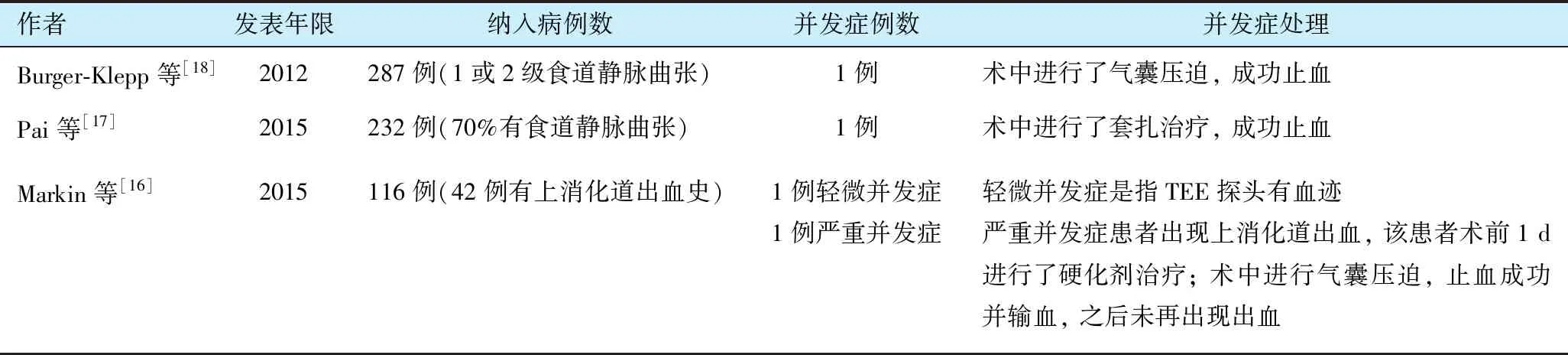
作者发表年限纳入病例数并发症例数并发症处理Burger-Klepp等[18]2012287例(1或2级食道静脉曲张)1例术中进行了气囊压迫, 成功止血 Pai等[17]2015232例(70%有食道静脉曲张)1例术中进行了套扎治疗, 成功止血 Markin等[16]2015116例(42例有上消化道出血史)1例轻微并发症1例严重并发症轻微并发症是指TEE探头有血迹严重并发症患者出现上消化道出血, 该患者术前1 d进行了硬化剂治疗; 术中进行气囊压迫, 止血成功并输血, 之后未再出现出血
术中应用TEE的其他风险包括牙齿损伤、 口咽部损伤、 吞咽痛、 食道穿孔、 食道黏膜撕裂、 菌血症、 血肿、 气管插管移位和喉麻痹。 术后应注意观察食道损伤的症状和体征, 包括持续的咽喉痛, 吞咽困难或呕血[14]。
基于以上可查阅的文献, 认为对于非3级食道静脉曲张和无急性上消化道出血史的肝移植患者, 放置TEE是安全的。 但每一个即将行肝移植的患者应用TEE的安全性都应经过肝病专科团队(包括消化内科、 肝胆外科、 麻醉科等)的讨论评估[2]。
4 结论
麻醉医生在肝移植期间会面临各种心肺病理改变带来的血流动力学挑战, 这使得术中应用TEE合理化; 肝移植术中应用TEE依然存在较大个体差异, 但在肝移植手术各个时期, 出现持续的无法解释的低血压、 肺动脉压或右心室充盈压增高, 无预期或严重的心输出量下降以及突发和持续的血流动力学参数改变, 麻醉管理都可能从TEE发现中得到指导; 1~2级食道静脉曲张且近期无急性上消化道出血的患者应用TEE是相对安全的。

