合欢皮小分子化合物对单胺氧化酶A抑制作用的分子对接研究
李好好 吴俊勇 叶艳 俞灵志

摘 要: 单胺氧化酶A是治疗抑郁症药物的重要靶点,中药合欢皮提取物具有单胺氧化酶A抑制作用,但作用机制还未探明。通过查相关文献收集合欢皮已知的5个小分子化合物,从酶蛋白数据库下载了人体单胺氧化酶A晶体结构pdb文件。采用分子对接软件autodock4.2虚拟筛选出合欢皮中与单胺氧化酶较好结合作用的化合物。对接结果有助于阐释抗抑郁作用机制,为合欢皮治疗抑郁症研究提供一定的参考。
关 键 词:单胺氧化酶A;抑郁症;合欢皮;分子对接
中图分类号:R964; Q615 文献标识码: A 文章编号: 1671-0460(2020)01-0006-04
Analysis on Molecular Docking of Monoamine Oxidase A
Inhibition by Constituents of Albiziajulibrissin
LI Hao-hao, WU Jun-yong*, YE Yan, YU Ling-zhi
(School of Pharmaceutical and Materials Engineerin, Taizhou University, Zhejiang Taizhou 318000, China)
Abstract: Monoamine oxidase A (MAO A) is considered as an important target for therapy of depression. The extract of Albizziajulibrissin cortex has the inhibitory effect of MAO A, but the mechanism of action has not been clarified. Five known small molecular compounds in Albizziajulibrissin were collected by consulting pertinent literatures about chemical research of Albizziajulibrissin. The crystal structure PDB files of MAO A were downloaded from the Protein Data Bank. Molecular docking software autodock 4.2 was used to screen out the compounds with good binding to monoamine oxidase A in the cortex of Albiziajulibrissin. The docking results are helpful to elucidate the mechanism of antidepressant action and provide some reference for the study of Albiziajulibrissin in the treatment of depression.
Key words: Monoamine oxidase A; Depression; Albizziajulibrissin; Molecular docking
抑郁症是一种常见的情感障碍性精神疾病,青年为多发病群体,且发病率逐年上升,预测2020年患有抑郁症的人将达到总人口数的10%,成为全球仅次于心脏病的第二大常见疾病[1]。抑郁症是一个多机制复杂的病症,现在单胺假说提出抑郁症的发病机理是由于中枢神经系统中5-羟色胺(5-HT)、NE释放下降,突触间隙含量减少缺乏所致[2]。在治疗抑郁症过程,抗抑郁药物的作用机制通常是采用提高突触间隙的单胺类神经递质的含量来达到抗抑郁作用的。临床显示,随着抗抑郁药物的给予,抑郁症状的改善,5-HT、NE含量增加,故而抑郁癥的发生与5-HT、NE量的改变有着紧密的关系。单胺氧化酶(monoamine oxidase, MAO) A是人体内天然存在的一种酶,它能催化单胺类物质进行氧化脱氨反应[3,4]。所以抑郁症的发生则是因为单胺氧化酶的异常分泌导致5-HT、NE降解过多,含量减少导致的。目前的一些单胺氧化酶A(MAOA)抑制剂如吗氯贝胺等西药由于起效慢,副作用大等缺点,患者耐受性较差,影响其治疗[5]。传统中药通过整体调整,具有副作用不良反应少等优势。从中草药中寻找合研制理想的抗抑郁药,正日益受到人们的重视。合欢皮为豆科植物合欢的干燥树皮,多于夏秋季节剥取,晒干而成。外表面灰棕色至灰褐色,性味甘、平。有解郁、和血、宁心、消痈肿之功,有治心神不安、忧郁、失眠之效[6-8]。近年来,一些学者对合欢皮的镇静安神和解郁等功效进行了较多的研究,但对其抗抑郁作用的机理研究未见报道。
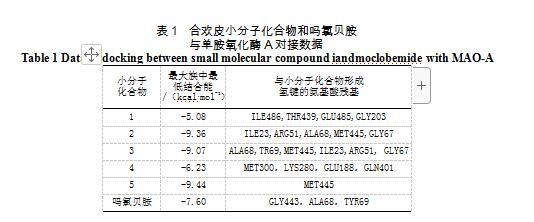
分子对接可以模拟受体生物大分子蛋白酶和配体小分子化合物之间的相互作用[9-12]。通过计算机模拟,可以预测两者之间的结合构象和结合能,从而实现对药物的模拟筛选,大大提高了药物研究的效率[13-20]。本文主要是对合欢皮中的5种已鉴定的主要成分及药物吗氯贝胺与MAO-A的分子对接进行研究,可以给出小分子与蛋白作用的氢键和结合自由能作为依据用来评价对接结果,能量越低说明小分子与蛋白结合越牢靠,确认合欢皮中抗抑郁作用的主要成分。
1 实验方法
1.1 受体和配体文件准备
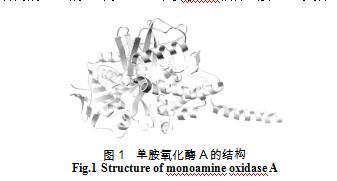
受体人体单胺氧化酶A的晶体结构数据从蛋白数据库(http://www.rcsb.org/pdb)下载,人体单胺氧化酶A的晶体结构的PDB的ID为2Z5X。用PyMOL软件去掉PDB文件中所有的结晶水和配体骆驼蓬碱(图1)。
通过查相关文献[21]得知合欢皮中化学成分分离鉴定的有5个小分子化合物(图2),分别为:(1) 2 (-)-丁香树脂酚-4-O-β-D-呋喃芹糖基-(1→2)-β-D-吡喃葡萄糖苷[22]、(2)(R)-2-反式-2, 6-二甲基-6-O-β-D-吡喃鸡纳糖基-2,7-辛二烯酸、(3) (S)2-反式-2,6-二甲基-6-O-β-D-吡喃鸡纳糖基-2,7-辛二烯酸、(4)5,5 -dimethoxy-7-oxolariciressinol和(5)(-)-丁香树脂酚。为了对比,配体加上已经上市的单胺氧化酶A抑制剂类抗抑郁药吗氯贝胺,标记为分子(6)。使用ChemBio3D Ultra 2014绘制配体化合物三维结构,使用MM2力场进行能量优化,再使用量子化学软件GAUSSIAN 03[23]在B3LYP/ 6-31G水平上对分子进一步几何结构优化[24], 将优化好的分子保存为 PDB格式备用。
1.2 分子对接
采用AutoDockTools-1.5.6对删除掉所有的结晶水和配体的靶蛋白2Z5X进行加电荷和加氢处理,保存为受体PDBQT格式文件,靶蛋白采用刚性分子处理[25]。配体合欢皮小分子化合物(包含抗抑郁药吗氯贝胺)可扭转键保持设置为可自由旋转,进行半柔性对接,添加电荷,最后保存为PDBQT格式[26]。采用Autogrid4.2进行格点能的计算,根据靶蛋白2Z5X中原配体骆驼蓬碱的空间位置设置盒子中心坐标34.70,28.13,-20.10,大分子受体格点盒子大小为9.2 nm×8.9 nm×9.3 nm,每个小格子間距为0.037 5 nm[25,26]。使用AutoDock4.2采用拉马克遗传算法进行半柔性对接,对小分子配体的位置和构象进行全局搜索,且对每个配体进行100次独立的对接,能量评定设置为最大值[24],对接的结果根据均方根偏离标准0.2 nm进行归类成簇。其他参数设置为默认值,评分函数为半经验的自由能计算方法(图2)。
2 结果和讨论
2.1 吗氯贝胺(Moclobemide)和MAO-A对接
由图3和表1可见,吗氯贝胺(Moclobemide)与MAO-A对接后形成3个氢键。第一个是由吗氯贝胺上的氢与单胺氧化酶A的氨基酸残基GLY443羰基上的氧形成的氢键。第二个氢键是由吗氯贝胺上的氢与酸残基ALA68羰基上的氧形成的。第三个氢键是由吗氯贝胺上的氢与酸残基TYR69上的氧形成的。最大族中最低结合能为-7.60 kcal/mol。
2.2 化合物(1)2 (-)-丁香树脂酚-4-O-β-D-呋喃芹糖基-(1→2)-β-D-吡喃葡萄糖苷和MAO-A对接
由图4和表1可见,(-)-丁香树脂酚-4-O-β-D-呋喃芹糖基-(1→2)-β-D-吡喃葡萄糖苷与MAO-A对接共形成了4个氢键。4个氢键分别由(-)-丁香树脂酚-4-O-β-D-呋喃芹糖基-(1→2)-β-D-吡喃葡萄糖苷上的氢原子与氨基酸残基ILE486, THR439, GLU485, GLY203的羰基上的氧原子形成。最大族中最低结合能为-5.08 kcal/mol。
2.3 化合物(2)(R)-2-反式-2,6-二甲基-6-O-β-D-吡喃鸡纳糖基-2,7-辛二烯酸和MAO-A对接
由图5和表1可见化合物(2)(R)-2-反式-2, 6-二甲基-6-O-β-D-吡喃鸡纳糖基-2, 7-辛二烯酸与单胺氧化酶A的氨基酸残基ILE23, ARG51, ALA68, MET445, GLY67形成5个氢键。最大族中最低结合能为-9.36 kcal/mol。
2.4 化合物(3)(S)-2-反式-2,6-二甲基-6-O-β-D-吡喃鸡纳糖基-2,7-辛二烯酸和MAO-A对接
由图6和表1可见化合物(3)(S)-2-反式-2,6-二甲基-6-O-β-D-吡喃鸡纳糖基-2,7-辛二烯酸与单胺氧化酶A的氨基酸残基ALA68,TR69,MET445,
ILE23,ARG51和GLY67形成6个氢键。最大族中最低结合能为-9.07 kcal/mol。
2.5 化合物(4)5,5 -dimethoxy-7-Oxolariciressi-nol与单胺氧化酶A对接
由图7和表1可见化合物(4)与单胺氧化酶A的氨基酸残基MET300,LYS280,GLU188,GLN401形成4个氢键,最大族中最低结合能为-6.23 kcal/mol。
2.6 化合物(5)(-)-丁香树脂酚与单胺氧化酶A对接
由图8和表1可见(-)-丁香树脂酚与单胺氧化酶A的MET445氨基酸残基形成1个氢键,最大族中最低结合能为-9.44 kcal/mol。
3 结论
从对接结果可知,合欢皮5个小分子化合物和吗氯贝胺与人体单胺氧化酶A相互作用的结合能大小顺序是化合物5>2>3>吗氯贝胺>4>1, 结合能大于抗抑郁药吗氯贝胺的化合物有化合物(2) (R)-2-反式-2, 6-二甲基-6-O-β-D-吡喃鸡纳糖基-2 ,7-辛二烯酸、(3)(S)2-反式-2, 6-二甲基-6-O-β-D-吡喃鸡纳糖基-2 , 7-辛二烯酸和(5)(-)-丁香树脂酚。所以得出合欢皮具有很好的抗抑郁作用。化合物(5)(-)-丁香树脂酚与单胺氧化酶A相互作用的结合能最大,抑制效果可能最强。
参考文献:
[1]叶光明,姜云云,瞿发林,等.抗抑郁药的研究进展[J].中国药师,2006,9(10):954-956.
[2]赵静,龙彬;朱丽萍.柴胡疏肝散在抑郁症治疗中的研究进展[J].精神医学杂志, 2018,31(3):237-240.
[3]Andres A M, Soldevila M A, Kidd K K, et al. Positive selection in MAOA gene is human exclusive: determination of the putative amino acid change selected in the human lineage[J]. Human Genetics, 2004, 115(5):377-386.
[4]宋明贵, 何秉踊, 韩隽,等. 单胺氧化酶抑制剂的研究进展[J]. 浙江化工, 2011, 42(4):12-18.
[5]杜刚.药物氟西汀中间体3-氯-1-苯基丙醇的生物催化合成研究[J].当代化工,2014, 43(6):913-916.
[6]宋立人.现代中药学大辞典[M].北京:人民卫生出版社,2001:876-879.
[7]霍长虹,存书,作平,等.合欢皮水煎剂催眠作用的药理试验研究[J].河北医科大学学报,2002,23(4):216-217.
[8]刘宝恒,陈燕.合欢皮安神功效之我见[J]. 吉林中医药,1999,19(4): 51-51.
[9]陈亮,王鑫,冯心池,等.分子对接技术筛选石菖蒲中γ氩基丁酸转氨酶抑制成分[J].沈阳药科大学学报,2015,32 (3):204-207.
[10]冀树伸,黄新安,罗荣华,等.分子对接技术筛选抗HIV-1逆转录酶活性化合物[J].广州中医药大学学报,2015,32 (4):725-727.
[11]马宏跃,周婧,段金廒,等.分子对接虚拟筛选蟾毒灵结合蛋白[J].南京中医药大学学报,2009,25(5):370-372.
[12]朱春玉,李雪娇,张力,等.基于分子对接技术筛选中草药中潜在的HlNI病毒神经氨酸酶抑制剂[J].生物信息学,2012,10(4):254-258.
[13]王婧超,徐翠翠,蔡绍曦.姜烯酚与NF-kB分子对接蛋白构象分析研究[J].内蒙古医科大学学报,2016,38(5):401-405.
[14]郑琴,刘丹,王佳,等.P-糖蛋白及多药耐药相关蛋白1抑制剂促进天麻素跨膜转运作用机制研究[J].中草药2016,47(21): 3840-3847.
[15]劉小利.计算机辅助μ阿片受体激动剂的虚拟筛选与分子设计[D].首都师范大学硕士论文,2009.
[16]金瑾.黄连解毒汤化学成分分析及其抗高脂血症作用的研究[D].吉林大学博士论文,2008.
[17]吴琼.芳烃钌(Ⅱ)配合物的微波辅助合成及其抗肿瘤作用机制D].广东药学院硕士论文,2013.
[18]龙伟.中药复方黄连解毒汤药效物质基础的计算机虚拟筛选研究[D].中国协和医科大学硕士论文,2008.
[19] 吴静.重组人ADAM15去整合素结构域蛋白的制备及其作用机理[D].江南大学博士论文,2008.
[20]涂名扬,与动脉粥样硬化靶点相关的中药化学成分虚拟筛选[D].广东药科大学硕士论文,2018.
[21]佟文勇,米靓,梁鸿,赵玉英,合欢皮化学成分的分离鉴定[J].北京大学学报:医学版, 2003,35(2):180-183.
[22]乔春凤,朱新科.多波长高效液相色谱法同时测定夜宁合剂中4种有效成分的含量[J].中南药学,2014,8:793-796.
[23]Frisch M J, Trucks,G W, Schlegel H B, et al. Gaussian 03.Revision C.02.Gaussian[R]. Inc. Wallingford CT, 2004.
[24]顾勇亮,董珂珂,王伟,朱小蕾. DPP-4与氰基吡咯烷类抑制剂相互作用的分子动力学模拟[J].南京工业大学学报(自然科学版), 2015, 37 (3): 120-124.
[25]王雪洁,林志健,张冰,等.菊苣小分子化合物对黄嘌呤氧化酶抑制作用的分子对接研究[J].中国中药杂志,2015,40(19):3818-3825.
[26]王梅. 天名精内酯酮对小麦全蚀病菌呼吸链的影响[D]. 西北农林科技大学博士论文, 2018.
·

