补肾调周法联合炔雌醇环丙孕酮片、盐酸二甲双胍片治疗青春期多囊卵巢综合征临床研究
张丽萍 陆丽丹
(南京中医药大学常熟附属医院妇科,江苏 常熟 215500)
多囊卵巢综合征(polycystic ovarian syndrome,PCOS)是一种临床表现多样性和发病多因性的妇科常见内分泌疾病。PCOS大多始于青春期,临床主要表现为痤疮、多毛、肥胖、雄激素过多及持续无排卵,不仅会引起月经紊乱而致育龄期女性不孕,而且对女性各生命阶段的生活质量均造成不同程度的影响[1],若不给予及时诊治,易引起代谢紊乱、2型糖尿病、生殖功能障碍、心血管疾病等远期并发症[2]。因此,早期PCOS的诊断和治疗对改善育龄期女性生殖功能,减少成年后并发症发生风险具有重要的临床意义。西医治疗PCOS主要依赖促排卵药物和抑制高雄激素药物,同时辅助胰岛素增敏剂以纠正患者代谢功能紊乱[3]。但长期应用上述药物易引起消化道反应、肝肾损伤、卵巢过度刺激等多种不良反应。近年来,中医药治疗PCOS取得了较大进展,补肾调周法是夏桂成教授根据经间期、经前期、经期、经后期各阶段生理变化特征及阴阳变化规律所提出的调理月经周期的治疗方法。既往研究显示,调周法对卵巢储备功能下降性不孕、排卵障碍性不孕等妇科疑难病症具有显著的疗效[4-5]。2019-01—2020-03,我们在炔雌醇环丙孕酮片、盐酸二甲双胍片基础上采用补肾调周法治疗治疗青春期PCOS 60例,并与炔雌醇环丙孕酮片、盐酸二甲双胍片治疗60例对照,观察临床疗效及对临床症状、卵巢体积和性激素水平的影响,结果如下。
1 资料与方法
1.1 一般资料 全部120例我院妇科门诊青春期PCOS患者,按照随机数字表法分为2组。治疗组60例,年龄14~19岁,平均(17.32±0.85)岁;病程2~5年,平均(2.9±0.5)年;临床表现:月经稀发55例,闭经2例,肥胖3例。对照组60例,年龄13~19岁,平均(17.28±0.83)岁;病程2~4.8年,平均(2.6±0.4)年;临床表现:月经稀发57例,闭经1例,肥胖2例。2组一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 病例选择
1.2.1 西医诊断标准 参照《多囊卵巢综合征中国诊疗指南》[6]。①月经稀发,闭经,或出现不规则的子宫出血;②高雄激素血症或具备高雄激素表现;③超声检查显示卵巢多囊;④排除其他能够引起排卵异常和高雄激素的疾病。
1.2.2 中医辨证标准 参照《中药新药临床研究指导原则(试行)》[7]中肾虚证标准。主症:月经稀发,经后期,闭经,腰膝痠软;次症:头晕,耳鸣,失眠。舌脉:舌质红,苔少,脉细数,或舌质淡,舌苔白,脉弱。
1.2.3 纳入标准 符合上述西医诊断标准及中医辨证标准;年龄10~19周岁;病程≥2年;未婚未育;基础体温(BBT)均为单相;入院近3个月未予雌孕激素类药物治疗;本人或家属均签署知情同意书。
1.2.4 排除标准 合并能够引起高雄激素血症的疾病(如库欣综合征、肾上腺皮质增生、卵巢肿瘤等)者;合并甲状腺功能异常、糖尿病、高催乳素血症等内分泌疾病者;合并心血管疾病、脑血管疾病、肝肾功能异常及造血系统疾病者;过敏体质或对本研究用药成分过敏者;不能按照临床规定用药,或临床资料不全而影响疗效判定者。
1.3 治疗方法
1.3.1 对照组 予炔雌醇环丙孕酮片(拜尔医药保健有限公司广州分公司,国药准字J20100003)2 mg,自月经周期第5 d或撤药性出血第5 d开始服药,连续口服21 d,停止服用7 d后重复用药;盐酸二甲双胍片(中美上海施贵宝制药有限公司,国药准字H20023370)0.5 g,每日3次口服,经期不停药。
1.3.2 治疗组 在对照组治疗基础上联合补肾调周法治疗。①行经方(月经周期第1~4 d)药物组成:益母草、泽兰、续断、五灵脂、赤芍、丹参各10 g,艾叶5 g,共服4 d;②经后方(月经周期第5~13 d)药物组成:熟地黄、山茱萸、山药、白芍、炒当归、桑寄生、牛膝、炒牡丹皮各10 g,共服9 d;③经间方(月经周期第14~15 d)药物组成:莬丝子、续断、熟地黄、山药、炒当归、鹿角霜、炒五灵脂各10 g,红花、山茱萸各5 g,共服2 d;④经前方(月经周期第16~28 d)药物组成:莬丝子15 g,熟地黄、当归、山药、续断、枸杞子、紫石英各10 g,共服13 d。日1剂,水煎2次取汁300 mL,分早、晚2次饭后30 min服用。
1.3.3 疗程 2组均治疗3个月经周期。
1.4 观察指标及方法
1.4.1 临床症状评分 2组治疗前后均参照《中药新药临床研究指导原则(试行)》[7]对月经异常、痤疮、多毛进行量化评分,其中月经异常分值0~8分,痤疮分值0~5分,多毛分值0~10分。所有症状分值越高,代表症状越严重。
1.4.2 超声检查 2组治疗前后均采用DC-8PRO彩色多普勒超声诊断系统(迈瑞医疗国际股份有限公司)行腹部彩色超声检测,测量并计算卵巢体积,计算公式为:卵巢体积=0.523×长径(cm)×前后径(cm)×横径(cm)。
1.4.3 性激素检测 2组治疗前后分别于月经周期第3~5 d晨起空腹取肘静脉血,采用化学发光法检测血清卵泡刺激素(FSH)、睾酮(T)、黄体生成激素(LH)水平及LH/FSH比值。
1.4.4 不良反应情况 统计2组治疗期间不良反应发生情况。
1.5 疗效标准 参照《中药新药临床研究指导原则(试行)》[7]。痊愈:治疗后,月经恢复正常,症状改善明显,性激素基本恢复正常,彩超检测卵巢形态和大小基本正常,BBT双相,疗效指数>95%;有效:治疗后,月经得到明显改善,症状得到一定好转,性激素水平、彩超检测结果均得到一定改善,BBT双相,疗效指数30%~95%;无效:治疗后,月经未得到任何改善,无排卵现象,临床症状、性激素水平、彩超检测结果均未得到任何改善,BBT单相,疗效指数<30%。疗效指数=(治疗前总分-治疗后总分)/治疗前总分×100%。
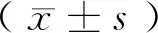
2 结 果
2.1 2组治疗前后卵巢体积比较 见表1。
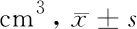
表1 2组治疗前后卵巢体积比较
由表1可见,治疗后2组卵巢体积均较本组治疗前降低(P<0.05),且治疗后治疗组低于对照组(P<0.05)。
2.2 2组治疗前后临床症状评分比较 见表2。

表2 2组治疗前后临床症状评分比较 分,
由表2可见,治疗后2组各临床症状评分及总分均较本组治疗前降低(P<0.05),且治疗后治疗组均低于对照组(P<0.05)。
2.3 2组治疗前后血清FSH、T、LH、LH/FSH水平比较 见表3。

表3 2组治疗前后血清FSH、T、LH、LH/FSH水平比较
由表3可见,治疗后2组T、LH、LH/FSH均较本组治疗前降低(P<0.05),且治疗后治疗组均低于对照组(P<0.05)。2组治疗前后FSH比较差异无统计学意义(P>0.05)。
2.4 2组疗效比较 见表4。

表4 2组疗效比较 例
由表4可见,2组总有效率比较差异有统计学意义(P<0.05),治疗组疗效优于对照组。
2.5 2组不良反应发生情况 治疗组60例,治疗期间出现胃肠道反应1例,不良反应发生率1.7%(1/60);对照组60例,治疗期间出现轻微呕吐、恶心等胃肠道反应5例,头痛2例,经间少量出血1例,不良反应发生率13.3%(8/60)。治疗组不良反应发生率低于对照组(P<0.05)。
3 讨 论
PCOS是一种多因素参与的内分泌失调性病变,患者临床表现为月经稀发甚至闭经、多毛、肥胖、痤疮、卵巢多囊改变及不孕等。近年来临床研究显示,PCOS除对女性生殖功能造成不良影响外,还会诱发代谢功能异常、2型糖尿病、子宫内膜癌、心血管疾病及血脂异常等并发症。目前,PCOS的病因尚不明确,多认为与遗传、环境、肥胖、高雄激素分泌、炎症及青春期发育亢进等因素有关[8]。青春期是下丘脑—垂体—卵巢轴发育成熟的过渡时期,中枢性负反馈抑制状态解除,促性腺激素释放激素呈脉冲式释放,易产生大量雄激素,进而诱发月经稀发、高胰岛素血症或胰岛素抵抗、多毛、痤疮及卵巢多囊改变等[9]。PCOS会伴随患者一生,因而青春期PCOS的治疗非常关键,目前临床对青春期PCOS的治疗原则以建立月经周期和纠正内分泌代谢紊乱为主[10]。避孕药是临床治疗PCOS的常用药物,其能够降低LH水平,增加性激素结合球蛋白分泌,减少雄激素和游离T水平,将月经周期调整至规律的时间段内。炔雌醇环丙孕酮片含有的环丙孕酮降低雄激素的作用非常强,故常作为PCOS患者的首选药物。二甲双胍是治疗胰岛素抵抗的重要药物,能够抑制雄激素释放,缓解高雄激素血症,是PCOS的重要补充治疗。但单纯应用西药治疗PCOS的疗效有限,且易产生多种不良反应。
中医古籍中并无青春期PCOS之病名记载,根据患者临床表现,可归属为中医学“经量少”“月经后期”“闭经”等范畴。中医学认为,肾为先天之本,发育生殖之源,肾精是月事的重要物质基础。女性从童稚阶段开始,肾气逐渐充养。二七之年,肾气充沛,天癸成熟,任冲二脉精血充盛,血海满盈,月事正常。若肾气不足,气血和精血化生无源,影响天癸泌至,癸水匮乏,肾精发育不成熟,阴液不足,阴阳转化受阻,天癸与冲任功能失衡,卵泡排出不畅,影响月经的周期和量,诱发PCOS及其他生殖系统疾病[11]。由此可见,青春期PCOS基本病机为先天肾气不足,天癸匮乏,治疗原则应为补肾益精,养血调经。本研究采用补肾调周法进行治疗。随着胞宫气血盈亏和阴阳消长的变化,女子月事呈现经行期、经后期、经间期及经前期4个阶段,遵循月经周期对青春期PCOS患者补益肾精,可显著提高临床疗效[12]。经行期为月经来潮第1~4 d,血海满盈,子宫泻而不藏,此时应用活血调经之法,促进经血排出。经行方中,赤芍、丹参活血祛瘀,调经止痛;五灵脂活血调经;益母草活血调经,祛瘀生新;艾叶理气调经,促进排经顺畅;泽兰活血行水;续断补肾。全方共奏活血调经、益气养血之功。经后期为月经周期第5~13 d,血海空虚逐渐恢复至盛,子宫藏而不泻,呈阴长变化。经后方中白芍、炒当归敛阴养血;熟地黄、山茱萸、山药滋阴补虚;炒牡丹皮滋肾助阴,寓通于补;因天癸之水源自肾,阴长需阳气支持,故方中加入牛膝、桑寄生以补肾滋阴。全方共奏滋阴养血之功。经间期为月经周期第14~15 d,此时为阴盛阳动和重阴转阳的时期,同时也是排卵的重要时期。经间期排卵不畅多与阴重阳虚、阴阳失衡有关,需在补肾同时辅以活血通络,促进排卵。经间方中,莬丝子、续断、熟地黄、鹿角霜、山药、山茱萸温阳补肾,固肾益精,促进阳气升发;炒当归、炒五灵脂、红花活血祛瘀,调经通络,促进冲任气血运行,有助于排卵。全方共奏补肾温阳、活血通络之功。经前期为月经周期第15~28 d,此时阴盛阳生,肾阳增长,阴阳俱盛,此时应补肾助阳,固肾填精,促进卵泡发育成熟。经前方中,熟地黄、当归养血补血;莬丝子、山药、续断、枸杞子、紫石英补肾助阳。全方共奏补肾助阳、调经养血之功。现代药理研究表明,补肾调周法能有效调节下丘脑—垂体—卵巢—子宫轴,促进性腺激素分泌,纠正内分泌代谢水平失调,顺应月经周期生理演变[13];益母草具有双向调节子宫平滑肌的作用,同时还具有抑制血小板聚集、抗炎、镇痛的作用[14];丹参具有抑制血小板聚集、对抗血栓形成、改善局部微循环、镇痛、抗炎、调节机体免疫力的作用,对月经不调具有显著的治疗作用[15];当归-菟丝子配伍能够通过活血补肾发挥抗炎、调节血脂水平、改善胰岛素抵抗及促进局部微循环等作用,对PCOS具有显著的治疗作用[16]。
临床已证实,高雄激素是PCOS的核心发病机制之一,患者除血清T水平升高外,其体内高雄激素在芳香化酶的作用下转化为雌酮,刺激下丘脑—垂体分泌释放大量LH,FSH水平降低,导致LH/FSH≥2[17]。另外,PCOS患者卵巢内卵泡发育不成熟,不能形成优势卵泡,众多窦卵泡聚集于卵巢内,导致卵巢呈多囊性改变,卵巢体积显著增大。采用腹部超声检查有助于了解卵巢体积、形态等变化,联合性激素等指标检测,有助于提高PCOS诊断的准确性[18]。研究结果显示,2组治疗后血清T、LH、LH/FSH水平、卵巢体积及临床症状评分均明显降低(P<0.05),治疗组上述指标改善情况均优于对照组(P<0.05),且治疗组临床疗效优于对照组(P<0.05)。说明2种治疗方法均能调节患者性激素水平,改善卵巢功能,缓解临床症状,但补肾调周法治疗效果更为显著,与张秋仔[19]研究结果一致。另外,治疗组不良反应发生率低于对照组(P<0.05),说明补肾调周法联合西药常规治疗能够降低药物不良反应,安全性高。
综上所述,补肾调周法联合炔雌醇环丙孕酮片、盐酸二甲双胍片治疗青春期PCOS疗效显著,安全性高,值得在临床上推广。

