PD-1抑制剂对比化学药物治疗进展期黑色素瘤有效性和安全性的Meta分析
达丽隽 滕元君 宋飞雪
(兰州大学第二医院,兰州 730000)
恶性黑色素瘤是起源于胚胎期神经嵴的恶性肿瘤,起病隐匿,致死率高,预后极差[1]。该肿瘤多发生于皮肤,居皮肤恶性肿瘤第3位,约占6.8%~20%[2]。进展期恶性黑色素瘤的五年存活率不足10%。全身化疗是目前最重要的治疗手段之一,传统一线化疗药物包括达卡巴嗪(dacarbazine,DTIC)、替莫唑胺(temozolomide,TMZ)或以DTIC/TMZ为主的联合化疗。其中,DTIC是经 FDA 批准用于进展期黑色素瘤治疗的唯一化疗药物,被誉为全身化疗的“金标准”,然而,相关研究表明[3],其有效率仅仅只有5%~20%,完全缓解率小于5%,中位生存期只有5.6~11个月。因此,迫切需要更为有效的治疗方案。
近年来,免疫治疗在恶性肿瘤治疗中受到越来越多的关注,其中关于“程序性死亡受体1(programmed death protein 1,PD-1)”与其配体“细胞程序性死亡配体1(programmed death-ligand 1,PD-L1)”的研究取得了突破性进展。PD-1是一种多表达于T细胞表面的跨膜受体,是细胞表面负性免疫检测点,在抑制细胞程序性死亡过程中发挥重要作用[4]。PD-L1作为PD-1配体,主要表达于淋巴细胞、抗原提呈细胞、造血细胞、上皮细胞[5]。在正常体细胞中,PD-L1通常呈现低表达或不表达,但在恶性黑色素瘤、乳腺癌、肺癌、肾癌等肿瘤细胞中PD-L1表达水平显著升高[6]。该配体通过与PD-1结合抑制T细胞活性,导致免疫逃逸,从而促进肿瘤细胞异常增殖并转移[7]。因此,阻断PD-1与PD-L1的相互结合,提高免疫系统活性,可为肿瘤的治疗提供新的思路[8]。
Nivolumab和Pembrolizumab作为PD-1抑制剂的代表药物,于2014年先后被FDA批准用于治疗不可切除或进展期黑色素瘤[9],于2018年进入中国市场。Nivolumab是一种针对PD-1受体的完全人源免疫球蛋白G4(IgG4)单克隆抗体。研究表明,Nivolumab单药对比DTIC治疗进展期黑色素瘤,能显著提高患者总生存期(overall survival,OS)、无进展生存期(progression-free survival,PFS)及客观有效率[10,11]。Pembrolizumab是另一种针对PD-1的IgG4拮抗剂单克隆抗体,在一项Pembrolizumab对比卡铂联合紫杉醇治疗进展期黑色素瘤的随机对照试验中,Pembrolizumab展现出较高的客观有效率[12],但对于PD-1抑制剂带来的不良反应同样不容忽视。
因此,本文采用Cochrane系统评价方法,全面检索国内外相关的随机对照试验,对PD-1抑制剂与化疗在进展期黑色素瘤治疗中的临床有效性及安全性进行比较分析,旨在为临床应用提供进一步循证医学证据。
1 材料与方法
1.1纳入及排除标准
1.1.1研究类型 国内外公开发表的PD-1抑制剂对比全身化疗治疗进展期黑色素瘤的临床随机对照试验(RCT)。
1.1.2研究对象 ①年龄大于18岁;②由病理学及影像学确诊的Ⅲ期或Ⅳ期黑色素瘤患者;③ECOG评分0~2分。
1.1.3干预措施 实验组:PD-1抑制剂(Nivolumab或Pembrolizumab)治疗组;对照组:单纯化疗治疗组,方案不限(DTIC单药、TMZ单药、联合化疗等)。
1.1.4结局指标 有效性指标:①总有效率(ORR);②总生存期(OS);③无进展生存期(PFS)。安全性指标:①任何级别治疗相关性不良反应;②3~5级治疗相关性不良反应;③不良反应的亚组分析。
1.1.5排除标准 ①非随机及半随机临床试验;②非临床试验研究(回顾性研究、病例报道等);③随访资料不完整的研究。
1.2资料来源和检索策略 计算机检索PubMed、EMbase、中国期刊全文数据库(CNKI)、维普中文科技期刊数据库(VIP)、万方数字化期刊全文数据库(Wanfang Data)、中国生物医学文献数据库(CBM)中的相关文献。检索时间均为自建库时间至2018年12月。中文检索词:PD-1、纳武单抗、派姆单抗、化疗、恶性黑色素瘤等;英文检索词:PD-1、Nivolumab、Pembrolizumab、chemotherapy、Melanoma等。
1.3质量评价及资料提取 采用Cochrane Handbook 5.1提供的偏倚风险评估标准对纳入文献进行质量评价,包括:①随机分配方法;②分配方案隐藏;③盲法;④选择性报告研究结果;⑤不完整结果数据;⑥其他偏倚来源。质量评价及资料提取由两位研究者独立进行并交叉核对,如遇到分歧,与第三名研究者协商解决。
1.4统计学分析 采用RevMan 5.3软件进行数据统计分析。计数资料采用比值比(odds ratio,OR)及其95%的可信区间(confidence interval,CI)为效应分析统计量。计量资料采用风险比(hazard ratio,HR)及其95%CI为效应分析统计量。采用χ2检验对研究结果进行异质性检验,若各研究结果间无统计学异质性(P>0.10,I2<50%),则采用固定效应模型进行数据分析;若各研究结果间存在统计学异质性(P≤0.10,I2≥50%),则采用随机效应模型进行数据分析,并分析异质性来源,必要时行敏感性及描述性分析。
2 结果
2.1文献检索与筛选 共检索出中英文文献1 946篇,通过排除重复文献及阅读题目、摘要、全文,再结合纳入、排除标准,最终纳入5篇随机对照试验,均为英文文献,共2 273例进展期恶性黑色素瘤患者(图1)。
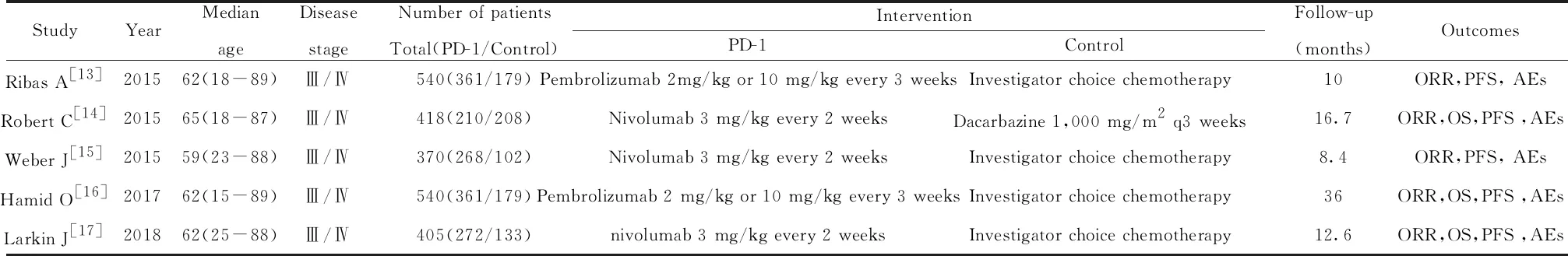
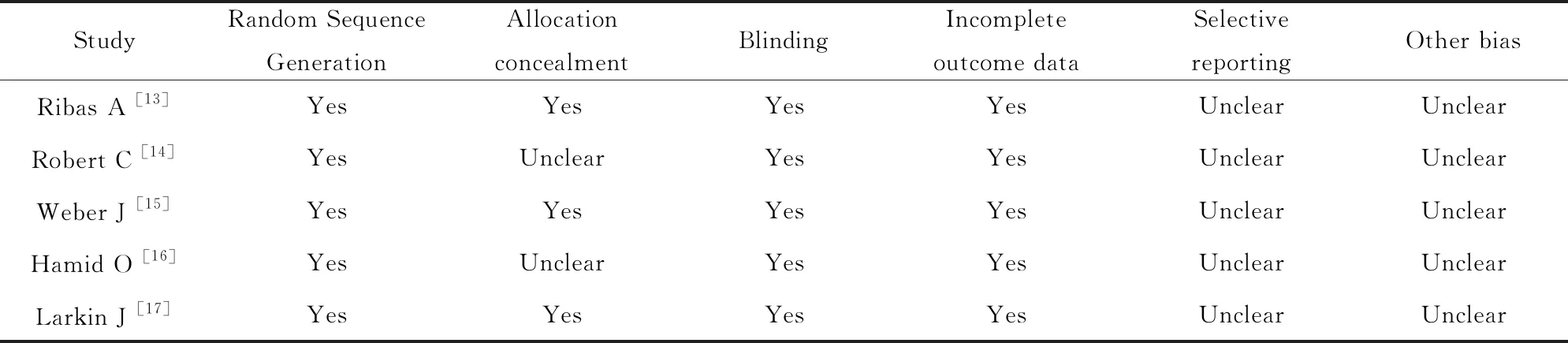
2.2纳入研究的基本特征和质量评价 纳入研究的基本特征见表1,所有纳入研究的基线均具有可比性。质量评价结果见表2。
2.3Meta分析结果
2.3.1总有效率 共纳入5个研究,包含2 070例患者(PD-1抑制剂组1 324例,化疗组746例)。研究结果间无统计学异质性(P=0.51,I2=0%),故采用固定效应模型进行Meta分析。结果显示:患者应用PD-1抑制剂组总有效率明显高于化疗组,且有统计学差异[OR=4.77,95%CI(3.55,6.42),P<0.000 01](图2)。
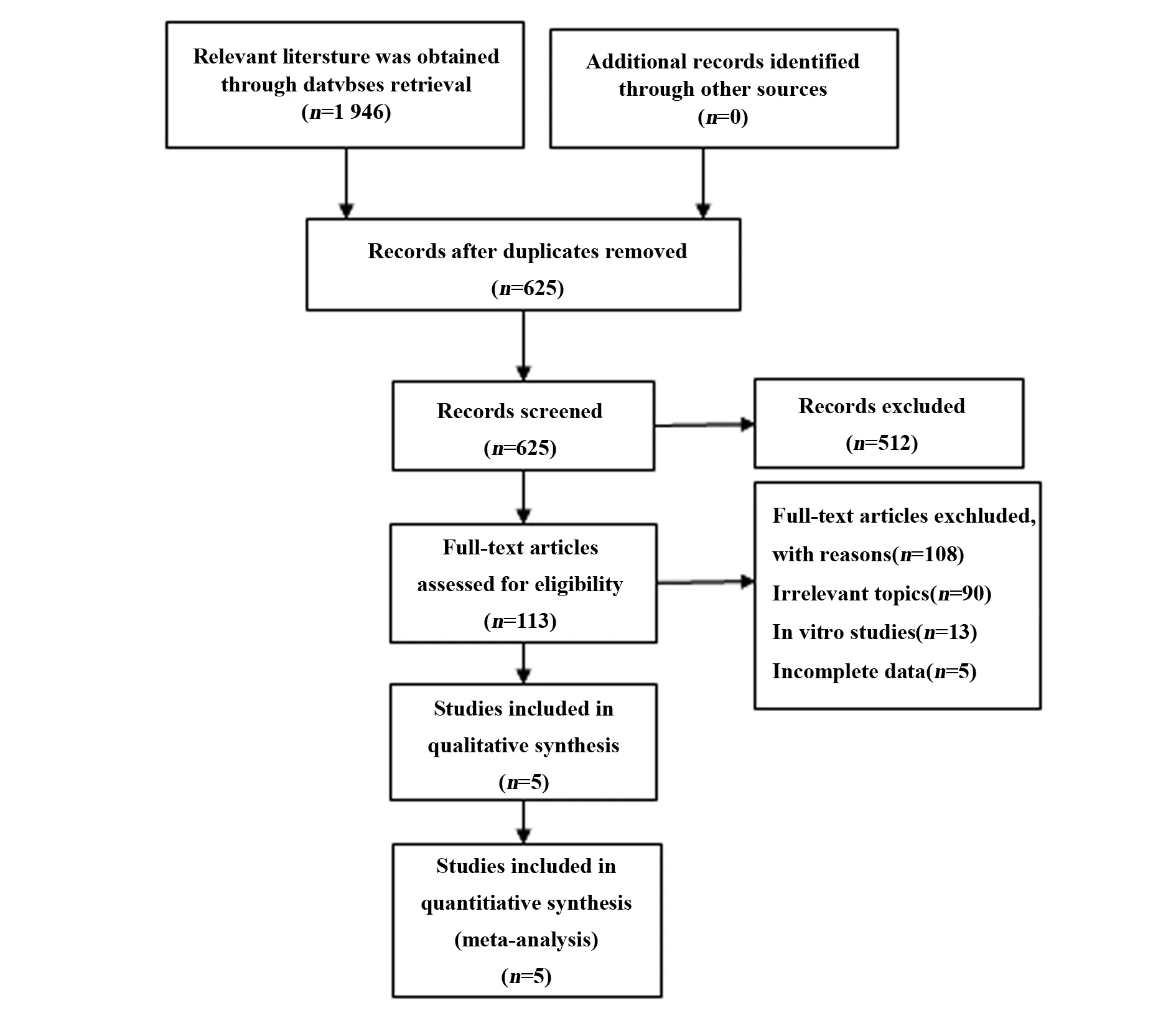
图1 文献筛选流程图Fig.1 Literature retrieval and selection process
2.3.2无进展生存期 5个研究报告了无进展生存期情况,研究结果间有统计学异质性(P<0.000 1,I2=85%),故采用随机效应模型进行Meta分析。结果显示:患者应用PD-1抑制剂组无进展生存期较化疗组明显延长,且有统计学差异[HR=0.60,95%CI(0.44,0.82),P=0.001](图3)。
2.3.3总生存期 3个研究[14,16,17]报告了总生存期情况,研究结果间有统计学异质性(P=0.03,I2=72%),故采用随机效应模型进行Meta分析。结果显示:两种治疗组患者总生存期无统计学差异[HR=0.72,95%CI(0.50,1.03),P=0.07](图4)。
2.3.4不良反应事件
2.3.4.1任何级别的不良反应事件 5个研究均报告了任何级别的不良反应事件,研究结果间无统计学异质性(P=0.47,I2= 0%),故采用固定效应模型进行Meta分析。结果显示:患者应用PD-1抑制剂组发生任何级别的不良反应事件较化疗组显著降低[OR=0.66,95%CI(0.53,0.82),P=0.000 2](图5)。
2.3.4.23、4、5级不良反应事件 5个研究均报告了3、4、5级别不良反应事件,研究结果间有统计学异质性(P=0.09,I2=50%),故采用随机效应模型进行Meta分析。结果显示:与化疗组比较,患者应用PD-1抑制剂组的3、4、5级别不良反应事件明显减少,差异有统计学意义[OR=0.38,95%CI(0.28,0.53),P<0.000 01](图5)。
2.3.4.3不良反应的亚组分析 5个研究均报告了治疗相关性常见不良反应:疲乏、腹泻、瘙痒、皮疹和恶心。疲劳、皮疹的研究结果间有统计学异质性(P=0.08,I2=52%)、(P=0.000 2,I2= 82%),故采用随机效应模型进行Meta分析,其余采用固定效应模型。亚组分析显示:患者应用PD-1抑制剂组发生瘙痒的概率显著增高[OR=6.45,95%CI(4.28,9.71),P<0.000 01];化疗组患者发生疲乏、恶心的概率显著增高[OR=0.70,95%CI(0.53,0.93),P=0.01]、[OR=0.20,95%CI(0.16,0.25),P<0.000 01];两组间发生皮疹、腹泻的概率差异无统计学意义[OR=2.18,95%CI (0.90,5.26),P=0.08]、[OR=1.05,95%CI(0.80,1.37),P=0.73](图6)。
表1 纳入研究的基本特征
Tab.1 Basic characteristics of included studies
StudyYearMedianageDiseasestageNumber of patientsTotal(PD-1/Control)InterventionPD-1ControlFollow-up(months)OutcomesRibas A[13]201562(18-89)Ⅲ/Ⅳ540(361/179)Pembrolizumab 2mg/kg or 10 mg/kg every 3 weeksInvestigator choice chemotherapy10ORR,PFS, AEsRobert C[14]201565(18-87)Ⅲ/Ⅳ418(210/208)Nivolumab 3 mg/kg every 2 weeksDacarbazine 1,000 mg/m2 q3 weeks16.7ORR,OS,PFS ,AEsWeber J[15]201559(23-88)Ⅲ/Ⅳ370(268/102)Nivolumab 3 mg/kg every 2 weeksInvestigator choice chemotherapy8.4ORR,PFS, AEsHamid O[16]201762(15-89)Ⅲ/Ⅳ540(361/179)Pembrolizumab 2 mg/kg or 10 mg/kg every 3 weeksInvestigator choice chemotherapy36ORR,OS,PFS ,AEsLarkin J[17]201862(25-88)Ⅲ/Ⅳ405(272/133)nivolumab 3 mg/kg every 2 weeksInvestigator choice chemotherapy12.6ORR,OS,PFS ,AEs
表2 纳入研究的偏倚风险评估
Tab.2 Methodological quality evaluation results of included studies
StudyRandom SequenceGenerationAllocationconcealmentBlindingIncompleteoutcome dataSelectivereportingOther biasRibas A [13]YesYesYesYesUnclearUnclearRobert C [14]YesUnclearYesYesUnclearUnclearWeber J [15]YesYesYesYesUnclearUnclearHamid O [16]YesUnclearYesYesUnclearUnclearLarkin J [17]YesYesYesYesUnclearUnclear
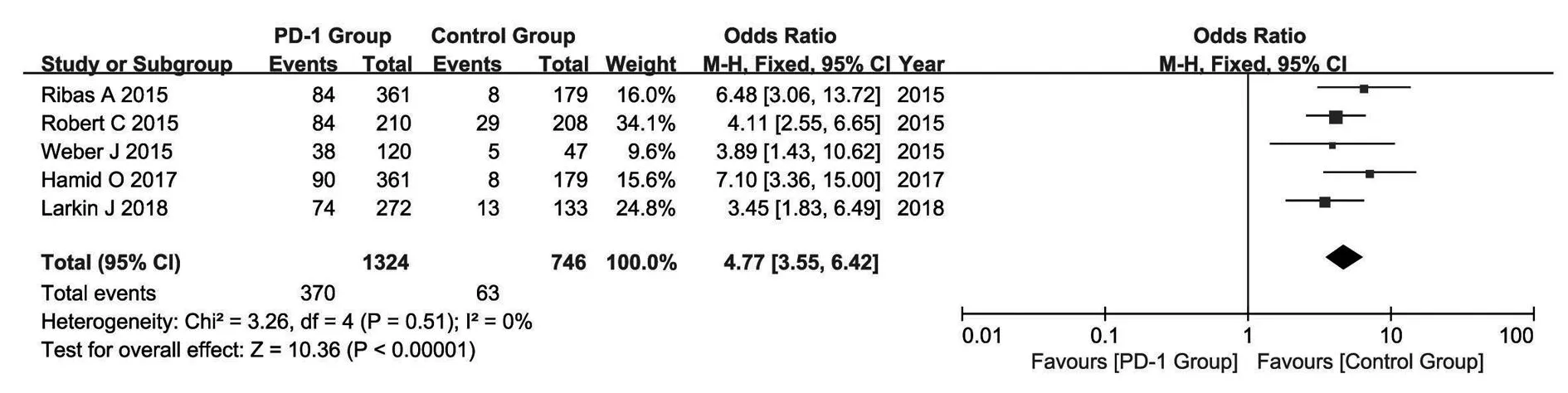
图2 PD-1组与化疗组患者总有效率的Meta分析结果Fig.2 Meta-analysis of ORR between PD-1 inhibitors group and chemotherapy group
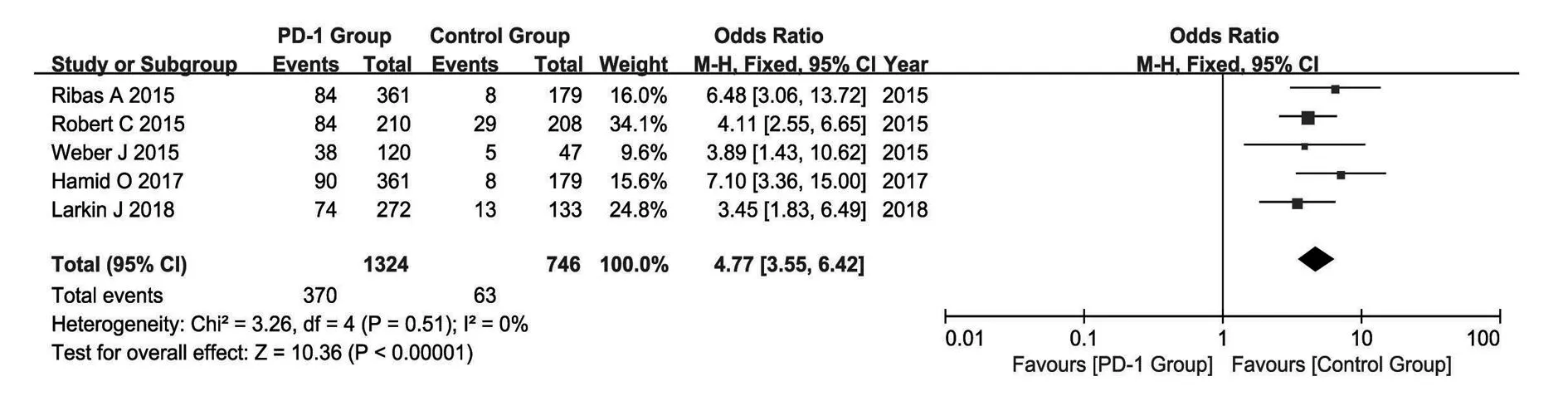
图3 PD-1组与化疗组患者无进展生存期的Meta分析结果Fig.3 Meta-analysis of PFS between PD-1 inhibitors group and chemotherapy group

图4 PD-1组与化疗组患者总生存期的Meta分析结果Fig.4 Meta-analysis of OS between PD-1 inhibitors group and chemotherapy group
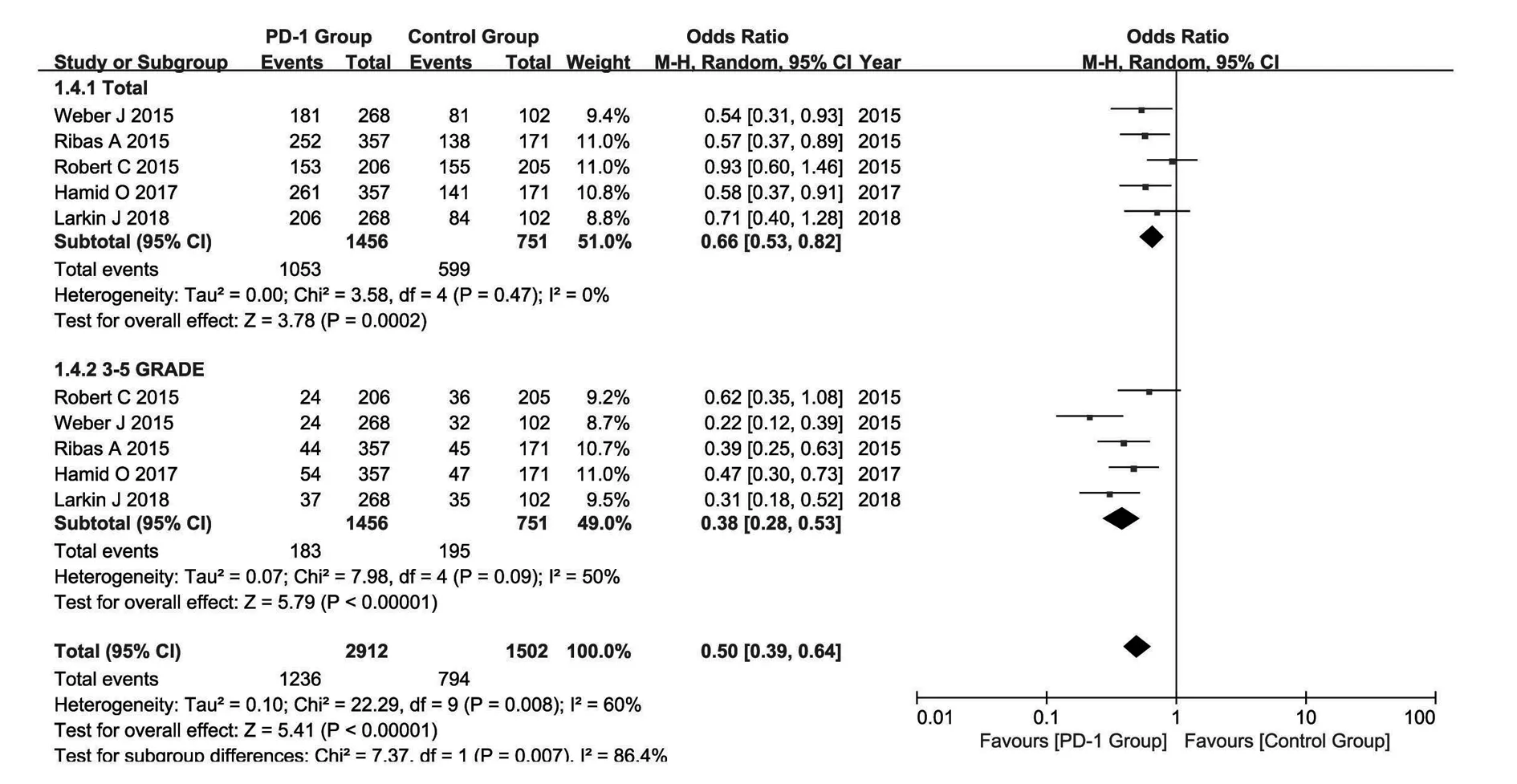
图5 PD-1组与化疗组治疗患者相关不良事件的Meta分析结果Fig.5 Meta-analysis of treatment-related adverse effect between PD-1 inhibitors group and chemother-apy group
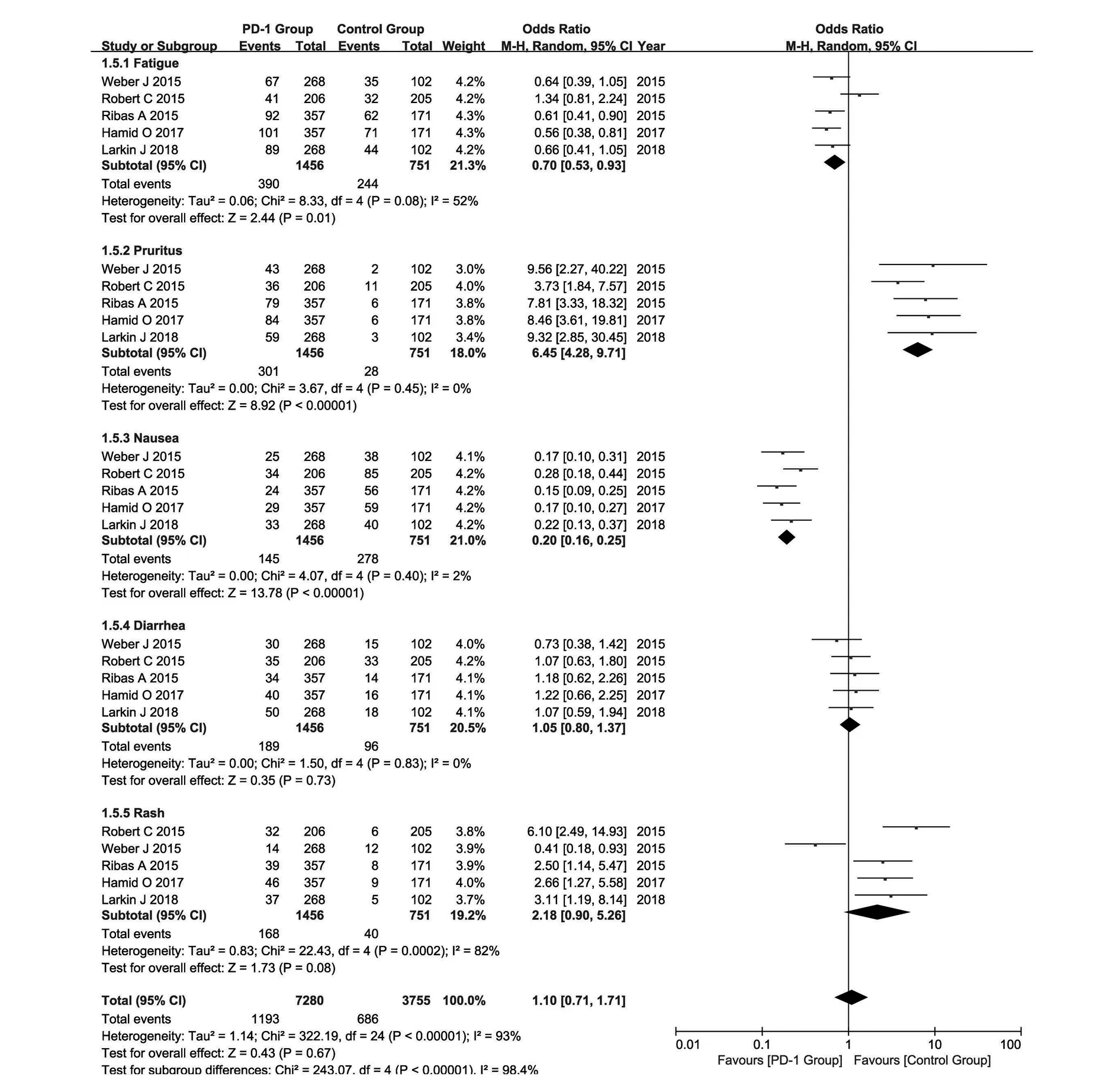
图6 PD-1组与化疗组患者不良事件的亚组分析结果Fig.6 Subgroup analysis of treatment-related adverse effect between PD-1 inhibitors group and chemotherapy group
3 讨论
近年来,恶性黑色素瘤的发病率以每年4.1%的速度显著上升,高于其他任何一种恶性肿瘤[18],全世界每年确诊为黑色素瘤的新增患者高达80 000例[19]。目前,仍未找到治疗进展期黑色素瘤最为有效的方法,各种化疗药物有效率均低于20%。恶性黑色素瘤是人类常见的免疫原性肿瘤,黑色素瘤细胞常呈现自身抗原,不能被免疫系统有效杀灭,这一免疫耐受性称为免疫逃逸。PD-1/PD-L1通过抑制T细胞增殖来调控免疫应答,参与肿瘤免疫逃逸[20]。因此,PD-1抑制剂的应用为黑色素瘤的免疫治疗带来了新的希望[21]。为了验证PD-1抑制剂在进展期黑色素瘤患者中的有效性和安全性,本文进行了相关研究的系统分析。
该Meta分析比较了PD-1抑制剂对比全身化疗在进展期黑色素瘤患者中的总有效率、总生存期及无进展生存期。结果表明PD-1抑制剂可以显著提高进展期黑色素瘤患者的总有效率、延长无进展生存期,但在总生存期方面,两者并无统计学差异。其次,我们对PD-1抑制剂对比化疗在进展期黑色素瘤患者中的不良反应进行了比较。治疗相关的常见不良反应包括:疲乏、腹泻、瘙痒、皮疹、恶心等。亚组分析显示:化疗组中恶心、疲乏的发生率显著高于PD-1抑制剂组,但PD-1抑制剂组中瘙痒的发生率显著高于化疗组;皮疹、腹泻在两组中的发生率并无明显差异。合并的任何级别的不良反应在PD-1抑制剂组和化疗组中的发生率分别为:72.0%、79.9%;3、4、5级别不良反应在两组中的发生率分别为:12.6%、30.0%,表明PD-1抑制剂在进展期黑色素瘤患者的治疗中,在安全性方面存在一定优势。
本研究仍存在一定的局限性:第一,虽纳入标准为随机对照实验,但部分纳入文献质量有待提高;第二,部分研究样本量较小,且研究结果指标不统一,使纳入Meta分析的研究较少,可能会对研究结果造成一定影响;第三,本文纳入研究之间存在一定临床异质性,化疗组方案并不统一,可能会降低文章结论的可信度;第四,因随访时间限制,未对患者生活质量以及远期转归做出有效评价。因此,仍需大样本、高质量的随机对照试验对本文证据进行进一步验证。

