血性宫颈脱落细胞标本对人乳头瘤病毒DNA检测结果的影响
王克迪,徐东江,苏建荣△
(1.首都医科大学附属北京友谊医院临床检验中心,北京 100050;2.北京积水潭医院检验科,北京 100035)
人乳头瘤病毒(HPV)属于乳头瘤病毒科的乳头瘤病毒属,为球形无包膜的双链DNA病毒,能引起人体皮肤黏膜鳞状上皮细胞增殖。99%宫颈癌病例都与生殖系统的HPV感染有关[1-2]。目前,HPV基因检测已成为筛查宫颈癌的有效手段之一。荧光定量PCR技术具有特异度和灵敏度高等优势,是目前HPV-DNA检测最常用的方法。血性宫颈脱落细胞标本中含有一定量的血红蛋白,而血红蛋白会抑制PCR反应,造成假阴性结果。但是,血性标本中血红蛋白的水平对PCR检测结果的影响尚不明确,本文拟通过比较不同血红蛋白水平的宫颈脱落细胞标本中HPV-DNA定性和定量结果,探讨血红蛋白对HPV-DNA检测结果的影响程度及有效的预处理措施。
1 资料与方法
1.1一般资料 收集2019年1月就诊于北京友谊医院妇科门诊的女性患者宫颈脱落细胞标本。其中20例未溶血,且HPV-DNA检测为阳性的标本作为HPV阳性组,20例未溶血,且HPV-DNA检测为阴性的标本作为HPV阴性组,年龄25~55岁,平均(38.5±5.2)岁。
1.2仪器与试剂 HPV-DNA提取分别采用全自动核酸提取仪(购自瑞士罗氏公司,型号Cobas x480)和之江全自动核酸提取仪(购自中国上海之江生物科技股份有限公司);HPV-DNA荧光定量检测分别采用罗氏全自动荧光定量PCR分析仪(购自瑞士罗氏公司,型号Cobas z480)和宏石全自动荧光定量PCR仪(购自中国上海宏石医疗科技有限公司,型号SLAN-96P);所用试剂分别购自瑞士罗氏产品诊断有限公司和中国上海之江生物科技股份有限公司。
1.3方法
1.3.1标本采集 所有标本均经本人知情同意,严格按照宫颈脱落细胞标本采集规范采集,采集后标本尽快送检。采集的标本置于4℃冰箱保存,24 h内检测。
1.3.2含血红蛋白的宫颈脱落细胞标本制备 收集10个重度溶血的宫颈脱落细胞标本,检测血红蛋白水平以确定所制备溶血标本的血红蛋白水平范围。根据试验需要,将血红蛋白分为5个水平梯度0.0、2.5、5.0、10.0、20.0 g/L。收集1个体检健康者EDTA-K2抗凝的O型全血标本4 mL,加入10 mL离心管,2 000 r/min离心5 min后弃去血浆,加入10 mL 0.9% NaCl缓冲液并震荡混匀。2 000 r/min离心5 min后去上清,重复洗涤2次。加入0.9% NaCl缓冲液悬浮红细胞,使红细胞悬液的血红蛋白水平达到120 g/L,-30 ℃与常温10 min分别冻融1次,制成含部分未裂解红细胞的血红蛋白悬液。取原始标本1 000 μL,分别加入500.00、468.75、437.50、375.00、250.00 μL 0.9% NaCl缓冲液,再分别加入0.00、31.25、62.50、125.00、250.00 μL血红蛋白悬液并混匀,得到血红蛋白终水平分别为0.0、2.5、5.0、10.0、20.0 g/L而HPV水平相同的模拟溶血标本。
1.3.3含血红蛋白的宫颈脱落细胞标本预处理 采用红细胞裂解液对不同水平血红蛋白的宫颈脱落细胞标本进行预处理,操作流程如下:向含血红蛋白的宫颈脱落细胞标本中加入500 μL红细胞裂解液,充分混匀,静置5 min,2 000 r/min离心5 min后去上清。向沉淀中加入10 mL 0.9% NaCl缓冲液并充分混匀,2 000 r/min离心5 min后去上清,重复洗涤2次,去除残余的血红蛋白。向沉淀中加入1 500 μL 0.9% NaCl缓冲液,充分混匀备用。
1.3.4HPV-DNA检测步骤 主要检测步骤包括HPV-DNA提取和荧光定量PCR检测,每一步均严格按照试剂说明书进行操作。
1.3.5结果判断 HPV-DNA检测结果根据PCR扩增曲线的循环阈值(Ct值)进行判断,判断标准参照HPV核酸检测试剂盒操作。Cobas z480系统检测结果为定性结果,报告格式为HPV-DNA 阳性/阴性,SLAN-96P系统软件检测结果为相对定量结果,报告格式以HPV-DNA的拷贝数(copies/104细胞)表示。
1.4统计学处理 采用SPSS20.0软件进行数据处理分析,参照《医学实验室质量和能力认可准则在分子诊断领域的应用说明》[3],定量结果用偏倚来表示,偏倚=(Ct实验组-Ct靶值)/Ct靶值×100%,至少80%样品测量结果偏倚<7.5%,即为可接受判断标准。定性结果用符合率表示,符合率>80%,即为可接受判断标准。
2 结 果
2.1不同水平血红蛋白对HPV-DNA定性检测结果的影响 HPV阳性组中,当宫颈脱落细胞标本中血红蛋白水平为2.5和5.0 g/L时,HPV-DNA阳性标本数为20个,符合率为100%,在可接受范围内;当血红蛋白水平达到10.0和20.0 g/L时,HPV-DNA阳性标本数分别为13个和0个,符合率分别为65%和0%,不在可接受范围内。HPV阴性组中,HPV-DNA在不同水平血红蛋白间均为阴性,符合率为100%,在可接受范围内。见表1。
2.2不同水平血红蛋白对HPV-DNA定量检测结果的影响 HPV阳性组中,当宫颈脱落细胞标本中血红蛋白水平为2.5和5.0 g/L时,所有标本HPV-DNA扩增Ct值的偏倚均小于7.5%,在可接受范围内。当宫颈脱落细胞标本中血红蛋白水平达到10.0和20.0 g/L时,分别有40%和95%标本HPV-DNA扩增Ct值的偏倚超过7.5%,不在可接受范围内。HPV阴性组中,HPV-DNA均无扩增曲线,定量检测结果为0,偏倚也为0,在可接受范围内。见表2。
2.3预处理后的含血红蛋白标本中HPV-DNA检测结果 向血红蛋白水平为2.5、5.0、10.0、20.0 g/L标本中加入红细胞裂解液进行预处理,再进行HPV-DNA载量检测。不同水平血红蛋白组的标本经过预处理后,HPV-DNA定性检测结果与血红蛋白水平为0.0 g/L一致,符合率100%,定量检测结果Ct值偏倚均小于7.5%,在可接受范围内。见表3、4。

表1 不同水平血红蛋白对HPV-DNA定性检测结果的影响
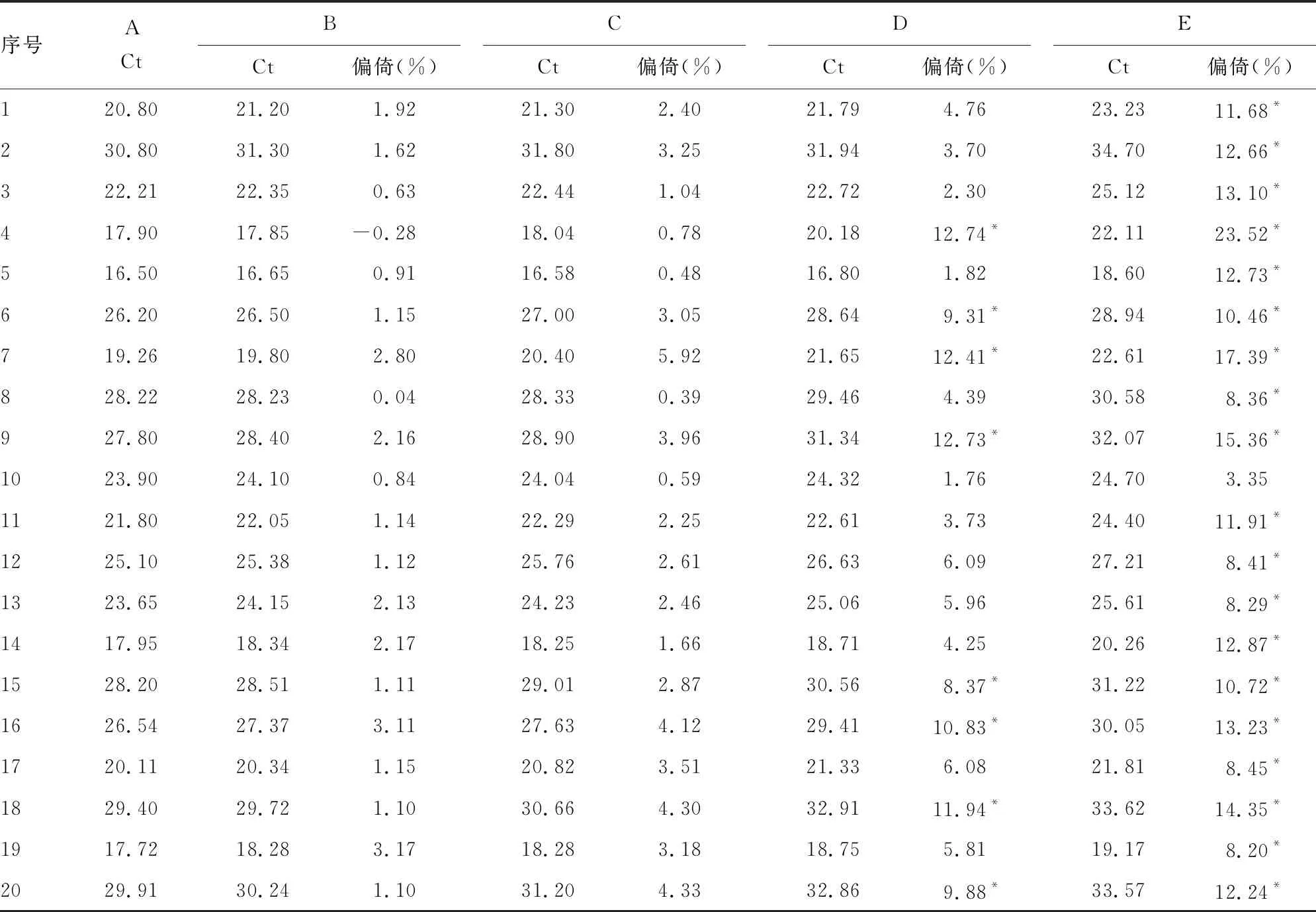
表2 不同水平血红蛋白对HPV-DNA定量检测Ct值的影响
注:A表示血红蛋白水平为0.0 g/L;B表示血红蛋白水平为2.5 g/L;C表示血红蛋白水平为5.0 g/L;D表示血红蛋白水平为10.0 g/L;E表示血红蛋白水平为20.0 g/L;*表示偏倚大于7.5%。

表3 预处理后的含血红蛋白标本中HPV-DNA定性检测结果
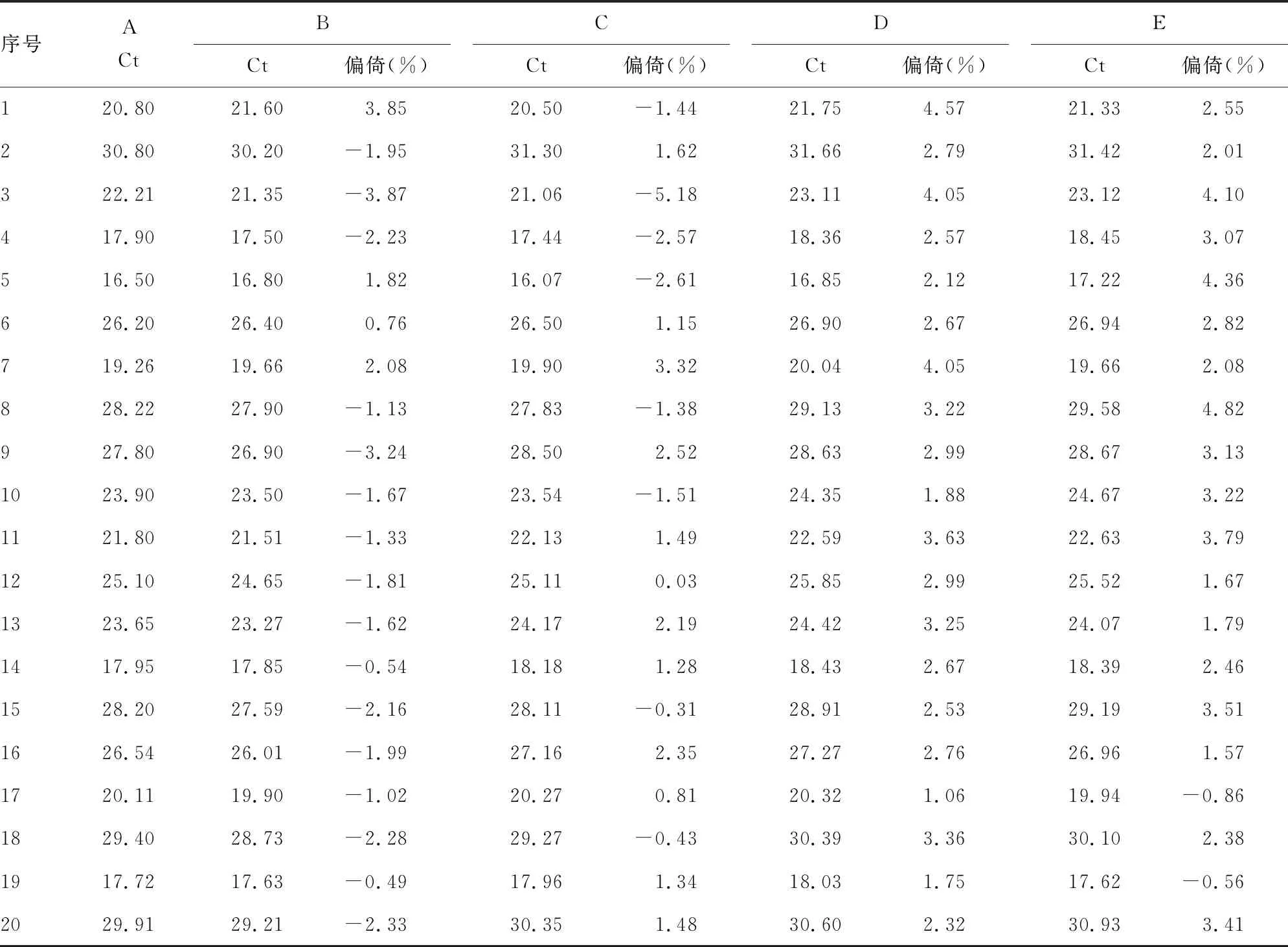
表4 预处理后的含血红蛋白标本中HPV-DNA定量检测结果
注:A表示血红蛋白水平为0.0 g/L;B表示血红蛋白水平为2.5 g/L;C表示血红蛋白水平为5.0 g/L;D表示血红蛋白水平为10.0 g/L;E表示血红蛋白水平为20.0 g/L;*表示偏倚大于7.5%。
3 讨 论
目前,已发现的HPV型别多达118种,其中与人类生殖道黏膜感染相关的约40种,与宫颈癌及其癌前病变密切相关的仅有13~18种[4-7]。一项来自国际癌症研究机构的多中心病例对照研究显示,高危型HPV感染患者罹患宫颈癌的风险是非感染者的158.2倍[8]。因此,HPV基因型的检测对于宫颈癌的预防、早期识别、治疗和预后都有非常重要的意义。
HPV在体外很难进行培养,而且并不是所有的HPV感染患者都有明显的体液免疫反应,因此,通过病原学和免疫学方法很难诊断HPV感染。核酸检测是一种灵敏度和特异度高的检测手段,适用于HPV感染检测。目前,应用于HPV分型检测的方法主要包括多重荧光定量PCR法、核酸杂交捕获法以及PCR结合核酸杂交法,本研究中的两种HPV-DNA检测方法都是应用多重荧光定量PCR法检测多种高危型HPV。PCR技术具有特异度高、灵敏度高、快速、方便等优势,是目前HPV-DNA定量检测最常用的方法,普遍应用于HPV感染的诊断和动态监测[9-11]。
荧光定量PCR是监测原始待测核酸模板的扩增过程,任何干扰PCR扩增的因素,都会影响扩增效率和定量的准确性。血红蛋白是DNA聚合酶的抑制剂,当标本中存在红细胞时,红细胞破坏释放出血红蛋白,血红蛋白则会不同程度地影响PCR过程,造成假阴性结果[12-14]。在临床工作中,很多妇科疾病,如宫颈炎性反应、宫颈癌等,常伴有阴道不规则出血,宫颈脱落细胞标本中就会含有不同量的红细胞,可能会造成实验结果的假阴性。但是,能够影响HPV-DNA检测结果的血红蛋白水平下限以及不同水平的血红蛋白对HPV-DNA检测结果影响是否一致的报道较少。葛燕梅等[15]报道,血性宫颈脱落细胞标本有可能导致流式荧光杂交法HPV分型检测假阴性结果,未见关于血红蛋白对荧光定量PCR法检测HPV-DNA的影响。
本文通过制备不同水平血红蛋白的宫颈脱落细胞标本,检测各组HPV-DNA的载量,比较不同水平血红蛋白对HPV-DNA检测结果的影响,发现血红蛋白水平低于5.0 g/L时,HPV-DNA定性结果与原始标本完全一致,符合率为100%,定量结果中所有标本的Ct值偏倚均小于7.5%,均在可接受范围内。当血红蛋白水平达到10.0 g/L时,HPV-DNA定性结果有35%与原始标本结果不一致,符合率仅为65%,定量结果中有40%标本Ct值偏倚超过7.5%,不在可接受范围内。当血红蛋白水平达到20.0 g/L时,HPV-DNA定性结果全部为阴性,与原始标本的符合率为0%,定量结果中有95%标本Ct值偏倚超过7.5%,二者均不在可接受范围内。全自动核酸提取仪一般采用磁珠法进行核酸提取,首先将游离的核酸分子特异地吸附到磁性颗粒表面,与蛋白质等杂质分离,在磁场作用下经过2次洗涤,血红素中的卟啉环和黏蛋白等干扰物均能被有效去除,从而保证核酸提取的高纯度。由此可见,当标本中血红蛋白水平较低于5.0 g/L时,HPV-DNA定性和定量检测结果均不受影响;当标本中血红蛋白水平高于10.0 g/L,HPV-DNA定性和定量检测结果均受到明显干扰,定性结果出现假阴性,定量结果Ct值明显增大,检测结果不可靠。
对于血性的宫颈脱落细胞标本,本研究进行了预处理实验,即通过加入红细胞裂解液破坏红细胞,生理盐水洗涤去除残留血红蛋白,并对预处理后的标本进行检测,发现所有预处理后的标本中HPV-DNA定性和定量检测结果均与原始标本一致,符合率和偏倚均在可接受范围内,因此,该方法适合于严重溶血的宫颈脱落细胞标本的预处理。此外,本研究还纳入了20例HPV-DNA阴性组,发现无论血红蛋白水平多少,均不会对其结果产生影响。
本研究从临床送检标本中选取了10个溶血程度较严重的标本进行血红蛋白水平检测,得到血红蛋白水平均小于10.0 g/L,提示临床送检的宫颈脱落细胞标本中所含的血红蛋白水平对HPV-DNA检测结果影响不大,但是如果肉眼观察到溶血程度较严重的标本应给予重视,有必要进行标本预处理,降低待测标本中血红蛋白的水平,保证检测结果的准确性。
4 结 论
血红蛋白在一定程度上会影响荧光定量PCR法检测宫颈脱落细胞标本中HPV-DNA的载量,轻度溶血标本,即血红蛋白水平低于5.0 g/L时,标本无需进行预处理,当标本中血红蛋白水平超过10.0 g/L时,需要采用红细胞裂解液预处理标本后再进行检测,以排除血红蛋白对HPV-DNA检测结果的影响。

