砷对大鼠附睾转化生长因子β1表达及精子顶体蛋白酶的影响
戴研平,高晓勤,秦海霞
(1.贵州医科大学基础医学院 病理学与病理生理学教研室,贵州 贵阳 550004;2.遵义医药高等专科学校 基础医学院,贵州 遵义 563006;3.乌兰察布医学高等专科学校,内蒙古 乌兰察布 012000)
砷是一种生殖毒物,慢性砷中毒是一个重要的全球性卫生健康问题,研究表明中国的高砷暴露人口超过300万[1]。然而,目前关于砷中毒的机制研究还有待深入,尚无有效的治疗药物[2]。转化生长因子β1(trans forming growth factor β1,TGF-β1)是一类具有多种生物活性的细胞因子,参与调节细胞的增殖、分化、发育、凋亡等多种生命活动[3]。TGF-β1信号通路能够参与肿瘤的发生、发展和转移[4]。TGF-β1是已经公认的参与细胞生长、分化、凋亡和迁移的有效调节因子[5]。人类TGF-β1信号通路元件的改变与肿瘤密切相关,TGF-β1的过度表达与人体多种肿瘤的发展和患者的预后有关[6-7]。慢性砷中毒具有致癌作用,可对人体多系统造成损害,影响男性生殖功能,其导致男性不育的病理生理机制仍值得深入研究,进而探索有效的预防及治疗方法。精子是一种具有特殊形态的细胞,顶体位于精子的前端,其内有顶体蛋白酶,顶体蛋白酶在精子顶体反应、精卵结合、精子穿越透明带等过程中起重要作用。检测精子顶体酶的活性,是判断精液质量、评估精子受精功能的重要指标[8]。砷中毒是一个多种细胞因子介导的复杂的病理过程,目前有关慢性砷中毒是否会对大鼠附睾TGF-β1及精子顶体蛋白酶活性造成影响,进而影响男性生育力尚未见报道。
本实验通过复制慢性砷中毒的大鼠模型,研究TGF-β1在大鼠附睾的表达变化,检测精子顶体酶活性,为慢性砷中毒导致男性不育的防治提供科学依据。
1 材料与方法
1.1 材料及分组
选择健康清洁级雄性SD大鼠40只,体重160~200 g,由贵州医科大学实验动物中心提供。动物饲养环境温度20~25℃,相对湿度为60%~67%,昼夜交替各 12 h。
适应性饲养1周后,将大鼠随机分为高(60.0 mg/L)、中(12.0 mg/L)、低(2.4 mg/L)剂量砷染毒组及对照组(蒸馏水),每组10只。测量并记录大鼠体重和每日饮水量。实验期间,大鼠可自由摄食、饮水,采用自由饮用方式连续染毒6个月。
1.2 主要试剂与仪器
亚砷酸钠(分析纯,北京化工厂),TGF-β1兔抗鼠多克隆抗体(美国 Gene Tex公司),Syn Gene Genius天才紫外凝胶成像系统(美国Bio-Rad公司),Image J图像分析软件(美国Bio-Rad公司)。
1.3 免疫组织化学染色二步法
采用二步法进行免疫组织化学染色:附睾组织石蜡切片用二甲苯化蜡至水,0.01 mmol/L(pH 6.0)枸橼酸钠缓冲液微波修复15 min,冷却至室温,30 ml/L过氧化氢封闭内源性过氧化物酶15 min,10 ml/L Triton-100浸泡30 min以增加细胞通透性,山羊血清37℃封闭30 min后加一抗(1∶500),4℃孵育过夜,恢复室温30 min后滴加山羊抗兔IgG,37℃孵育1 h,DAB显色3 min,苏木精复染2 min,常规脱水、透明、封片。以上步骤间均用 0.01 mmol/L(pH 7.0~ 7.4)磷酸盐缓冲液(phosphate buffered saline,PBS)洗 3 次,5 min/次。显微镜拍照,计算阳性细胞平均灰度值。
1.4 Western blotting
每组随机选取3只大鼠,提取大鼠左侧附睾组织匀浆,制作样品蛋白,煮沸10 min,制作分离胶,每个孔蛋白上样量为20 μl,室温静至2.5 h后电泳。转膜后用含5%脱脂奶粉封闭2 h,孵育一抗(TGF-β1:1∶1 000)4℃过夜,洗涤3次,10 min/次,GAPDH作为内参。孵育二抗 2 h,洗膜 3次,10 min/次,用电化学发光液曝光成像,Image J软件进行灰度值分析。
1.5 实时荧光定量聚合酶链反应
提取大鼠右侧附睾组织总RNA并测定浓度,逆转录为cDNA,在实时荧光定量聚合酶链反应(quantitative real-time polymerase chain reaction,qRTPCR)中作为模板。TGF-β1正向引物:5'-ACTACGCCA AAGAAGTCACCC-3',反向引物:5'-ACGCCAGGAATT GTTGCTAT-3';GAPDH 正向引物:5'-CAAGTTCAACG GCACAGTCAA-3',反向引物:5'-CGCCAGTAGACTCC ACGACA-3'。采用 SYBR Green I荧光染料法在 ABI 7900定量PCR仪上进行操作,PCR反应条件为:95℃预变性 10min,95℃变性 10s,60℃退火 30s,72℃延伸34s,40个循环,GAPDH为内参,检测各模板的Ct值。
1.6 精子顶体蛋白酶活性检测
处死大鼠,每组随机选取3只大鼠,仔细分离右侧附睾尾部,待精液流出后,室温下2000r/min(离心半径16cm)离心2次,10min/次,PBS清洗,将沉淀物悬浮于2倍以上PBS中。取备用的PBS精子悬浮液1~2滴涂于改良明胶底物膜片上,放入37℃恒温恒湿箱中孵育3h,检测精子顶体蛋白酶阳性率及活性强度。
1.7 观察指标
1.7.1 顶体蛋白酶阳性率 终止孵育后,每份切片于光学显微镜下均匀选取5、6个视野观察200个精子的头部,其周围出现晕环者视为顶体蛋白酶阳性反应,计算精子顶体蛋白酶阳性率。
1.7.2 顶体蛋白酶活性强度 每个精子头部晕环直径的大小采用微尺测量,计算平均反应直径(μm),作为判断顶体蛋白酶活性强度的指标。
1.8 统计学方法
数据分析采用SPSS 13.0统计软件。计量资料以均数±标准差(±s)表示,符合正态性和方差齐性的数据多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验,P<0.05为差异有统计学意义。
2 结果
2.1 各组大鼠附睾TGF-β1灰度值及表达
TGF-β1阳性产物主要位于附睾上皮细胞的胞质及胞核、附睾管腔内的精子及附睾管间质的细胞胞质。各组TGF-β1的表达水平差异有统计学意义(P<0.05)。不同剂量砷染毒组与对照组两两比较,差异有统计学意义(P<0.05)。见表1和图1。
2.2 各组大鼠附睾TGF-β1蛋白表达水平比较
各组大鼠附睾TGF-β1蛋白表达水平比较,差异有统计学意义(P<0.05)。与对照组比较,不同剂量砷染毒组TGF-β1的蛋白表达水平下调(P<0.05)。见表2和图2。
2.3 各组大鼠附睾TGF-β1 mRNA表达水平的比较
各组大鼠附睾TGF-β1mRNA的表达水平比较,差异有统计学意义(P<0.05)。与对照组比较,不同剂量砷染毒组TGF-β1mRNA 表达水平下调(P<0.05)。见表3。
表1 各组大鼠附睾TGF-β1灰度值比较(n =10,±s)

表1 各组大鼠附睾TGF-β1灰度值比较(n =10,±s)
注:†与对照组比较,P <0.05。
组别 灰度值对照组170.14±11.57低剂量砷染毒组119.80±0.82†中剂量砷染毒组104.75±0.40†高剂量砷染毒组84.47 ±0.35†F值 191.000 P值 0.004

图1 TGF-β1 在大鼠附睾组织中的表达 (SP ×400)
表2 各组大鼠附睾TGF-β1蛋白表达水平比较(n=10,±s)
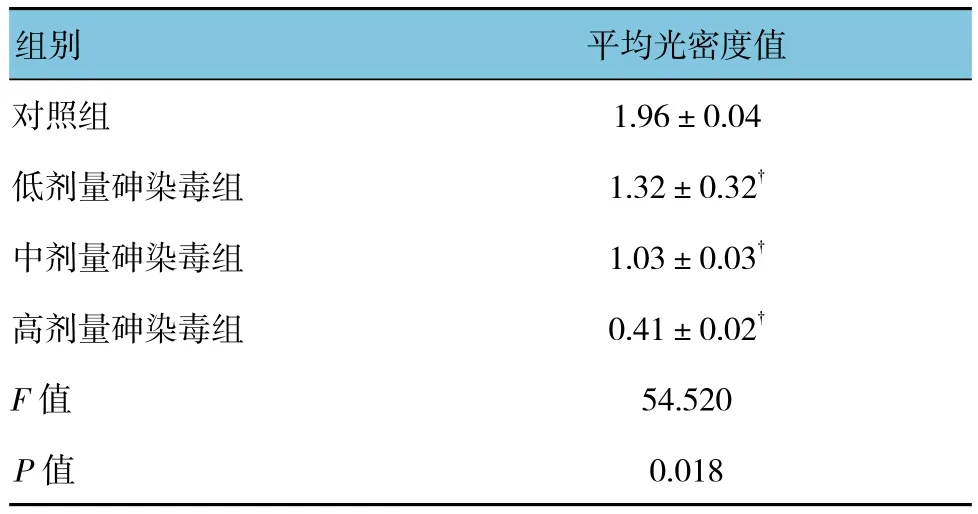
表2 各组大鼠附睾TGF-β1蛋白表达水平比较(n=10,±s)
注:†与对照组比较,P <0.05。
组别 平均光密度值对照组1.96±0.04低剂量砷染毒组1.32±0.32†中剂量砷染毒组1.03±0.03†高剂量砷染毒组0.41±0.02†F值 54.520 P值 0.018

图2 大鼠附睾中TGF-β1蛋白表达水平
2.4 精子顶体蛋白酶活性分析
2.4.1 光学显微镜下观察 对照组精子头部晕环明显(视为顶体蛋白酶阳性反应),直径较大,数量较多。随着砷剂量的增加,砷染毒组精子头部孵育2h后,晕环的直径变小,数量减少。见图3。
表3 各组大鼠附睾TGF-β1 mRNA表达的比较(n =10,±s)
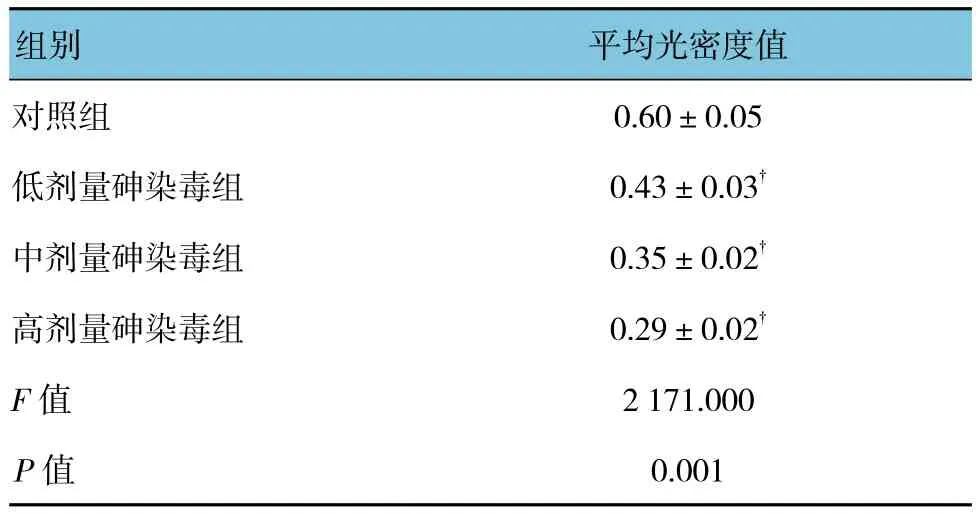
表3 各组大鼠附睾TGF-β1 mRNA表达的比较(n =10,±s)
注:†与对照组比较,P <0.05。
对照组0.60±0.05低剂量砷染毒组0.43±0.03†中剂量砷染毒组0.35±0.02†高剂量砷染毒组0.29±0.02†F值 2 171.000images/BZ_16_1285_1014_2248_1085.pngimages/BZ_16_1285_1439_2248_1510.png

图3 各组大鼠精子顶体蛋白酶阳性反应和活性观察 (台盼蓝染色×400)
2.4.2 精子 ACE 活性 如表4 所示,各组顶体蛋白酶阳性率、活性强度比较,差异有统计学意义(P<0.05)。与对照组比较,低剂量砷染毒组精子顶体蛋白酶阳性率和活性强度差异无统计学意义(P>0.05);与对照组比较,中、高剂量砷染毒组的精子顶体蛋白酶阳性率和活性强度呈逐渐下降趋势(P<0.05)。
表4 各组大鼠精子顶体蛋白酶阳性率和活性强度比较(n =10,±s)
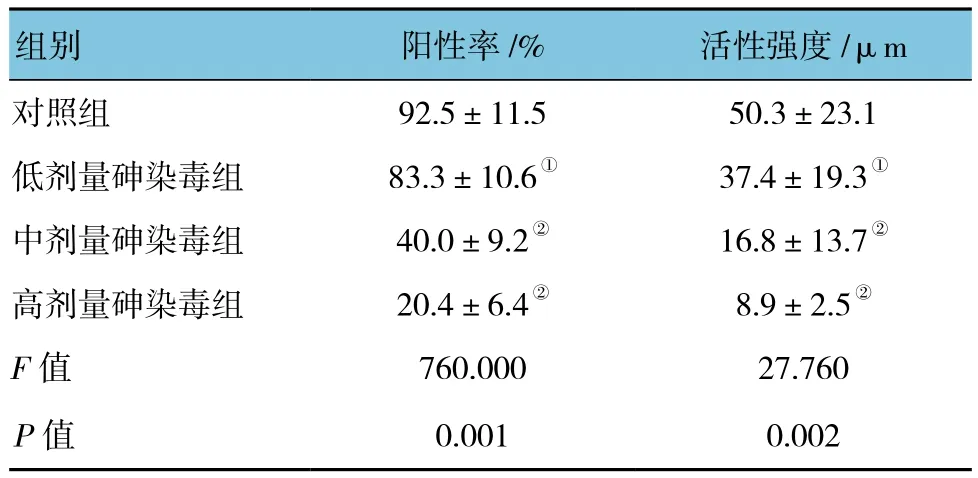
表4 各组大鼠精子顶体蛋白酶阳性率和活性强度比较(n =10,±s)
注 :①与对照组比较,P >0.05;②与对照组比较,P <0.05。
组别 阳性率/% 活性强度/μm对照组92.5±11.5 50.3±23.1低剂量砷染毒组83.3±10.6① 37.4±19.3①中剂量砷染毒组40.0±9.2② 16.8±13.7②高剂量砷染毒组20.4±6.4② 8.9±2.5②F值 760.000 27.760 P值 0.001 0.002
3 讨论
砷是一种环境内分泌干扰物,可显著影响睾酮和雌激素,导致代谢紊乱和生殖障碍[9]。研究表明砷化物对细胞的影响因剂量不同而有所不同[10]。研究发现,砷超过一定剂量时对男性性功能造成严重影响。砷能在附睾产生蓄积,损害雄性生殖细胞[11]。
TGF-β1是TGF-β家族的主要亚型,在局部炎症和肿瘤的发生、发展过程中起非常重要的作用。TGF-β1作为一种能够调节细胞生长与分化的多肽,与细胞的生长、分化、免疫功能等密切相关[12]。抑制TGF-β1的表达可以在一定程度控制疾病的发展,因此TGF-β1已经成为临床疾病治疗研究的重要靶点[13]。
细胞凋亡在病理情况下可导致肿瘤的发生,是一个由多基因参与的细胞死亡过程。本课题组前期研究结果表明,慢性砷中毒能够引起大鼠附睾上皮细胞的凋亡,进而影响男性生殖功能[14]。而国外学者报道TGF-β1在肿瘤早期发挥抗凋亡的作用[3],能够促进细胞增殖,提示TGF-β1可能作为一种保护因子参与慢性砷中毒机制。本研究免疫组织化学结果示TGF-β1表达于附睾上皮细胞胞质和胞核及部分精子。与对照组比较,不同剂量砷染毒组TGF-β1的免疫组织化学表达强度呈下降趋势。Western blotting、qRT-PCR结果显示,与对照组比较,不同剂量砷染毒组TGF-β1的蛋白及mRNA表达水平均较低。以上结果说明砷可能通过影响大鼠附睾TGF-β1的表达,进而对附睾上皮细胞的增殖、分化、发育产生影响,导致病理状态下的凋亡细胞增加,影响附睾微环境的形成和精子的成熟,最终影响男性生育力。
附睾是精子成熟的场所,精子必须在附睾中才能获得功能上的成熟。本课题组前期研究发现,砷能够对大鼠附睾中肝细胞生长因子及其受体c-met、凋亡诱导因子表达与透明质酸酶活性造成影响,可能与男性不育有关[15-16]。精子顶体蛋白酶和透明质酸酶都是受精过程中的关键酶,顶体蛋白酶能够水解透明带,顶体蛋白酶的阳性率和活性降低是导致男性不育的重要因素[17-18]。本实验采用本课题组已经成熟的固定明胶底膜法检测慢性砷中毒对顶体蛋白酶活性的影响[19-20],发现中、高剂量砷染毒组精子顶体蛋白酶活性和阳性率较对照组下降,其原因可能为精子含有大量的高尔基复合体和大量线粒体,线粒体作为细胞的供能器,其可能是砷发挥毒性作用的亚细胞器,而线粒体的变化又从多方面引起细胞凋亡。以上结果说明慢性砷染毒可能通过影响附睾因子TGF-β1的表达和附睾微环境的形成,进而影响精子顶体的完整性,导致精子顶体蛋白酶的流失,最终影响精子受精能力下降,引起男性不育。
综上所述,砷能够对男性生殖系统造成损害。TGF-β1表达的异常可能会对附睾微环境及精子的顶体蛋白酶产生影响,可能与砷中毒导致男性不育的病理机制密切相关。

