SF6气体的过热分解特性随温度的发展趋势研究
张广东 杨军亭 唐露 温定筠 刘康 王永奇 王津

摘 要:为了深入探究故障温度与SF6过热分解之间的关系,克服对运行中设备进行故障发展程度监测的困难,通过设计局部发热元件进行过热故障模拟,在该平台上开展200 ℃ ~ 360 ℃模拟实验。结果表明:SF6在200 ℃时就开始出现分解,故障温度较低时,SF6分解产物主要存在形式为SO2;中温段开始新生成SOF2;SO2F2、COS、H2S在高温下才产生,该三种产物的检出可表征设备已发生严重过热故障。此外,还定义了C(SO2F2 + SOF2)/C(SO2)特征比值量,其与故障发展趋势紧密相关,该值越大,揭示了SF6气体绝缘劣化越严重,电气设备故障发展程度就越严重。
关键词:过热故障、SF6分解产物、特征比值
中图分类号:TM835 文献标识码:A
Study on Development Trend of Overheated Decomposition
Characteristics of SF6 Gas with Temperature
ZHANG Guang-dong1,YANG Jun-ting1,TANG Lu2,WEN Ding-jun1,
LIU kang1,WANG Yong-qi1,WANG Jin1
(1. Gansu Electric Power Research Institute of State Grid,Lan Zhou,Gansu 730070,China;
2. School of Electric and Information Engineering,Hunan University,Changsha,Hunan 410082,China)
Abstract:In order to deeply probe into the relationship between fault temperature and SF6 overheating decomposition,and overcome the difficulty of monitoring the fault development of equipment in operation,serials of simulation experiments were carried out at 200 ℃ ~ 360 ℃ on the experiment apparatus.The results showed that SF6 started to decomopose at 200 ℃,and the maindecomposition products of SF6 was SO2 when the fault temperature was low.In the middle temperature section,SOF2 were generated,while SOF2、COS and H2S were generated at high temperature.The detection of these three products indicated that serious overheating fault has occurred in the equipment.Furthermore,component characteristicratioC(SO2F2 + SOF2)/C(SO2) is defined in this paper,which is closely related to the fault development trend.The lager the value is,the more serious the SF6 gas insulation deterioration is,the more serious the fault development degree of electrical equipment is.
Key words:thermal fault;SF6 decomposition products;characteristic ratio
SF6氣体绝缘设备因其检修周期长、占地面积小,抗污染能力强等优良性能而在电力行业中大量使用。在长时间运行下,SF6绝缘设备受其自身内部构造及复杂的外界环境影响,会发生触头或触指接触不良、导体连接处螺栓松动、接触部位有效面积减少等缺陷,会引起不正常发热导致局部温度升高,其中因触头接触异常引发的过热故障占比接近三分之一[1]。此时其内部充入的SF6气体受热分解生成高活性的SFx分子,在微量水和氧气的作用下,进一步生成SO2、SOF2、SO2F2、H2S等化合物。同时由于设备中大量使用环氧树脂等绝缘材料及含C金属材料,还会产生CO、CO2、CF4、COS等气体。以上分解产物可能会加速破坏设备的绝缘能力,增加了重大电力事故的发生率,因此对于SF6绝缘设备过热故障的监测非常必要。目前电力行业中主要使用红外测温法、回路电阻检测法、振动法、局部放电检测等手段对过热故障进行初步诊断。其中红外体本身对于红外光的强吸收性以及运行环测温技术受制于发热部位结构、SF6气境条件,所测的实际温度可靠性较低、波动性较大[2];回路电阻测量法虽然原理简单、操作方便,但只能对导电回路连接完整性以及触头接触状况进行初步判断,测量误差较大[3];振动法通常利用接触异常的触头处电压波形会发生畸变的原理进行在线故障监测,然而此方法对传感器灵敏度以及环境条件的要求较高,现场应用效果不甚理想。本文通过一系列实验,对分解产物形成机制及特性进行深入研究,提出了基于SF6分解产物类型揭示故障发展严重程度的诊断方法,此外,构造了C(SO2F2 + SOF2)/C(SO2)特征比值量,研究发现该值越大,设备故障情况越恶劣。
1 模拟试验
1.1 试验平台:
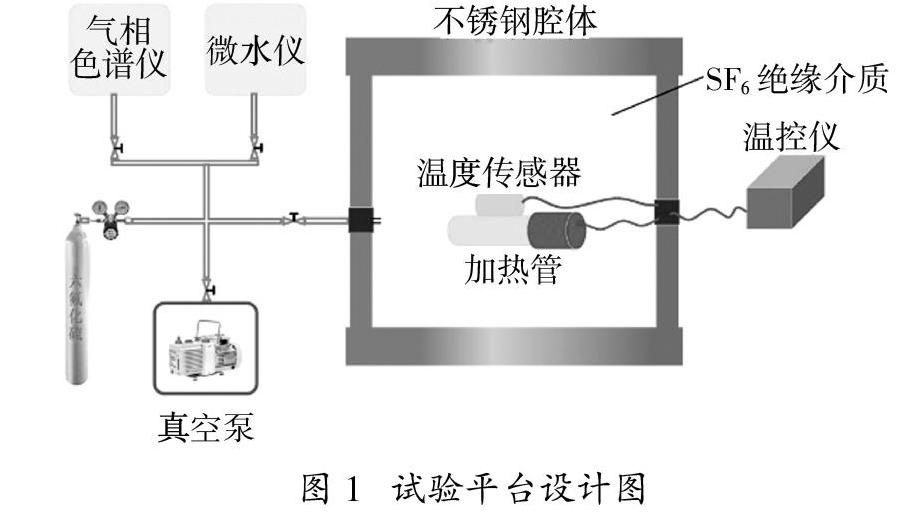
SF6局部过热模拟实验平台如图1所示,该平台由真空试验设备、发热体元件、气相色谱仪、SF6气瓶组成,其中真空试验设备腔体为不锈钢材料(可容纳20 L气体,内壁进行Teflon喷涂处理)。腔体前后两侧开有一大一小石英玻璃观察窗口,大视窗拆卸方便可随时对发热体进行更换;腔内放置一温湿度传感器与腔外显示仪可靠连接,实时掌握罐内温湿度变化;真空试验设备下部由抽真空系统、温度控制系统及气压显示仪组成;试验平台还配备微水仪,实验过程中微水含量严格控制在规程要求范围内。另外,气体管路连接一小型真空泵每次采样前后对管道进行抽真空处理,减少管道分解气体残留及空气混入。本文过热元件设计为不锈钢电热管(管径10 mm,长80 mm,功率250 W),放置于罐内底部,电热管核心镍发热丝产生高温作为局部热源,内部填充物采用导热快、高度耐温、绝缘性能好的MgO,发热管表面固定一灵敏传感器,通过自动温控系统设置温度模拟不同过热温度下的SF6分解。
1.2 分解气体检测系统
使用GC-9760B便携式气相色谱仪检测气体,如图2所示,主要由检测器、色谱柱箱、电路单元、气路单元等组成。该系统采用中心切割与反吹技术,进样阀采用六通或十通阀,连同快速连接接头、取样接头等部件一起组成一套完整的分析整体解决方案。仪器配备脉冲放电氦离子化(PDHID)检测器,采用外标法对气体组分含量进行定量分析,PDHID是一种灵敏度极高的通用型检测器,可以对H2、O2、N2、CF4、CO、CO2、C2F6、C3F8、SO2F2、SOF2、SO2、H2S、COS、CS2等多种分解产物进行有效分析检测。
PDHID利用氦气中稳定、低能耗的脉冲直流放电作为电离源,使被测组分电离产生信号。无组分流入时该信号为载气电离产生的基流信号,被测组分流入时电流增大,电流增大的程度与组分浓度成正比,从而实现定量检测。电离过程由三部分组成:(1)氦中放电发射出13.5 eV~17.7 eV的连续辐射光进行光电离;(2)被高压脉冲加速的电子直接电离组分AB产生信号,或电离载气产生基流;(3)亚稳态氦与组分反应产生信号。电离反应过程如式(1)到(3)所示。
e + AB→AB+ + 2e (1)
e + He→He**→He* + hν (2)
He* + AB→AB+ + e + He (3)
1.3 实验方法步骤
1)将电热管置于真空试验设备腔体底部,正确连接装置,气体管路各部位用检漏液进行气密性检查,符合实验要求后对腔体抽真空;每次实验前用无水乙醇反复擦拭腔体内壁减少杂质附着量,充入适量氮气干燥气室再反复将气室抽真空。
2)打开罐体进气孔阀门,充入一个大气压SF6新气洗气三次,最后一次洗气完成后让气室静置2小时,检测其中水分含量,采样一次若结果不满足实验条件再反复进行步骤二。
3)以一定流速向GIS模拟腔体充入纯度为
99.995%的SF6气体(气压控制在0.4 MPa),加热前进行一次样气采集分析,作为空白对照组,设定所需温度开始加热,每次采样前后用小型真空泵将气体管路抽真空避免管道气体残留干扰实验。
4)实验结束待气室温度降至室温后,打开抽真空系统将腔体内分解气体全部排出,在分解产物含量较大的情况下,需要多次使用氮气对气室进行冲洗,降低对下一次实验的影响。
2 实验结果与分析
纯净的SF6气体是一种无色、无嗅、基本无毒的卤素化合物,它的化学性质非常稳定,在空气中不燃烧,不助燃,與水、强碱、氨、盐酸、硫酸等不反应。但在大功率电弧、火花放电、电晕放电及POT(局部过热故障)作用下,SF6会分解游离出多种产物,并在特定条件下与气室内的杂质反应生成多种较稳定的分解特征产物。在搭建的实验平台上,从 200 ℃开始探究SF6分解过程,温度梯度为20,每个温度点下持续加热10小时。发现当发热体表面温度处于200 ℃左右时,实验结束后密闭罐体内检测到少量带有刺激性气味的SO2,说明SF6在200 就开始出现分解,通过温控系统将实验温度不断增加,多种硫化产物开始大量生成,分解产生的硫化物出现顺序依次为SO2、SOF2、SO2、F2、H2S、COS。将温度划分为200 ℃ ~ 240 ℃、260 ℃ ~ 300 ℃、320 ℃ ~ 360 ℃对应低、中、高三个温度区间并分别对各区间内分解产物变化规律进行探究。
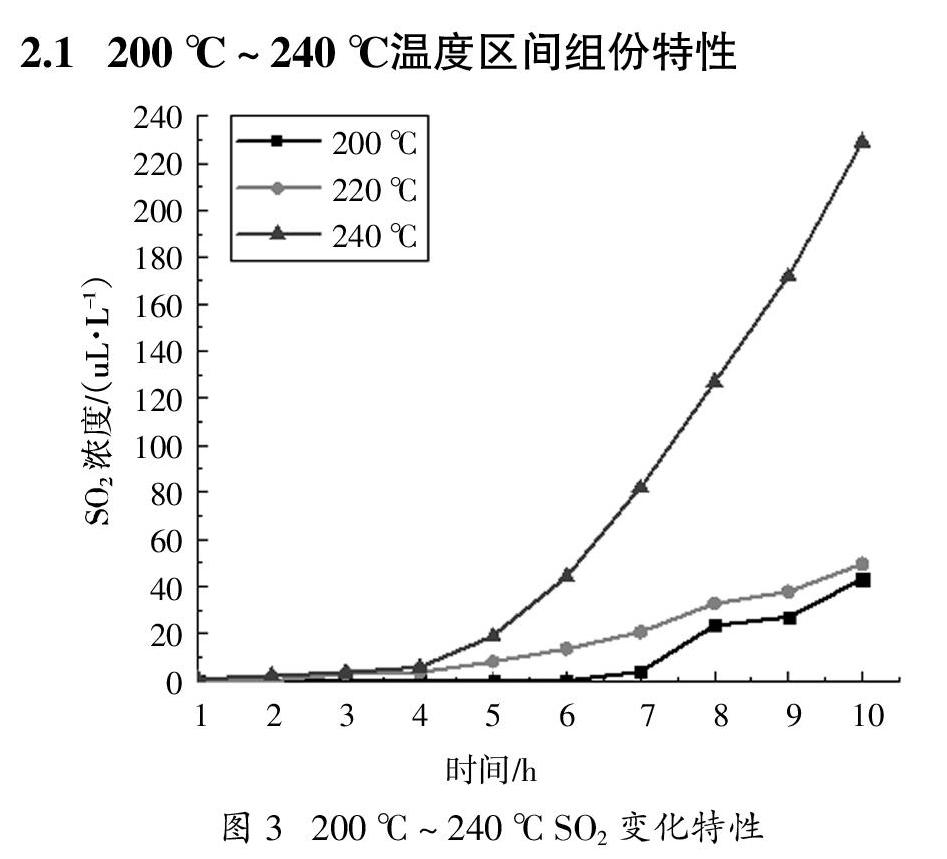
2.1 200 ℃ ~ 240 ℃温度区间组份特性
上图所示为200 ℃ ~ 240 ℃温度区间内分解产物变化特性,该低温段含S产物只检测到SO2,说明SF6在200 ℃即存在分解,跟以往文献提到的SF6初始分解温度在300 ℃左右有出入[4],分析其原因一在于电极材料可与SF6或其初级分解物发生反应,不同电极材料反应活性不同,对反应速率的影响不同,将进一步改变过热下的SF6分解特性[5-8],原因二在于电极材料表面构造的差异性使得吸附的H2O和O2分子量不同,对SF6分解过程的促进作用也不同[9]。随着过热时间的延长,SO2产量增加,各温度点下的变化趋势各不相同。200 ℃、220 ℃温度点下曲线增长平缓,当过热温度升高到240 ℃时,SO2产气量呈J型增长。
SO2的生成途径主要有三条,第一条通过SOF与气室内游离的O反应生成SO2F中间体,SO2F稳定性较差,反应式(4)放出的大量热可促进SO2F进一步裂解产生SO2和F原子,涉及反应式如下:
SOF + O→SO2F (4)
SO2F→SO2 + F (5)
其中SOF生成途径十分复杂,主要包括以下几个反应:
SF + O→SOF (6)
SF + OH→SFOH→SOF + H (7)
SF2 + O→SOF2→SOF + F (8)
SF2 + OH→SF2OH→SOF + HF (9)
SO2F不仅可以分解脱F,还可以与气室内的SF5发生反应(10),这是产生SO2的第二条途径。
SO2F + SF5→SF6 + SO2 (10)
从化学机理形成角度分析,发生该反应需要克服较高的能垒,温度较低时,外界所能提供的能量有限,反应(10)对于SO2的产生贡献并不大。往往在故障温度发展到较高时发生。如果密闭气室内有H2O分子存在,SO2还可以由SOF2水解得来,发生反应(11)-(12),该途径受初始反应物H2O的影响较大,H2O含量越多,反应正向进行的速率加快,最终产物SO2也越高,文献[10]提出H2O分子可以减弱反应所需活化能,起“自催化”作用使反应更易进行,也大大提高了SO2的生成量。但是GIS等电气设备在实际运行中会严格控制H2O含量,H2O分子量始终处于较低水平,SOF2水解这条途径也会相应受到抑制。
SOF2 + H2O→SOFOH + HF (11)
SOFOH→SO2 + HF (12)
综上所述在该200 ℃ ~ 240 ℃温度区间,SO2主要由途径一产生,但由于故障温度较低,SF6分解形成的SF及SF2量甚少,后续与游离的OH及O反应生成的SOF随之减少,使得实验10小时末气相色谱仪检测到其含量值仅为228.9 ul/l。
2.2 260 ℃ ~ 300 ℃温度区间组分特性
图4展示了SO2、SOF2分别在260 ℃、280 ℃、300 ℃下产气量与时间的关联关系,该区间内,SO2浓度增长速率明显高于低温区间,说明温度对反应的促进作用十分明显。300 时,10 h末检测到SO2量达到了496.3 ul/l,比该温度下SOF2含量值220.83 ul/l高出275.47 ul/l,属于SF6过热故障中产气量最大的分解组份,值得重点关注。同时检测到新的分解产物SOF2,其浓度变化与故障时间和温度都表现正相关关系,较SO2不同的是,三个温度点下,SOF2一开始便有趋于饱和的发展态势,而SO2在实验中期,增长速率达到最大,此后,单位时间内增长量慢慢减少并最终趋于饱和。
前文提到的SOF活性很强可以与F快速复合产生SOF2,但该路径比SOF氧化为SO2F更难发生,SOF2主要由中间产物SF3OH分解产生。SF3OH极不稳定,通过S-F键的断裂及H-F键的结合,最终裂解成SOF2和HF。SF4与H2O相互作用可以产生SF3OH,SF6在持续高温作用下断键产生的SF3碎片与H2O解离出来的OH反应也是SF3OH的来源之一,反应方程式分别为(13)、(14)、(15)。式(15)是个自发进行的放热反应,但由于游离的OH大部分来自于H2O的电离,SF6受热产生SF3较SF4需要更高的能量,导致SF4水解在SOF2形成过程中占据主导地位。然而在不锈钢罐体内,H2O分子的含量十分有限,成为了SF4水解反应的一个重要限制因素,因此,各温度下SOF2浓度变化曲线增长缓慢,并随加热时间逐渐趋于饱和状态。
SF3OH→SOF2 + HF (13)
SF4 + H2O→SF3OH + HF (14)
SF3 + OH→SF3OH (15)
2.3 320 ℃ ~ 360 ℃温度区间组分特性
该三组实验分别在320 ℃、340 ℃、360 ℃下展开,图5可知,故障后期,SO2产气量增长变缓,产气速率开始下降。一方面因为SO2与F2碎片反应消耗了部分SO2,另一方面SO2F2与SO2在某种程度上存在相互竞争关系[11-15],该温度点下SO2F可与F原子复合成SO2F2,如式(17)所示,使气室中参与反应(5)的SO2F的量减小,从这一途径得到的产物SO2必然随之减少。温度继续升高,对各反应的促进作用加强,SO2又出现急剧增长,含量始终是SF6过热分解组份中产气量最显著的。除了以上提及的形成路徑,SOF4也会发生像SF4一样发生类似的水解反应(18)形成SO2F2,SOF4水解反应速率常数远小于SO2F与F原子结合反应[16]。此外,SF6气体分子裂解产生单个F原子所需能量条件较高,限制了F的供应,经反应(17)产生的SO2F2气体分子量十分有限,可推知反应(16)是SO2F2的主要形成途径。图5 ~ 7中SO2F2的变化规律基本相同,与同期产生的其他硫化物相比,浓度始终处于较低水平,因为SO2、SOF4及SO2F都是由其他的分解物再参与复合或者裂解得来,以下反应都属于次级反应,最终SO2F2产气量自然不多。
SO2 + F2→SO2F2 (16)
[7] ASHOK K V. The nature of metal electrodes SF6 reactions in SF6 decomposition due to directcurrent interruption under simulated circuit-breaker conditions[J]. IEEE Transactions on Electrical Insulation,1976,11(4):157-160.
[8] HIROOKA K,KUWAHARA H,NOSHIRO M,et a1. Decomposition products of SF6 gas by high current arc and their reaction mechanism [J]. Electrical Engineering in Japan,1975,95(6):14-19.
[9] 陳晓清,任明,彭华东,丁彬,董明. GIS设备中SF6气体分解影响因素分析[J]. 电网与清洁能源,2010,26(07):34-38.
[10] 陈俊.基于气体分析的SF6电气设备潜伏性缺陷诊断技术研究及应用[D]. 武汉:武汉大学,2014.
[11] BECHER W,MASSONNE J. Contribution to the decomopsition of sulfur hexafluoride in electric arcs and sparks[R]. [S.l]:[s.n],1978.
[12] DERDOURI A,CASANOVAS J,GROB R,et al. Spark decomposition of SF6 /H2O mixtures[J]. IEEE Transactionson Electrical Insulation,1989,24 (6):1147 -1157.
[13] FREES L,SAUERS I,ELLIS H,et al. Positive ions in spark breakdown of SF6[J]. Journal of Physics D:Applied Physics,1981(14):1629-1637.
[14] BARTAKOVA B,KRUMP J,VOSAHLIK V. The effect of partial discharges upon SF6[J]. Electrotechnicky Obzor Prague,1978(67):230-241.
[15] Van BRUNT R,HERRON J. Fundamental processes of SF6 decomposition and oxidation in glow and corona discharges[J]. IEEE Transactions on Electrical Insulation,1990,25(1):75-94.
[16] FU Y,RONG M,YANG K,et al. Calculated rate constants of the chemical reactions involving the main byproducts SO2F,SOF2,SO2F2 of SF6 decomposition in power equipment[J]. Journal of Physics D-Applied Physics,2016,49(15):1-15.

