蜂窝状CuCl2/SCR催化剂制备及其脱汞性能
程广文,杨 嵩,刘文娟,郭中旭,付康丽
蜂窝状CuCl2/SCR催化剂制备及其脱汞性能
程广文,杨 嵩,刘文娟,郭中旭,付康丽
(西安热工研究院有限公司,陕西 西安 710054)
本文以CuCl2为活性组分,制备了一种蜂窝状SCR脱汞催化剂单体CuCl2/SCR,并研究 了制备工艺及催化剂在真实烟气中对元素汞的催化氧化性能。具体制备工艺为:先在助剂KCl的作用下将脱汞活性组分CuCl2负载在-Al2O3上形成复合粉末CuCl2-KCl/-Al2O3,再将CuCl2-KCl/-Al2O3作为一个整体组分加入传统SCR脱硝催化剂混料工艺中,同时用四甲基氢氧化铵代替氨水调节混料pH值,然后挤出、干燥、煅烧。结果表明:在真实烟气条件下,所得催化剂单体对元素汞的催化氧化效率在75%左右;助剂KCl可防止CuCl2因高温挥发而流失;CuCl2在催化剂中以铝酸铜和表面氯化铜2种形式存在,且均对元素汞表现出催化氧化活性;用四甲基氢氧化铵调节pH值可避免CuCl2因铜氨反应而失效。
工业锅炉;蜂窝状催化剂;脱汞;制备;真实烟气;催化;氧化率;盐析
近年来,随着国家对环保的重视,工业锅(窑)炉烟气脱汞受到了广泛关注。国家、各行业和各 地区都颁布了相应的锅(窑)炉大气污染物排放标准,均对汞的排放值提出了约束性指标(50mg/m3(GB 13271—2014),8mg/m3(DB 50/659—2016),30mg/m3(DB 31/387—2017),8mg/m3(DB 31/860—2014)。因此,研究适合工业锅(窑)炉的烟气脱汞技术具有重要意义。
选择性催化还原(SCR)脱汞技术是利用SCR催化剂将烟气中难除去的元素汞(Hg0)催化氧化为易捕集的离子汞(Hg2+),再利用现有污染物控制设备除去离子汞,从而实现烟气脱汞。与已在大型燃煤电站获得工程应用的活性炭喷射法相比,SCR脱汞成本低、工艺简单、更适合在工业锅(窑)上应用。
目前,研究人员开发了多种SCR脱汞催化剂,按活性组分分,主要有氧化锰类[1-3]、氧化铈类[4-6]、氧化铜类[7-8]、氧化钌类[9-10]和氧化钒类[11-14]等催化剂。上述催化剂的脱汞效率除受配方本身影响外,受烟气中的卤化氢浓度的影响也较显著[15-19]。元素汞的氧化率随烟气中卤化氢浓度的增加而增加,而我国燃煤大多为低氯煤,因此这些脱汞催化剂在真实烟气中的汞氧化效率均较低。
对此,作者所在课题组通过前期研究[20],在实验室制备了一种CuCl2改性的SCR脱汞催化剂(CuCl2/SCR),有效克服了烟气中卤化氢浓度对汞氧化效率的影响。目前,实验室蜂窝状CuCl2/SCR单体的制备方法主要有2种:1)用CuCl2水溶液浸渍蜂窝状SCR脱硝催化剂后干燥煅烧;2)将CuCl2粉末作为一种组分,加入蜂窝状SCR脱硝催化剂制备工艺中(混料阶段)。由于实验室催化剂制备工艺不适用于生产工业上常见的蜂窝状催化剂单体,限制了CuCl2/SCR催化剂在工程上的应用。
CuCl2是可溶性盐,在干燥煅烧过程中,易随水的蒸发从催化剂基体内部向催化剂表面转移并形成富集,即所谓“盐析”或“泛霜”[21-22],导致活性组分在催化剂中分散不均,影响催化活性;同时,CuCl2属于挥发性物质,长期在高温下运行,活性组分易流失,影响催化剂使用寿命;此外,在传统蜂窝状SCR催化剂成型过程中,有大量氨的加入和释放,而CuCl2可与氨发生铜氨反应,导致催化剂活性消失。可见,作为CuCl2/SCR催化剂的主要活性组分,CuCl2易发生“盐析”、“高温挥发”和“铜氨反应”,显著影响催化剂的活性与寿命,这也是该催化剂工程应用前必须解决的问题。
鉴于此,本文研究了适合工程应用的蜂窝状CuCl2/SCR单体的制备工艺,并在自主搭建的实验台上,测试了真实烟气条件下催化剂单体的汞氧化性能。
1 实验内容
1.1 原料
氯化铜、氯化钾、三氧化二铝(γ-Al2O3,微米级)、钛钨粉、钛钨硅粉、四甲基氢氧化铵、硬脂酸、乳酸、玻璃纤维、阔叶木浆、聚氧乙烯醇、羧甲基纤维素、乙醇等原料均为工业级,且从商业获得。水为去离子水。
1.2 催化剂制备
蜂窝状CuCl2/SCR单体的制备分2步进行: 1)三氧化二铝负载氯化铜-氯化钾粉末(CuCl2-KCl/Al2O3)的制备;2)蜂窝状催化剂单体的成型。
CuCl2-KCl/Al2O3粉末采用浸渍法制备:将适量的γ-Al2O3作为载体加入CuCl2和KCl水溶液中,搅拌8~12 h后,干燥(在110~120 ℃下干燥4~6 h)、煅烧(在500~550 ℃下煅烧4~8 h),再用球磨机研磨。
蜂窝状催化剂单体的成型参照传统SCR脱硝催化剂的制备工艺:
1)将计量的钛钨粉、钛钨硅粉和CuCl2-KCl/Al2O3粉末加入捏合机中进行初步混合(15~ 20 min)后,加入四甲基氢氧化铵(pH调节剂)、去离子水、硬脂酸(2%,占混料总质量的比例,下同)的乙醇溶液(脱模剂)和乳酸(1%,分散剂),继续混炼(80~100 min),最后加入玻璃纤维(5%,增强剂)、阔叶木浆(0.5%,造孔剂)、羧甲基纤维素(0.7%)和聚氧乙烯醇(0.75%)水溶液(黏合剂),接着混炼(60~80 min)至泥料满足一定条件(湿度约为27%,pH值约为7.5)后结束混料,将泥料装入密封袋,于常温下放置24 h进行陈化;
2)将陈化后的泥料加入真空炼泥机中,在500 Pa的真空度下,利用双螺杆挤压混炼2~3次,炼泥结束后,将泥料装入密封袋,于常温下放置24 h进行陈化;
3)将陈化后的真空炼泥料放入挤出机中挤出,挤出压力为2 MPa,挤出催化剂的壁厚1.0 mm,孔径6.5 mm,节距7.5 mm,长度30 cm;
4)将挤出的催化剂放在初始湿度为80%,温度为30 ℃的环境内干燥,之后每天将湿度降低5%、温度升高1 ℃,直至催化剂湿度降为10%,结束干燥,将干燥后的催化剂放入煅烧炉中进行煅烧,升温制度为150 ℃/2 h+180 ℃/2 h+200 ℃/2 h+450 ℃/ 2 h+ 600 ℃/2 h,为连续升温,升温速度为3 ℃/min,煅烧结束后,自然降温。
1.3 催化剂表征
利用X射线衍射仪(XRD)、X射线荧光光谱分析仪(XRF)以及全自动比表面积及孔隙分析对所制备粉末及催化剂单体进行结构表征。
采用滴定法对所制备粉末及催化剂单体中铜含量进行了测定:首先将样品加入质量比为1:3硝酸中,加热溶解,蒸发至不再有红棕色气体产生,冷却后用蒸馏水标定;向标定液中加入碘化钾,以质量分数为1%的淀粉溶液作为指示剂,用硫代硫酸钠滴定,按式(1)、式(2)计算铜含量。
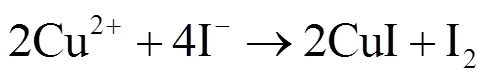
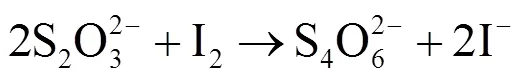
1.4 催化剂脱汞活性测试
在真实烟气条件下,针对蜂窝状CuCl2/SCR催化剂单体进行Hg0的催化氧化性能测试。实验台设置在某燃煤锅炉上,其脱汞系统如图1所示。从SCR反应器入口烟道(喷氨后)引一股真实烟气进入脱汞反应器,脱汞反应器内放置一层CuCl2/SCR催化剂单体,在压差作用下,烟气经过催化剂后直接进入静电除尘器入口烟道。
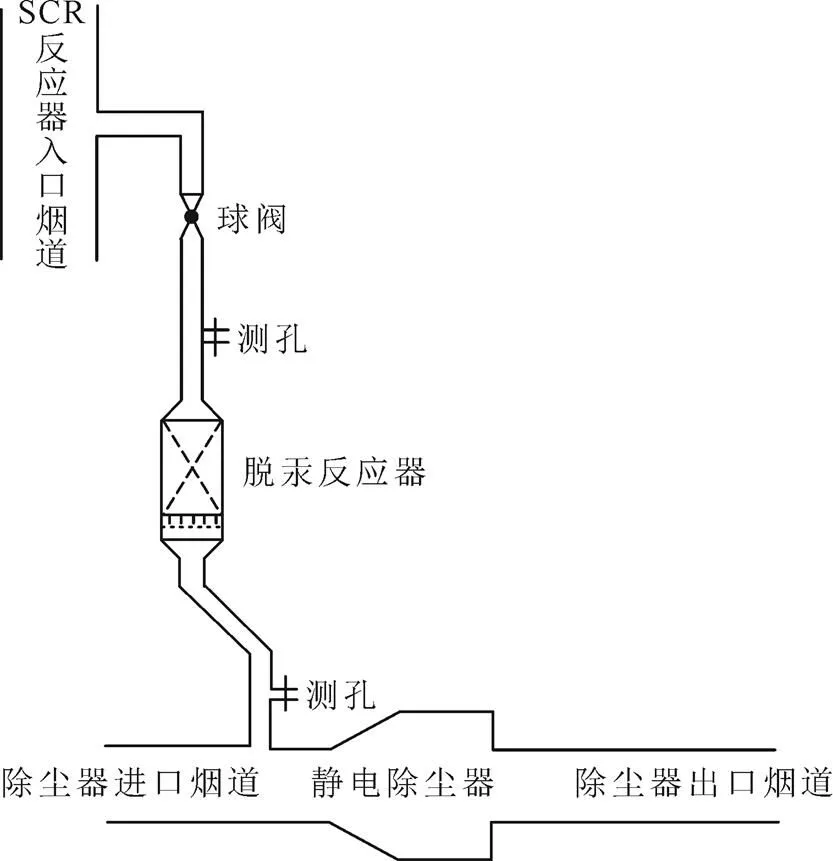
图1 真实烟气脱汞系统示意
脱汞反应器中烟气流量通过球阀调节。实验台所有管道和反应器均做保温处理,反应温度根据机组运行负荷来调节。利用安大略法(OHM)测试脱汞反应器进出口处烟气中元素汞质量浓度,按式(3)计算CuCl2/SCR催化剂对元素汞的催化氧化效率。
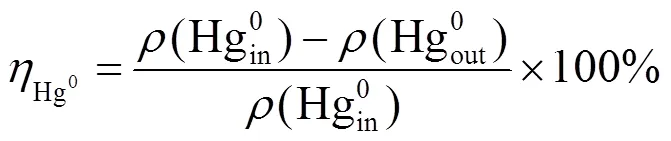
安大略法采样系统(图2)包括保温管、过滤箱、“八大瓶”、主机和抽气泵。在抽气泵作用下,烟气通过保温管进入过滤箱,过滤箱中的旋风分离器和石英膜将烟气中的颗粒汞捕集;“八大瓶”中装有KCl溶液的洗气瓶收集烟气中的Hg2+,装有H2SO4/KMnO4溶液的洗气瓶则捕集烟气中的Hg0。捕集到的Hg0样品用RA-915M型测汞仪(图3)进行分析。

图2 安大略法现场采样系统

图3RA-915M型测汞仪及其配件
2 结果与分析
2.1 蜂窝状CuCl2/SCR单体制备
针对现有技术在制备蜂窝状CuCl2/SCR单体时存在的“盐析”、“高温挥发”和“铜氨反应”等问题,本工作对传统蜂窝状SCR催化剂的制备工艺进行了改性。
1)先将脱汞活性组分CuCl2负载在γ-Al2O3上,形成CuCl2-KCl/Al2O3复合粉末,再将复合粉末作为一个整体组分加入蜂窝状SCR催化剂的混料工艺中,然后挤出成型、干燥煅烧,得到蜂窝状单体,这样可最大程度避免溶液浸渍导致的“盐析”现象。
2)在复合粉末过程中,加入碱金属盐与CuCl2形成共熔物,有效防止了CuCl2“高温挥发”导致的活性组分流失。
3)为避免“铜氨反应”的发生,用四甲基氢氧化铵代替氨水调节混料过程中泥料的pH值,尽量减少体系中氨的存在。
一般认为,CuCl2在载体γ-Al2O3上的存在形式有2种[23-24]:与载体作用形成铝酸铜(骨架铜);分散在载体表面的氯化铜(表面铜)。前者镶嵌在载体骨架中,不溶于有机溶剂如丙酮,而后者通常以无定形的形式存在于载体表面,可溶于有机溶剂。鉴于此,以丙酮为溶剂,在索氏提取器中对CuCl2-KCl/Al2O3样品进行反复提取,将样品中的氯化铜溶解,只剩下铝酸铜。用滴定法测试提取前后样品中铜的含量,结果见表1。从表1可看出,CuCl2-KCl/Al2O3样品中确实存在溶于丙酮的CuCl2和不溶于丙酮的骨架铜,而且骨架铜含量随总铜量的增加而增加,当总铜量达到8%左右,骨架铜含量趋于稳定。
表1CuCl2-KCl/Al2O3中铜质量分数
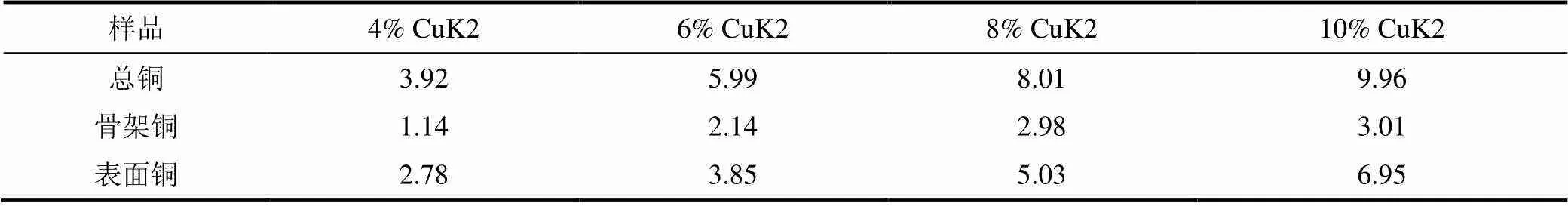
Tab.1 The mass fractions of Cu in CuCl2-KCl/Al2O3 %
注:4% CuK2表示CuCl2-KCl/Al2O3中铜质量分数的理论值为4%,Cu与K摩尔比为1:2,以此类推,下同。
图4为CuCl2-KCl/Al2O3粉末的XRD谱图。由图4可以看出:未出现铜物质的衍射峰,说明铜物种在载体上以无定形形式存在;谱图上存在明显的KCl特征衍射峰(2=28.3o、40.5o、50.2o)[25-26],表明KCl以晶相形式存在,并且随着K含量的增加,衍射峰强度逐渐增加。
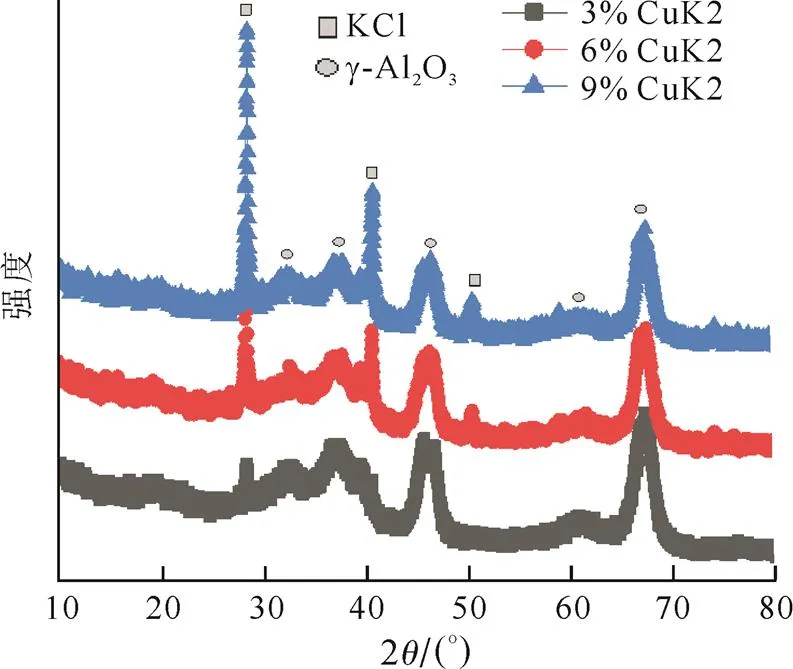
图4 CuCl2-KCl/Al2O3粉末的XRD谱图
为了研究KCl的加入对CuCl2-KCl/Al2O3粉末的影响,表2展示了添加KCl的CuCl2-KCl/Al2O3粉末在高温处理(400 ℃/168 h)前后的铜质量分数。由表2可以看出:不添加KCl,高温处理后样品铜质量分数只剩下0.50%,铜流失严重;添加KCl后,铜流失很少,这可能是因为CuCl2与KCl形成了共溶体,不易挥发所致[27]。KCl的加入显著提高了CuCl2的高温稳定性。四甲基氢氧化铵加入混料体系后,将首先与乳酸反应生成乳酸四甲基铵,该物质无法与铜离子发生铜氨反应,有效避免了脱汞活性组分(CuCl2)的失效。
表2CuCl2-KCl/Al2O3处理前后的铜质量分数

Tab.2 The mass fractions of Cu in CuCl2-KCl/Al2O3 before and after the treatment at high temperature %
按照改性后的工艺制备蜂窝状CuCl2/SCR单体,其XRD谱图如5所示。由图5可见,存在明显的锐钛矿型TiO2(2=25.29°、37.80°、48.03°、53.94°、55.09°、62.71°和75.02°)[28]、KCl、γ-Al2O3衍射峰,未出现CuCl2的特征衍射峰。这是因为载体表面的CuCl2以无定形形式存在,但滴定法测得催化剂中铜质量分数(表3)与理论值接近,说明脱汞活性组分CuCl2已成功加入催化剂单体。负载CuCl2后催化剂单体的比表面积、孔容和孔径分别为43 m2/g、0.22 mL/g和19.4 nm。
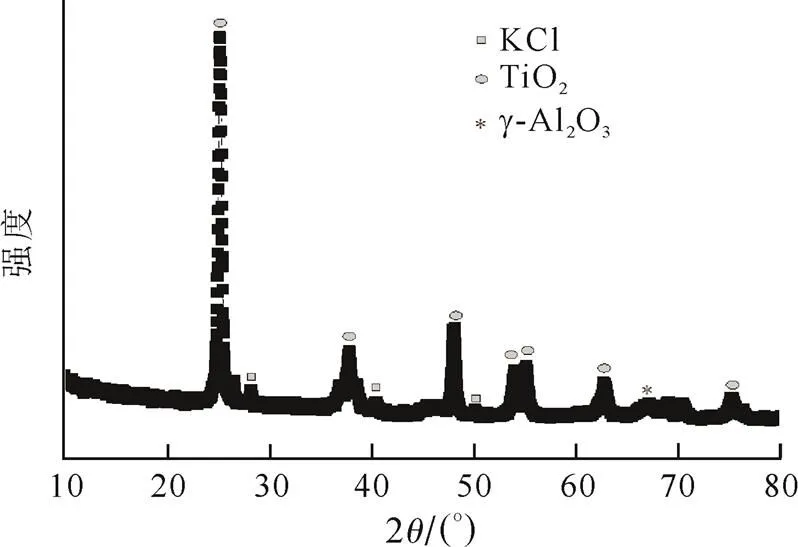
图5CuCl2/SCR单体的XRD谱图
表3 催化剂单体中铜质量分数

Tab.3 The mass fractions of Cu in the catalyst %
2.2 蜂窝状CuCl2/SCR单体对Hg0催化氧化性能
本文分析了真实烟气下反应温度和空速对催化剂单体汞氧化性能的影响,以及催化剂单体中不同形态铜的催化氧化活性,和KCl对催化剂寿命的影响。
1)反应温度的影响 烟气流速为50 m3/h,O2体积分数为2.3%,NO质量浓度为48.5 mg/m3,NH3质量浓度为0.84 mg/m3,SO2质量浓度为2 560 mg/m3,水蒸气体积分数为7%,粉尘质量浓度为30 g/m3,燃煤中氯质量分数为0.065%,烟气流量调节空速 4 000 h–1。改变反应温度,测得Hg0氧化率见表4。从表4可看出,CuCl2/SCR单体对Hg0的催化氧化效率随反应温度的增加而缓慢增加,这是因为高温有利于CuCl2释放活性氯来氧化汞。该规律与模拟烟气条件下类似[20],但真实烟气条件下催化剂对元素汞的氧化率低于模拟烟气条件,可能是由于烟气中粉尘和水蒸气影响了元素汞在催化剂表面的吸附所致。
表4 反应温度对汞氧化率的影响

Tab.4 The effect of reaction temperature on Hg0 oxidation efficiency
2)空速的影响 反应温度为370 ℃,O2体积分数为2.5%,NO质量浓度为39.9 mg/m3,NH3质量浓度为0.84 mg/m3,SO2质量浓度为2 560 mg/m3,水蒸气体积分数为7%,粉尘质量浓度为30 g/m3,燃煤中氯质量分数为0.65%。改变烟气流量调节空速,测得Hg0氧化率见表5。从表5可看出,随着空速增加,催化剂单体对元素汞的催化氧化效率逐渐降低。这是因为空速增加缩短了气(Hg0)固(催化剂)接触时间,导致反应时间缩短所致。
表5 空速对汞氧化率的影响

Tab.5 The effect of air velocity on Hg0 oxidation efficiency
3)铜形态的影响 与CuCl2-KCl/Al2O3粉末相似,铜在CuCl2/SCR单体中的存在形式也有骨架铜和表面铜2种。为考察铜的存在形式对催化剂汞催化氧化性能的影响,用丙酮对CuCl2/SCR单体进行了反复漂洗,直至洗出液中检测不出CuCl2,然后在与表4相同烟气条件下对漂洗前后催化剂单体的汞催化氧化性能进行了测试,结果如图6所示。
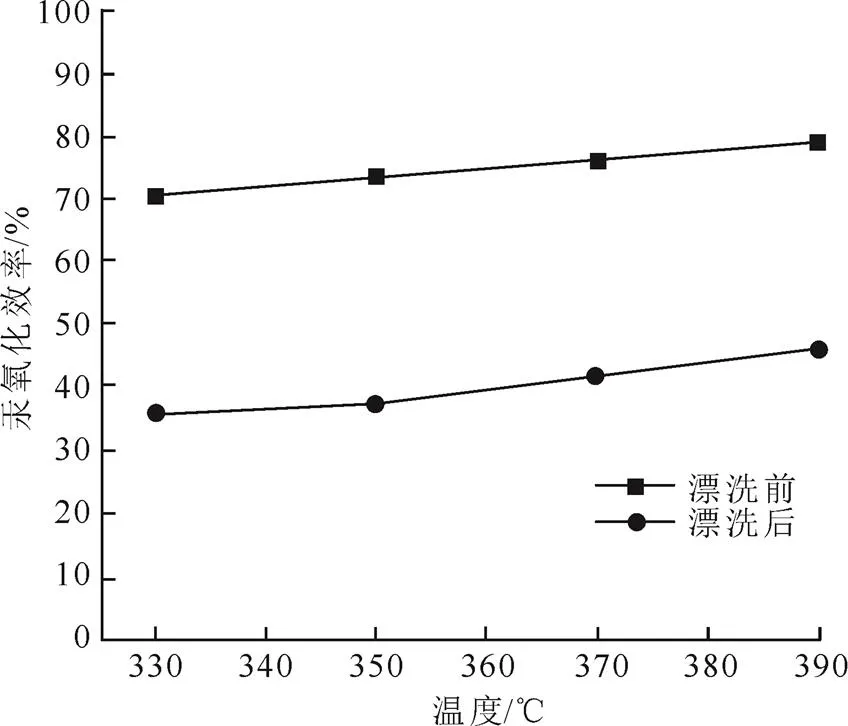
图6 铜形态对汞氧化效率的影响
从图6可以看出,催化剂单体中的骨架铜和表面铜对元素汞的氧化都表现出了一定的催化活性,汞氧化效率与温度及铜含量正相关。
4)KCl的影响 首先制备了Cu与K摩尔比分别为1:0、1:2、1:4的10% CuK0、10% CuK2和10% CuK4 3种粉末,然后按照CuCl2/SCR成型工艺,制备了3种催化剂单体CuCl2/SCR(K0)、CuCl2/SCR(K2)和CuCl2/SCR(K4)。在相同烟气条件下对其进行了汞氧化性能测试,结果如图7所示。
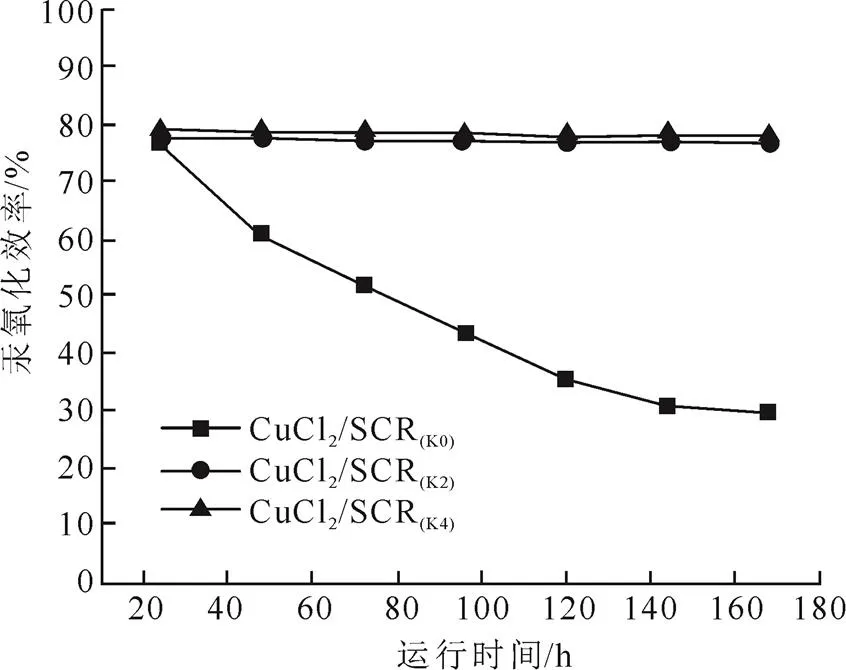
图7KCl对汞氧化效率的影响
从图7可看出:未加KCl的催化剂单体,汞氧化效率随时间的增加而逐渐降低,可能是由于活性组分高温流失所致;加入KCl后的催化剂单体,汞氧化效率随反应时间变化甚微,说明KCl确实可以稳定活性组分,防止其高温流失。
3 结 论
1)将脱汞活性组分CuCl2与助剂KCl负载在γ-Al2O3上,形成CuCl2-KCl/Al2O3复合粉末,再将复合粉末作为一个整体组分加入蜂窝状SCR催化剂的混料工艺中,然后挤出成型-干燥煅烧,可得到一种蜂窝状CuCl2/SCR脱汞催化剂单体。
2)CuCl2在催化剂中的存在形式有骨架铜和表面铜,2种铜对元素汞都表现出了一定的催化氧化活性。
3)KCl加入催化剂组分中,可与活性组分CuCl2形成共溶体,防止CuCl2的高温挥发,确保催化剂使用寿命。催化剂成型过程中,用四甲基氢氧化铵代替氨水调pH值,可防止活性组分因铜氨反应失活。
4)CuCl2/SCR催化剂单体在真实烟气条件下对元素汞表现出了较好的催化氧化性能,汞氧化效率可达75%左右。
[1] ZHANG S B, ZHAO Y C, WANG Z H, et al. Integrated removal of NO and mercury from coal combustion flue gas using manganese oxides supported on TiO2[J]. Journal of Environmental Sciences, 2017, 53: 141-150.
[2] ZHANG S B, ZHAO Y C, YANG J P, et al. Simultaneous NO and mercury removal over MnO/TiO2catalyst in different atmospheres[J]. Fuel Processing Technology, 2017, 166: 282-290.
[3] LIU X, JIANG S J, LI H L, et al. Elemental mercury oxidation over manganese oxide octahedral molecular sieve catalyst at low flue gas temperature[J]. Chemical Engineering Journal, 2019, 356: 142-150.
[4] LI Z, SHEN Y S, LI X H, et al. Synergetic catalytic removal of Hg0and NO over CeO2(ZrO2)/TiO2[J]. Catalysis Communications, 2016, 82: 55-60.
[5] HE C, SHEN B X, CHI G L, et al. Elemental mercury removal by CeO2/TiO2-PILCs under simulated coal-fired flue gas[J]. Chemical Engineering Journal, 2016 300: 1-8.
[6] YANG Y J, LIU J, ZHANG B K, et al. Experimental and theoretical studies of mercury oxidation over CeO2-WO3/TiO2catalysts in coal-fired flue gas[J]. Chemical Engineering Journal, 2017, 317: 758-765.
[7] XU W Q, WANG H R, ZHOU X, et al. CuO/TiO2catalysts for gas-phase Hg0catalytic oxidation[J]. Chemical Engineering Journal, 2014, 243: 380-385.
[8] LI H L, ZHANG W L, WANG J, et al. Coexistence of enhanced Hg0oxidation and induced Hg2+reduction on CuO/TiO2catalyst in the presence of NO and NH3[J]. Chemical Engineering Journal, 2017, 330: 1248-1254.
[9] LIU Z Y, SRIRAM V, LEE J Y. Heterogeneous oxidation of elemental mercury vapor over RuO2/rutile TiO2catalyst for mercury emissions control[J]. Applied Catalysis B: Environmental, 2017, 207: 143-152.
[10] LIU Z Y, LI C, SRIRAM V, et al. XANES study of elemental mercury oxidation over RuO2/TiO2and selective catalytic reduction catalysts for mercury emissions control[J]. Fuel Processing Technology, 2016, 153: 156-162. 2014, 253: 243-250.
[11] LI B, WANG H L, XU Y Y, et al. Study on mercury oxidation by SCR catalyst in coal-fired power plant[J]. Energy Procedia, 2017, 141: 339-344.
[12] STOLLE R, KOESER H, GUTBERLET H, et al. Oxidation and reduction of mercury by SCR deNOcatalysts under flue gas conditions in coal fired power plants[J]. Applied Catalysis B: Environmental, 2014, 144: 486-497.
[13] GAO W, LIU Q C, WU C Y, et al. Kinetics of mercury oxidation in the presence of hydrochloric acid and oxygen over a commercial SCR catalyst[J]. Chemical Engineering Journal, 2013, 220: 53-60.
[14] HE J, REDDY G K, THIEL S W, et al. Simultaneous removal of elemental mercury and NO from flue gas using CeO2modified MnO/TiO2materials[J]. Energy & Fuels, 2013, 27: 4832-4839.
[15] YANG H M, PAN W P. Transformation of mercury speciation through the SCR system in power plants[J]. Journal of Environmental Sciences 2007, 19: 181-184.
[16] CAO Y, CHEN B, WU J, et al. Study of mercury oxidation by a selective catalytic reduction catalyst in a pilot-scale slipstream reactor at a utility boiler burning bituminous coal[J]. Energy & Fuels, 2007, 21(1): 145-156.
[17] KAMATA H, UENO S I, NAITO T, et al. Mercury oxidation over the V2O5(WO3)/TiO2commercial SCR catalyst[J]. Industrial & Engineering Chemistry Research, 2008, 47: 8136-8141.
[18] CAO Y, WANG Q H, CHEN C W, et al. Investigation of mercury transformation by HBr addition in a slipstream facility with real flue gas atmospheres of bituminous coal and powder river basin coal[J]. Energy & Fuels, 2007, 21: 2719-2730.
[19] QU Z, YAN N Q, LIU P, et al. Bromine chloride as an oxidant to improve elemental mercury removal from coal-fired flue gas[J]. Environmental Science & Technology, 2009, 43: 8610-8615.
[20] 程广文, 张强, 白博峰. 一种改性选择性催化还原催化剂及其对零价汞的催化氧化性能[J]. 中国电机工程学报, 2015, 35(3): 623-630.
CHENG Guangwen, ZHANG Qiang, BAI Bofeng. A modified SCR catalyst and its catalytic oxidation for Hg0[J]. Proceedings of the CSEE, 2015, 35(3): 623-630.
[21] 张召述. 用工业废渣制备CBC复合材料基础研究[D]. 昆明: 昆明理工大学, 2007: 47-150.
ZHANG Zhaoshu. Study on the preparation of chemically bonded ceramics by using industrial waste residues[D]. Kunming: Kunming University of Science and Technology, 2007: 47-150.
[22] 宋学锋, 郭思琦, 陈帆, 等. 水泥基粘结剂的力学性能与泛霜抑制性能研究[J]. 西安建筑科技大学学报(自然科学版), 2015, 47(1): 103-107.
SONG Xuefeng, GUO Siqi, CHEN Fan, et al. Research on the mechanical properties and efflorescence resistance of tile adhesive based on cementitious materials[J]. Journal of Xi’an University of Architectural Science and Technology (Natural Science Edition), 2015, 47(1): 103-107.
[23] GARILLI M, CARMELLO D, CREMASCHI B, et al. Copper species in CuCl2/γ-Al2O3catalyst for ethylene oxychlorination[J]. Studies in Surface Science and Catalysis, 2000, 130: 1817-1822.
[24] LEOFANTI G, PADOVAN M, GARILLI M, et al. Alumina-supported copper chloride: 1. characterization of freshly prepared catalyst[J]. Journal of Catalyst, 2000, 189(1): 91-104.
[25] 李超. 稀土元素(La, Ce)改性CuCl2基催化剂上乙烷氧氯化制氯乙烯的研究[D]. 长春: 吉林大学, 2012: 41-42.
LI Chao. Study on rare earth element (La, Ce) modified CuCl2-based catalysts for ethane oxychlorination to vinyl chloride[D]. Changchun: Jinlin University, 2012: 41-42.
[26] 吕学举, 刘杰, 周广栋, 等. CuCl2-KCl-LaCl3/γ-Al2O3对乙烷氧氯化反应的催化性能[J]. 催化学报, 2005, 26(7): 587-590.
LYU Xueju, LIU Jie, ZHOU Guangdong, et al. Catalytic oxychlorination of ethane over CuCl2-KCl-LaCl3/ γ-Al2O3[J]. Chinese Journal of Catalysis, 2005, 26(7): 587-590.
[27] WATTIMENA F, SACHTLER W M H. Catalyst research for the shell chlorine process[J]. Studies in Surface Science and Catalysis, 1982, 7: 816-827.
[28]SHI A J, WANG X Q, YU T, et al. The effect of zirconia additive on the activity and structure stability of V2O5/WO3-TiO2ammonia SCR catalysts[J]. Applied Catalysis B: Environmental, 2011, 106: 359-369.
The honeycomb CuCl2/SCR catalyst: preparation and its mercury removal performance
CHENG Guangwen, YANG Song, LIU Wenjuan, GUO Zhongxu, FU Kangli
(Xi’an Thermal Power Research Institute Co., Ltd., Xi’an 710054, China)
A honeycomb catalyst for mercury removal, CuCl2/SCR, was prepared. The preparation of CuCl2/SCR was similar to that of the commercial SCR catalyst, the differences lied in the addition manner of active component and the pH adjusting agent. A composite powder was firstly obtained through loading CuCl2in γ-Al2O3in the presence of KCl, and then the powder as an integral component was added into the mixing process. Meanwhile, choosing tetramethyl ammonium hydroxide as the pH adjusting agent instead of aqueous ammonia. These changes helped to obtain a honeycomb CuCl2/SCR catalyst. Moreover, the catalytic oxidation performance of the above preparation process and catalyst on elemental mercury in real flue gas was also studied. The results showed that, in real flue gas, the CuCl2/SCR catalyst showed a catalytic efficiency of about 75% for Hg0 oxidation. The aid agent KCl could prevent CuCl2from volatilizing at high temperature in the catalyst, where CuCl2existed in the form of skeleton copper and surface copper. The two kinds of copper both showed catalytic activity for Hg0 oxidation. The use of tetramethyl ammonium hydroxide could avoid the deactivity of CuCl2/SCR resulting from the copper ammonia reaction.
industrial boiler, honeycomb catalyst, mercury removal, preparation, real flue gas, catalyze, oxidation efficiency, salting out
Science and Technology Project of China Huaneng Group Co., Ltd. (HNKJ18-H06, HNKJ18-H07)
TQ534.9
A
10.19666/j.rlfd.201907151
程广文, 杨嵩, 刘文娟, 等. 蜂窝状CuCl2/SCR催化剂制备及其脱汞性能[J]. 热力发电, 2019, 48(12): 52-57. CHENG Guangwen, YANG Song, LIU Wenjuan,et al. The honeycomb CuCl2/SCR catalyst: preparation and its mercury removal performance[J]. Thermal Power Generation, 2019, 48(12): 52-57.
2019-07-04
中国华能集团有限公司总部科技项目(HNKJ18-H06,HNKJ18-H07)
程广文(1980),男,博士后,高级工程师,主要研究方向为火电厂烟气净化技术,chengguangwen@tpri.com.cn。
(责任编辑 杨嘉蕾)

