分叉型腹主动脉覆膜支架可疑不良事件相关数据分析
王长燕 吕 杰②③*
为加强医疗器械不良事件监测和再评价,及时、有效控制医疗器械上市后风险,保障人体健康和生命安全,我国已于2019年1月1日起施行《医疗器械不良事件监测和再评价管理办法》(国家市场监督管理总局令第1号),通过发现和识别上市后医疗器械存在的不合理风险,对存在安全隐患的医疗器械采取有效的控制措施,提高产品的安全性,防止伤害事件的重复发生和蔓延,从而保障公众用械安全[1-2]。
美国食品药品监督管理局(Food and Drug Administration,FDA)制造商和用户设备实践(manufacturer and user facility device experience,MAUDE)数据库是FDA针对上市后医疗器械不良事件监测的重要工具之一[3-4]。MAUDE数据库面向公众免费开放检索,从中可获取医疗器械上市后的不良事件信息。本研究通过对美敦力爱尔兰MEDTRONIC,IRELAND公司生产的分叉型腹主动脉覆膜支架植入所致可疑不良事件报告进行统计分析,为该器械的临床合理、安全应用提供有效信息。
1 分叉型腹主动脉覆膜支架植入研究资料与方法
登录FDA MAUDE数据库高级检索模式,在Manufacturer信息框中输入“Medtronic Ireland”,在Brand Name信息框中输入“Endurant IIs Bifurcated Stent Graft”,在Data Report Received by FDA信息框中输入“07/01/2017to12/31/2018”,即可检索得到2017年7月1日至2018年12月31日该数据库收集到的关于美敦力爱尔兰公司生产的分叉型腹主动脉覆膜支架植入致可疑医疗器械不良事件。
本研究根据上述检索方法,获得美敦力爱尔兰公司生产的分叉型腹主动脉覆膜支架植入致可疑医疗器械不良事件219例,并对其不良事件报告进行翻译,对事件描述进行分析,分别按故障类型、事件类型和报告日期进行分类统计[5-9]。
2 分叉型腹主动脉覆膜支架植入研究结果
2.1 不良事件器械故障类型
对219例Endurant IIs分叉型腹主动脉覆膜支架植入致不良事件报告中的器械故障类型进行统计分析,除去4例故障原因描述不清,215例报告中泄漏出现最多,为104例(占48.37%),其次是无确定的设备或使用问题45例(占20.93%),装置错位27例(占12.56%),另有11例(占5.10%)为设备内闭塞,见表1。
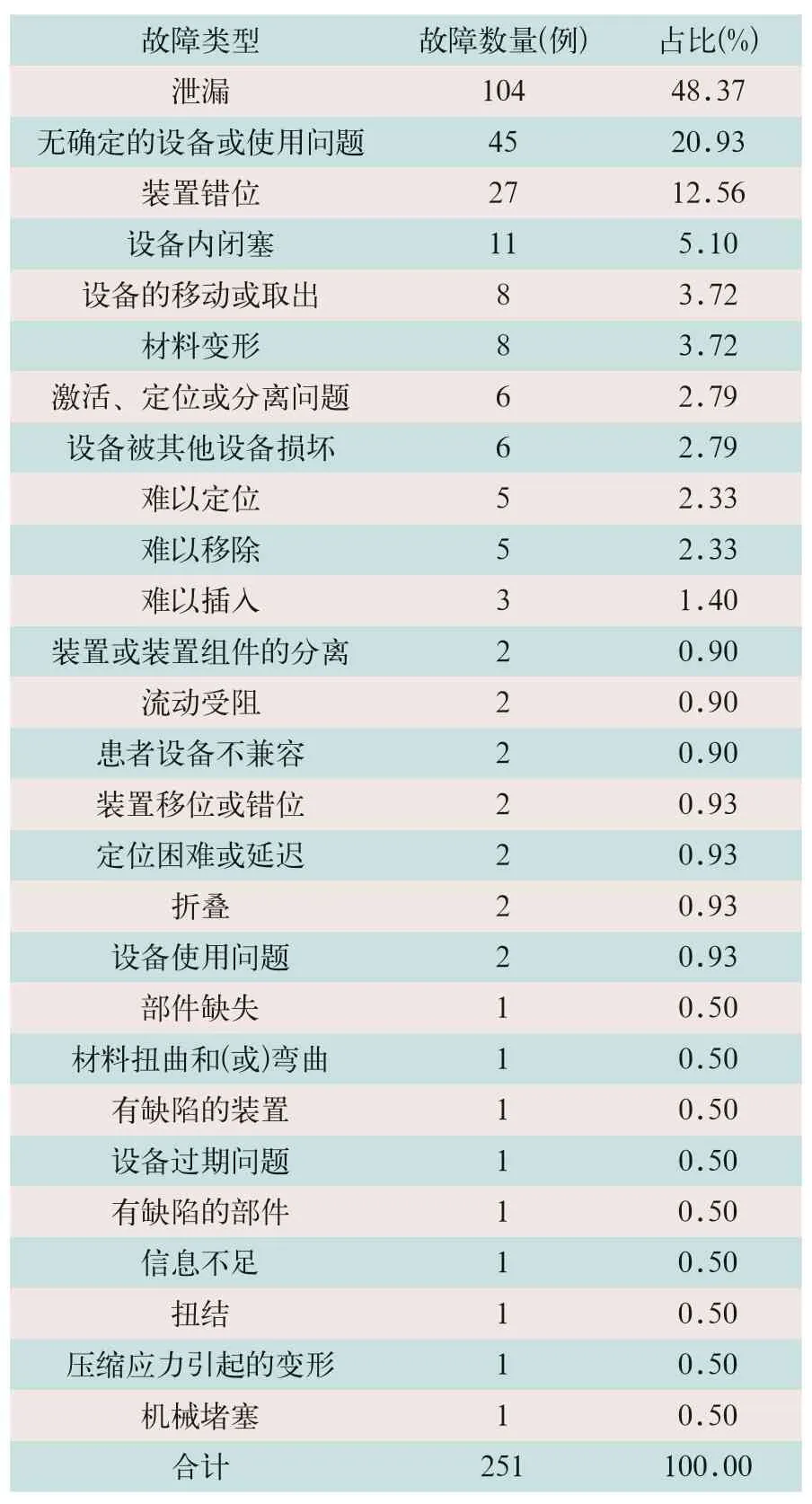
表1 215例不良事件器械故障类型统计
2.2 不良事件人身伤害事件类型
219例不良事件中造成人身伤害的不良事件类型有3类,分别是死亡、损伤和未对人身产生影响,其中,导致损伤的事件类型数量最多,为154例,占总事件的70.3%,见表2。
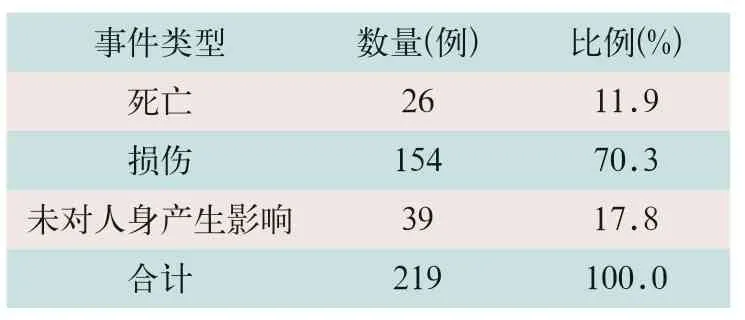
表2 219例不良事件人身伤害事件类型统计
2.3 不良事件报告日期
检索到219例不良事件在每个月份的分布较为均匀,其中,2018年10月接收到不良事件报告数量最多,为23例,见图1。
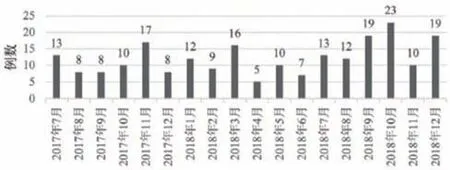
图1 不良事件月报告统计
3 分叉型腹主动脉覆膜支架植入不良事件分析
3.1 不良事件临床表现
分叉型腹主动脉覆膜支架植入常见不良事件报告中所涉及的不良事件主要有:①活动性出血,且无法确定出血来源;②器官栓塞;③动脉破裂;④内漏;⑤扭曲和钙化;⑥肢体疼痛;⑦尿中有血,痔疮出血;⑧恶心,呕吐,腹胀等。其中IA型内漏发生频率较大。
3.2 常见不良事件分析
3.2.1 内漏原因分析
常见的I型内漏形成与血管病变情况、支架的种类等因素有关。有研究显示,当颈部血管发生形态明显异常、有严重的附壁血栓及钙化等类似情况时,将会使锚定区贴合不良从而引起支架脱位,治疗的关键在于能否选择合适型号的支架,使支架与锚定区紧密贴合[10]。
3.2.2 血管栓塞原因分析
血管栓塞多发于早期支架内血栓,常见情况为支架的贴壁不良、扩张不全、过长以及置入多个串联支架和支架置入术后残余狭窄,其中,支架贴壁不良是发生支架内血栓的最常见因素。①开口病变、分叉病变、成角及钙化病变等情况下,若在术中选择直径偏小的支架或支架扩张压力不足和(或)充盈时间不够均会导致支架贴壁不良;②在支架过长情况下,置入多个串联支架,会导致血管内皮损伤,使内膜下组织和胶原暴露过多,从而激活血小板和纤维蛋白附着及沉积导致形成血栓和血栓瀑布效应;③斑块脱落、碎屑样物质进入远端血管从而引起弥漫性血管内凝血并向近端延伸,最终形成支架内血栓;④远端血管持续性痉挛或严重狭窄也可引发支架内血栓[11]。
3.2.3 肢体疼痛原因分析
可能是植入支架手术过程中导丝导管对血管壁有一定的损伤,导致患者术后肢体疼痛。
3.3 不良事件控制
随着科技的进步,分叉支架应用日趋广泛,也因此使许多患者恢复了健康,故要更加注重避免IIs分叉支架不良事件的出现[12]。
3.3.1 生产企业职责
要及时吸取不良事件教训,努力改进产品性能和研发新产品;要加强对企业人员的培训,通过更加详细的说明书告知医务人员产品的适用症状及操作要点和注意事项,保证支架的安全使用,减少不良事件发生。
3.3.2 临床医务人员使用
分叉支架使用前认真研读使用说明书,明确分叉支架类型及注意事项等;医务人员要提升自身技术水平和专业技能,手术过程中对支架的使用尽量地熟练且尽最大可能减少手术对患者身体的伤害。
4 结语
本研究通过检索FDA MAUDE数据库,对美敦力爱尔兰MEDTRONIC,IRELAND公司生产的Endurant IIs分叉型腹主动脉覆膜支架进行植入所致不良事件报告的统计分析,其器械故障的主要表现为泄漏,对患者产生的影响主要是造成损伤。基于此,进一步分析了引起内漏、血管栓塞和肢体疼痛的可能原因,提出相应策略,为临床合理、安全运用该器械提供参考。

