菠菜中磷含量的测定
赵俊英
(陇东学院 化学化工学院,甘肃 庆阳 745000)
目前磷作为食品中的一种常量元素,主要以核蛋白、磷蛋白、磷酯等有机态存在[1]。磷对生命体有着不可低估的作用,因此准确测定蔬菜中磷的含量和存在形式显得尤为重要。常见的测定磷含量的方法有钼蓝比色法[2]、钒钼黄比色法[3]、气相色谱法[4]、原子吸收光谱法[5]、生化分析仪法[6]等测定样品中磷的含量。与钼蓝比色法相比,钒钼黄比色法适用范围较广,但精密度差;气相色谱法主要用于有机磷农药残留的检测。相比而言,大多数方法需要进行繁琐的样品前处理,耗时间,且仪器价格昂贵,需专业人员维护,成本过高,不适用于普通的实验测定。而钼蓝分光光度法可以弥补上述方法的缺点,是一种成本低、快速、简单、可用于简单实验的分析方法。
实验室一般采用微波消解[7]、湿法消解[8]和干法消解[9]进行样品前处理,微波消解需要的实验设备较昂贵,而干法消解耗时较长,用量大且易损失;湿法消解用量少、操作简便,在短时间内就能消解完全,因此本文选择湿法消解进行样品前处理,使有机磷转化为磷酸盐形式。然后在酸性条件下,使之与钼酸铵反应生成磷钼酸铵,被还原剂还原成亮蓝色的配合物-钼蓝的原理,测定其吸光度,进而测定试样中磷的含量。
1 实验部分
1.1 试剂与仪器
721型分光光度计(上海第三分析仪器厂)、菠菜(市售)、钼酸铵(AR)、对苯二酚(AR)、亚硫酸钠(AR)、磷酸二氢钾(AR)、浓硫酸、浓硝酸、30%H2O2。
1.2 样品处理及试剂配制
准确称取1 g的菠菜样品于150 mL锥形瓶中,分别加入5 mL的浓硝酸和浓硫酸,加热至冒烟,然后待冷却后加入5 mL 30%H2O2,继续缓慢加热,重复以上的步骤直至瓶内不再冒烟,溶液呈无色透明或淡黄色,冷却后加入5 mL的硝酸(1∶1)溶液,加热使酸彻底分解,用蒸馏水稀释至50 mL的容量瓶中待测,用同样的方法制备空白溶液。
磷标准储备溶液:精确称取在105℃下干燥后的磷酸二氢钾0.4394 g用水溶解并稀释至100 mL,此溶液每毫升含磷1000 μg。
磷标准使用溶液:用移液管准确移取10.00 mL磷标准储备溶液至100 mL容量瓶中,加水稀释至刻度,混匀,此溶液磷的浓度是100.0 μg·mL-1;再用移液管准确移取100.0 μg·mL-1磷标准溶液10.00 mL至100 mL容量瓶中,加水稀释至刻度混匀,此溶液磷的浓度为10.00 μg·mL-1,相当于0.01 mg·mL-1[10]。
2 结果与讨论
2.1 波长的确定
准确吸取磷标准使用液0.00、1.00 mL分别置于25 mL的比色管中。依次加入2.00 mL的钼酸铵(50 g·L-1),摇匀,静置几秒后,分别加入1.00 mL亚硫酸钠(20 g·L-1)和1.00 mL的对苯二酚(5 g·L-1),加水至刻度摇匀,从波长630 nm处开始,隔10 nm测一次数据,见表1。以波长为横坐标,吸光度为纵横坐标作图,见图1。

表1 不同波长下的吸光度
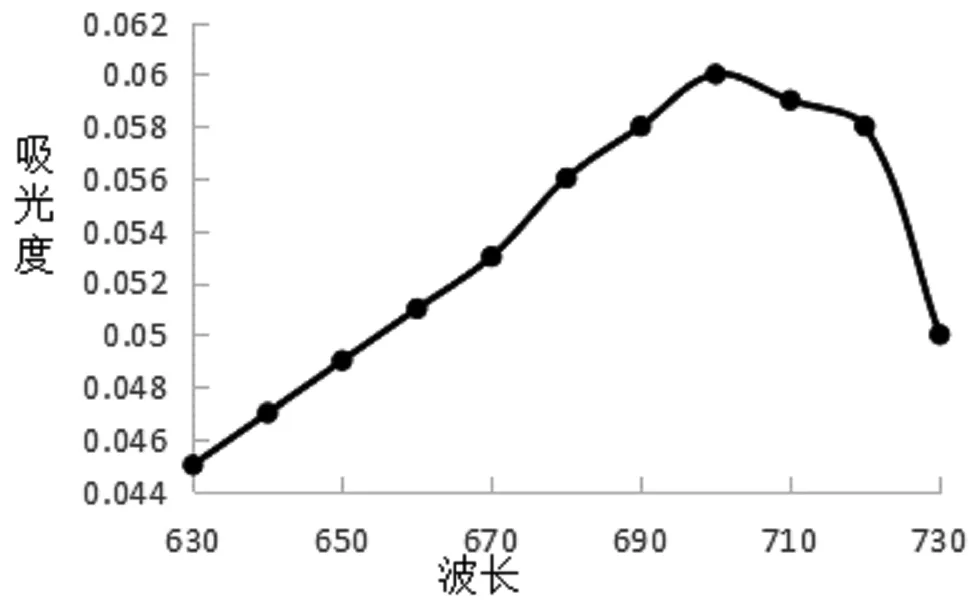
图1 波长与吸光度的关系
由图1可知,随着波长增加,吸光度逐渐增加,在波长700 nm处吸光度最大,因此本文确定测定波长为700 nm。
2.2 显色温度和显色时间的确定
当室温低于15℃时,由于试样中总磷含量浓度较低,分子间稀疏,低温时分子运动缓慢,有效碰撞的概率低,使得显色时间较长[10],因此本实验采取在20~30℃的水浴中加热进行,达到缩短显色时间的目的。取磷标准使用液0.00、1.00 mL在水浴中分别静置10、15、20、25、30、35 min后测定吸光度,数据见表2,根据表2数据以显色时间对吸光度作图,见图2。之后在相同温度下,缩小时间的测定范围,分别静置20、22、24、26、28、30、32 min后测定,数据见表3,据表3数据以显色时间对吸光度作图,见图3。

表2 显色时间对吸光度的影响
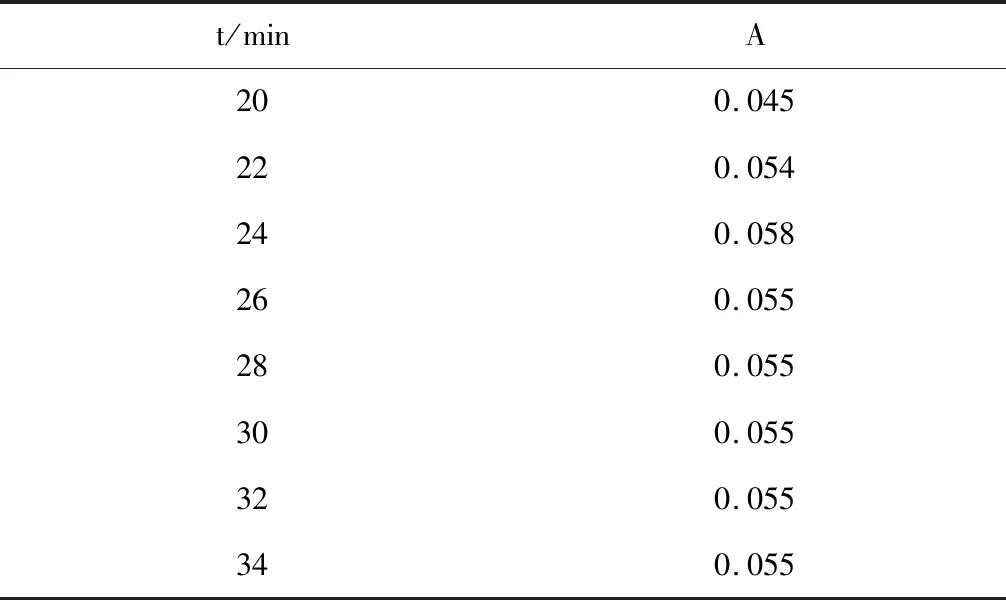
表3 显色时间对吸光度的影响
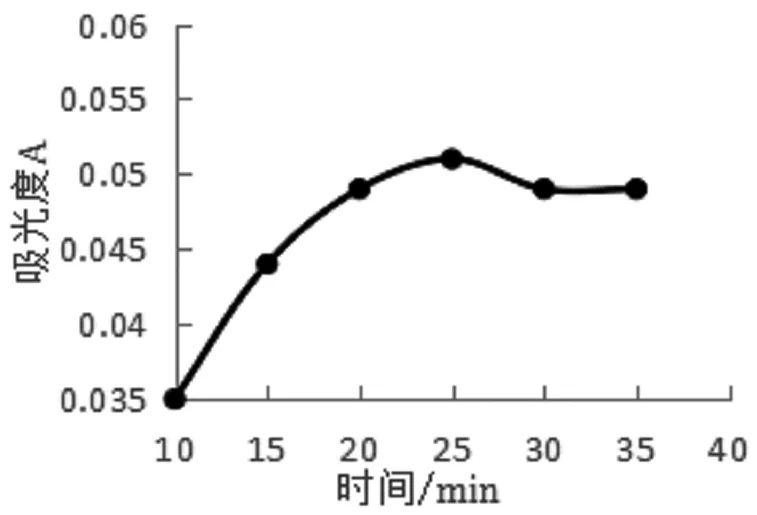
图2 显色时间和吸光度的关系
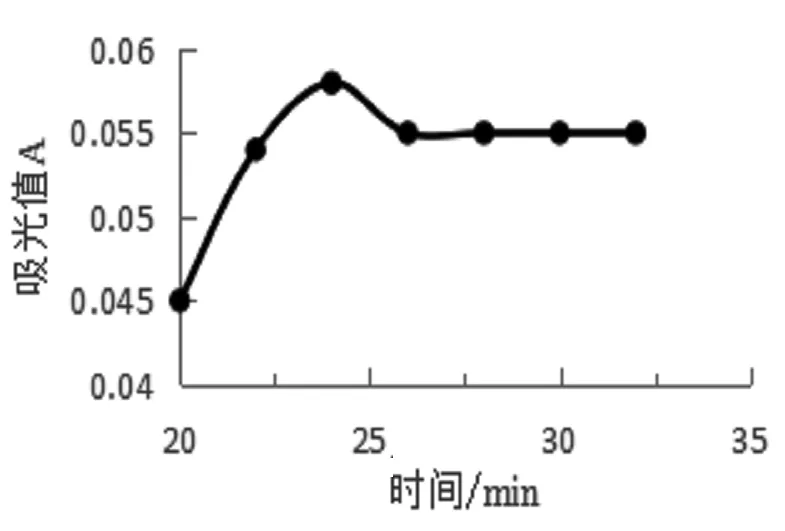
图3 显色时间和吸光度的关系
由图2和图3可知,随显色时间的增加,吸光度逐渐增加,在24 min时吸光度最大,因此本文选择在水浴中静置24 min之后测定吸光度。
2.3 还原剂用量的确定
取十只25 mL比色管,用移液管移取磷标准液1.00 mL,加入2.00 mL钼酸铵,静置几秒后,分别加入还原剂0.20、0.40、0.60、0.80、1.00、1.20、1.40、1.60、1.80、2.00 mL,然后加水至刻度充分摇匀,静置24 min后以不加还原剂的空白溶液做参比,测定数据见表4,根据表4数据以还原剂对吸光度作图,见图4。由图4可知,随着还原剂用量的增加,吸光度逐渐增大,之后逐渐减小,在1.80 mL时吸光度最好,故本文选用1.80 mL还原剂进行测定,在实验过程中还原剂必须现配现用,避免配置时间过长而引起还原失效和溶液浑浊。

表4 还原剂用量对吸光度的影响
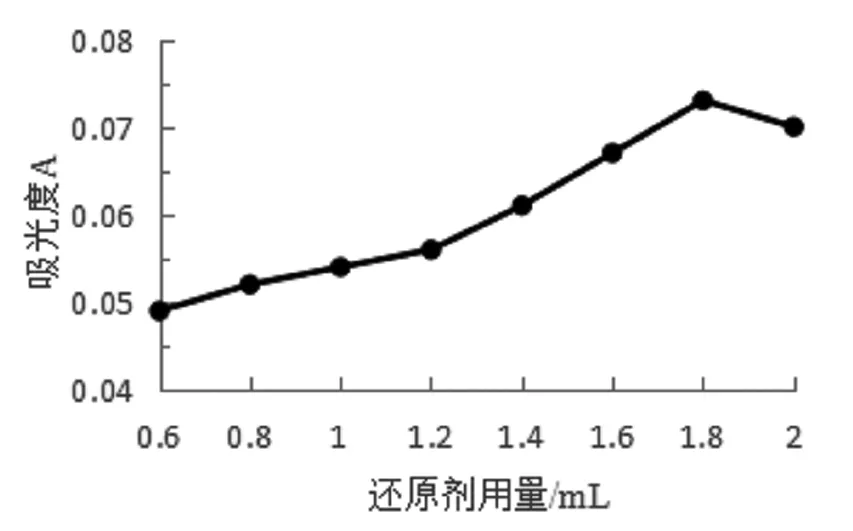
图4 还原剂用量与吸光度的关
2.4 显色剂用量的确定
取六只25 mL比色管,用移液管移取磷标准溶液1.00 mL,分别加入钼酸铵1.00、1.50、2.00、2.50、3.00 mL,摇匀,静置几秒后,分别加入1.80 mL亚硫酸钠和1.80 mL对苯二酚,摇匀,加水至刻度,静置24 min后,空白液参比调零,在波长700 nm处测定吸光度,数据见表5,据表5数据以钼酸铵为横坐标,吸光度为纵坐标作图,见图5。
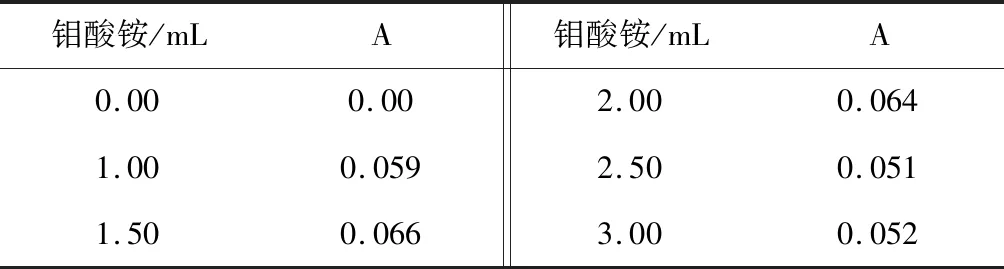
表5 显色剂用量对吸光度的影响
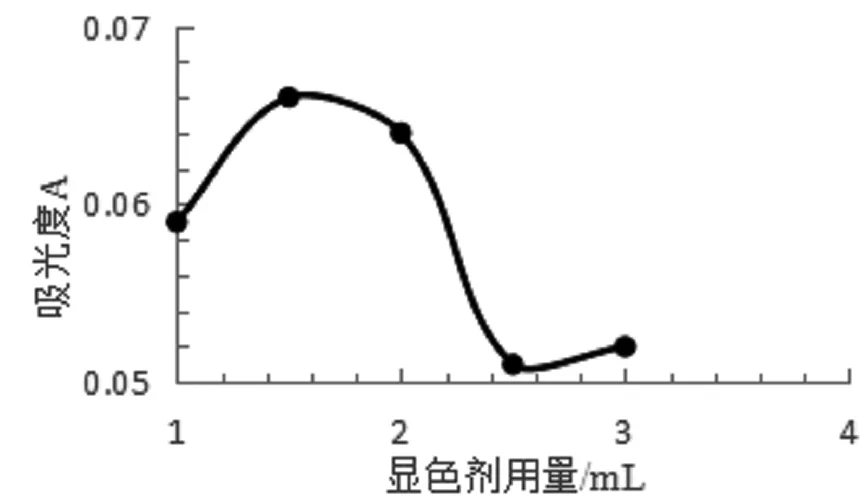
图5 显色剂用量与吸光度的关系
由图5可知,当显色剂用量为1.50 mL时,吸光度最大,显色剂加入过多或过少都会使吸光度降低,因此本文确定显色剂用量为1.50 mL。
2.5 磷标准曲线的绘制
准确移取磷标准使用液0、1.00、2.00、3.00、4.00、5.00、6.00 mL,分别置于25 mL的比色管中,依次加入1.5 mL的钼酸铵,摇匀,静置几秒后,分别加入1.8 mL亚硫酸钠和1.8 mL对苯二酚摇匀,加水至刻度,静置24 min后,空白液参比调零,在波长700 nm处测定吸光度,数据见表6,以磷标准使用液的体积为横坐标,以吸光度为纵坐标,绘制磷标准曲线,见图6。其线性回归方程为:y=0.0506x-0.0069,R2=0.9989,线性关系良好。
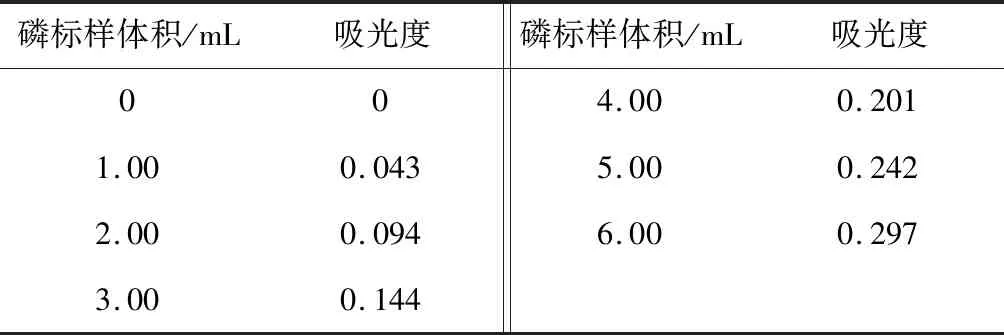
表6 体积与吸光度的关系
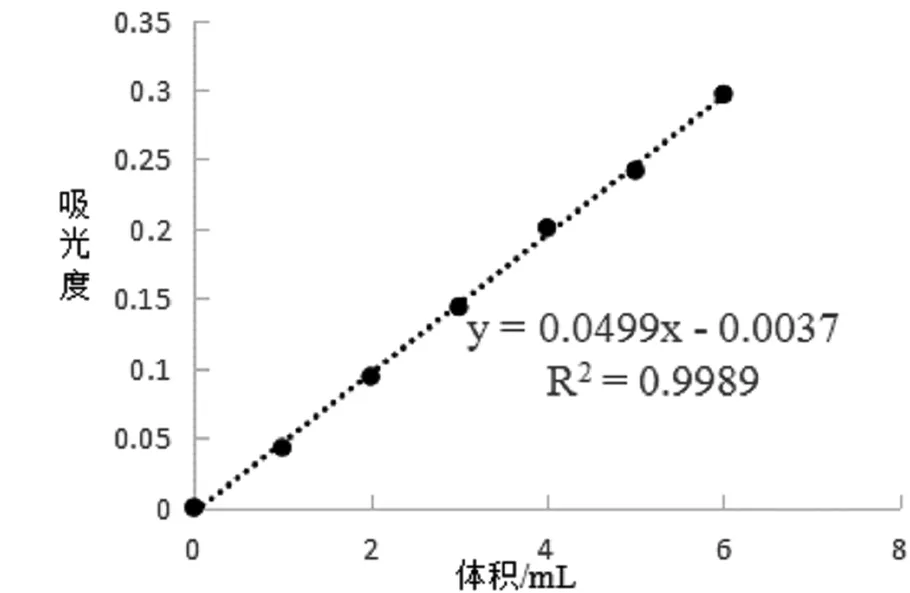
图6 磷标准曲
2.6 样品的测定
准确移取试样测试液2.00 mL及同量的空白溶液分别置于25 mL比色管中,依次加入1.50 mL钼酸铵摇匀,静置几秒,加入1.80 mL亚硫酸钠、1.80 mL对苯二酚加水至刻度摇匀,水浴静置24 min,后,在700 nm波长处测定样品的吸光度并计算磷含量。测定时应注意尽量按浓度从低到高的顺序测定,减少因磷钼蓝在比色皿上的吸附而产生的误差。数据见表7。

表7 试样中磷含量
测定结果表明,菠菜中磷的平均含量为597.325 mg·kg-1。本实验进一步证实了分光光度法是测定蔬菜中磷等微量元素的有效方法,同时该方法可作为蔬菜质量检验的参考方法。
2.7 加标回收率
在样品中分别添加不同含量的磷标准液,按本实验方法法每组平行测定3次,数据见表8,通过计算可知,回收率在98%~100%之间,说明方法准可靠。
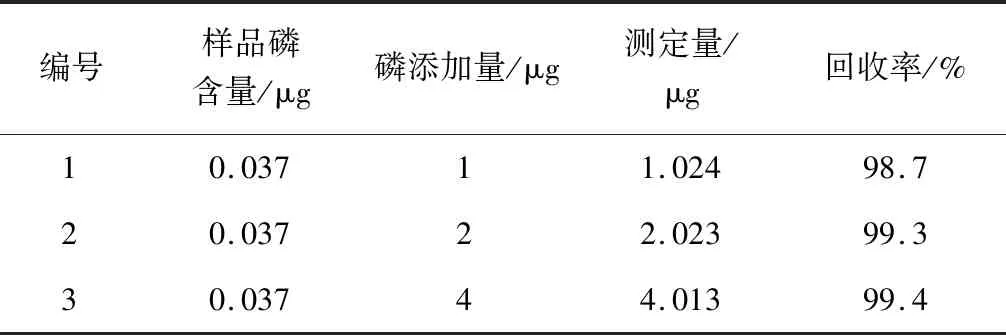
表8 回收率实验结果(n=3)
3 结语
本文采用钼蓝分光光度法,通过对波长、显色时间、显色剂和还原剂等条件的优化,在波长700 nm处加入钼酸铵1.50 mL、还原剂1.80 mL测定了菠菜中磷的含量,结果显示菠菜中磷的平均含量为597.325 mg·kg-1。该方法具有操作简单、试剂用量少、消解速度快、灵敏度高、选择性好、仪器设备简单等优点,是一般实验室测定微量元素的一种行之有效的方法。该方法对进一步研究蔬菜食用价值有一定的参考价值,为磷含量的测定提供了一定的理论依据。

