药物涂层球囊PTA治疗下肢动脉硬化闭塞症
谈洪统,李 威,郭欢庆,满文玲,陈 薇,杨 坡
(哈尔滨医科大学附属第四医院介入血管外科,黑龙江 哈尔滨 150000)
下肢动脉硬化闭塞症(lower extremity atherosclerotic occlusive disease, LEAOD)的症状与血管腔残余内径相关,早期症状多为畏寒、间歇性跛行,逐渐发展为静息痛、局部甚至大范围皮肤溃烂[1]。目前我国约有2 000万LEAOD患者,以老年男性居多,其在70岁以上人群中的发病率约为20%,在70岁以下人群中为3%~10%[2-3]。经皮腔内血管成形术(percutaneous transluminal angioplasty, PTA)是临床治疗LEAOD的首选方法[4-5],其中传统单纯球囊扩张PTA手术成功率较高,但后期再狭窄率高达30%~60%[6]。自2016年7月国内首款外周血管药物球囊经批准上市以来,药物洗脱球囊逐渐应用于临床,降低了PTA术后再狭窄率。本研究探讨药物涂层球囊PTA治疗LEAOD的临床效果。
1 资料与方法
1.1 一般资料 选取2018年3月—2019年3月我院收治的43例LEAOD患者(43条患肢),男25例,女18例,年龄40~80岁,平均(56.5±15.4)岁,将其随机分为观察组(21例)和对照组(22例)。观察组中男13例,女8例,平均年龄(63.9±11.3)岁,吸烟18例,糖尿病13例,高血压14例;对照组中男15例,女7例,平均年龄(64.9±9.9)岁,吸烟19例,糖尿病15例,高血压13例。
纳入标准:①一侧下肢病变、对侧下肢正常;②年龄40~80岁;③患侧下肢血管无手术史;④患侧股浅动脉狭窄程度>50%或闭塞;⑤无充盈缺陷;⑥病变段远端至足之间的血管可见血流。排除标准:①存在介入手术禁忌证;②血肌酐>200 μmol/L;③对阿司匹林、紫杉醇及对比剂等过敏;④术前1个月内发生脑出血或其他部位严重出血;⑤预计生存期小于本次研究设定的最长随访期(180天)。
1.2 仪器与方法 采用Philips Brilliance大孔径64层螺旋CT及Philips FD20 DSA机。所有患者术前均接受下肢动脉CTA检查,以明确靶动脉病变部位及长度,之后均接受PTA治疗。根据影像学检查结果决定穿刺入路,其中患侧腘动脉逆行穿刺15例、患侧股动脉顺行穿刺9例、健侧股动脉穿刺19例。注射对比剂明确靶动脉后,应用不同型号亲水性涂层导丝反复尝试,直至导丝进入远端真腔;交换适当型号的普通球囊,并对狭窄或闭塞部位进行预扩张。对观察组以直径与参考血管直径相同的药物球囊再次扩张靶血管病变部位(药物球囊范围超出病变血管段两端各1 cm,扩张时间 3 min);对照组在相同条件下以普通球囊再次扩张靶血管病变部位。复查造影,若病变部位恢复血流供应、残余狭窄<30%,则认为扩张满意;交换血管缝合器以缝合血管,不能使用缝合器时,则徒手压迫止血、包扎。患者出院后予以口服二联抗凝药物进行序贯治疗[7]。
1.3 效果评价与随访 2组术前及术后7天均评估Fontaine分期;分别于术前及术后1、3、6个月统计靶动脉段股浅动脉血管内径、再狭窄率(再狭窄诊断标准:下肢动脉CTA或DSA示靶血管在随访期内狭窄程度>50%甚至再闭塞[8])及踝肱指数[9](ankle brachial index, ABI)(ABI=胫后动脉或胫前动脉收缩压/肱动脉收缩压);统计术后6个月时靶动脉段股浅动脉血管狭窄率。
1.4 统计学分析 采用SPSS 22.0统计分析软件。符合正态分布的计量资料以±s表示,多组间比较采用方差分析,两两比较采用LSD-t检验;计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2组患者性别(χ2=0.186,P=0.665)、年龄(t=0.978,P=0.333)、吸烟(χ2=1.850,P=0.173)及并发糖尿病(χ2=0.186,P=0.665)、高血压(χ2=0.263,P=0.607)差异均无统计学意义。
43例患者均顺利完成PTA,术后均给予扩血管、止痛、抗凝等治疗,均未出现球囊扩张爆破、血肿、动脉破裂等并发症,截止随访终点均未出现手术相关死亡。
2组患者术后7天Fontaine分期均较术前降低(P均<0.05),见表1。
观察组术后1、3、6个月靶动脉段股浅动脉内径均大于对照组(P均<0.05),再狭窄率均低于对照组(P均<0.05);术后1个月时,2组ABI差异无统计学意义(P>0.05),术后3、6个月观察组ABI均大于对照组(P均<0.05),见表2及图1、2。
术后6个月时,观察组14例靶动脉段股浅动脉血管狭窄率<30%、4例30%~50%、3例>50%(无100%者),对照组2例狭窄率<30%、10例狭窄率30%~50%、10例>50%(2例100%),组间比较差异有统计学意义(χ2=15.829,P=0.001),见表3。

表1 2组手术前后Fontaine分期比较[例(%)]

表2 2组靶动脉段股浅动脉内径、术后再狭窄率、ABI指数比较
注:*:与对照组同时间点比较,P<0.05

表3 2组术后6个月靶动脉段股浅动脉血管狭窄率比较[例(%)]
3 讨论
LEAOD的病理基础是下肢动脉血管壁出现粥样硬化斑块,引起血流动力学改变等并发症,导致下肢动脉管腔逐渐变窄甚至闭塞,患者从无明显不适到行走距离逐渐缩短、疼痛等,最终可因下肢无血流供应而危及下肢功能。重度下肢缺血预后不良,死亡率高,截肢率达30%左右[10-11]。目前治疗LEAOD的主要方法包括PTA、支架植入术、导管溶栓术、SilverHawk斑块切除术、激光血管成形术及超声消融术等,其中PTA和支架植入术因手术成功率高、术后并发症发生率及病死率低等成为目前治疗LEAOD的首选方法。导管溶栓术主要适用于血管腔已有狭窄或闭塞基础上新发血栓患者;SilverHawk斑块切除术、激光血管成形术及超声消融术目前临床尚未广泛应用[12]。但下肢PTA和支架植入术后再狭窄率仍较高,如何降低术后再狭窄率成为重要临床问题之一。
既往研究[13]提示,相较于普通球囊,使用药物球囊扩张PTA可降低术后再狭窄率。药物球囊表面覆盖一层抑制血管内皮细胞增殖的药物,可有效抑制血管内膜增厚,在抑制再狭窄发生的同时降低支架使用率,缩短治疗时间。本研究采用紫杉醇药物涂层球囊行PTA,并与普通球囊对比,观察药物涂层球囊PTA治疗LEAOD的临床效果,结果显示术后1、3、6个月,观察组靶动脉段股浅动脉血管内径维持度较对照组更理想,再狭窄率更低,提示药物球囊的疗效相较于普通球囊更好。术后1个月2组ABI差异无统计学意义,术后3、6个月观察组ABI均高于对照组,考虑在术后下肢动脉血供恢复的前提下,药物球囊PTA血供维持更稳定;观察组术后6个月ABI与术前差异较大,而普通球囊PTA术后6个月ABI与术前无明显差异,提示后者术后血供维持度随时间延长降幅明显,即药物球囊较普通球囊在维持血供方面具有优势。术后6个月靶动脉段股浅动脉管腔狭窄率分段统计结果表明,无论是药物球囊还是普通球囊,靶动脉段股浅动脉在PTA后均可发生不同程度狭窄,但观察组狭窄程度更轻,多数患者狭窄率<30%,而普通球囊狭窄率多为30%~50%和>50%,提示药物球囊可有效预防再狭窄。

图1 患者男,67岁,观察组 A.术前双下肢动脉CTA示病变血管段; B.药物涂层球囊PTA术后造影示血运恢复、血流速度满意,未见明显血管夹层等并发症; C.术后6个月复查下肢动脉CTA见原病变段管腔内对比剂充盈满意,管腔内径、ABI(0.88)均理想,患者无明显不适
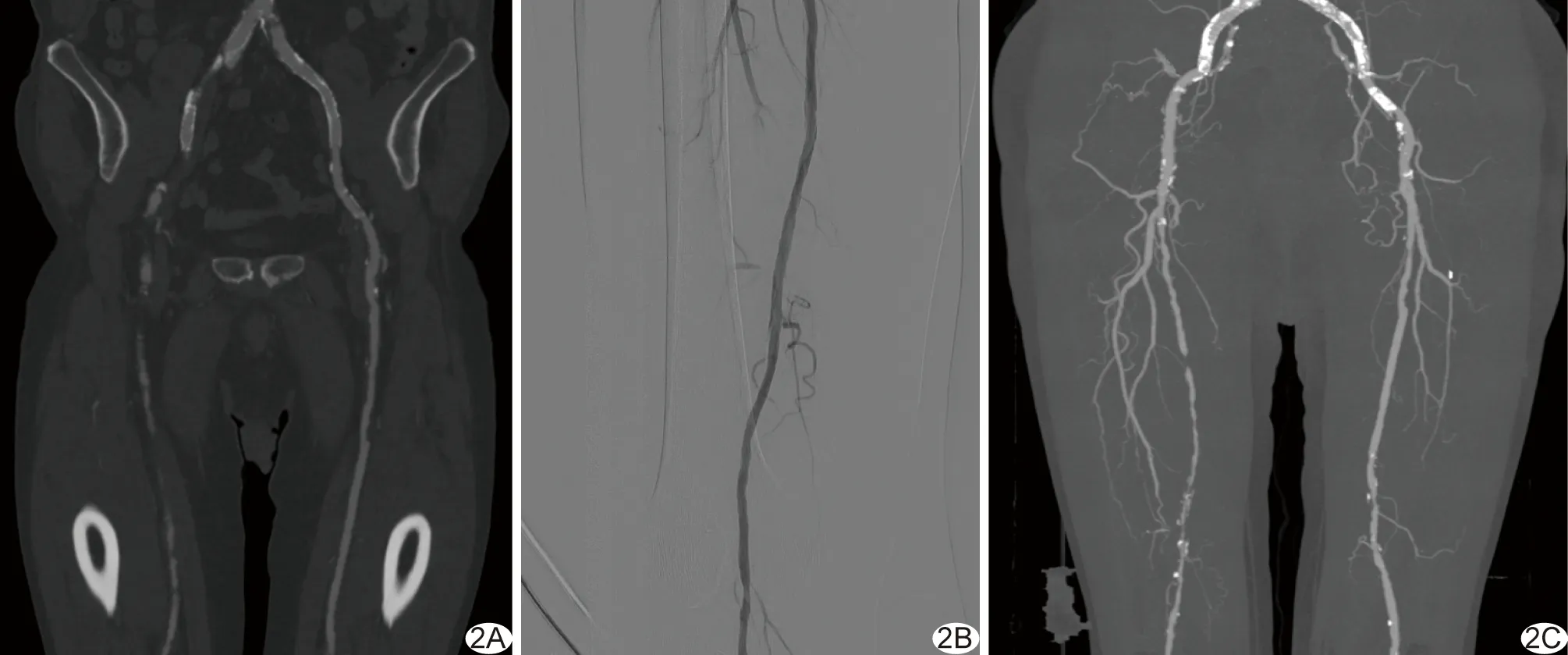
图2 患者女,59岁,对照组 A.术前双下肢动脉CTA示病变血管段; B.普通球囊PTA术后造影示血运恢复可,远端血流速度满意,可见轻度非血流限制性夹层,远端局部管腔内径轻度狭窄; C.术后6个月复查下肢动脉CTA,原病变段血管再次明显狭窄,管腔内径不一,伴多发节段性管腔闭塞,ABI为0.43,再次出现患肢静息痛等症状
综上所述,药物涂层球囊PTA治疗LEAOD安全、有效,能够降低再狭窄率,且近期疗效优于普通球囊。但由于存在药物涂层球囊来源厂家单一、研究样本量相对不足、随访周期较短等问题,有待进一步完善。

