动脉瘤形态学特征对胼周动脉瘤破裂的影响因素分析
翟晓东 李传捷 于嘉兴 任健 张鸿祺
胼周动脉瘤(pericallosal artery aneurysms,PAAs)是指前交通动脉以远的大脑前动脉及其分支部位的动脉瘤,也称大脑前动脉远端动脉瘤[1-2],仅占所有颅内动脉瘤的1%~9%[2-5],但其临床处理非常棘手[6-8]。临床中,PAAs以小尺寸动脉瘤多见,其破裂倾向远高于其他部位动脉瘤[5,9]。随着对颅内动脉瘤形态学研究的深入,目前认为,除外动脉瘤大小,其纵横比、尺寸比、长宽比及动脉瘤表面是否规则等形态学参数同样为预测颅内动脉瘤破裂风险的重要指标[10-14]。因此,本研究拟通过评估PAAs的形态学相关指标,探讨其具高破裂风险的形态学特征,以期为临床治疗提供参考。
1 对象与方法
1.1 对象
回顾性连续纳入2013年1月至2017年5月首都医科大学宣武医院神经外科收治的PAAs患者40例,其诊断参照文献[2,5]标准,且于术前经全脑血管DSA确诊。40例患者中,男17例,女23例;年龄16~77岁,平均(52±11)岁;单发PAAs为36例,多动脉瘤为10例,包括多发PAAs 4例(1例有3个,3例分别有2个);高血压病史21例,糖尿病史4例,冠心病史3例,既往脑血管病史16例;共有45个PAAs,其中位于大脑前动脉A2 主干、A3 主干、A4 主干、A3下段分叉、A3前段分叉、A3 上段分叉分别为7、3、1、4、24、6个,不规则PAAs共29个(64.4%)。根据PAAs是否破裂,将40例患者分为破裂组(22例)和未破裂组(18例)。破裂组中,22个单发PAAs;男8例,女14例;年龄37~77岁,平均(57±10)岁。未破裂组中,23个PAAs(单发14个,多发9个);男、女各9例;年龄16~71岁,平均(53±12)岁。两组患者性别、年龄及多发动脉瘤构成比的差异均无统计学意义(均P>0.05),具有可比性。本研究方案经首都医科大学宣武医院伦理委员会审核批准,患者或其家属签署了知情同意书。
1.2 纳入及排除标准
纳入标准:(1)入院后48 h内完成全脑血管DSA检查,并确诊为PAAs;(2)临床及影像学数据完整,且影像质量满足动脉瘤形态学参数的测量。排除标准:(1)创伤性、感染性、假性、夹层和梭形动脉瘤;(2)复发的PAAs。
1.3 评价方法
高血压病、冠心病和糖尿病的诊断标准分别参照《中国高血压防治指南(2010版)》[15]、《中国心血管病预防指南(2017)》[16]和《中国2型糖尿病防治指南(2010版)》[17]。
1.4 形态学参数测量及计算方法
为保证结果的准确性,形态学参数的测量与计算基于二维或三维旋转造影数据,并以动脉瘤数进行数据统计。由GE医用血管造影X射线机(IGS-630,通用电气公司,美国)进行影像数据采集,导入ST-PACS V3.138工作站(思创数码科技股份有限公司,中国),进行形态学参数的计算。
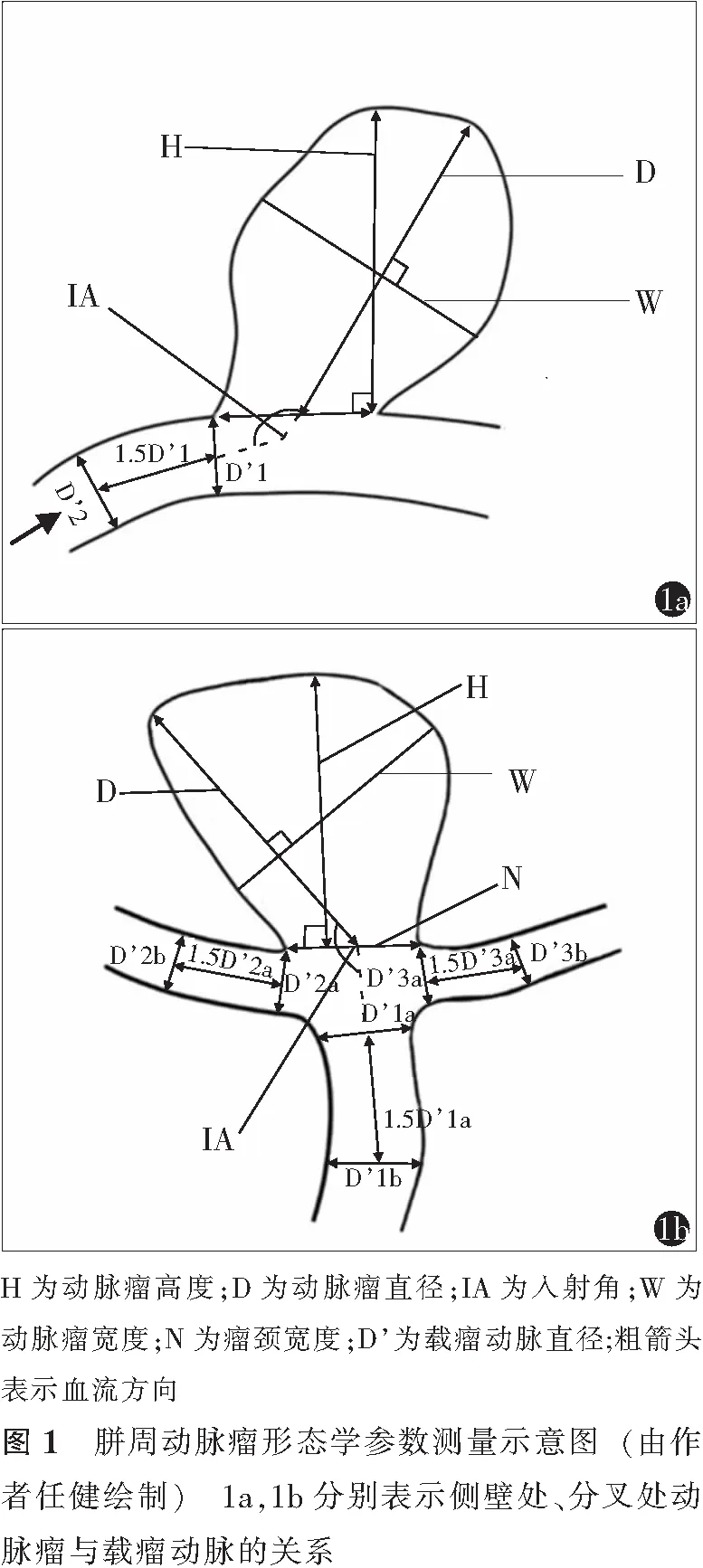
参照文献[11-13]选定动脉瘤形态学指标,包括动脉瘤的直径、高度、宽度,瘤颈宽度,载瘤动脉直径以及流入角度等,并进一步计算每个动脉瘤的纵横比、尺寸比和长宽比(动脉瘤直径/动脉瘤宽度)。纵横比分别采用两种计算方法,即动脉瘤高度/瘤颈宽度和动脉瘤直径/瘤颈宽度;尺寸比同样分别采用两种计算方法,即动脉瘤高度/载瘤动脉直径和动脉瘤直径/载瘤动脉直径[11]。根据动脉瘤位于侧壁处或分叉处,将载瘤动脉的直径分别进行计算,即侧壁处直径=(直径1+直径2)/2,其中直径2与直径1的距离为1.5倍直径1(图1a);分叉处直径=(直径1+直径2+直径3)/3,其中直径i=(直径ia+直径ib)/2,i分别指1、2、3,直径1b与1a、2b与2a、3b与3a的距离分别为1.5倍直径1a、2a、3a(图1b)[11,13]。将动脉瘤分叶、子囊和波浪状瘤顶定义为不规则动脉瘤[12-13],将PAAs按所处部位划分为A2主干、A3主干、A4主干、A3下段分叉、A3前段分叉和A3上段分叉动脉瘤[4]。胼周动脉瘤形态学参数的测量方法见示意图(图1)。
1.5 统计学分析

2 结果
2.1 一般资料比较
两组患者年龄、男性、多发动脉瘤和心脑血管疾病危险因素的差异均无统计学意义(均P>0.05)。见表1。
2.2 形态学特征比较
破裂组长宽比、不规则动脉瘤比例均高于未破裂组,组间差异均有统计学意义(均P<0.01);两组动脉瘤直径、高度、宽度、载瘤动脉直径、纵横比、入射角度、瘤颈、尺寸比的差异均无统计学意义(均P>0.05)。见表2。破裂组位于A2主干、A3主干、A4主干、A3下段分叉、A3前段分叉和A3上段分叉处的动脉瘤数分别为2、1、0、2、15、2个,A3前段分叉动脉瘤数比例为68.2%(15/22);未破裂组位于A2主干、A3主干、A4主干、A3下段分叉、A3前段分叉和A3上段分叉处的动脉瘤数分别为5、2、1、2、9、4个,A3前段分叉动脉瘤数比例为39.1%(9/23)。45个动脉瘤中,A3前段分叉处动脉瘤数占53.3%。两组位于A3前段分叉处动脉瘤数比例的差异无统计学意义(χ2=0.381,P=0.051)。

表1 破裂组与未破裂组胼周动脉瘤患者一般资料比较
注:a为t检验,b为χ2检验,c为连续修正检验,d为Fisher确切概率法;“-”表示无数据

表2 破裂组与未破裂组胼周动脉瘤形态学参数比较

组别瘤数(个)入射角(°)瘤颈(mm)x-±s长宽比不规则动脉瘤[个(%)]尺寸比(x-±s)H/D’D/D’破裂组22149±202.5±1.01.35±0.3620(90.9)3.5±1.83.7±1.8未破裂组23145±213.0±1.31.01±0.2209(39.1)3.3±2.33.4±2.6检验值-0.60a1.53a-3.85a8.01b-0.36a-0.39aP值-0.55a0.13a<0.01a0.005-0.72a-0.69a
注:a为t检验,b为χ2检验;H为动脉瘤高度,D为动脉瘤直径,N为瘤颈宽度,D’为载瘤动脉直径
2.3 PAAs破裂的形态学影响因素分析
计算45个PAAs的长宽比均值(1.18),以此为界定值将其转换为二分类变量(≤1.18定义为1,>1.18定义为2)。以PAAs破裂为因变量,将形态学参数单因素分析中长宽比(>1.18)、不规则动脉瘤纳入多因素Logistic回归分析,结果显示,长宽比值>1.18、不规则动脉瘤为PAAs破裂的独立危险因素。见表3。
3 讨论
PAAs位于大脑前动脉远端的大脑纵裂之间,小尺寸PAAs瘤体多生长于相对纤细的载瘤动脉之上,并且狭窄的手术操作空间和深远的微导管入路等因素,使得无论显微外科手术还是血管内介入治疗均存在较高的技术难度[8,18-20]。有研究表明,相较于其他部位的颅内动脉瘤,PAAs具有很高的破裂率(P=0.011)和术中再出血率(P=0.03),其破裂可进一步导致脑水肿、与周围脑组织黏连和血管痉挛等并发症,增加治疗的难度[2,5-7],并且其复发风险较高(P=0.0388)[9,21]。因此,探讨PAAs的形态学特征有重要意义。

表3 胼周动脉瘤破裂的形态学影响因素分析
动脉瘤的形态学特征是其破裂风险的重要预测因素之一[22],随着颅内动脉瘤尺寸的增大,破裂风险升高[12,23-24]。相对小尺寸动脉瘤的破裂风险同样不可忽视,因其可能具有更危险的形态特征和复杂的血流动力学关系,故动脉瘤大小并非唯一的形态学预测因素[12-14,24]。动脉瘤的长宽比、表面规则程度、纵横比和尺寸比等形态学因素可预测动脉瘤的破裂风险,是动脉瘤破裂风险相关形态学预测因素的补充[11,25-26]。
长宽比的比值越高表示动脉瘤相对越“细长”,进入瘤腔内的血流消耗的能量就越多,与之相对应的壁面切应力降低,使得动脉瘤的破裂风险增大[11,27]。本研究结果显示,单因素分析中破裂组PAAs的长宽比值高于未破裂组(P<0.01),提示破裂组PAAs的形态可能相对更“细长”;在多因素分析中,长宽比值>1.18导致PAAs破裂的风险是长宽比≤1.18的1.84倍(OR=1.84,95%CI:1.42~28.11,P=0.016),提示长宽比值增大,动脉瘤的破裂风险增大。本研究结果与文献报道一致。本研究显示,在45个动脉瘤中,A3前段分叉处(胼缘动脉与胼周动脉交界部位)动脉瘤数占53.3%,破裂组和非破裂组的比例分别为68.2%和39.1%(P=0.051)。上述结果可能由于大脑纵裂生长空间狭窄,以及胼周与胼缘动脉间分叉角度相对狭小,其共同作用使该部位的PAAs以相对“细长”的形态生长,组间的长宽比值差异有统计学意义。
本研究结果显示,破裂组形态不规则的PAAs比例高于未破裂组(90.9%比39.1%,P=0.005)。在不规则动脉瘤腔内血流动力学关系更为复杂,瘤壁退变不良可使动脉瘤壁表面不规律,易致血流不稳定,而使形态不规则的动脉瘤具有更高的破裂倾向[13,28-29]。本研究多因素分析结果显示,不规则动脉瘤是PAAs破裂的危险因素(OR=2.06,95%CI:1.66~37.11,P=0.009)。然而,也有研究表明,与颅内动脉瘤破裂前的影像学结果比较,动脉瘤破裂后的形态特征也可发生较大变化,可能由于血肿形成,使动脉瘤移位形成分叶状动脉瘤的形态[30]。但由于动脉瘤的发生、发展和破裂为动态过程,临床中较难获取动脉瘤破裂前瞬时的形态学特征。
有研究表明,纵横比和尺寸比是动脉瘤破裂风险的重要形态学预测指标[31-32]。纵横比是指动脉瘤深度与瘤颈的比值,狭窄的瘤颈使进入瘤腔内血流速度相对减慢,且相对大的瘤体使血流更容易在瘤腔内淤滞。因此,高纵横比值提示血流在瘤腔内停留时间相对较长,动脉瘤破裂的风险随之增大[33]。尺寸比是指动脉瘤深度与载瘤动脉直径的比值,因此,高尺寸比值不仅提示动脉瘤拥有更大的瘤体深度,还与纤细的载瘤动脉相关。既往研究证实,高尺寸比与动脉瘤的低壁面切应力具有相关性,并且低壁面切应力与动脉瘤的发生、发展和破裂具有相关性,且动脉瘤的血流入射角度较大,在高血流速度与动能冲击下,其破裂风险也更高[34-35]。本研究中,虽然纵横比、入射角度、尺寸比的组间差异均无统计学意义(均P>0.05),但不排除是因总体样本量较小而产生的影响。
综上所述,高长宽比和动脉瘤表面形态不规则提示PAAs具有破裂倾向,因此,临床中应注重对PAAs形态学参数的评估,对拥有高破裂风险的PAAs给予积极合理的治疗措施。本研究仅对PPAs形态学参数进行了初步的探讨,总体样本量较小,结果有待于大样本及多中心研究进一步验证。

