以双氰胺为原料制备氨基胍碳酸盐
秦 欣,田 杰,田亚楠,陈红余
(山东第一医科大学 化学与制药工程学院,山东 泰安 271000)
1 引言
氨基胍碳酸盐是一种重要的基础化工原料,尤其是以氨基胍为原料合成的系列含氮杂环化合物在医药和印染工业有着广阔的应用,利用氨基胍也可以实现许多重要化合物的合成,尤其是含氮杂环化合物。近百年来,科学家们对氨基胍碳酸盐的合成工艺进行了深入的研究。总结起来,主要有三种类型的研究工艺:肼化、肼解和还原[1]。
相对于其余两种合成方法,还原工艺具有一定的优势:通常氨基胍碳酸盐是氨基胍盐中溶解度最小的,方便将氨基胍从水溶液中分离出来[2]。并且随着硝基胍生产成本的不断降低,水合肼成本的不断上升,开发高效率的硝基胍还原工艺制备氨基胍逐渐会具有一定的成本优势[3-4]。同时,硝基胍便于提纯,相对于单氰胺原料来说纯度易于保证,因此通过硝基胍还原法可以得到高纯度的医药用氨基胍盐[5-7]。由于实验室购买硝基胍受到一定的限制,本课题首先从双氰胺开始先合成硝酸胍,用浓硫酸处理得到硝基胍,然后分别利用铁粉、锌粉和保险粉还原硝基胍得到氨基胍碳酸盐。并对相关工艺进行优化,对产品进行定性和定量分析。
2 实验部分
2.1 试剂与仪器
2.1.1 试剂
双氰氨(分析纯)、硝酸铵(分析纯)、氯化铵(分析纯)、碳酸氢钠(分析纯)、浓硫酸(98%)、盐酸(2%)、冰醋酸、乙醇(95%)、锌粉(90%)、铁粉(98%)
2.1.2 仪器
GFL-45型电热鼓风干燥箱、RE-52AA型旋转蒸发仪、SHZ-D(Ⅲ)循环水式真空泵、SZCL-2型数显智能控温磁力搅拌器、JB300-D型 强力电动搅拌机、Avater370傅立叶变换红外分光光度计、FA2004N型电子天平、微机差热天平(综合热分析)
2.2 实验过程

图1 硝酸胍的合成
Fig.1 Synthesis of guanidine nitrate
(1)称取双氰氨42.0 g(0.5 mol)和硝酸铵88.0 g(1.1 mol)混合后置于500 mL烧瓶,引入110℃油浴,将油浴温度在在1h之内调至160℃,加热50 min之后,白色固体变为透明状开始有液体出现,加热1h 18 min之后,体系变为完全透明含带气泡的液体,加热1h 58 min之后,开始有固体出现,加热3h之后,固体变为白色,停止加热,冷却。在烧瓶中加入400 mL水,加热至沸腾,趁热过滤掉不溶物,再次加热至沸腾,二次过滤,弃滤饼,将滤液进行旋蒸,旋蒸结束后,冷却,结晶,抽滤,干燥得白色固体79.88 g,滤液继续旋蒸,旋蒸结束后,冷却,结晶,抽滤,弃滤液,干燥,共得白色固体2.83 g,共得白色固体82.71 g[8]。
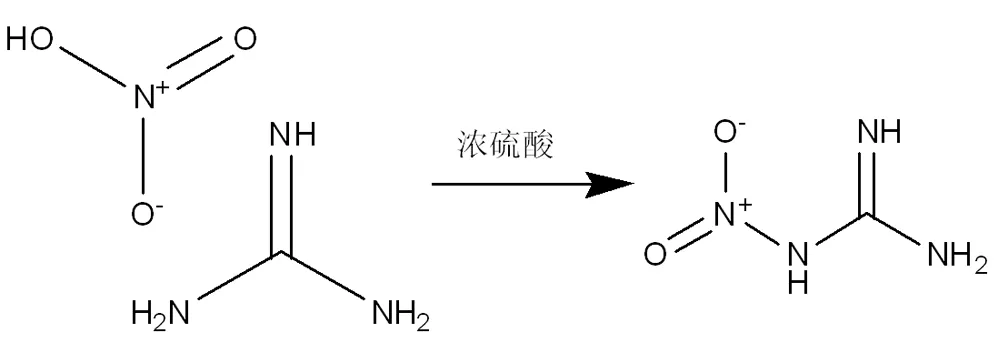
图2 硝基胍的合成Fig.2 Synthesis of nitroguanidine
(2)量取50 mL浓硫酸置于500 mL三口烧瓶,加入磁子,将烧瓶置于冷水浴磁力搅拌,2h分批缓慢加入46.0 g硝酸胍,在加入过程中烧杯上方有发烟现象,体系黏度越来越大,温度控制在20℃以下,硝酸胍加入完毕,体系变为白色粘稠液体,磁子已搅拌不动,静置,过夜,将烧瓶中的固体倒入烧杯,加1000 mL碎冰和水,搅拌半小时,进行抽滤,得白色粘稠物,弃滤液,将白色固体倒入烧杯,加水至1000 mL,加热至固体完全溶解,然后继续加热至溶液沸腾,趁热过滤,冷却结晶,将冷却结晶的产品进行抽滤,烘干,得白色针状晶体32.23 g,滤液进行旋蒸,旋蒸后,将液体加热至沸,冷却结晶,抽滤,干燥得白色针状晶体1.60 g,共得针状晶体33.83 g[9-10]。

图3 氨基胍碳酸盐的制备
Fig.3 Preparation of aminoguanidine carbonate
(3)a.锌粉还原
称取80.0 g锌粉置于烧杯,加200 mL 2%稀盐酸搅拌一分钟,过滤,加200 mL水洗涤,过滤,将过滤后的锌粉置于布式漏斗,加200 mL稀盐酸洗涤,静置过滤,加200 mL水洗涤,静置过滤,加200 mL 95%的乙醇洗涤,静置过滤,将乙醇滤液再次洗涤,静置,抽滤,抽干乙醇,得活化后的锌粉。称取活化后锌粉35.39 g,硝基胍10.4 g,混合研磨加少量水,将研磨好的混合糊状物转移至烧杯,冰浴冷却。量取6 mL冰醋酸置于250 mL烧瓶,冰浴,机械搅拌,一个小时分多次加入糊状物和50 mL冰水,加料过程中温度超过10℃,加毕后,温水浴加热至T=40℃,继续搅拌5 min,抽滤,将滤饼抽干,得黄绿色透明滤液,灰色滤饼,将滤饼转移至烧杯,加50 mL水搅拌,过滤,得黄绿色滤液,灰色滤饼,再次将滤饼转移至烧杯,加50 mL水搅拌,过滤,得黄绿色滤液,灰色滤饼,加水多次洗涤滤饼,将滤液归入一起,滤液转移至烧瓶,黄绿色透明溶液,加入10.0 g氯化铵,加入后完全溶解,搅拌加热至T=40℃,10 min中之内加入11.0 g碳酸氢钠,搅拌20 min,体系由浅黄色透明溶液体系变为浅黄色浑浊液体,进而变成蛋黄色浑浊液体,冰浴冷却,体系出现分层,上层为黄色透明溶液,下面为白色沉淀,过滤,得白色固体,自然风干[11],得白色粉末 6.32 g。
b.铁粉还原
称取铁粉22.40 g和水120 mL,置于250 mL烧瓶,搅拌加热,加入5.08 g氯化铵,pH值变至6,滴加硫酸,pH值=3,加热至T=91℃,体系变为黑色,沸腾后开始加入硝基胍,3h分批加入硝基胍10.40 g,冷却过滤,得浅黄色透明滤液,再次过滤,得紫红色透明滤液,再次过滤,得玫红色透明溶液,滴加少许硫酸溶液pH值由8变为3,滤液由枚红色变为浅黄色,搅拌,加热至T=40℃,加入碳酸氢钠11.24 g,碳酸氢钠加毕后,溶液变为乳粉白色,停止搅拌加热,溶液变为上层为浅绿色浑浊液体,下层为白色沉淀,冰浴冷却,过滤,得白色固体,自然风干,得白色粉末5.17 g。
3 结果与讨论
本论文以双氰胺和硝酸铵为原料,经过中间产物硝酸胍和硝基胍,以铁粉和锌粉为还原剂在酸性条件下,将硝基还原为氨基。应用铁粉和锌粉作还原剂,具有工艺简单、操作方便、投资少、应用范围广等优点。以下是分别应用铁粉和锌粉为还原剂还原硝基胍的得到的实验结果:
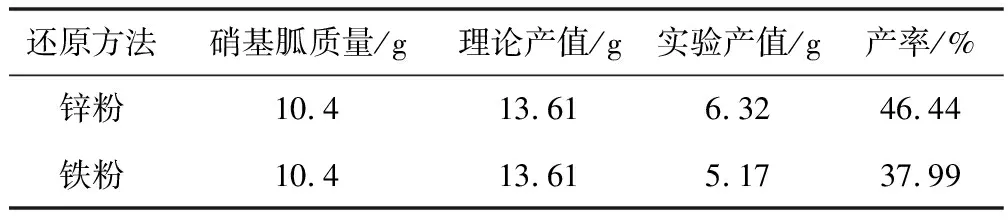
表1 锌粉和铁粉还原硝基胍的产率对比
实验结果表明,锌粉还原硝基胍的产率相对于铁粉来说更高,因为锌的金属性更强,比铁更活泼,并且由于新的锌粉表面都有一层氧化膜,所以在空气中相对较稳定,但经酸洗后,除去氧化膜,锌粉活化,在空气中很快氧化,同时反应性增强。锌粉和铁粉都可以回收再利用,更加绿色经济,根据如今的原子经济化理论,使用更加绿色经济的方法是大势所趋,但是由于产率还达不到要求,因此对于反应条件的优化还有很长的一段路要走。
4 表征
4.1 氨基胍碳酸盐红外分析
氨基胍碳酸盐红外分析见图4。
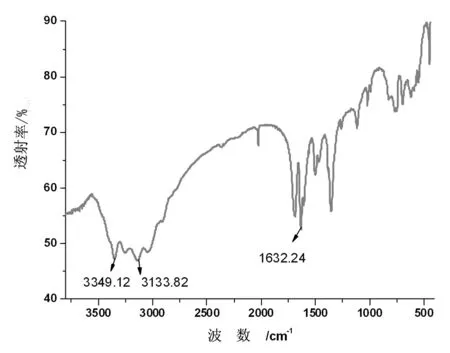
图4 氨基胍碳酸盐红外分析图
将氨基胍碳酸盐产品用Origin处理作图,由图4可以看出在3349.12cm-1有一个特征吸收峰,根据对照红外光谱各基团特征峰的峰位,可以得出此峰为-NH-键的峰,3133.82cm-1处的峰是-NH2的特征峰,1632.24cm-1处的峰是-C=N的特征峰,根据以上分析,以及对基团周围原子团对该基团的影响分析,可以得出该化合物是氨基胍碳酸盐。
5 结论
本文以双氰胺和硝酸铵为原料合成氨基胍碳酸盐,并经历了中间产物硝酸胍和硝基胍的合成,再由硝基胍通过用铁粉和锌粉还原得到氨基胍。通过测中间产物的热重,检测了中间产物的纯度。通过对比两种还原产物,表明用锌粉还原的产率明显高于用铁粉还原的产率,并通过红外光谱对两种最终产物进行了表征。并经过与标准谱图的对比,可以看出产品与标准品的红外谱图的峰型相同,峰位可以对上,所得到的产品能达到一般工业纯度要求。
——非均布滤饼的局部比阻与平均比阻的测定与计算方法

