扫描及重建参数对肺磨玻璃结节体积测量影响的体模研究
李 艳,程 勇,冯茜茜,沈 倩,兰永树
(西南医科大学附属医院放射科,四川 泸州 646000)
随着CT筛查的普及CT技术的发展,小、中等肺结节的检出率越来越高,其中多数为良性[1],无需进一步的临床干预,因此需长期随访观察来评估肺结节。Walter等[2]认为,结节处理是以体积和倍增时间为基础,因此结节体积测量的可重复性及准确率尤为重要。相较于人工测量,利用后处理软件进行三维体积测量更具准确性[3],但在复查随访的临床工作中扫描及重建的条件不一致可能会影响肺结节体积测量的准确率。本研究采用不同扫描及重建参数对肺磨玻璃结节体模进行扫描并测量,探讨其对结节容积测量的影响,以期为肺磨玻璃结节的随访条件提供参考。

表1 扫描参数

图1 肺体模(A)及8个磨玻璃结节(B)
1 材料与方法
1.1 材料 体模采用岛津公司研制的多用途男性胸部模型N1及8个球形小结节体模(图1),该仿真体模长40 cm、宽43 cm、高48 cm,质量18 kg,胸围94 cm。根据2017版Fleischer Society指南[4]:对于偶发直径<6 mm(体积<100 mm2)结节的人群,无论有无肺癌高危因素,都无需常规随访,因此本研究中采用直径≥5 mm的结节。8个结节:2种CT值(-800 HU、-630 HU)、4种直径(5 mm、8 mm、10 mm、12 mm)。将8个结节随机放置于体模的左侧肺。
1.2 扫描及重建参数 采用GE light speed VCT,扫描范围自体模头端至足端,以螺旋方式扫描。在Philips portal工作站进行重建,探究某一种影响因素时,其他条件不变。根据影响因素的不同分为管电压组及管电流组,探究扫描参数时重建参数固定为:重建层厚0.625 mm,重建野36 cm,重建算法Standard,结果显示80 kV、150 mA组绝对错误率(absolute percentage error,APE)值最小,因此对80 kV、150 mA的原始数据行不同层厚、算法及重建野进行重建,分别为不同层厚组、不同算法组、不同重建野组,重建野为18 cm时只重建左侧肺。具体扫描及重建参数设定见表1、2,其余参数:采用滤波反投影重建算法,螺距0.984,转速0.6 s/rot,矩阵512 ×512。
1.3 数据测量及容积分析 将扫描所得图像上传至Philips portal工作站,在工作站自动肺窗(WL=-600 HU,WW=1 500 HU)利用Lung nodule assessment软件对磨玻璃结节进行体积测量,由2名高年资放射科医师独立选取结节显示的最大直径层面及其邻近上下层面共3个层面,在3个层面连续分割3次并自动显示结节的三维图像及结节的信息,记录其体积V测量(图2)。每个结节可测得3个数据,由于结节为规则球形,实际体积可以根据公式计算:V实际=(3/4)πr3。结节容积测量的APE:APE=[(V测量-V实际)]/V实际×100%。
1.4 辐射剂量 记录不同扫描参数组合的辐射剂量长度乘积(dose-length product, DLP),并通过公式计算有效剂量(effect dose, ED),ED=DLP×k(成人胸部权重因子k=0.014)。
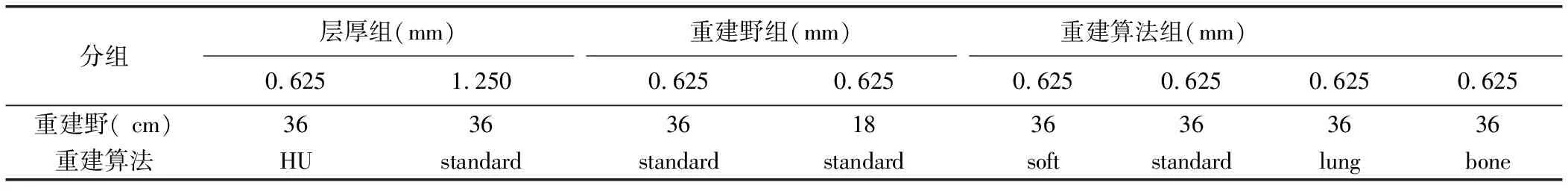
表2 80 kV、150 mA组重建参数

图2 磨玻璃结节(CT=-630 HU,直径12 mm)的三维图像及信息图 A.Philips portal工作站用Lung nodule assessment软件进行分割后所形成的三维图像,显示结节边缘毛糙,但结节、血管及胸膜三者关系更清楚、立体; B.显示结节的基本信息
1.5 统计学分析 采用SPSS 25.0统计分析软件。经检验数据不符合正态分布,计量资料以中位数(上下四分位数)表示。不同管电流、管电压及重建算法的比较采用Friedman检验,两两比较用q检验,不同重建野及重建层厚比较采用Wilcoxon符号秩和检验。采用组内相关系数(intraclass correlation coefficient, ICC)评估2名诊断医师对肺磨玻璃结节体积测量结果的一致性。P<0.05为差异有统计学意义。
2 结果
随着管电压或管电流增大,有效辐射剂量增大; 固定管电流为200 mA时,管电压为120 kV比80 kV时有效辐射剂量高65.6%;固定管电压为80 kV时,管电流为200 mA时较150 mA有效辐射剂量提高25.1%,见表1。2名医师对肺磨玻璃结节体积测量的ICC值为0.98。管电压为80 kV、100 kV、120 kV时对各小结节的APE值分别为4.20%(2.26%,8.68%)、6.08%(3.08%,12.48%)、4.70%(3.04%,10.33%),差异无统计学意义(P=0.056)。管电流为100 mA、150 mA、200 mA时,APE值分别为5.22%(2.23%,9.45%)、3.84%(1.90%,8.84%)、4.20%(2.26%,8.68%)(P=0.02),两两比较示100 mA vs 150 mA(调整P=0.012)、150 mA vs 200 mA(调整P=0.004),差异有统计学意义;100 mA vs 200 mA(调整P=1.0)差异无统计学意义。采用80 kV、150 mA原始数据进行重建,0.625 mm、1.250 mm层厚各结节的APE值分别为3.84%(1.90%,8.84%)、4.12%(1.11%,6.56%),差异无统计学意义(P=0.91)。当重建野为18 cm、36 cm时,APE值分别为1.59%(0.43%,5.51%)、3.84%(1.90%,8.84%),差异有统计学意义(P<0.001)。采用soft、standard、lung、bone重建算法时结节APE值分别为4.49%(1.99%,9.50%)、3.84%(1.90%,8.84%)、1.78%(1.14%,5.36%)、3.82%(2.51%,8.91%),差异有统计学意义(P=0.005),两两比较,除lung vs bone(调整P=0.007)、lung vs soft(调整P=0.031)差异有统计学意义,其余两两比较差异均无统计学意义(P均>0.05);lung算法APE值较小,更接近结节真实值。低密度小结节(CT值为-800 HU,直径5 mm)在各种条件的APE值均>10%。不同管电压、不同重建野及不同重建算法条件下磨玻璃结节图像见图3。
3 讨论
肺磨玻璃结节包括纯磨玻璃结节及部分磨玻璃结节,多数为良性。Henschke等[5]认为部分实性磨玻璃结节恶性率为63%,纯磨玻璃结节恶性率为18%,远高于实性结节,因此对磨玻璃结节良恶性的鉴别是临床诊断中的一个挑战。Kim等[6]研究报道,结节边缘分叶或毛刺更倾向于恶性,而王海燕等[7]认为以磨玻璃结节的CT征象来预测病理结果不准确,因此以CT征象预测磨玻璃结节的性质还需进一步验证。临床目前常用结节的体积变化及倍增时间来随访和评估结节的良恶性,传统的二维轴向测量难以准确评估结节的生长,且观察者之间的可重复性差也是其中一个缺点[3,8]。目前三维测量逐渐成为评价肺结节生长速度的首选方法[9-10]。然而,这种三维方法测量受许多因素的影响,如扫描和重建参数、分割软件和结节特性。研究[11]报道显示,需要同样的机器设备对肺结节进行随访,且Botelho等[12]研究认为迭代重建算法更适合用于肺结节的三维容积分析。
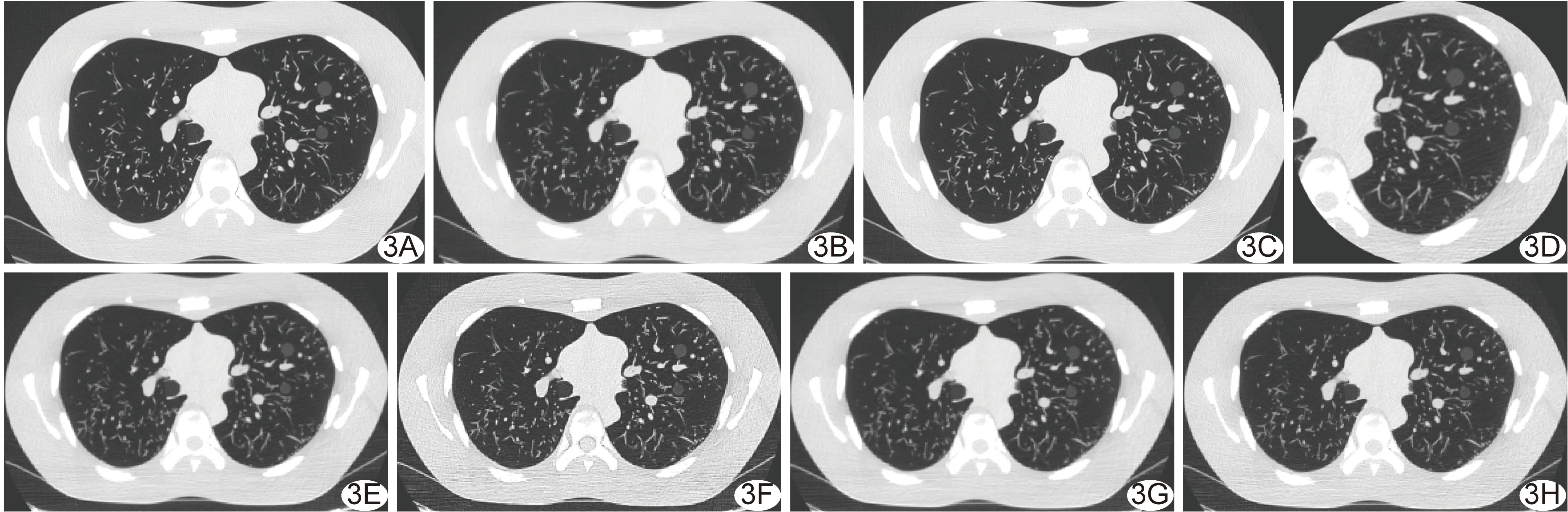
图3 不同条件下2枚结节(CT=-630 HU,直径10、12 mm)的轴位CT A~C.分别显示管电压为80 kV(A)、 100 kV(B)、120 kV(C)的磨玻璃结节,人眼未见确切变化; D.18 cm重建野重建的左侧肺,较36 cm重建野的图像视野放大,结节边缘及细节显示更清楚; E~H.分别示soft(E)、standard(F)、lung(G)、bone(H)重建算法下的磨玻璃结节,肺算法时显示结节的边缘更锐利
本研究对扫描参数进行探究时发现不同管电压对肺磨玻璃结节的APE值无影响,但不同管电流条件下,150 mA时APE值最小。杨文洁等[13]研究认为,不同扫描参数不会影响肺结节容积测量的准确率;苏大同等[14]也认为不同管电流对肺实性结节容积定量无影响。可能是因为肺磨玻璃结节密度很低,对X线的衰减也较低,因而超过80 kV的管电压并不会明显影响结节对X线的衰减,结节分割准确性也不会改变,反而会大幅增加辐射剂量;而管电流150 mA时肺磨玻璃结节的测量准确率较高,可能是因为100 mA管电流会使图像噪声增加,从而影响软件的分割,而管电流超过200 mA时可能是机器自动使用大焦点,导致肺磨玻璃结节周围的半影增大,边缘变得模糊,使软件不能准确识别边界,造成体积测得不准确。因此对于磨玻璃结节使用适当低剂量的扫描参数可以提高肺磨玻璃结节容积测量的准确性,并降低辐射剂量,而且对于需要多次随访的磨玻璃结节可以明显减少受检者所受的累加辐射剂量。
在重建参数方面,本研究结果显示肺算法的APE值更小,所测得体积更接近真实值,而孙海宁等[15]采用FUYO模型分析不同重建层厚及重建算法对实性结节容积测量准确性的影响,结果显示肺算法误差最大,而1.25 mm层厚与0.625 mm层厚的容积测量结果无差异。本研究与孙海宁等[15]结果不同,可能原因是本研究使用的材料为仿真体模及模拟肺磨玻璃结节,与实性结节不同的是肺算法使磨玻璃结节边界更锐利,因此各自适宜的算法可能不一致;两种层厚未影响其APE值,与上述结果相符,但在临床工作中0.625 mm层厚会使后处理工作更加繁重,数据更多,因此建议使用1.25 mm层厚进行重建。随着重建野缩小,容积测量准确率提高,可能因为重建野缩小从而每个结节的像素数目增多、体积变小,软件分析时受部分容积效应的影响也变小,结节分割更准确,因此需要结合靶重建对肺磨玻璃结节进行分析。因为本研究需要保证8个结节参数的一致,故仅比较了36 cm(全肺)和18 cm(左肺)两种FOV,但在临床中可以根据磨玻璃结节的具体情况,设置更小的FOV。低密度小结节在各种条件的APE值均大于10,可能是软件自动勾画时包含了结节周围的肺组织或血管,低密度小结节所受影响会更明显,从而造成测量体积过大,因此认为在临床随访中低密度小结节不适合用肺结节分析软件来测量容积。
本研究的局限性:①使用的仿真体模不能完全模拟临床中患者的呼吸及心脏活动对测量的影响,而且体模研究获取的研究数据较少;②所使用的磨玻璃结节密度均匀且为规则球形,难以对其他密度不均匀、形态不规则的结节进行分析,因此在以后的研究中将对临床中的肺磨玻璃结节进行进一步研究。
综上所述,在肺磨玻璃结节随访时低剂量扫描结合靶重建、肺算法可以在尽量减少辐射剂量的情况下,提高肺磨玻璃结节的软件测量的准确率。低密度小结节不适合用肺结节分析软件分析。