Cl-和SO42-杂质离子对燃料电池催化剂性能的影响
王维铎,陈心拓
(北京化工大学 化学工程学院,北京 100000)
随着社会经济的发展,人类对于能源的要求也越来越高,能源不仅仅是国民经济的发展动力,也是衡量一个国家综合国力、国家文明发达程度和人民生活水平的重要指标[1]。为了适应社会发展和全球文明的进步,发展没有环境污染的绿色能源是实现可持续发展战略的最佳途径之一,其中燃料电池[2]已经成为科研工作者重点关注的对象。通过将反应物质的氧化和还原反应分别放在电池的阳极和阴极来进行,阳极所产生的电子经外电路从阳极到达阴极,燃料电池从而对外做功,使得化学能转变为电能。但是实际应用时,电池环境很难保持绝对纯净,各种杂质离子如Cl-和SO42-会存在于电解液中,甚至附着于电极上。本实验通过对照组,得出了以上两种杂质离子分别存在于电解液时对催化效果的具体影响。
1 材料与方法
1.1 实验药品及仪器
实验中使用的药品及仪器见表1。
1.2 催化剂和电极的制备
催化剂是由0.15 mL异丙醇、0.5 mL超纯水和2 μL Nafion溶液(作为催化剂的涂层和载体)搅拌均匀制成。
工作电极的制备方法如下:用氧化铝抛光粉抛光玻碳电极,再在去离子水超声清洗几分钟后干燥。将煅烧好的催化剂以1 mg/mL的浓度加入到75%(体积分数)的乙醇水溶液,再加入总溶液5‰体积的5%浓度的萘酚。超声搅拌器上搅拌 10 min,然后取催化剂油墨(1 mg/mL)10 μL,滴在磨好的玻碳电极上,待晾干后安装在电化学工作站上。催化剂的载量为51.02 μg/cm2。
1.3 电解质溶液的配制
本实验中电解质液体主体为纯度71%的高氯酸。通过稀释盐酸和硫酸溶液,经计算分别配制出氯离子或硫酸根离子浓度为10-5和10-6mol/L的总体积为40 mL的电解液。
1.4 测试方法
本实验采用的电化学工作站中,对电极为石墨棒,参比电极为Ag/AgCl电极。采用循环伏安法测量,扫描电位为-0.8~0.2 V(Ag/AgCl),扫速速率为50 mV/s。当电解液中Ar或O2饱和后,先扫描10圈以活化催化剂,直至电流稳定后记录数据并和其他条件下所得的数据进行对比。
2 结果与分析
2.1 Cl-对Pt/C催化剂的影响
在酸性条件下,阴极主要进行析氢反应(HER),阳极主要进行析氧反应(OER)。根据目前已有的共识[3-4],Pt/C催化剂的CV曲线具有三个特征电位区:-0.27~0.05 V的氢吸脱附区域、0.05~0.20 V的双电层区、大于0.20 V的OHad可逆吸附区。
Ar氛围下不同浓度Cl-的CV特性曲线如图1所示。其中,A表示Pt-H的脱附,B表示02的产生,C表示Pt-O的还原,D表示Pt-H的吸附。可以看出,由于痕量Cl-的存在,ABCD四个区域的曲线发生了收缩,表明催化剂的活性受到抑制作用。其中可以发现A区域氢脱附峰面积明显减少,导致之后的ECSA计算数值偏小。同时,随着Cl-浓度的增加,四个区域的曲线进一步收缩,说明浓度增加会使催化剂活性进一步下降。
根据ORR极化曲线,发现Cl-浓度增加,极化电流密度下降,说明Cl-对极化过程有抑制作用,从而降低了催化剂的催化活性。
O2氛围下不同浓度Cl-的CV特性曲线如图2所示。可以看出,不同扫速下随Cl-浓度增加,曲线下端平台对应电流密度数值降低。由此可以肯定,Cl-至少通过抑制极化过程而使电化学催化活性下降,并且其对极化过程的抑制程度随浓度增加而增加。
2.2 SO42-对Pt/C催化剂的影响
Ar氛围下不同浓度SO42-下的CV特性曲线如图3所示。各过程与之前相同,A表示Pt-H的脱附、B表示O2的产生、C表示Pt-O的还原、D表示Pt-H的吸附。由图3可以看出,类似于Cl-,可以发现由于SO42-离子的存在,催化剂活性也有显著的下降,并且催化剂活性受抑制程度随SO42-浓度的增加而增加。不过有在E处,即表征H2产生的峰,在SO42-离子为10-6mol/L时峰值突然变大,意味着浓度为10-6mol/L的SO42-可能促进了H2的产生。

图3 Ar氛围下不同浓度SO42-下的CV特性曲线
根据ORR极化曲线,发现极化电流密度下降,说明SO42-对极化过程有抑制作用,从而降低了催化剂的催化活性。随浓度的增加,下端平台对应的电流密度数值更低,见图4。因此SO42-的存在抑制了极化过程,并且其抑制程度随浓度增加而增加。
2.3 电化学活性面积的计算和ORR活性计算
电催化剂的电化学活性面积(ECSA)可以通过测量循环伏安曲线中的氢脱附峰的面积而得到。脱附峰进行积分得到氢气脱附过程的电量QH。进而计算ECSA值[5-8],见图5。
通过比较ECSA值可以发现,Cl-和SO42-的存在均会导致催化剂的活性显著下降,Cl-使ECSA下降约12.4%,SO42-使ECSA下降约19.0%;并且两种离子浓度越高,ECSA值越低。还可以发现在浓度相同时,SO42-杂质对催化剂活性的抑制能力更强。
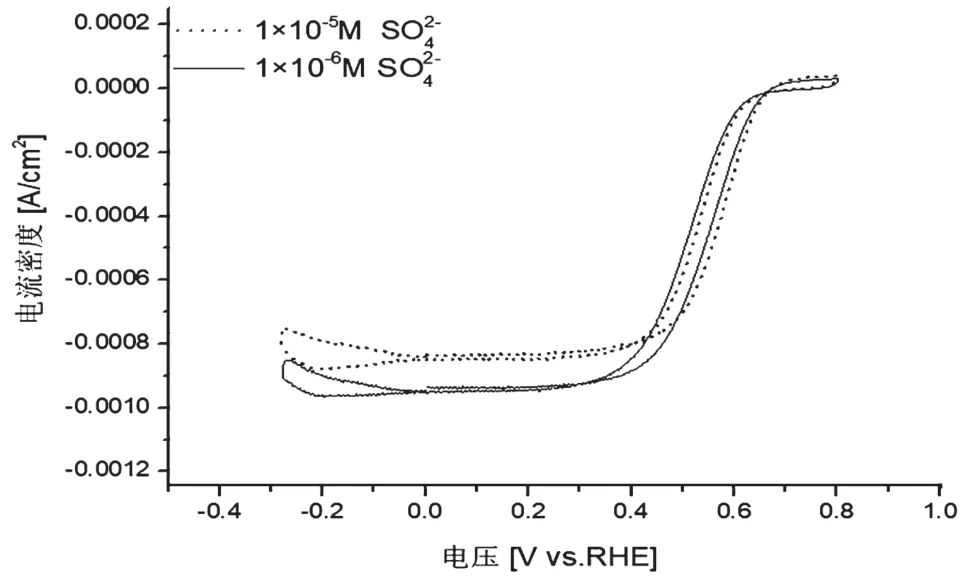
图4 O2氛围下10mV/s扫速下不同浓度SO42-的CV特性曲线

图5 Cl-和SO42-相同浓度存在下ECSA值比较
3 结论
通过一系列催化效果性能表征和相关计算,可以发现Cl-和SO42-对Pt/C燃料电池催化剂的活性均有较强的抑制作用,而且随着其浓度的增大,抑制作用也逐渐加强。推测一方面可能是由于杂质离子占据了电极表面的活性位点,使得电极表面的Pt/C催化活性面积减小;另一方面,杂质离子存在影响电解液里的传质过程,从而降低了极化电流,使得催化效果下降。一般来说Cl-存在使ECSA下降约12.4%,SO42-存在使ECSA下降约19.0%。
目前进行酸性条件下的催化剂性能测试时,一般采用HClO4作为酸性溶剂。在一定温度下,HClO4会分解产生Cl-,并且温度越高分解产生的Cl-越多。如果温度过高,得出的催化剂化学表征曲线(如CV曲线)都会受到这些痕量离子的影响,从而与真实情况产生较大的偏差。此外,目前电动汽车采用的燃料电池多使用商业Pt/C燃料电池催化剂。如果空气中SO2含量较高,则电池中可能产生SO42-,使得催化剂性能下降,造成电池效率下降。

