荧光定量技术检测牛奶中四环素类药物残留准确性的研究与探讨
文/贾 涛 方 芳 郑君杰 孙志伟 卢春香
(北京市饲料监察所)
四环素类药物包含四环素、金霉素、土霉素、强力霉素,为广谱抗生素,主要用于治疗奶牛立克次氏体、衣原体、支原体等致病微生物感染病症,多为添加在饲料和饮用水中使用或注射使用。奶牛用药后,四环素类药物会残留在牛奶中,对人类健康造成危害,尤其是对婴幼儿的身体健康危害更为突出,其危害主要表现在对婴幼儿的肝脏、肾脏、牙齿与骨骼等方面的影响。因此,牛奶中四环素类药物的快速检测尤为重要,本试验利用荧光定量技术检测牛奶中四环素类药物残留,并与仪器法比较,以研究其准确性。
1 材料与仪器
1.1 试验材料
四环素类荧光定量检测卡。
1.2 仪器
移液器(移液枪)、计时器、荧光免疫定量分析仪(型号:FQ-S1)。
2 检测方法
2.1 检测原理
采用竞争性免疫荧光层析法检测目标物的残留浓度,荧光标记的抗体预先包被在释放垫上。当待测样品滴加在加样区时,样品中的目标物在毛细渗移的过程中,与荧光标记的特异性单克隆抗体结合,抑制了抗体与T区包被抗原的结合,使T区荧光减弱,利用免疫荧光定量分析仪读取T线与C线位置的荧光强度,通过仪器内置的标准曲线即可计算出样品中靶标物质的含量。
2.2 样品制备
空白样品:生鲜乳(牛奶),在检测时提前恢复至室温,并充分摇匀样品(奶样不能有结块、酸味或沉淀等性状)。
添加样品:向空白样品加入四环素类标准品至所需浓度。
2.3 最低检测限的测定
取20 份空白生鲜乳样品,打开铝箔袋,取所需量的金标微孔和试纸条,做好标记,并置于桌面上(取出所需微孔和检测卡,立即密封铝箔袋,以防受潮);吸取200 μL样本液于金标微孔中,小心吹打至孔底的紫红色颗粒完全溶解(注意吹打时动作要轻柔,避免产生气泡),室温(25±2)℃孵育3 min;取120 μL金标微孔中样品加入到加样孔中,并开始计时,准确反应10 min后,插入荧光定量分析仪读数。计算其平均值,再加上3倍标准差,即为最低检测限。
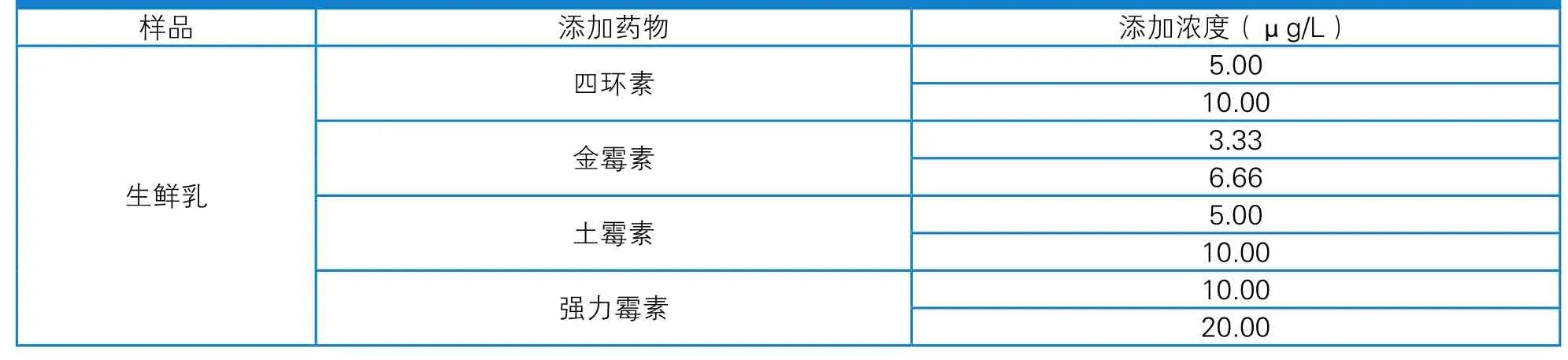
表1 空白样品添加浓度

表2 空白生鲜乳样品四环素类含量测定结果
2.4 准确度和精密度的测定
采用3 个批次四环素类荧光定量快速检测卡,对添加四环素类药物的生鲜乳样品进行测定。样品添加药物浓度为对应的最低检测限(Limit of Detection,LOD)和2倍LOD(表1),每个添加浓度做5个平行,计算样品添加回收率和批内、批间的变异系数。
2.5 与仪器方法进行比较
采用四环素类荧光定量检测卡和仪器法,分别对50 份生鲜乳盲样进行测定,比较测定结果。仪器方法按照GB/T 22990—2008《牛奶和奶粉中土霉素、四环素、金霉素、强力霉素残留量的测定液相色谱-紫外检测法》中所述的检测方法进行操作。
3 试验结果
3.1 最低检测限的测定
取20 份空白生鲜乳样品,按照四环素类荧光定量检测卡的操作说明书方法进行检测,计算其平均值,再加上3 倍标准差,即为最低检测限(表2)。
结果表明,以四环素为对照物建立标准曲线,得出该药物的最低检出限为4.93 μg/L,为保障产品的稳定性,可认为四环素类荧光定量检测卡在生鲜乳中的检测限为5.00 μg/L。
3.2 准确度和精密度
准确度是指测定值与真实值的符合程度,按2.4中的步骤操作,结果见表3。结果表明,所有样品各添加浓度的回收率均在84.60%~113.94%。各添加浓度的批内、批间变异系数均低于15.00%。
3.3 与仪器方法比较
采用该四环素类荧光定量检测卡和仪器法,分别对50 份生鲜乳盲样进行测定,比较测定结果,以检测限作为阴、阳性判定值,小于四环素类荧光定量检测卡检测限的检测结果记为“-”,仪器结果记为“ND”,大于四环素类荧光定量检测卡检测限,以实际检测值表示(表4)。结果显示,二者的符合率为100%。
4 分析与讨论
为评价本试验研制的四环素类免疫荧光定量检测卡的可靠性,采用空白样本进行回收率试验,分别从检出限、准确度、精密度和与仪器方法比较等4 个方面进行验证。
4.1 最低检测限
取20 份空白样本进行检测,检测信号值,并通过标准曲线得出待测物浓度,计算各对应浓度值的标准差,由平均值加3 倍标准差即为该样本的最低检测限。经试验发现,四环素类荧光定量检测卡在生鲜乳中的检测限为5.00 μg/L。
4.2 精密度与准确度
选取空白样本,添加各药物检测限浓度标准品并检测,每个浓度重复验证10 次,并统计添加回收率和相对标准偏差。用3 个批次荧光定量检测系统,对空白添加样品进行测定,每种样品的添加浓度为LOD和2LOD,每个添加浓度做5 个平行,计算样品的添加回收率和批内、批间变异系数。经试验,所有样品各添加浓度的回收率均在84.60%~113.94%,各添加浓度的批内、批间变异系数均低于15.00%。
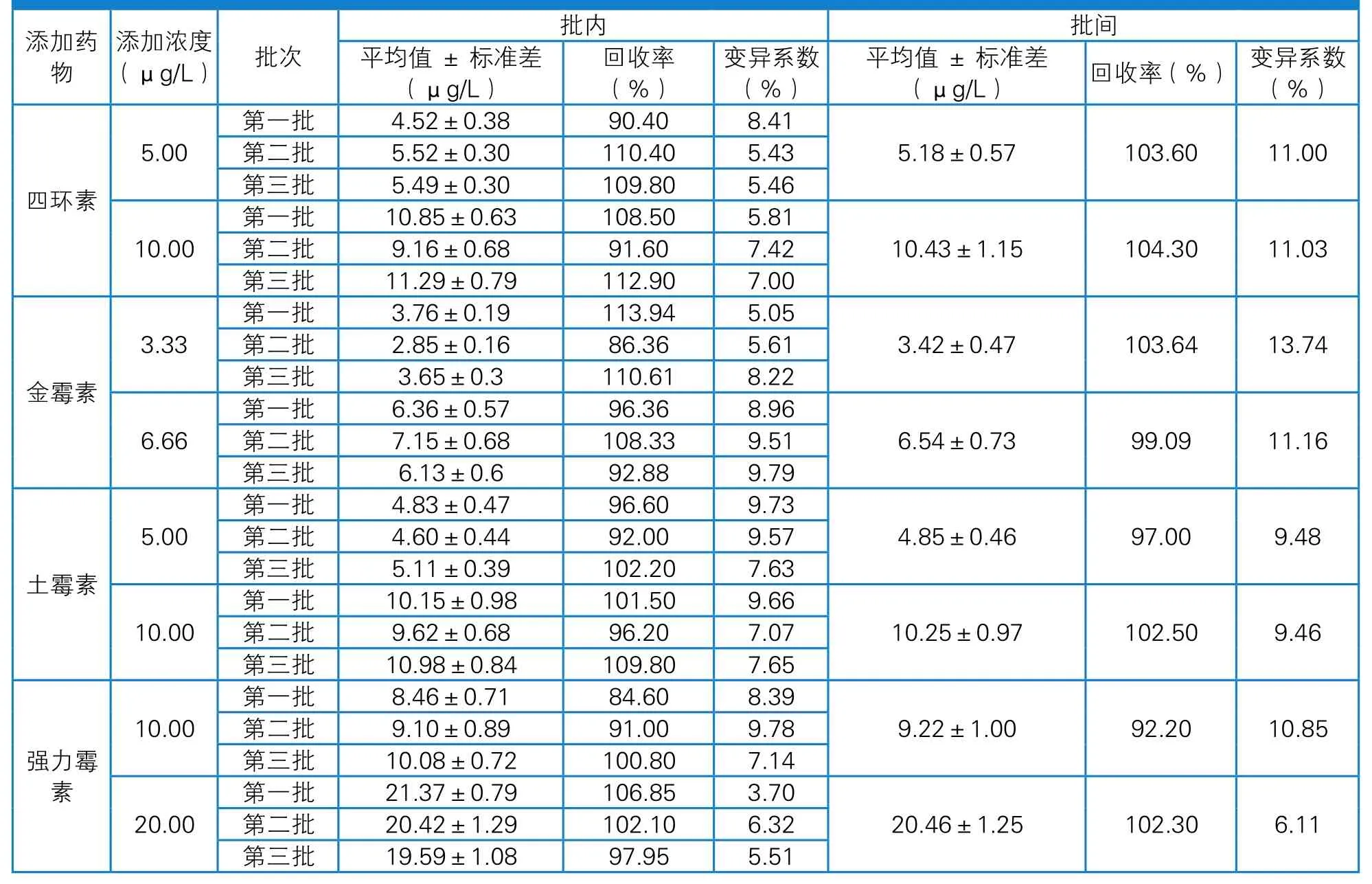
表3 准确度和精密度
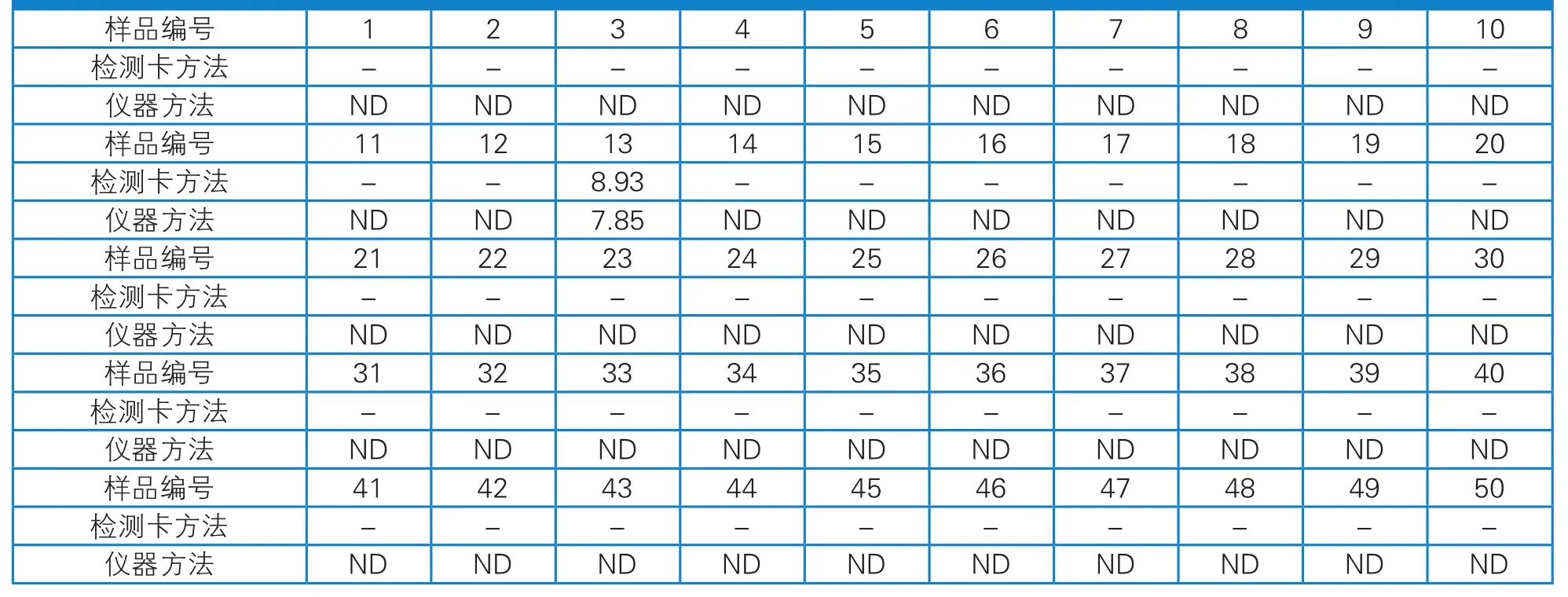
表4 与仪器方法比较结果 单位:μg/L
4.3 与仪器方法进行比较
本试验研制的荧光定量检测卡和仪器法分别对50 份生鲜乳盲样进行测定,比较测定结果。仪器方法根据国家标准规定进行操作,结果显示,通过对盲样的测定,四环素类荧光定量检测卡和仪器法的阳性符合率为100.00%。

