羟氯喹与贝伐单抗协同抑制HUVEC细胞生长的作用及机制
宣自学,杨 慧,叶 强,张 夙,石佳娜,王 维,张国兵,邵燕飞,王如意,方晴霞
(浙江省人民医院,杭州医学院附属人民医院药学部,浙江 杭州 310014)
肿瘤血管为肿瘤提供了氧分、营养和散播途径,靶向肿瘤血管可以达到“饿死”肿瘤的治疗效果[1]。贝伐单抗(bevacizumab,BEV)能够特异性地靶向血管内皮生长因子VEGF-A,抑制血管新生和肿瘤生长[2]。但是,肿瘤血管新生涉及到多个蛋白或信号通路,单靶药物抑制某一蛋白后,血管生成往往出现代偿性现象,进而引起肿瘤反弹性生长、转移以及耐药[3]。临床上在使用贝伐单抗时,往往需要与其他抗肿瘤药物联用,以提高对肿瘤的抑制作用。
细胞自噬能够通过降解细胞内受损的细胞器、细胞质以及入侵的微生物等,来维持肿瘤的稳态,因此,抑制细胞自噬可以阻滞肿瘤的进展[4]。抗疟药羟氯喹(hydroxychloroquine,HCQ)可抑制自噬体与溶酶体的融合及降解,从而抑制细胞自噬[5]。羟氯喹目前主要用于风湿免疫性疾病的治疗,近年来,它的抗肿瘤作用逐渐被揭示[6]。但是,羟氯喹的抗肿瘤作用机制非常复杂,目前报道的作用机制有:抑制细胞自噬、影响溶酶体功能、调节免疫、抑制炎症反应、影响内涵体功能、诱导细胞凋亡、增敏放化疗等。
有研究提示,贝伐单抗与羟氯喹联用可以协同抑制多种肿瘤的生长[7]。然而,羟氯喹与贝伐单抗联用对肿瘤血管的作用及机制尚不明确。由于人脐静脉内皮细胞(human umbilical vein endothelial cell,HUVEC)在血管新生过程中发挥重要作用,也常被用于肿瘤血管新生的实验,因此,本实验拟通过实时无标记细胞分析技术(real time cellular analysis,RTCA)和流式细胞凋亡检测,分别研究羟氯喹与贝伐单抗联用对HUVEC细胞增殖和凋亡的影响,然后利用体外血管形成实验,研究羟氯喹与贝伐单抗联用对HUVEC细胞血管形成的作用。此外,本实验拟通过Western blot检测LC3、p62蛋白的表达,电镜观察自噬体和线粒体变化,以及利用转录组测序(RNA-seq)进一步阐明羟氯喹与贝伐单抗联用,协同抑制HUVEC细胞生长的作用机制。
1 材料与方法
1.1 材料
1.1.1细胞 人脐静脉内皮细胞HUVEC,购自美国ScienCell实验室。
1.1.2药物与试剂 Matrigel胶(BD公司);RPMI 1640培养基(HyClone);贝伐单抗(罗氏公司);羟氯喹(Sigma-Aldrich);LC3抗体(Cell Signaling Technology);p62抗体(Abcam公司);Annexin V-FITC试剂盒(Kengen);xCElligence RTCA S16(艾森生物);RTCA板(艾森生物);胰蛋白酶、胎牛血清(Gibco)。
1.1.3仪器 LSM880激光扫描共聚焦显微镜(Zeiss);H-7650透射电子显微镜(日立);流式细胞仪(Millipore);xCELLigence RTCA S16(ACEA Biosciences)。
1.2 方法
1.2.1RTCA实验 首先,在E-Plate板的孔中加入50 μL培养基,并放置在RTCA Station上。RTCA自动扫描,并开始检测基线,以确定所选择的孔接触正常。等待所有孔的基线处于40~120之间后,取出E-Plate板,并且在孔中加入100 μL HUVEC细胞悬液(3 000个/孔)[13]。随后,分别加入羟氯喹(5 mg·L-1)、贝伐单抗(100 mg·L-1)、羟氯喹(5 mg·L-1)联合贝伐单抗(100 mg·L-1)。将E-Plate板放到细胞培养箱中的RTCA Station上,系统会检测细胞Cell Index值[8]。
1.2.2流式凋亡实验 取对数生长期的HUVEC细胞,经胰酶消化后,离心,并收集细胞。将HUVEC细胞(2.5×108·L-1)接种至6孔板中,细胞培养板放置于培养箱中过夜。分别加入羟氯喹(5 mg·L-1)、贝伐单抗(100 mg·L-1)、羟氯喹(5 mg·L-1)联合贝伐单抗(100 mg·L-1)处理,48 h后收集细胞。经1×PBS清洗、离心及收集细胞后,加入300 μL的1×Binding Buffer重悬细胞。然后将5 μL的Annexin V-FITC加入细胞悬液,混匀后室温避光孵育20 min。最后加入5 μL的PI,混匀后室温避光孵育5 min,补加200 μL的1×Binding Buffer后,流式上机检测。
1.2.3血管状结构形成实验 将处于对数期的HUVEC细胞离心,然后将HUVEC细胞(6.0×106·L-1),加入提前铺好Matrigel基质胶的96孔板,并且按要求加入不同浓度的药物。培养12 h后,各组细胞置于显微镜下观察,并采用Leica Application Suite软件照相(×100),分析各组细胞血管形成能力[9]。
1.2.4Western blot检测p62、LC3的表达 收集羟氯喹(5 mg·L-1)、贝伐单抗(100 mg·L-1)、羟氯喹(5 mg·L-1)联合贝伐单抗(100 mg·L-1)处理的HUVEC细胞,PBS清洗1次,加入蛋白解裂解液,然后置于冰上裂解细胞,并且4 ℃、13 000 r·min-1离心10 min,取上清分装于1.5 mL离心管中,并置于-80 ℃保存。BCA蛋白浓度检测,计算样品的蛋白浓度。然后经过制胶、转膜、封闭、孵育一抗、洗膜、孵育二抗、洗膜,最后将PVDF膜置于保鲜膜上,取适量ECL试剂盒中等体积的A液和B液混合,混匀后加在膜的表面,移入凝胶成像分析仪中,化学光敏模式曝光显影。照片以TIF格式导出后,在ImageJ软件下分析各条带光密度[10-11]。
1.2.5透射电镜观察细胞超微结构 将羟氯喹(5 mg·L-1)、贝伐单抗(100 mg·L-1)、羟氯喹(5 mg·L-1)联合贝伐单抗(100 mg·L-1)处理的HUVEC细胞样本用细胞刮刀刮下,PBS清洗3遍后,加入2.5%戊二醇,4 ℃过夜,利用透射电镜观察细胞超微结构的变化。
1.2.6LC3双荧光质粒转染观察自噬实验 取对数生长期的HUVEC细胞,胰酶消化后,800 r·min-1离心5 min,计数板下计数,调整细胞密度为1×107·L-1,铺24孔板,爬片。每孔均加入1 mL,放入培养箱中静置过夜。d 2换1% FBS培养基继续培养,转入mCherry-EGFP-LC3红绿双荧光质粒,d 3加入羟氯喹(5 mg·L-1)、羟氯喹(5 mg·L-1)联合贝伐单抗(100 mg·L-1),24 h后多聚甲醛固定15 min,荧光显微镜下拍照、分析。
1.2.7RNA-seq测序 本实验中,我们首先提取各组细胞的总RNA,然后通过质量检测、分选纯化mRNA及片段化、合成第一链cDNA、第二链cDNA等过程后,分步进行双链cDNA末端修复反应和3’末端加“A”反应。然后,按照操作流程,加入连接缓冲液和双链测序接头,利用T4 DNA连接酶将illumina测序接头连接至文库DNA两端。应用Agencourt SPRIselect核酸片段筛选试剂盒在纯化文库的同时,对片段大小进行筛选。再利用PCR扩增DNA文库,并对文库的质量检测后,利用Illumina Hiseq平台,以2×150 bp双端测序模式进行高通量测序,获得FastQ数据。最后整理原始数据、过滤及质量评估,整理参考基因组注释信息,比对到参考基因组及结果评估等,并且进行mRNA表达定量分析、mRNA差异表达分析、差异表达基因GO(Gene Ontology)和KEGG(Kyoto Encyclopedia of Genes and Genomes)富集分析[12],研究羟氯喹联合贝伐单抗抑制HUVEC细胞生长的作用机制。

2 结果
2.1 羟氯喹与贝伐单抗联用,协同抑制HUVEC细胞增殖利用RTCA实验检测各组HUVEC细胞的Cell Index值。结果显示,与空白对照组相比,羟氯喹、贝伐单抗组细胞的Cell Index值降低,提示羟氯喹、贝伐单抗均对HUVEC细胞的增殖有抑制作用。与单药组相比,羟氯喹和贝伐单抗联合给药Cell Index值更低,抑制作用更强(Fig 1A)。
2.2 羟氯喹与贝伐单抗联用,协同促进HUVEC细胞凋亡利用Annexin V-FITC流式凋亡检测,发现羟氯喹(5 mg·L-1)、贝伐单抗(100 mg·L-1)能够明显促进HUVEC细胞凋亡,并且羟氯喹与贝伐单抗联用后,凋亡的比例增加,提示羟氯喹与贝伐单抗联用能够协同促进HUVEC细胞凋亡(Fig 1B、1C)。
2.3 羟氯喹与贝伐单抗联用,协同抑制HUVEC体外血管状结构形成如Fig 2所示,羟氯喹(5 mg·L-1)、贝伐单抗(100 mg·L-1)均能够抑制HUVEC体外血管状结构形成,当贝伐单抗与羟氯喹联用后,血管状结构形成抑制作用更明显。该实验结果表明,羟氯喹与贝伐单抗联用可以协同抑制HUVEC体外血管状结构形成。
2.4 羟氯喹可以抑制HUVEC细胞自噬LC3主要以胞质和胞膜结合的两种状态存在,一种是弥散的胞质状态的LC3-Ⅰ,一种是膜结合状态的LC3-Ⅱ。在自噬诱导时,LC3-Ⅰ的C端在ATG4/ATG7/ATG3 等酶的作用下,被磷脂酰乙醇胺(PtdEth,PE)修饰后,转换成LC3-Ⅱ。因此,LC3-Ⅱ是目前常用的自噬标志物。此外,细胞内p62含量的变化也能反映自噬水平抑制或诱导,因为p62既是自噬受体,也可作为自噬底物被降解。
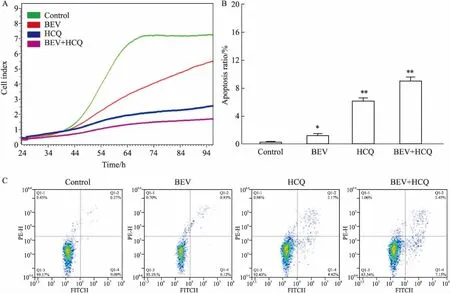
Fig 1 Synergistic inhibition effect on proliferation and apoptosis of HUVECs by HCQ combined with
A:The cell index of HUVECs after treated by HCQ,BEV,and HCQ combined with BEV; B:The cell apoptosis of HUVECs after treated by HCQ,BEV,and HCQ combined with BEV; C:The results of apoptosis assay by flow cytometry.*P<0.05,**P<0.01vscontrol

Fig 2 Synergistic inhibition effect on formation of vascular structures in HUVECs by HCQ combined with BEV(scale bar=10 μm)
本实验采用Western blot检测内源性LC3-Ⅱ变化以及辅助性检测p62水平,进而检测细胞自噬。研究结果显示,羟氯喹(5 mg·L-1)组HUVEC细胞的LC3-Ⅱ/LC3-Ⅰ比值明显增加,p62蛋白水平表达也增加,提示羟氯喹抑制自噬潮后期,使LC3-Ⅱ降解受到抑制,并使p62的降解减少。然而,贝伐单抗(100 mg·L-1)不影响LC3-Ⅱ、LC3-Ⅰ、p62蛋白的表达,羟氯喹与贝伐单抗联合组与羟氯喹单药组HUVEC细胞的LC3-Ⅱ、LC3-Ⅰ、p62蛋白的表达也无明显差异(Fig 3)。
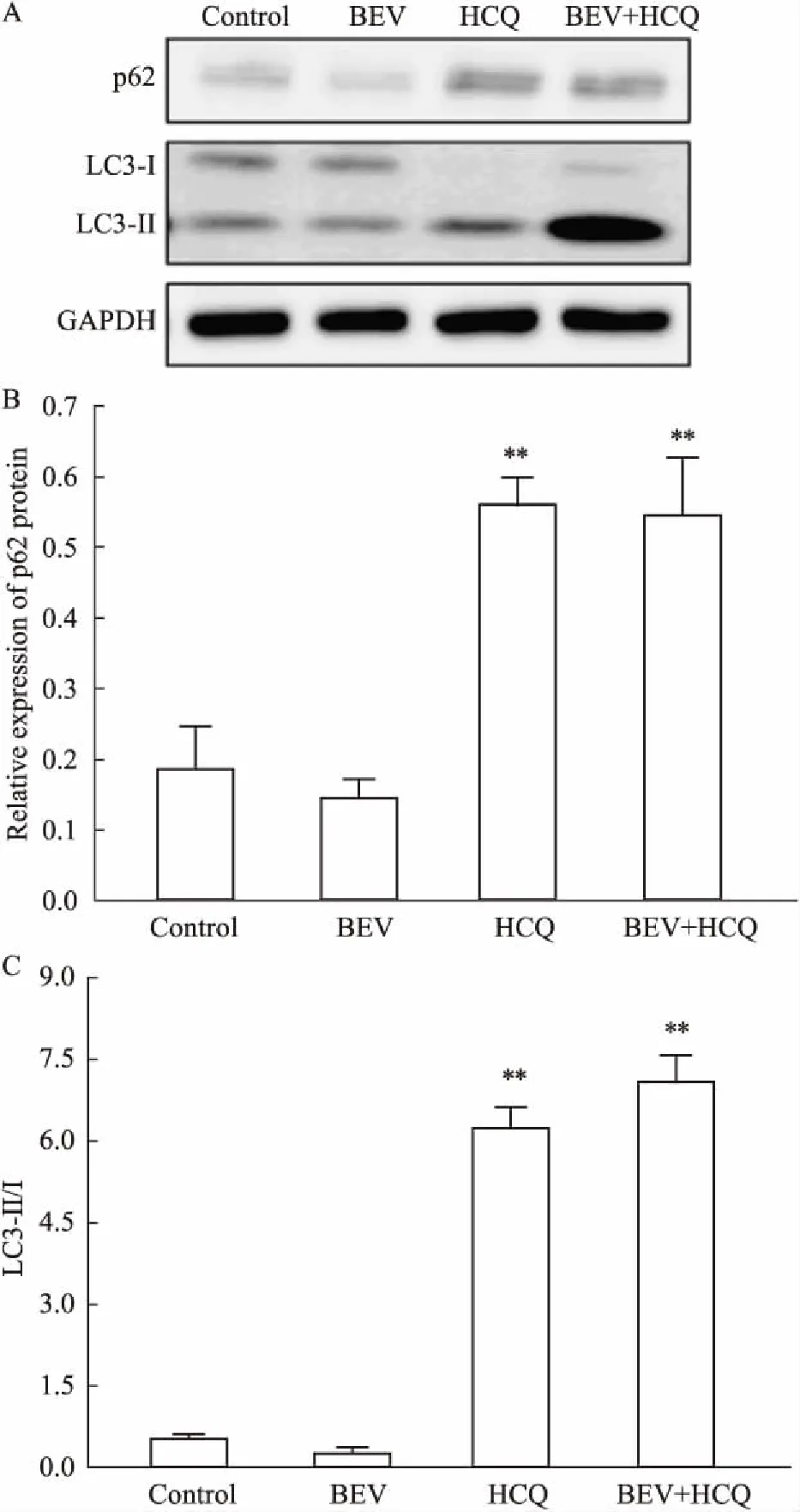
Fig 3 Synergistic inhibition effect on proteins expression of p62 and LC3 in HUVECsafter treated by HCQ
**P<0.01vscontrol
mCherry-EGFP-LC3双荧光标记能通过颜色变化确定自噬潮水平高低。本实验中,羟氯喹能使HUVEC细胞中的LC3产生点状聚集,羟氯喹与贝伐单抗联合组与羟氯喹单药组HUVEC细胞相比,无明显变化(Fig 4)。
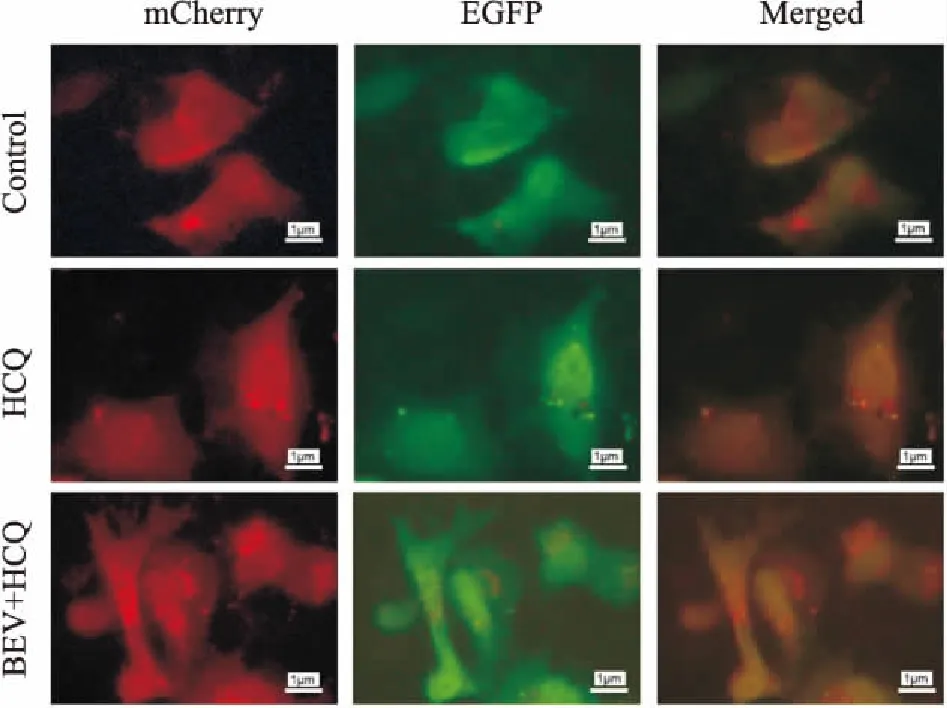
Fig 4 Effect of HCQ combined with BEV on autophagy in HUVECs using mCherry-EGFP-LC3 double fluorescence labeling(scale bar=1 μm)
2.5 电镜观察细胞自噬体及细胞线粒体自噬情况如Fig 5所示,电镜细胞形态观察(低倍):正常HUVEC细胞的细胞核大,形状规则,细胞触手生长正常。贝伐单抗组的HUVEC细胞质出现一些空泡,细胞核出现核质聚集现象;羟氯喹单独处理组细胞核边集,萎缩,染色质聚集,胞质变少,细胞触手明显变少,贝伐单抗和羟氯喹联合处理组的HUVEC细胞同时出现了羟氯喹和贝伐单抗处理后出现的现象。
电镜自噬体观察(高倍):正常HUVEC细胞可见少许自噬体,贝伐单抗处理组与对照组无明显差异。羟氯喹处理组细胞内出现大量的双膜小泡,可见新月状或者杯状的双膜或多层膜结构,并且有包绕胞质成分的趋势,提示有线粒体自噬现象。联合处理组与羟氯喹处理组自噬体表达情况相似。
电镜线粒体观察(高倍):正常HUVEC细胞的线粒体数量、形态正常,贝伐单抗处理组的细胞粗面内质网扩张、线粒体肿胀。羟氯喹处理组的细胞线粒体外室明显肿胀变性。贝伐单抗和羟氯喹联合处理组的细胞线粒体损伤更加明显,线粒体肿胀变性,有些线粒体周围形成空泡状结构,或者被空泡包裹。
以上结果提示:羟氯喹抑制自噬,自噬体未能与溶酶体融合、降解,完成细胞自噬过程。此外,贝伐单抗和羟氯喹均可以损伤HUVEC细胞线粒体,联合用药可能通过线粒体途径诱导HUVEC细胞凋亡。

Fig 5 Effect of HCQ combined with BEV on autophagosomes and mitochondria of HUVECs(scale bar=1 μm)
2.6 转录组测序,发现羟氯喹与贝伐单抗联用协同抑制HUVEC的可能机制按差异表达大于2倍的基因统计,如Fig 6A所示,与空白对照组相比,贝伐单抗组有1 801个基因下调,23个基因上调。羟氯喹组有3 774个基因下调,950个基因下调。为研究羟氯喹与贝伐单抗联用协同抗肿瘤机制,我们比较了羟氯喹或贝伐单抗单药组与联合用药组的差异表达基因,结果发现:与贝伐单抗组相比,联合用药组有2 096个基因表达发生上调,945个基因表达发生下调。与羟氯喹组相比,联合用药组有80个基因表达发生上调,36个基因表达发生下调。这其中有69个共同的差异表达基因(Fig 6B、6C)。KEGG信号通路分析,发现这些差异表达基因主要富集在磷酸肌醇代谢(inositol phosphate metabolism)、RNA运输(RNA transport)等代谢过程,以及与肿瘤相关的MAPK、ErbB、Ras、HIF-1、FoxO信号通路,此外,还富集在EGFR酪氨酸激酶抑制剂耐药、铂类耐药、内分泌耐药(endocrine resistance)的过程(Fig 6D)。最后通过蛋白网络图分析,发现羟氯喹与贝伐单抗联用可能主要通过调控RICTOR(雷帕霉素不敏感的哺乳动物雷帕霉素靶蛋白伴侣,rapamycin insensitive companion of mammalian target of rapamycin)、PIK3CA等“hub”基因协同抑制HUVEC细胞(Fig 6E)。
3 讨论
在肿瘤血管新生过程中,血管内皮生长因子(VEGF)和其受体VEGFR结合产生的活化信号发挥着至关重要的作用。贝伐单抗是一种人源化的重组单克隆抗体,能够特异性地靶向VEGF-A,阻止其结合VEGFR,从而抑制血管新生。目前,已被批准用于治疗结直肠癌、非小细胞肺癌、宫颈癌、卵巢癌、肾细胞癌和转移性胶质瘤。然而,无论是化疗,还是靶向治疗,都能够诱导肿瘤细胞产生自噬,进而帮助肿瘤细胞耐受抗肿瘤药物引起的恶劣代谢环境,从而存活下来并形成抗药性。有研究显示,贝伐单抗能诱导胶质瘤细胞自噬[13]。
羟氯喹不仅是溶酶体抑制剂,可以阻断自噬过程,造成自噬小体和LC3Ⅱ出现明显的的累积[7],而且还具有抗肿瘤活性,也能够促进血管正常化、增加抗血管药物的治疗作用,只是羟氯喹的抗肿瘤机制非常复杂,尚未研究清楚。血管内皮细胞也在血管新生中发挥关键作用,并且HUVEC常被用于进行肿瘤血管新生的实验。因此,本研究重点阐明羟氯喹与贝伐单抗联用对HUVEC细胞生长的作用及机制。
本研究发现,羟氯喹、贝伐单抗均对HUVEC细胞的增殖有抑制作用,对HUVEC细胞凋亡有促进作用,使血管状结构形成减少。与单药组相比,羟氯喹和贝伐单抗联合能够协同抑制HUVEC细胞增殖,促进HUVEC细胞凋亡,抑制HUVEC细胞血管状结构形成。此外,我们发现羟氯喹能够增加LC3-Ⅱ/LC3-Ⅰ比值和p62蛋白水平,表明羟氯喹使自噬潮后期受到抑制,导致LC3-Ⅱ降解受到抑制,及p62的降解减少。mCherry-EGFP-LC3双荧光标记和电镜自噬体观察也都证实羟氯喹可以抑制HUVEC细胞自噬。抑制细胞自噬可能是羟氯喹协同贝伐单抗抑制HUVEC细胞的机制之一。电镜结果还发现,贝伐单抗和羟氯喹联合处理组的HUVEC细胞线粒体损伤更加明显,线粒体肿胀变性,有些线粒体周围形成空泡状结构,或者被空泡包裹。为进一步阐明贝伐单抗和羟氯喹联合抑制HUVEC细胞的机制,我们还采用了转录组测序的方法。通过对实验结果的分析,发现羟氯喹比贝伐单抗引起的差异表达基因多,羟氯喹与贝伐单抗联用会产生69个共同的差异表达基因,主要富集在磷酸肌醇代谢、RNA运输、肿瘤相关的信号通路(如MAPK、ErbB、Ras、HIF-1、FoxO信号通路等),以及EGFR酪氨酸激酶抑制剂耐药、铂类耐药、内分泌耐药等过程。蛋白网络图结果表明,羟氯喹与贝伐单抗联用可能主要通过调控RICTOR、PIK3CA等“hub”基因,发挥协同抑制HUVEC细胞的作用。研究表明,肿瘤的发生发展、肿瘤细胞自噬均与PI3K/Akt/mTOR密切相关[14]。众所周知,mTOR是一种PI3K相关激酶,能够通过mTOR信号复合物1(mTORC1)和mTOR信号复合物2(mTORC2)参与肿瘤细胞凋亡、周期以及细胞自噬等生物学过程。并且PIK3CA是PI3K的一个催化亚基,PIK3CA突变可促进激酶活性,激活下游Akt,进而增加细胞侵袭和转移能力。RICTOR是mTORC2的骨架蛋白,对其稳定性至关重要,它参与调节机体内细胞的新陈代谢、增殖、凋亡、细胞自噬。例如,Lamanuzzi等[15]研究发现,RICTOR可能通过影响VEGF、CD31及MMP-9的合成和分泌,进而调控肿瘤组织内血管形成,影响体内肿瘤细胞转移。Xu等[16]发现,shRNA敲除RICTOR可以抑制自噬。
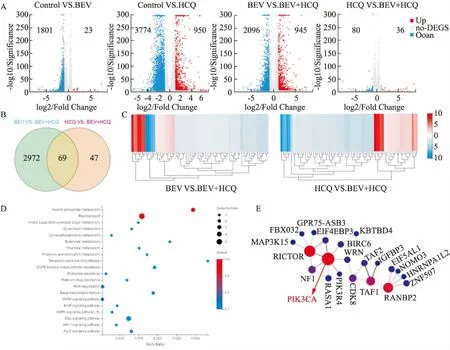
Fig 6 Transcriptome sequencing analysis of inhibitory mechanisms of HCQ combined with BEV in HUVECs
A:Quantitative analysis chart of differentially expressed genes among groups; B:Venn diagram of different expressed genes; C:Heatmap of different expressed genes among groups; D:KEGG analysis of different expressed genes; E:Protein network diagram analysis of the “hub” regulatory gene affected by HCQ combined with BEV.
综上所述,本研究发现,羟氯喹和贝伐单抗联用具有协同抑制HUVEC细胞增殖,促进HUVEC细胞凋亡,抑制HUVEC细胞血管状结构形成等作用,提示羟氯喹与贝伐单抗联用可能是一种可靠的抑制肿瘤血管的治疗策略。此外,本研究还发现,羟氯喹与贝伐单抗联用抑制肿瘤血管的机制不仅与羟氯喹抑制细胞自噬有关,而且还可能与RICTOR、PIK3CA等“hub”基因调控相关。